Международный эндокринологический журнал Том 19, №4, 2023
Вернуться к номеру
Математична модель оцінки прогностичної значущості дефіциту 25(OH)D у прогресуванні діабетичної ретинопатії у хворих на цукровий діабет 2-го типу
Авторы: Нетребін Л.І. (1), Паньків В.І. (2), Кирилюк М.Л. (3)
(1) — Національний медичний університет імені О.О. Богомольця МОЗ України, м. Київ, Україна
(2) — Український науково-практичний центр ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України, м. Київ, Україна
(3) — ТОВ «Академічний медичний центр», м. Київ, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
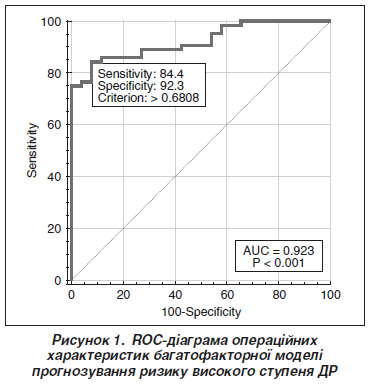
Актуальність. У сучасній медицині моделювання патологічних процесів активно впроваджується в клінічну ендокринологію та офтальмологію. Цей процес дає можливість спрогнозувати ризик виникнення, перебіг, прогноз і розвиток ускладнень цукрового діабету (ЦД), зокрема діабетичної ретинопатії (ДР). На сьогодні особлива увага приділяється перебігу ДР на тлі дефіциту вітаміну D. Але математичні моделі оцінки ризику прогресування ДР у хворих на ЦД 2-го типу на тлі дефіциту вітаміну D у науковій літературі відсутні. Мета роботи полягала в розробці адекватної математичної моделі оцінки прогностичної значущості дефіциту загального вітаміну D (25(OH)D) у прогресуванні діабетичної ретинопатії у хворих на ЦД 2-го типу. Матеріали та методи. Проведено відкрите спостережне одноцентрове одномоментне вибіркове дослідження у хворих на ДР при ЦД 2-го типу. Включення пацієнтів у групи з ДР відбувалося відповідно до протоколу ETDRS (2019) і наказу МОЗ України від 22.05.2009 № 356 у редакції наказу МОЗ України від 05.08.2009 № 574. Головними критеріями виключення були ЦД 1-го типу, хвороби та стани, що супроводжуються порушенням фосфорно-кальцієвого обміну, а також пошкодження зорового нерва, клінічно значуща макулопатія, глаукома, зріла катаракта. Дослідження проведено у 29 пацієнтів з ДР першої стадії, 23 пацієнтів з ДР другої стадії та 19 пацієнтів з ДР третьої стадії (чоловіки і жінки, середній вік 61,9 ± 2,4 року, середній рівень глікованого гемоглобіну (HbA1c) 8,12 ± 0,91 %). Концентрацію HbA1c у плазмі крові визначали методом високошвидкісної колонкової рідинної хроматографії, вітаміну D (25(OH)D) — хемілюмінесцентного імунного аналізу. Статистичний аналіз включав однофакторний дисперсійний і регресійний аналіз з побудовою логістичних моделей регресії. Результати. Показано, що при стандартизації математичного порівняння за статтю і вмістом HbA1c виявлено вірогідне (p < 0,001) зниження ризику високого ступеня ДР при збільшенні концентрації 25(OH)D у плазмі крові на кожен нг/мл (співвідношення шансів 0,46 (95% довірчий інтервал (ДІ) 0,32–0,67)). Показник псевдокореляції (Nagelkerke) R2 = 0,54; площа під кривою операційних характеристик — 0,92 (95% ДІ 0,85–0,97), що свідчить про наявність сильного зв’язку між ризиком високого ступеня ДР і концентрацією 25(OH)D у крові, статтю і рівнем HbA1c. Отримана багатофакторна модель була подана відповідною математичною формулою. При виборі оптимального (за Youden Index) порогу прийняття рішення чутливість отриманої моделі логістичної регресії прогнозування ризику високого ступеня ДР дорівнює 84,4 % (95% ДІ 73,1–92,2 %), специфічність — 92,3 % (95% ДІ 74,9–99,1 %). Висновки. Розроблена адекватна математична модель логістичної регресії оцінки прогностичної значущості дефіциту загального вітаміну D у прогресуванні ДР у хворих на ЦД 2-го типу, прогностична значущість якої становить 96,4 % (95% ДІ 87,7–99,0 %).
Background. In modern medicine, modeling of pathological processes is actively implementing in clinical endocrinology and ophthalmology. This process provides an opportunity to predict the risk of occurrence, course, prognosis and development of complications of type 2 diabetes mellitus (T2DM), in particular diabetic retinopathy (DR). Nowadays, special attention is paid to the course of DR against the background of vitamin D deficiency. But in the scientific literature, there are no mathematical models for assessing the risk of DM progression in patients with type 2 diabetes against the background of vitamin D deficiency. Aim of the study is to develop an adequate mathematical model for assessing the prognostic significance of 25(OH)D deficiency in the progression of diabetic retinopathy in patients with type 2 diabetes. Materials and methods. An open observational single-center one-stage selective study was conducted. It was approved by the Local Ethics Committee. Seventy-one patients (138 eyes) with T2DM and DR (men and women; mean age 61.9 ± 2.4 years; mean HbA1c 8.12 ± 0.91 %) were divided into 3 groups, based on the stage of DR (according to fundus instrumental examination). The inclusion of patients in groups with DR was carried out in accordance with the ETDRS protocol (2019). Statistical processing included ANOVA, MANOVA and regression analysis with the construction of logistic regression models. Results. A statistically significant (p < 0.001) decrease in the risk of a high degree of DR was found with an increasing concentration of 25(OH)D in the blood plasma for each 1 ng/ml (odds ratio = 0.46 (0.32–0.67)). The pseudocorrelation index (Nagelkerke) R2 is 0.54, area under a receiver operating characteristic curve is 0.92 (95% confidence interval (CI) 0.85–0.97), which indicates the presence of a strong relationship between the risk of a high degree of DR and the concentration of 25(OH)D in the blood, gender and HbA1c level. The obtained multifactorial model was represented by the appropriate mathematical formula. The sensitivity (according to the Youden index) of the obtained logistic regression model is 84.4 % (95% CI 73.1–92.2), specificity is 92.3% (95% CI 74.9–99.1). Conclusions. An adequate mathematical model of logistic regression was developed to assess the prognostic significance of total vitamin D deficiency in the progression of DR in patients with T2DM. Its prognostic significance is 96.4 % (95% CI 87.7–99.0).
діабетична ретинопатія; цукровий діабет 2-го типу; вітамін D; математична модель
diabetic retinopathy; type 2 diabetes; vitamin D; mathematical model
Вступ
Матеріали та методи
Результати
Обговорення
Висновки
- Savitskyi I.V., Semenko V.V., Serdiuk V.M. Metabolic correction of experimental diabetic retinopathy. J. Ophthalmol. (Ukraine). 2017. 6. 72-77. doi.org/10.31288/oftalmolzh201767277.
- Alifanov I.S., Sakovych V.M. Prognostic risk factors for diabetic retinopathy in patients with type 2 diabetes mellitus. J. Ophthalmol. (Ukraine). 2022. 6. 19-23.
- Kyryliuk M.L., Mogilevskyy S.Yu., Serdiuk V.M. Evaluation of the Prognostic Significance of Adipose Tissue Hormones in the Development of Diabetic Retinopathy in Patients With Type 2 Diabetes Mellitus. Journal of the Endocrine Society. 2021. 5(1) April-May. 412-413. doi.org/10.1210/jendso/bvab048.841.
- Korobov К. Association of glycation markers with the progression of the initial stages of diabetic non-proliferative retinopathy in type 2 diabetes mellitus. Journal of Education, Health and Sport. 2021. 3. 97-112. https://doi.org/10.12775/JEHS.2021.11.03.011.
- International Council Of Ophthalmology. ICO Guidelines for Diabe–tic Eye Care (2017). https://icoph.org/eye-care-delivery/diabetic-eye-care.
- Pankiv V.I., Yuzvenko T.Yu., Pashkovska N.V., Pankiv I.V. The relationship between serum vitamin D concentrations and deve–lopment of diabetic retinopathy in type 2 diabetes mellitus. International Journal of Endocrinology (Ukraine). 2022. 18(8). 432-435. doi: 10.22141/2224-0721.18.8.2022.1221.
- Solomon S.D., Goldberg M.F. ETDRS Grading of Diabetic Retinopathy: Still the Gold Standard? Ophthalmic Res. 2019. 62(4). 190-195. https://doi.org/10.1159/000501372.
- Martínez-Camblor P., Pardo-Fernández J.C. The Youden Index in the Generalized Receiver Operating Characteristic Curve Context. Int. J. Biostat. 2019 Apr 3. 15(1). /j/ijb.2019.15.issue-1/ijb-2018-0060/ijb-2018-0060.xml. doi: 10.1515/ijb-2018-0060. PMID: 30943172.
- Urbanovych A., Shykula S. Vitamin D and diabetes mellitus. International Journal of Endocrinology (Ukraine). 2022. 18(1). 78-83. https://doi.org/10.22141/2224-0721.18.1.2022.1148.
- Li X., Liu Y., Zheng Y., Wang P., Zhang Y. The Effect of Vitamin D Supplementation on Glycemic Control in Type 2 Diabetes Patients: A Systematic Review and Meta-Analysis. Nutrients. 2018 Mar 19. 10(3). 375. doi: 10.3390/nu10030375.
- Jamali N., Wang S., Darjatmoko S.R., Sorenson C.M., Sheibani N. Vitamin D receptor expression is essential during retinal vascular development and attenuation of neovascularization by 1, 25(OH)2D3. PLoS One. 2017 Dec 22. 12(12). e0190131. doi: 10.1371/journal.pone.0190131.
- Tecilazich F., Formenti A.M., Giustina A. Role of vitamin D in diabetic retinopathy: Pathophysiological and clinical aspects. Rev. Endocr. Metab. Disord. 2021 Dec. 22(4). 715-727. doi: 10.1007/s11154-020-09575-4. PMID: 33026598; PMCID: PMC7538371.
- Pankiv I. Vitamin D: New Aspects of Application, Effective Doses. The Current State of the Problem. International Journal of Endocrinology (Ukraine). 2021. 17(1). 38-42. doi: 10.22141/2224-0721.17.1.2021.226430.
- Luo B.A., Gao F., Qin L.L. The Association between Vitamin D Deficiency and Diabetic Retinopathy in Type 2 Diabetes: A Meta-Analysis of Observational Studies. Nutrients. 2017 Mar 20. 9(3). 307. doi: 10.3390/nu9030307.
- Alam U., Amjad Y., Chan A.W., Asghar O., Petropoulos I.N., Malik R.A. Vitamin D deficiency is not associated with diabetic retinopathy or maculopathy. J. Diabetes Res. 2016. 2016. 6156217. doi: 10.1155/2016/6156217.
- Herrmann M., Sullivan D.R., Veillard A.S., McCorquoda–le T., Straub I.R., Scott R. et al.; FIELD Study Investigators. Serum 25-hydroxyvitamin D: a predictor of macrovascular and microvascular complications in patients with type 2 diabetes. Diabetes Care. 2015 Mar. 38(3). 521-8. doi: 10.2337/dc14-0180.
- Xiao Y., Wei L., Xiong X., Yang M., Sun L. Association Between Vitamin D Status and Diabetic Complications in Patients With Type 2 Diabetes Mellitus: A Cross-Sectional Study in Hunan China. Front. Endocrinol. 2020. 11. 564738. doi: 10.3389/fendo.2020.564738.