Международный эндокринологический журнал Том 19, №4, 2023
Вернуться к номеру
Стан мікробіому товстої кишки в жінок при гестаційному діабеті
Авторы: Джуряк В.С., Міхєєв А.О., Сидорчук Л.І., Паньків І.В.
Буковинський державний медичний університет, м. Чернівці, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
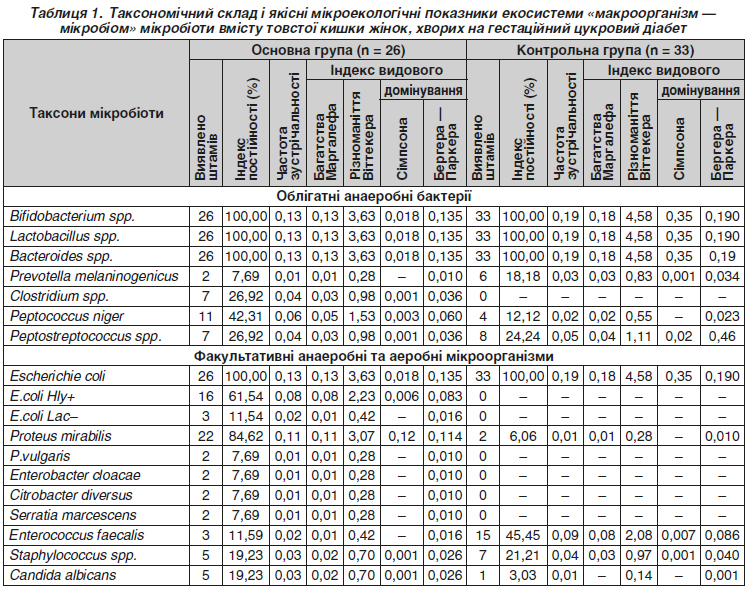
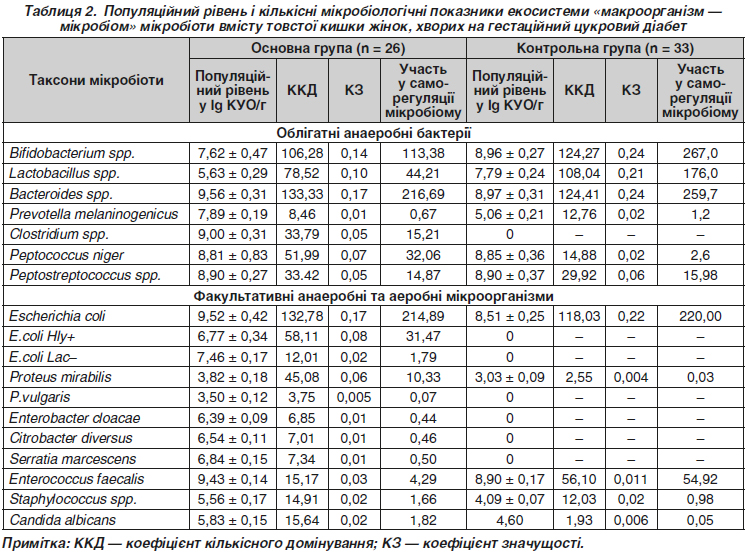
Актуальність. Гестаційний цукровий діабет — це стан, що виникає внаслідок розладу метаболічних процесів на тлі інсулінорезистентності й підвищення рівня глюкози крові впродовж вагітності. Ця патологія призводить до значної кількості ускладнень вагітності й пологів, високої дитячої перинатальної захворюваності та смертності, його поширеність відрізняється в усьому світі. Метою роботи було встановити таксономічний склад, популяційний рівень і мікроекологічні показники екосистеми «макроорганізм — мікробіом» симбіотичної мікробіоти товстої кишки жінок, хворих на гестаційний цукровий діабет. Матеріали і методи: мікробіологічне обстеження вмісту порожнини товстої кишки проведено у 26 вагітних жінок віком від 18 до 35 років. Клінічним матеріалом для мікробіологічного обстеження був свіжий вміст (фекалії) порожнини товстої кишки, взятий із середніх порцій, який відбирався в стерильні (після автоклавування) флакончики. Результати. За результатами роботи встановлено, що при гестаційному цукровому діабеті порушуються таксономічний склад і мікроекологічні показники екосистеми «макроорганізм — мікробіом» мікробіоти вмісту порожнини товстої кишки жінок за рахунок контамінації біотопу патогенними (Е.coli HLy+) та умовно-патогенними (Е.coli Lac–, P.mirabilis, P.vulgaris, E.cloacae, C.diversus, S.marcescens), ентеробактеріями, C.albicans, P.niger і бактеріями роду Clostridium. Зміни таксономічного складу і мікроекологічних показників мікробіому товстої кишки в жінок, хворих на гестаційний цукровий діабет, призводять до різнонаправлених, залежно від таксону, змін: знижується популяційний рівень бактерій, найважливіших за представництвом у складі товстокишкового мікробіому людини, з мультифункціональною роллю у підтримці мікроекологічного гомеостазу (бактерії роду Bifidobacterium — на 17,59 %, Lactobacillus — на 38,37 %), відбувається підвищення або формується стабільна тенденція до підвищення популяційного рівня умовно-патогенних ентеробактерій P.mirabilis на 26,67 %, в інших ентеробактерій популяційний рівень досягає високих показників (від 6,390 ± 0,009 lg КУО/г до 7,46 ± 0,17 lg КУО/г), рівень Staphylococcus зростає на 35,94 %, C.albicans — на 26,74 %, P.melaninogenicus — на 55,93 %.
Background. Gestational diabetes is a condition that arises due to impaired metabolic processes against the background of insulin resistance and an increase in blood glucose levels during pregnancy. This pathology leads to a significant number of pregnancy and childbirth complications, high child perinatal morbidity and mortality, and its prevalence varies throughout the world. The aim of the work was to determine the taxonomic composition, population level and microecological indicators of the macroorganism-microbiome ecosystem of the symbiotic colon microbiota in women with gestational diabetes. Materials and methods. The microbiological examination of the colon contents was carried out in 26 pregnant women aged 18 to 35 years. The clinical material for microbiological examination was the fresh colon contents (faeces) taken from medium portions, which were collected in sterile (after autoclaving) vials. Results. According to the results of the work, it was found that during gestational diabetes, the taxonomic composition and microecological parameters of the macroorganism-microbiome ecosystem of the colon microbiota in women are impaired due to the biotope contamination with pathogenic microorganisms (E.coli HLy+) and opportunistic pathogens (E.coli Lac-, P.mirabilis, P.vulgaris, E.cloacae, C.diversus, S.marcescens), enterobacteria, C.albicans, P.niger and bacteria of the genus Clostridium. Alterations in the taxonomic composition and microecological indicators of the colon microbiome in women with gestational diabetes lead to multidirectional changes depending on the taxon: a decrease in the population level of bacteria, which are the most important in terms of representation in the human colon microbiome, with a multifunctional role in maintaining microecological homeostasis (bacteria of the genus Bifidobacterium — by 17.59 %, Lactobacillus — by 38.37 %) and an increase or a stable trend towards an increase in the population level of opportunistic enterobacteria P.mirabilis by 26.67 %; among other enterobacteria, the population reaches high levels (from 6.390 ± 0.009 lg CFU/g to 7.46 ± 0.17 lg CFU/g), the level of Staphylococcus in increased by 35.94 %, C.albicans — by 26.74 %, P.melaninogenicus — by 55.93 %.
гестаційний цукровий діабет;, мікробіом товстої кишки; таксономічний склад; мікроекологічні показники екосистеми «макроорганізм — мікробіом»
gestational diabetes; colon microbiome; taxonomic composition; microecological indicators of the macroorganism-microbiome ecosystem
Вступ
Матеріали та методи
Результати
Обговорення
Висновки
- Lende M., Rijhsinghani A. Gestational Diabetes: Overview with Emphasis on Medical Management. Int. J. Environ. Res Public. Health. 2020 Dec 21. 17(24). 9573. doi: 10.3390/ijerph17249573. PMID: 33371325; PMCID: PMC7767324.
- Payenok O., Korytko О., Petruniak R. Hormones of Adipose Tissue and Gestational Diabetes. International Journal of Endocrinology (Ukraine). 2013. 7(55). 60-66. https://doi.org/10.22141/2224-0721.7.55.2013.84680.
- Falalyeyeva T., Mamula Y., Scarpellini E., Leshchenko I., Humeniuk A., Pankiv I., Kobyliak N. Probiotics and obesity associated disease: an extended view beyond traditional strains. Minerva Gastroenterol (Torino). 2021 Dec. 67(4). 348-356. doi: 10.23736/S2724-5985.21.02909-0. PMID: 35040301.
- Mack L.R., Tomich P.G. Gestational Diabetes: Diagnosis, Classification, and Clinical Care. Obstet. Gynecol. Clin. North Am. 2017 Jun. 44(2). 207-217. doi: 10.1016/j.ogc.2017.02.002. PMID: 28499531.
- Alejandro E.U., Mamerto T.P., Chung G., Villavieja A., Gaus N.L., Morgan E., Pineda-Cortel M.R.B. Gestational Diabetes Mellitus: A Harbinger of the Vicious Cycle of Diabetes. Int. J. Mol Sci. 2020 Jul 15. 21(14). 5003. doi: 10.3390/ijms21145003. PMID: 32679915; PMCID: PMC7404253.
- Mustad V.A., Huynh D.T.T., López-Pedrosa J.M., Campoy C., Rueda R. The Role of Dietary Carbohydrates in Gestational Diabetes. Nutrients. 2020 Jan 31. 12(2). 385. doi: 10.3390/nu12020385. PMID: 32024026; PMCID: PMC7071246.
- Sugino K.Y., Hernandez T.L., Barbour L.A., Kofonow J.M., Frank D.N., Friedman J.E. A maternal higher-complex carbohydrate diet increases bifidobacteria and alters early life acquisition of the infant microbiome in women with gestational diabetes mellitus. Front. Endocrinol (Lausanne). 2022 Jul 28. 13. 921464. doi: 10.3389/fendo.2022.921464. PMID: 35966074; PMCID: PMC9366142.
- de Mendonça E.L.S.S., Fragoso M.B.T., de Oliveira J.M., Xavier J.A., Goulart M.O.F,. de Oliveira A.C.M. Gestational Diabetes Mellitus: The Crosslink among Inflammation, Nitroxidative Stress, Intestinal Microbiota and Alternative Therapies. Antioxidants (Basel). 2022 Jan 7. 11(1). 129. doi: 10.3390/antiox11010129. PMID: 35052633; PMCID: PMC8773111.
- Zhang Y., Chen T., Zhang Y., Hu Q., Wang X., Chang H. et al. Contribution of trace element exposure to gestational diabetes mellitus through disturbing the gut microbiome. Environ Int. 2021 Aug. 153. 106520. doi: 10.1016/j.envint.2021.106520. Epub 2021 Mar 25. PMID: 33774496; PMCID: PMC8638703.
- Fuhler G.M. The immune system and microbiome in pregnancy. Best Pract. Res Clin. Gastroenterol. 2020 Feb-Apr. 44-45. 101671. doi: 10.1016/j.bpg.2020.101671. Epub 2020 Mar 6. PMID: 32359685.
- Chen T., Qin Y., Chen M., Zhang Y., Wang X., Dong T. et al. Gestational diabetes mellitus is associated with the neonatal gut microbiota and metabolome. BMC Med. 2021 May 27. 19(1). 120. doi: 10.1186/s12916-021-01991-w. PMID: 34039350; PMCID: PMC8157751.
- Hasain Z., Mokhtar N.M., Kamaruddin N.A., Mohamed Ismail N.A., Razalli N.H., Gnanou J.V., Raja Ali R.A. Gut Microbiota and Gestational Diabetes Mellitus: A Review of Host-Gut Microbiota Interactions and Their Therapeutic Potential. Front. Cell. Infect. Microbiol. 2020 May 15. 10. 188. doi: 10.3389/fcimb.2020.00188. PMID: 32500037; PMCID: PMC7243459.
- Medici Dualib P., Ogassavara J., Mattar R., Mariko Koga da Silva E., Atala Dib S., de Almeida Pititto B. Gut microbiota and gestational Diabetes Mellitus: A systematic review. Diabetes Res Clin. Pract. 2021 Oct. 180. 109078. doi: 10.1016/j.diabres.2021.109078. Epub 2021 Sep 29. PMID: 34599971.
- Cortez R.V., Taddei C.R., Sparvoli L.G., Ângelo A.G.S., Padilha M., Mattar R., Daher S. Microbiome and its relation to gestational diabetes. Endocrine. 2019 May. 64(2). 254-264. doi: 10.1007/s12020-018-1813-z. Epub 2018 Nov 12. PMID: 30421135.
- Wang J., Zheng J., Shi W., Du N., Xu X., Zhang Y. et al. Dysbiosis of maternal and neonatal microbiota associated with gestational diabetes mellitus. Gut. 2018 Sep. 67(9). 1614-1625. doi: 10.1136/gutjnl-2018-315988. Epub 2018 May 14. PMID: 29760169; PMCID: PMC6109274.
- Tsarna E., Christopoulos P. The role of gut microbio–me in prevention, diagnosis and treatment of gestational diabetes mellitus. J. Obstet. Gynaecol. 2022 Jul. 42(5). 719-725. doi: 10.1080/–01443615.2021.1959534. Epub 2021 Oct 25. PMID: 34693846.
- Neri C., Serafino E., Morlando M., Familiari A. Microbiome and Gestational Diabetes: Interactions with Pregnancy Outcome and Long-Term Infant Health. J. Diabetes Res. 2021 Nov 25. 2021. 9994734. doi: 10.1155/2021/9994734. PMID: 34869780; PMCID: PMC8639280.
- Koerner R., Groer M., Prescott S. Scoping Review of the Relationship Between Gestational Diabetes Mellitus and the Neonatal and Infant Gut Microbiome. J. Obstet. Gynecol. Neonatal. Nurs. 2022 Sep. 51(5). 502-516. doi: 10.1016/j.jogn.2022.06.037. Epub 2022 Jul 13. PMID: 35839839.
- Farhat S., Hemmatabadi M., Ejtahed H.S., Shirzad N., Larijani B. Microbiome alterations in women with gestational diabetes mellitus and their offspring: A systematic review. Front. Endocrinol (Lausanne). 2022 Dec 8. 13. 1060488. doi: 10.3389/fendo.2022.1060488. PMID: 36568098; PMCID: PMC9772279.
- Homayouni A., Bagheri N., Mohammad-Alizadeh-Charandabi S., Kashani N., Mobaraki-Asl N., Mirghafurvand M. et al. Prevention of Gestational Diabetes Mellitus (GDM) and Probiotics: Mechanism of Action: A Review. Curr. Diabetes Rev. 2020. 16(6). 538-545. doi: 10.2174/1573399815666190712193828. PMID: 31544699.
- Callaway L.K., McIntyre H.D., Barrett H.L., Foxcroft K., Tremellen A., Lingwood B.E. et al. Probiotics for the Prevention of Gestational Diabetes Mellitus in Overweight and Obese Women: Findings From the SPRING Double-Blind Randomized Controlled Trial. Diabetes Care. 2019 Mar. 42(3). 364-371. doi: 10.2337/dc18-2248. Epub 2019 Jan 18. PMID: 30659070.
- Deng Y.F., Wu L.P., Liu Y.P. Probiotics for preventing gestational diabetes in overweight or obese pregnant women: A review. World J. Clin. Cases. 2022 Dec 26. 10(36). 13189-13199. doi: 10.12998/wjcc.v10.i36.13189. PMID: 36683622; PMCID: PMC9851018.
- Zhou L., Ding C., Wu J., Chen X., Ng D.M., Wang H., Zhang Y., Shi N. Probiotics and synbiotics show clinical efficacy in treating gestational diabetes mellitus: A meta-analysis. Prim. Care Diabetes. 2021 Dec. 15(6). 937-947. doi: 10.1016/j.pcd.2021.08.005. Epub 2021 Aug 18. PMID: 34417122.
- Taylor B.L., Woodfall G.E., Sheedy K.E., O’Riley M.L., Rainbow K.A., Bramwell E.L., Kellow NJ. Effect of Probiotics on Metabolic Outcomes in Pregnant Women with Gestational Diabetes: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Nutrients. 2017 May 5. 9(5). 461. doi: 10.3390/nu9050461. PMID: 28475161; PMCID: PMC5452191.
- Wang C.C., Tung Y.T., Chang H.C., Lin C.H., Chen Y.C. Effect of Probiotic Supplementation on Newborn Birth Weight for Mother with Gestational Diabetes Mellitus or Overweight/Obesity: A Systematic Review and Meta-Analysis. Nutrients. 2020 Nov 12. 12(11). 3477. doi: 10.3390/nu12113477. PMID: 33198366; PMCID: PMC7696869.
- Franco-Duarte R., Černáková L., Kadam S., Kaushik K.S., Salehi B., Bevilacqua A. et al. Advances in Chemical and Biological Methods to Identify Microorganisms-From Past to Present. Microorganisms. 2019 May 13. 7(5). 130. doi: 10.3390/microorganisms7050130. PMID: 31086084; PMCID: PMC6560418.
- Lagier J.C., Hugon P., Khelaifia S., Fournier P.E., La Scola B., Raoult D. The rebirth of culture in microbiology through the example of culturomics to study human gut microbiota. Clin. Microbiol. Rev. 2015 Jan. 28(1). 237-64. doi: 10.1128/CMR.00014-14. PMID: 25567229; PMCID: PMC4284300.
- Gajdács M., Spengler G., Urbán E. Identification and Antimicrobial Susceptibility Testing of Anaerobic Bacteria: Rubik’s Cube of Clinical Microbiology? Antibiotics (Basel). 2017 Nov 7. 6(4). 25. doi: 10.3390/antibiotics6040025. PMID: 29112122; PMCID: PMC5745468.
- Mikhieiev A.O., Bendas V.V., Sydorchuk L.I., Yakovychuk N.D., Sydorchuk I.I. Peculiarities of violation of the taxonomic composition in the contents of the colon cavity in chronic obstructive bronchitis. International scientific and practical conference “Topical tendencies of science and practice”. 2021. Edmonton, Canada. 2021. 281-285.