Международный эндокринологический журнал Том 19, №4, 2023
Вернуться к номеру
Зв’язок між кардіоваскулярною патологією і порушенням метаболізму глюкози з дефіцитом вітаміну D (огляд літератури і власні дані)
Авторы: Гончарова О.А., Іманова Н.І.
Харківський національний медичний університет, м. Харків, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
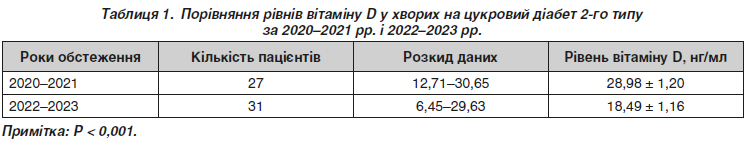
Актуальність. Вітамін D відіграє значну роль у багатьох процесах в організмі людини, що урізноманітнює симптоми його нестачі, тому не завжди вдається своєчасно діагностувати його дефіцит. Водночас за даними низки клінічних досліджень доведено обернений зв’язок між зниженим рівнем вітаміну D і смертністю від усіх причин і серцево-судинних захворювань (ССЗ), перебігом цукрового діабету (ЦД), артеріальної гіпертензії, хронічної хвороби нирок, атеросклерозу, коронарної хвороби серця і встановлено механізми впливу дефіциту вітаміну D на різні метаболічні процеси. Розвиток і прогресування ССЗ і судинних ускладнень ЦД на сьогодні є основними причинами інвалідизації і смерті хворих. Усе це обґрунтовує необхідність контролювати забезпечення вітаміном D хворих із цією коморбідною патологією. Мета: дослідити наявність і вираженість дефіциту вітаміну D у хворих на ЦД 2-го типу (ЦД2) з наявністю супутньої кардіальної патології. Матеріали та методи. Обстежено 31 пацієнта (17 чоловіків і 14 жінок віком 51,51 ± 1,73 року, тривалість ЦД 8,59 ± 1,70 року), які перебували на лікуванні в ендокринологічній клініці із жовтня 2022 по травень 2023 рр. і сформували основну групу. Групу порівняння становили 27 хворих на ЦД2, які перебували в цій клініці у 2020–2021 рр. Імуноферментним методом досліджували рівень 25-гідроксихолекальциферолу (25(ОН)D) у крові (лабораторна норма 30–50 нг/мл). При рівні вітаміну D у діапазоні 20–30 нг/мл діагностувалася його недостатність, а при рівні нижче за 20 нг/мл — дефіцит. Статистична обробка проводилася за допомогою Microsoft Excel і Statistica 6.0. Результати. Серед обстежених основної групи кардіальна патологія була представлена гіпертонічною хворобою, яка була встановлена в усіх обстежених (І ст. — 6 пацієнтів; ІІ ст. — 21 пацієнт і ІІІ ст. — 4 пацієнти); ішемічною хворобою серця і кардіосклерозом — у 7 хворих; серцевою недостатністю І або ІІ ст. — у всіх обстежених. Усі хворі основної групи мали дефіцит або недостатність вітаміну D: 15 осіб — дефіцит (12,96 ± 1,06 нг/мл), 16 — недостатність (23,68 ± 0,72 нг/мл). Щодо групи порівняння пацієнти основної групи мали вірогідно нижчий середній рівень вітаміну D (18,49 ± 1,16 нг/мл і 28,98 ± 1,20 нг/мл відповідно; p < 0,001). Висновки. У хворих на ЦД2 із коморбідною серцево-судинною патологією відзначається зниження рівня забезпечення вітаміном D. В умовах воєнного стану спостерігається вірогідне посилення дефіциту вітаміну D. Встановлений на сьогодні негативний вплив дефіциту вітаміну D на перебіг ЦД і серцево-судинної патології обґрунтовує необхідність моніторингу ступеня забезпечення таких хворих вітаміном D.
Background. Vitamin D plays a significant role in many processes in the human body, which diversifies the symptoms of its insufficiency, so it is not always possible to diagnose its deficiency in a timely manner. At the same time, according to a number of clinical studies, an inverse relationship has been proven between a reduced level of vitamin D and mortality from all causes and cardiovascular diseases, the course of diabetes mellitus (DM), hypertension, chronic kidney disease, atherosclerosis, coronary heart disease; and the mechanisms of the influence of vitamin D deficiency on various metabolic processes have been revealed. The development and progression of cardiovascular diseases and vascular complications of DM are currently the main causes of disability and mortality of patients. All this substantiates the need to control and monitor the vitamin D supply in patients with this comorbid pathology. Aim of the study is to investigate the presence and severity of vitamin D deficiency in patients with type 2 DM and the presence of concomitant cardiac pathology. Materials and methods. Main group included 31 patients (17 men and 14 women aged 51.51 ± 1.73 years, with duration of DM of 8.59 ± 1.70 years) who were treated in the endocrinology clinic from October 2022 to May 2023. The comparison group consisted of 27 patients with type 2 DM who stayed in this clinic in 2020–2021. Serum level of 25-hydroxycholecalciferol (25(OH)D) was studied using the enzyme-linked immunosorbent assay. The level of vitamin D less than 20–30 ng/ml was considered as its insufficiency, and the level below 20 ng/ml as deficiency. Statistical processing was carried out using Microsoft Excel and Statistica 6.0. Results. In the main group, cardiac pathology manifested itself by the presence of hypertension detected in all patients (stage I — 6 cases; stage II — 21 and stage IІI — 4); coronary heart disease and cardiosclerosis — in 7 patients; heart failure of the first or second degree — in all individuals. All patients in the main group were vitamin D deficient or insufficient: 15 had a deficiency (12.96 ± 1.06 ng/ml), and 16 had an insufficiency (23.68 ± 0.72 ng/ml). In contrast to the comparison group, patients from the main group had a significantly lower average level of vitamin D (18.49 ± 1.16 ng/ml vs 28.98 ± 1.02 ng/ml, p < 0.001). Taking into account a decrease in the level of vitamin D supply of patients, including those with comorbid pathology examined in 2022–2023, which is obviously associated with a long stay in shelters and a stressful situation caused by the state of war, and its impact on the course of cardiovascular diseases and diabetes, it is necessary to pay more attention to the detection and timely appropriate correction of vitamin D deficiency. Conclusions. In patients with type 2 diabetes and comorbid cardiovascular pathology, there is a decrease in the level of vitamin D supply. During the war in Ukraine, there is a probable deepening of vitamin D deficiency. The negative impact of vitamin D deficiency on the course of diabetes and cardiovascular pathology justifies the need to monitor vitamin D supply in such patients.
вітамін D; серцево-судинні захворювання; цукровий діабет
vitamin D; cardiovascular diseases; diabetes mellitus
Вступ
Матеріали та методи
Результати
Обговорення
Висновки
- Barbarawi M., Kheiri B., Zayed Y., Barbarawi O., Dhillon H., Swaid B., Yelangi A. et al. Vitamin D Supplementation and Cardiovascular Disease Risks in More Than 83 000 Individuals in 21 Randomi–zed Clinical Trials: A Meta-analysis. JAMA Cardiol. 2019 Aug 1. 4(8). 765-776. doi: 10.1001/jamacardio.2019.1870. Erratum in: JAMA Cardiol. 2019 Nov 6. PMID: 31215980; PMCID: PMC6584896.
- Neale R.E., Baxter C., Romero B.D. et al. The D-Health Trial: a randomised controlled trial of the effect of vitamin D on mortality. Lancet Diabetes Endocrinol. 2022 Feb. 10(2). 120-128. doi: 10.1016/S2213-8587(21)00345-4.
- Nudy M., Krakowski G., Ghahramani M., Ruzieh M., Foy A.J. Vitamin D supplementation, cardiac events and stroke: A systema–tic review and meta-regression analysis. Int. J. Cardiol. Heart Vasc. 2020 May 20. 28. 100537. doi: 10.1016/j.ijcha.2020.100537. Erratum in: Int. J. Cardiol. Heart Vasc. 2020 Dec 19. 32. 100698. PMID: 32462077; PMCID: PMC7240168.
- Manson J.E., Cook N.R., Lee I.M. et al. VITAL Research Group. Vitamin D Supplements and Prevention of Cancer and Cardiovascular Disease. N. Engl. J. Med. 2019 Jan 3. 380(1). 33-44. doi: 10.1056/NEJMoa1809944.
- Yang J., Ou-Yang J., Huang J. Low serum vitamin D levels increase the mortality of cardiovascular disease in older adults: A dose-response meta-analysis of prospective studies. Medicine (Baltimore). 2019 Aug. 98(34). e16733. doi: 10.1097/MD.0000000000016733.
- Emerging Risk Factors Collaboration/EPIC-CVD/Vitamin D Studies Collaboration. Estimating dose-response relationships for vitamin D with coronary heart disease, stroke, and all-cause mortality: observational and Mendelian randomisation analyses. Lancet Diabetes Endocrinol. 2021 Dec. 9(12). 837-846. doi: 10.1016/S2213-8587(21)00263-1.
- Degerud E., Nygård O., de Vogel S., Hoff R., Svingen G.F.T., Pedersen E.R., Nilsen D.W.T. et al. Plasma 25-Hydroxyvitamin D and Mortality in Patients With Suspected Stable Angina Pectoris. J. Clin. Endocrinol. Metab. 2018 Mar 1. 103(3). 1161-1170. doi: 10.1210/jc.2017-02328. PMID: 29325121.
- Amrein K., Scherkl M., Hoffmann M. et al. Vitamin D deficiency 2.0: an update on the current status worldwide. Eur. J. Clin. Nutr. 2020 Nov. 74(11). 1498-1513. doi: 10.1038/s41430-020-0558-y.
- Huang H.Y., Lin T.W., Hong Z.X., Lim L.M. Vitamin D and Diabetic Kidney Disease. Int. J. Mol. Sci. 2023. 24. 3751. doi: 10.3390/ijms24043751.
- Delrue C., Speeckaert R., Delanghe J.R., Speeckaert M.M. The Role of Vitamin D in Diabetic Nephropathy: A Translational Approach. Int. J. Mol. Sci. 2022. 23. 807. doi: 10.3390/ijms23020807.
- Goncharova O. Comorbidity in type 1 and type 2 diabetes mellitus. Vitamin D in the monitoring system. International Journal оf Endocrinology (Ukraine). 2021. 17(1). 20-25 (in Ukrainian). https://doi.org/10.22141/2224-0721.17.1.2021.226426.
- Urbanovych A., Shykula S. Vitamin D and diabetes mellitus. International Journal оf Endocrinology (Ukraine). 2022. 18(1). 78-83 (in Ukrainian). https://doi.org/10.22141/2224-0721.18.1.2022.1148.
- Li X., Liu Y., Zheng Y., Wang P., Zhang Y. The Effect of Vitamin D Supplementation on Glycemic Control in Type 2 Diabetes Patients: A Systematic Review and Meta-Analysis. Nutrients. 2018 Mar 19. 10(3). 375.
- Sempos C.T., Binkley N. 25-Hydroxyvitamin D assay standardisation and vitamin D guidelines paralysis. Public Health Nutr. 2020 May. 23(7). 1153-1164. doi: 10.1017/S1368980019005251.
- Raina A.H., Allai M.S., Shah Z.A., Changal K.H., Raina M.A., Bhat F.A. Association of Low Levels of Vitamin D with Chronic Stable Angina: A Prospective Case-Control Study. N. Am. J. Med. Sci. 2016 Mar. 8(3). 143-50.
- Raslan E., Soliman S.S.A., Nour Z.A. et al. Association of Vitamin D Deficiency with Chronic Stable Angina: A Case Control Study. High Blood Press. Cardiovasc. Prev. 2019. 26. 77-80. doi: 10.1007/s40292-018-0295-7.
- Dziedzic E.A., Gąsior J.S., Pawłowski M., Wodejko-–Kucharska B., Saniewski T., Marcisz A., Dąbrowski M.J. Vitamin D level is associated with severity of coronary artery atherosclerosis and incidence of acute coronary syndromes in non-diabetic cardiac patients. Arch. Med. Sci. 2019 Mar. 15(2). 359-368. doi: 10.5114/aoms.2019.83291. Epub 2019 Mar 4. PMID: 30899288; PMCID: PMC6425216.
- Ismail H.M., Algrafi A.S., Amoudi O. et al. Vitamin D and Its Metabolites Deficiency in Acute Coronary Syndrome Patients Undergoing Coronary Angiography: A Case-Control Study. Vasc. Health Risk Manag. 2021. 17. 471-480. doi: 10.2147/VHRM.S312376.
- Khater W.A., Alfarkh M.A., Allnoubani A. The Association Between Vitamin D Level and Chest Pain, Anxiety, and Fatigue in Patients With Coronary Artery Disease. Clinical Nursing Research. 2023. 32(3). 639-647. doi: 10.1177/10547738221126325.
- Chen S., Law C.S., Grigsby C.L., Olsen K., Hong T.T., Zhang Y., Yeghiazarians Y., Gardner D.G. Cardiomyocyte-specific deletion of the vitamin D receptor gene results in cardiac hypertrophy. Circulation. 2011 Oct 25. 124(17). 1838-47. doi: 10.1161/CIRCULATIONAHA.111.032680. Epub 2011 Sep 26. PMID: 21947295; PMCID: PMC4160312.
- Walters M.R., Wicker D.C., Riggle P.C. 1,25-Dihydroxyvitamin D3 receptors identified in the rat heart. J. Mol. Cell Cardiol. 1986. 18. 67-72. doi: 10.1016/s0022-2828(86)80983-x.
- Tishkoff D.X., Nibbelink K.A., Holmberg K.H., Dandu L., Simpson R.U. Functional Vitamin D Receptor (VDR) in the T-Tubules of Cardiac Myocytes: VDR Knockout Cardiomyocyte Contractility. Endocrinology. 2008. 149. 558-564. doi: 10.1210/en.2007-0805.
- Wong M.S.K., Delansorne R., Man R.Y.K., Vanhoutte P.M. Vitamin D derivatives acutely reduce endothelium-dependent contractions in the aorta of the spontaneously hypertensive rat. Am. J. Physiol. Heart Circ. Physiol. 2008. 295. 289-296. doi: 10.1152/ajpheart.00116.2008.
- Pike J.W., Meyer M.B. The vitamin D receptor: New para–digms for the regulation of gene expression by 1,25-dihydroxyvitamin D(3). Endocrinol. Metab. Clin. N. Am. 2010. 39. 255-269. doi: 10.1016/j.ecl.2010.02.007.
- Merke J., Milde P., Lewicka S., Hügel U., Klaus G., Mangelsdorf D.J. et al. Identification and regulation of 1,25-dihydroxyvitamin D3 receptor activity and biosynthesis of 1,25-dihydroxyvitamin D3. Studies in cultured bovine aortic endothelial cells and human dermal capillaries. J. Clin. Invest. 1989 Jun. 83(6). 1903-15. doi: 10.1172/JCI114097. PMID: 2542376; PMCID: PMC303911.
- Somjen D., Weisman Y., Kohen F., Gayer B., Limor R., Sharon O. et al. 25-hydroxyvitamin D3-1alpha-hydroxylase is expressed in human vascular smooth muscle cells and is upregulated by parathyroid hormone and estrogenic compounds. Circulation. 2005 Apr 5. 111(13). 1666-71. doi: 10.1161/01.CIR.0000160353.27927.70. Epub 2005 Mar 28. PMID: 15795327.
- Li Y.C., Qiao G., Uskokovic M.., Xiang W., Zheng W., Kong J. Vitamin D: a negative endocrine regulator of the renin-angiotensin system and blood pressure. J. Steroid Biochem. Mol. Biol. 2004 May. 89–90 (1–5). 387-92. doi: 10.1016/j.jsbmb.2004.03.004. PMID: 15225806.
- McMullan C.J., Borgi L., Curhan G.C., Fisher N., Forman J.P. The effect of vitamin D on renin-angiotensin system activation and blood pressure: a randomized control trial. J. Hypertens. 2017 Apr. 35(4). 822-829. doi: 10.1097/HJH.0000000000001220.
- Pankiv I. Vitamin D: New Aspects of Application, Effective Doses. The Current State of the Problem. International Journal of Endocrinology (Ukraine). 2021. 17(1). 38-42. doi:10.22141/2224-0721.17.1.2021.226430.
- Pankiv V.I., Yuzvenko T.Yu., Pashkovska N.V., Pankiv I.V. The relationship between serum vitamin D concentrations and deve–lopment of diabetic retinopathy in type 2 diabetes mellitus. International Journal of Endocrinology (Ukraine). 2022. 18(8). 432-435. doi: 10.22141/2224-0721.18.8.2022.1221.
- Wahba N.S., Ghareib S.A., Abdel-Ghany R.H. et al. Renoprotective effects of vitamin D3 supplementation in a rat model of metabolic syndrome. Eur. J. Nutr. 2021. 60. 299-316. doi: 10.1007/s00394-020-02249-6.
- Song N., Yang S., Wang Y.Y. et al. The Impact of Vitamin D Receptor Gene Polymorphisms on the Susceptibility of Diabetic Vascular Complications: A Meta-Analysis. Genet. Test Mol. Biomarkers. 2019 Aug. 23(8). 533-556. doi: 10.1089/gtmb.2019.0037.
- Akhlaghi B., Firouzabadi N., Foroughinia F. et al. Impact of vitamin D receptor gene polymorphisms (TaqI and BsmI) on the incidence and severity of coronary artery disease: a report from southern Iran. BMC Cardiovasc. Disord. 2023. 23. 113. doi: 10.1186/s12872-023-03155-5.
- Yan X., Wei Y., Wang D., Zhao J., Zhu K., Liu Y. et al. Four common vitamin D receptor polymorphisms and coronary artery disease susceptibility: A trial sequential analysis. PLoS ONE. 2022. 17(10). e0275368. https://doi.org/10.1371/journal.pone.0275368.
- Ma L., Wang S., Chen H. et al. Diminished 25-OH vitamin D3 levels and vitamin D receptor variants are associated with susceptibility to type 2 diabetes with coronary artery diseases. J. Clin. Lab. Anal. 2020 Apr. 34(4). e23137. doi: 10.1002/jcla.23137.
- Kiani A., Mohamadi-Nori E., Vaisi-Raygani A. et al. Vitamin D-binding protein and vitamin D receptor genotypes and 25-hydroxyvitamin D levels are associated with development of aortic and mitral valve calcification and coronary artery diseases. Mol. Biol. Rep. 2019. 46. 5225–5236. doi: 10.1007/s11033-019-04979-1.
- Dawson-Hughes B., Wang J., Barger K., Ceglia L. Effects of Vitamin D with Calcium and Associations of Mean 25-Hydroxyvitamin D Levels with 3-Year Change in Muscle Performance in Healthy Older Adults in the Boston STOP IT Trial. Calcif. Tissue Int. 2022 Dec. 111(6). 580-586. doi: 10.1007/s00223-022-01024-5. Epub 2022 Sep 26. PMID: 36161344.