Международный эндокринологический журнал Том 19, №4, 2023
Вернуться к номеру
Значення катестатину в діагностиці серцево-судинних і метаболічних розладів у коморбідних пацієнтів з артеріальною гіпертензією
Авторы: Дунаєва І.П., Біловол О.М.
Харківський національний медичний університет, м. Харків, Україна
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
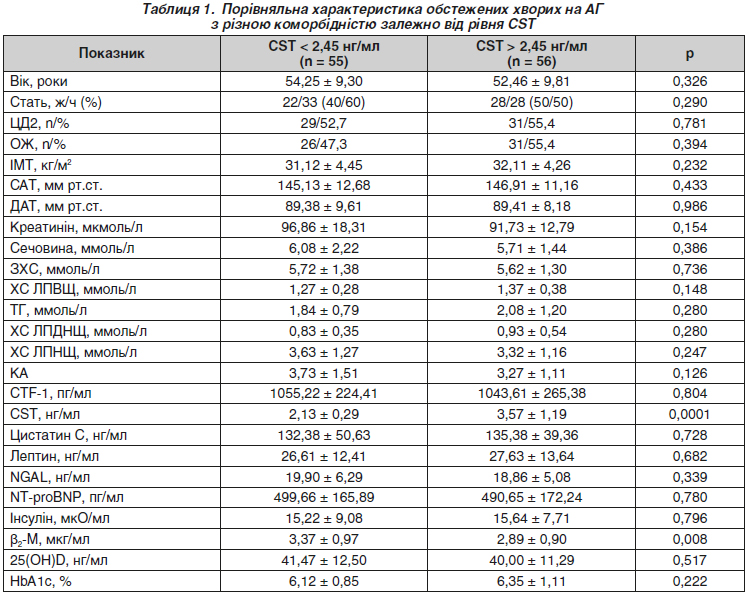
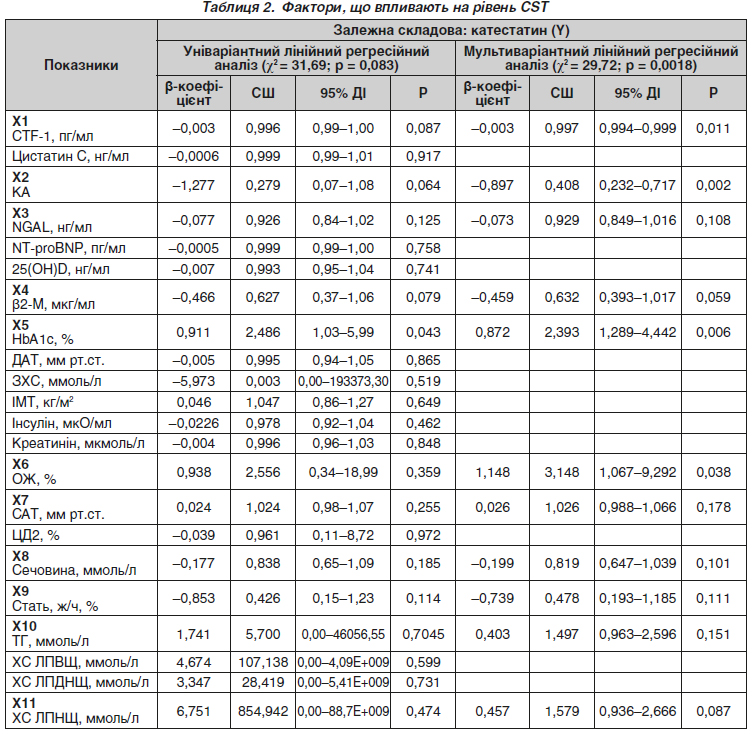
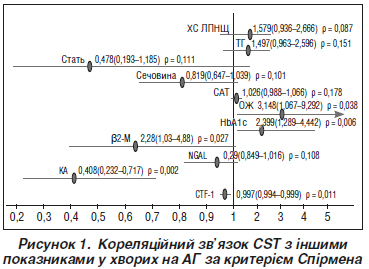
Актуальність. Артеріальна гіпертензія (АГ) є найбільшою пандемією в історії людства, яка визначає структуру серцево-судинної захворюваності й смертності. Очевидним є взаємозв’язок АГ з різними захворюваннями, які багато в чому визначають її прогресування і збільшують ризик розвитку кардіоваскулярних ускладнень. Важливу роль у прогресуванні цих ускладнень відіграють саме нейропептиди. На особливий науковий і практичний інтерес заслуговує катестатин (CST), який проявляє широкий спектр біологічних ефектів в організмі. Мета дослідження: визначення ролі CST у ранній діагностиці серцево-судинних і метаболічних ускладнень у коморбідних пацієнтів з артеріальною гіпертензією — представників української популяції. Матеріали та методи: обстежено 111 хворих на АГ, цукровий діабет 2-го типу (ЦД2), ожиріння (ОЖ) (чоловіків/жінок — 50/61) і 20 осіб контрольної групи. Усі хворі на АГ, ЦД2 і ОЖ були віком 54,37 ± 1,18 року. У процесі ретельного обстеження вони були розподілені на дві групи відносно медіани рівня CST, яка дорівнює 2,45 нг/мл. До першої групи увійшли 55 (49,5 %) пацієнтів, які мали рівень CST нижче за 2,45 нг/мл. До другої групи — 56 хворих (50,5 %), які мали рівень CST вище за 2,45 нг/мл. У всіх пацієнтів вимірювали масу тіла, зріст, розраховували індекс маси тіла (ІМТ), визначали рівні глікованого гемоглобіну (HbA1c), показники ліпідного обміну (концентрації в сироватці крові загального холестерину, тригліцеридів (ТГ), холестерину ліпопротеїнів високої щільності (ХС ЛПВЩ), холестерину ліпопротеїнів низької щільності, холестерину ліпопротеїнів дуже низької щільності); вимірювали рівень систолічного й діастолічного артеріального тиску. Визначали вміст CST, кардіотрофіну-1 (CTF-1), лептину, цистатину С, ліпокаліну, асоційованого з желатиназою нейтрофілів (NGAL), N-термінального мозкового натрійуретичного пептиду (NT-proBNP), 25(ОН)D, бета-2-мікроглобуліну (β2-М), рівень інсуліну в сироватці крові імуноферментним методом. Результати. Вірогідна різниця між групами виявлена за показником β2-М (p = 0,008). Після проведення уніваріантного і мультиваріантного лінійного регресійного аналізу встановлено негативний кореляційний зв’язок CST з CTF-1, NT-proBNP, NGAL, 25(OH)D. Позитивний кореляційний зв’язок CST встановлено з рівнем HbA1c, ІМТ, ТГ. Значущий кореляційний зв’язок за критерієм Спірмена CST встановлений в обстежених нами хворих на АГ з рівнем креатиніну (R = –0,21, p = 0,029), ХС ЛПВЩ (R = 0,207; p = 0,029), рівнем β2-М (R = 0,279; p = 0,0029). Висновки. Доведено, що зниження сироваткової концентрації катестатину є фактором ризику розвитку більш тяжкої коморбідної патології у хворих на АГ. Встановлені взаємозв’язки катестатину з креатиніном, сечовиною, β2-М дають підставу вважати, що CST є предиктором хронічної хвороби нирок у коморбідних хворих. Виявлений взаємозв’язок CST з ЛПВЩ, ОЖ, ІМТ, засвідчує його значення в профілактиці прогресування атеросклеротичних і метаболічних ускладнень у хворих на АГ, ЦД2, ОЖ.
Background. Hypertension is the major pandemic in human history, which determines the structure of cardiovascular morbidity and mortality. There is an obvious relationship between hypertension and various diseases that largely determine its development and increase the risk of cardiovascular complications. Neuropeptides appear to have a major impact on the progression of these complications. Catestatin (CST) is one of them, which deserves special scientific and practical concern, as it has a wide range of biological effects in the body. The aim of the study: to determine the place of CST in the early diagnosis of cardiovascular and metabolic complications in patients with comorbid hypertension among the Ukrainian population. Materials and methods. One hundred and eleven patients with hypertension, type 2 diabetes mellitus, obesity (men/women — 50/61) and 20 controls were examined. All patients with hypertension, type 2 diabetes mellitus, and obesity were aged 54.37 ± 1.18 years. Following a thorough examination and supervision, they were divided into 2 groups depending on the median CST level of 2.45 ng/ml. The first group included 55 (49.5 %) patients who had a CST level below 2.45 ng/ml, the second one consisted of 56 patients (50.5 %) who had a CST level above 2.45 ng/ml. In all patients, we measured body weight, height, calculated body mass index, evaluated glycated hemoglobin levels, lipid metabolism (serum concentrations of total cholesterol, triglycerides, high-density lipoprotein, low-density lipoprotein, and very low-density lipoprotein cholesterol); systolic and diastolic blood pressure. The content of CST, cardiotrophin 1, leptin, cystatin C, neutrophil gelatinase-associated lipocalin, N-terminal prohormone of brain natriuretic peptide, 25(OH)D, β2-microglobulin, and insulin levels in the blood serum were determined by enzyme-linked immunosorbent assay. Results. A reliable difference between the groups was found by β2-microglobulin (p = 0.008). Univariate and multivariate linear regression analysis revealed a negative correlation between CST and cardiotrophin 1, N-terminal prohormone of brain natriuretic peptide, neutrophil gelatinase-associated lipocalin, and 25(OH)D. A positive correlation was found between CST and the level of glycated hemoglobin, body mass index, and triglycerides. A statistically significant correlation was found between CST and creatinine (R = –0.21, p = 0.029), high-density lipoprotein cholesterol (R = 0.207, p = 0.029), and β2-microglobulin (R = 0.279, p = 0.0029) in the patients with hypertension. Conclusions. It has been proven that a decrease in serum catestatin concentration can be a risk factor for the development of more severe comorbidities in patients with hypertension. The detected relationships of catestatin with creatinine, urea, and β2-microglobulin suggest that CST is a predictor of chronic kidney disease in patients with comorbidities. The revealed correlation of CST with high-density lipoprotein, obesity, and body mass index suggests its importance in the prevention of atherosclerotic and metabolic complications in patients with hypertension, type 2 diabetes mellitus, and obesity.
артеріальна гіпертензія; цукровий діабет 2-го типу; ожиріння; катестатин; нейропептид
hypertension; type 2 diabetes mellitus; obesity; catestatin; neuropeptide
Вступ
Матеріали та методи
Результати
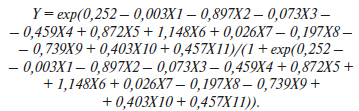
Обговорення
Висновки
- Pankova O. The potential of catestatin in the diagnostics of cardiovascular diseases: current data and perspectives. Shidnoevr. z. vnutr. simejnoi med. 2022. 2. 43-48 (in Ukrainian). doi: 10.15407/internalmed2022.02.043.
- Bourebaba Y., Mularczyk M., Marycz K., Bourebaba L. Catestatin peptide of chromogranin A as a potential new target for se–veral risk factors management in the course of metabolic syndrome. Biomed. Pharmacother. 2021 Feb. 134. 111-113. doi: 10.1016/j.biopha.2020.111113. Epub 2020 Dec 16. PMID: 33341043.
- Kumric M., Vrdoljak J., Dujic G., Supe-Domic D., Ticinovic Kurir T., Dujic Z., Bozic J. Serum Catestatin Levels Correlate with Ambulatory Blood Pressure and Indices of Arterial Stiffness in Patients with Primary Hypertension. Biomolecules. 2022 Aug 30. 12(9). 1204. doi: 10.3390/biom12091204. PMID: 36139043 Free PMC article.
- Bozic J., Kumric M., Ticinovic Kurir T., Urlic H., Martino–vic D., Vilovic M., Tomasovic Mrcela N., Borovac J.A. Catestatin as a Biomarker of Cardiovascular Diseases: A Clinical Perspective. Bio–medicines. 2021 Nov 25. 9(12). 1757. doi: 10.3390/biomedicines9121757. PMID: 34944578 Free PMC article. Review.
- Mahapatra N.R. Catestatin is a novel endogenous peptide that regulates cardiac function and blood pressure. Cardiovasc. Res. 2008 Dec 1. 80(3). 330-8. doi: 10.1093/cvr/cvn155. Epub 2008 Jun 9. PMID: 18541522 Review.
- Mahata S.K., Kiranmayi M., Mahapatra N.R. Catestatin: A Master Regulator of Cardiovascular Functions. Curr. Med. Chem. 2018. 25(11). 1352-1374. doi: 10.2174/0929867324666170425100416. PMID: 28443506 Review.
- Zhao Y., Zhu D. Potential applications of catestatin in cardiovascular diseases. Biomark Med. 2016 Aug. 10(8). 877-88. doi: 10.2217/bmm-2016-0086. Epub 2016 Jul 14. PMID: 27415768 Review.
- Mazza R., Tota B., Gattuso A. Cardio-vascular activity of catestatin: interlocking the puzzle pieces. Curr. Med. Chem. 2015. 22(3). 292-304. doi: 10.2174/0929867321666141106114928. PMID: 25386823 Review.
- Wu Z., Zhu D. The important role of catestatin in cardiac remodeling. Biomarkers. 2014 Dec. 19(8). 625-30. doi: 10.3109/1354750X.2014.950331. Epub 2014 Aug 19. PMID: 25136978 Review.
- Ying W., Mahata S., Bandyopadhyay G.K., Zhou Z., Wollam J., Vu J. et al. Catestatin Inhibits Obesity-Induced Macrophage Infiltration and Inflammation in the Liver and Suppresses Hepatic Glucose Production, Leading to Improved Insulin Sensitivity. Diabetes. 2018 May. 67(5). 841-848. doi: 10.2337/db17-0788.
- Retraction: Catestatin Increases the Expression of Anti-Apoptotic and Pro-Angiogenetic Factors in the Post-Ischemic Hypertrophied Heart of SHR. PLOS ONE Editors. PLoS One. 2021 Feb 4. 16(2). e0246900. doi: 10.1371/journal.pone.0246900. eCollection 2021. PMID: 33539473 Free PMC article.
- Bandyopadhyay G.K., Mahata S.K. Chromogranin A Regulation of Obesity and Peripheral Insulin Sensitivity. Front. Endocrinol. (Lausanne). 2017 Feb 8. 8. 20. doi: 10.3389/fendo.2017.00020. eCollection 2017. PMID: 28228748 Free PMC article. Review.
- Bandyopadhyay G., Tang K., Webster N.J.G., van den Bogaart G., Mahata S.K. Catestatin induces glycogenesis by stimulating the phosphoinositide 3-kinase-AKT pathway. Acta Physiol. (Oxf.). 2022 May. 235(1). e13775. doi: 10.1111/apha.13775. Epub 2022 Feb 4. PMID: 34985191.
- Zalewska E., Kmieć P., Sworczak K. Role of Catestatin in the Cardiovascular System and Metabolic Disorders. Front. Cardiovasc. Med. 2022 May 19. 9. 909480. doi: 10.3389/fcvm.2022.909480. eCollection 2022. PMID: 35665253 Free PMC article. Review.
- Kojima M., Ozawa N., Mori Y., Takahashi Y., Watanabe-Kominato K., Shirai R. et al. Catestatin Prevents Macrophage-Driven Atherosclerosis but Not Arterial Injury-Induced Neointimal Hyperplasia. Thromb. Haemost. 2018 Jan. 118(1). 182-194. doi: 10.1160/TH17-05-0349. Epub 2018 Jan 5. PMID: 29304538.
- O’Connor D.T., Kailasam M.T., Kennedy B.P., Zieg–ler M.G., Yanaihara N., Parmer R.J. Early decline in the catecho–lamine release-inhibitory peptide catestatin in humans at genetic risk of hypertension. J. Hypertens. 2002 Jul. 20(7). 1335-45. doi: 10.1097/00004872-200207000-00020. PMID: 12131530.
- Sahu B.S., Mohan J., Sahu G., Singh P.K., Sonawane P.J., Sasi B.K. et al. Molecular interactions of the physiological anti-hypertensive peptide catestatin with the neuronal nicotinic acetylcholine receptor. J. Cell. Sci. 2012 May 1. 125 (Pt 9). 2323-37. doi: 10.1242/jcs.103176. Epub 2012 Feb 22. Erratum in: J Cell Sci. 2012 Jun 1. 125(Pt 11). 2787. Obbineni, Jagan M [corrected to Mohan, Jagan]. PMID: 22357947.
- Sahu B.S., Obbineni J.M., Sahu G., Allu P.K., Subrama–nian L., Sonawane P.J. et al. Functional genetic variants of the catecholamine-release-inhibitory peptide catestatin in an Indian population: allele-specific effects on metabolic traits. J. Biol. Chem. 2012 Dec 21. 287(52). 43840-52. doi: 10.1074/jbc.M112.407916. Epub 2012 Oct 26. PMID: 23105094; PMCID: PMC3527967.
- Durakoğlugil M.E., Ayaz T., Kocaman S.A., Kırbaş A., Durakoğlugil T., Erdoğan T. et al. The relationship of plasma catestatin concentrations with metabolic and vascular parameters in untreated hypertensive patients: Influence on high-density lipoprotein cholesterol. Anatol. J. Cardiol. 2015 Jul. 15(7). 577-85. doi: 10.5152/akd.2014.5536. Epub 2014 Jul 17. PMID: 25538000; PMCID: PMC5337039.
- Bandyopadhyay G.K., Vu C.U., Gentile S., Lee H., Biswas N., Chi N.W., O’Connor D.T., Mahata S.K. Catestatin (chromogranin A(352-372)) and novel effects on mobilization of fat from adipose tissue through regulation of adrenergic and leptin signaling. J. Biol. Chem. 2012 Jun 29. 287(27). 23141-51. doi: 10.1074/jbc.M111.335877. Epub 2012 Apr 25. PMID: 22535963; PMCID: PMC3391131.
- Koval S.M., Yushko K.O., Snihurska I.O., Starchenko T.G., Pankiv V.I., Lytvynova O.M., Mysnychenko O.V. Relations of angiotensin-(1–7) with hemodynamic and cardiac structural and functional parameters in patients with hypertension and type 2 diabetes. Arterial Hypertension. 2019. 23(3). 183-189. DOI: 10.5603/AH.a2019.0012