Журнал «Медицина неотложных состояний» Том 21, №8, 2025
Вернуться к номеру
Автофагія і структурна перебудова органів за повного тривалого голодування
Авторы: Кузів О.Є., Франчук В.В., Слива А.Ф., Юрик І.І., Юрик Я.І.
Тернопільський національний медичний університет імені І.Я. Горбачевського, м. Тернопіль, Україна
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
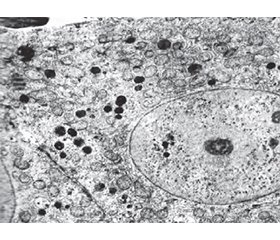
Актуальність. Автофагія є фундаментальним механізмом внутрішньоклітинної деградації і підтримки клітинного гомеостазу, особливо в умовах дефіциту поживних речовин. Голодування індукує автофагію, яка є ключовим компонентом адаптивної реакції клітин і тканин на депривацію. Дослідження впливу лікувального голодування на автофагію у здорових та хворих людей є актуальним напрямком сучасної біомедицини. Мета: виявити особливості впливу автофагії на субмікроскопічну активність нейтрофілів крові у пацієнтів з хронічними захворюваннями шлунково-кишкового тракту та структурну перебудову печінки в щурів у динаміці повного голодування. Матеріали та методи. Вивчена морфологія нейтрофільних гранулоцитів крові у 72 хворих, період повного голодування яких становив 21 добу. Забір венозної крові хворих здійснювали до початку голодування, на 7-му добу, 14-ту та 21-шу добу голодування і на 7-му добу відновленого харчування. Експериментальне дослідження проведене на 30 лабораторних щурах та 6 інтактних. Тварин із експерименту виводили через 1, 3 і 7 діб повного голоду та через 7 діб відновленого харчування. Ультрамікроскопічне дослідження зразків крові та печінки проводили згідно зі стандартною методикою. Результати. Встановлено, що відсутність макронутрієнтів ефективно індукує автофагію як у клітинах крові пацієнтів, так і в гепатоцитах щурів, ступінь вираженості якої залежав від терміну депривації. У перші 7 діб повного голоду в нейтрофілах крові хворих виявляли помірні ознаки активації автофагії — наростання лізосом, формування фагосом, а також появу клітин з ознаками помірно вираженої мембранної активності. Морфологічні ознаки інтенсифікації автофагії стають більш вираженими в клітинах на 14-ту — 21-шу добу повного голодування — гіперплазія лізосом, зростання вмісту фагосом, утворювались численні пальцеподібні та лопатоподібні вирости цитоплазми та формувались «контейнери» із лізосомами та глікогеном. На 7-му добу відновленого харчування структура нейтрофілів крові нормалізувалась, проте є багато клітин, цитоплазма яких густо насичена первинними та вторинними гранулами із максимально чітко контурованими мембранами ядер та органел. У щурів уже на ранніх етапах голодування (1-ша — 3-тя доба) спостерігається редукція гранулярного ретикулуму, зростання — агранулярного, поява дрібних ліпідних крапель, гіпертрофія комплексу Гольджі, численні лізосоми та автофагосоми. На 7-му добу повного голоду печінка зберігає часточкову будову, домінують регенераційні процеси в темних гепатоцитах із гіперплазією гранулярного ретикулуму і мітохондрій. На 7-й день відновленого харчування має місце повна реституція структури печінки з активацією клітин Купфера. Висновки. Лікувальне голодування індукує автофагію — ключовий механізм адаптації нейтрофільних гранулоцитів і гепатоцитів. Фагоцитарна активність нейтрофілів наростає до 21-го дня голодування і повертається до норми після рефідингу. В адаптивній перебудові печінки головними є активація автофагії, накопичення ліпідів та редукція гранулярного ендоплазматичного ретикулуму із подальшою реституцією структури печінки.
Background. Autophagy is a fundamental intracellular degradation mechanism that maintains cellular homeostasis, especially under nutrient deficiency. Fasting induces autophagy, serving as a key component of the adaptive response of cells and tissues to deprivation. Investigating the impact of therapeutic fasting on autophagy in both healthy and ill individuals is a relevant direction in modern biomedicine. Aim: to assess the role of autophagy in the submicroscopic activity of blood neutrophils in patients with chronic gastrointestinal diseases and to analyze structural liver remodeling in rats during complete fasting. Materials and methods. The morphology of neutrophilic granulocytes was studied in 72 patients undergoing a 21-day complete fasting protocol. Venous blood samples were collected before fasting, on days 7, 14, and 21 of fasting, and on day 7 of refeeding. An experimental study was conducted on 30 laboratory rats and 6 intact controls. Animals were sacrificed after 1, 3, and 7 days of fasting and 7 days of refeeding. Ultrastructural examination of blood and liver samples was performed using standard electron microscopy techniques. Results. Macronutrient deprivation effectively induced autophagy in both human neutrophils and rat hepatocytes, with intensity increasing according to fasting duration. In the first seven days of complete fasting, moderate autophagic activation was revealed with lysosomal proliferation, phagosome formation, and signs of membrane activity. By days 14–21, morphological signs of increased autophagy became more pronounced — lysosomal hyperplasia, phagosome accumulation, and formation of multiple cytoplasmic projections and vesicular “containers” with lysosomes and glycogen. By day 7 of refeeding, neutrophil structure largely normalized, though many cells exhibited cytoplasm rich in primary and secondary granules, with sharply delineated nuclear and organelle membranes. In rats, early fasting (days 1–3) was characterized by reduction of rough endoplasmic reticulum, expansion of smooth reticulum, appearance of lipid droplets, and Golgi hypertrophy, multiple lysosomes and autophagosomes. By day 7 of complete fasting, the liver preserved its lobular organization, regenerative processes dominated in dark hepatocytes with hyperplasia of rough endoplasmic reticulum and mitochondria. On day 7 of refeeding, full restitution of liver structure was observed, along with activation of Kupffer cells. Conclusions. Therapeutic fasting induces autophagy as a key adaptive mechanism in both neutrophilic granulocytes and hepatocytes. Neutrophil phagocytic activity progressively increases until day 21 of fasting and returns to baseline after refeeding. In the liver, adaptive remodeling involves autophagy activation, lipid accumulation, reduction of rough endoplasmic reticulum, and subsequent restitution of organ structure.
повне тривале голодування; автофагія; нейтрофільні гранулоцити; гепатоцити; електронна мікроскопія
prolonged complete fasting; autophagy; neutrophilic granulocytes; electron microscopy
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Klionsky DJ, Abdelmohsen K, Abe A, Abedin MJ, Abelio–vich H, Acevedo Arozena A, et al. Guidelines for the use and interpretation of assays for monitoring autophagy (3rd edition). Autophagy. 2016;12(1):1-222. doi: 10.1080/15548627.2015.1100356.
- Mizushima N, Komatsu M. Autophagy: renovation of cells and tissues. Cell. 2011;147(4):728-41. doi: 10.1016/j.cell.2011.10.026.
- Yang Z, Klionsky DJ. Eaten alive: a history of macroautophagy. Nat Cell Biol. 2010;12(9):814-22. doi: 10.1038/ncb0910-814.
- Ohsumi Y. Historical landmarks of autophagy research. Cell Res. 2014;24(1):9-23. doi: 10.1038/cr.2013.169.
- Liang XH, Jackson S, Seaman M, Brown K, Kempkes B, Hibshoosh H, Levine B. Induction of autophagy and inhibition of tumorigenesis by Beclin-1. Nature. 1999;402(6762):672-6. PMID: 10604474.
- Deretic V, Saitoh T, Akira S. Autophagy in infection, inflammation and immunity. Nat Rev Immunol. 2013;13(10):722-37. doi: 10.1038/nri3532.
- Deretic V, Levine B. Autophagy balances inflammation in innate immunity. Autophagy. 2018;14(2):243-51. doi: 10.1080/15548627.2017.1402992.
- Clarke AJ, Simon AK. Autophagy in the renewal, differentiation and homeostasis of immune cells. Nat Rev Immunol. 2019;19(3):170-83. doi: 10.1038/s41577-018-0095-2.
- Puleston DJ, Simon AK. Autophagy in the immune system: survival, differentiation and function of immune cells. Immunology. 2014;141(1):1-8. doi: 10.1111/imm.12165.
- Pua HH, Dzhagalov I, Chuck M, Mizushima N, He YW. A critical role for the autophagy gene Atg5 in T cell survival and proliferation. J Exp Med. 2007;204(1):25-31. doi: 10.1084/jem.20061303.
- Mortensen M, Soilleux EJ, Djordjevic G, Tripp R, Lutteropp M, Sadighi-Akha E, et al. The autophagy protein Atg7 is essential for hematopoietic stem cell maintenance. J Exp Med. 2011;208(3):455-67. doi: 10.1084/jem.20101145.
- Kirisako T, Baba M, Ishihara N, Miyazawa K, Ohsumi M, Yoshimori T, et al. Formation process of autophagosome is traced with Apg8/Aut7p in yeast. J Cell Biol. 1999;147(4):435-46. doi: 10.1083/jcb.147.2.435.
- Cuervo AM. Autophagy and aging: keeping that old broom working. Trends Genet. 2008;24(12):604-12. doi: 10.1016/j.tig.2008.09.001.
- Bagherniya M, Marofi F, Yekaninejad MS, Butler AE, Sahebkar A. The effect of fasting or calorie restriction on autophagy: a systematic review. Ageing Res Rev. 2018;47:123-34. doi: 10.1016/j.arr.2018.06.001.
- Madrigal-Matute J, Cuervo AM, Bhattacharya SK, Diaz-Meco MT, Diaz-Ruiz A, Fleming A, et al. Regulation of liver metabolism by autophagy. Gastroenterology. 2016;151(5):1064-78. doi: 10.1053/j.gastro.2016.08.005.