Международный эндокринологический журнал Том 21, №8, 2025
Вернуться к номеру
Оцінка перорального глюкозотолерантного тесту та індексованих параметрів вуглеводного метаболізму у пацієнтів з гострим коронарним та метаболічним синдромами і супутнім стеатозом печінки
Авторы: Комариця О.Й., Королюк О.Я., Радченко О.М., Боровець М.О., Стрільчук Л.М.
ДНП «Львівський національний медичний університет імені Данила Галицького», м. Львів, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
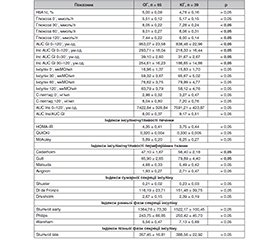
Актуальність. Пандемією сучасного світу вважаються метаболічні порушення та асоційована з ними жирова хвороба печінки, однак дотепер чітко не визначені зміни вуглеводного метаболізму на ранній її стадії — стадії метаболічно-асоційованого стеатозу печінки (МАСП). Мета: оцінити результати перорального глюкозотолерантного тесту та індексованих параметрів вуглеводного метаболізму у пацієнтів з гострим коронарним та метаболічним синдромами і супутнім МАСП. Матеріали та методи. До дослідження залучені 104 пацієнти з гострими формами ішемічної хвороби серця та метаболічним синдромом, які поділені на основну групу з супутнім МАСП (n = 65) та контрольну групу з інтактною печінкою (n = 39). Усім проведено пероральний глюкозотолерантний тест з визначенням рівнів глюкози (0´, 30´, 60´, 120´) та площ під кривою глюкози; визначено вміст інсуліну у динаміці (0´, 30´, 60´, 120´) та площу під кривою інсуліну; виміряно кількість С-пептиду у динаміці (0´, 120´); розраховано 14 індексів: HOMA-IR, QUICKI, McAuley, Cederholm, Gutt, Matsuda, Avignon, Shuster, DI deFronzо, Drivsholm, Stumvoll early, Philips, Wareham та Stumvoll late. Результати. Пацієнти з супутнім МАСП істотно відрізнялись від осіб з інтактною печінкою за істотно вищими значеннями рівнів глюкози на 30´, 60´, 120´, нижчими індексами периферійної інсуліночутливості тканин Cederholm і Gutt та вищими значеннями площ під кривою глюкози та наростаючих площ разом і ранньої та пізньої фаз глікемії. Індекси вуглеводного метаболізму корелювали з параметрами стану печінки, ліпідного метаболізму, швидкістю клубочкової фільтрації. Збільшення індексів інсулінорезистентності печінки та зменшення індексів інсуліночутливості периферійних тканин і сумарної секреції інсуліну супроводжувались ознаками дилатації порожнин шлуночків, гіпертрофії їх стінок та порушення систолічної й діастолічної функцій. Висновки. У пацієнтів із супутнім МАСП виявлені істотно гірші параметри вуглеводного метаболізму за пероральним глюкозотолерантним тестом й індексами інсуліночутливості та резистентності. Збільшення індексів інсулінорезистентності печінки та зменшення індексів інсуліночутливості периферійних тканин супроводжувались структурно-функціональними змінами серця.
Background. Metabolic dysfunction and associated fatty liver disease are a pandemic of the modern world. However, changes in carbohydrate metabolism in early stage of fatty liver disease — the stage of metabolically-associated liver steatosis (MALS) have not been clearly defined until now. The aim of the study was to evaluate the results of the oral glucose tolerance test and indexed parameters of carbohydrate metabolism in patients with acute coronary and metabolic syndromes and concomitant MALS. Materials and methods. The study included 104 patients with acute forms of coronary artery disease and metabolic syndrome. They were divided into two groups: the main one with concomitant MALS (n = 65) and the control group with an intact liver (n = 39). The oral glucose tolerance test was performed for everyone with the determination of glucose levels (0´, 30´, 60´, 120´) and areas under the glucose curve. The insulin content in the dynamics (0´, 30´, 60´, 120´) and the area under the insulin curve were determined. Also, the amount of C-peptide in the dynamics was measured (0´,120´). Then we calculated 14 indices of carbohydrate metabolism: HOMA-IR, QUICKI, McAuley, Cederholm, Gutt, Matsuda, Avignon, Shuster, DeFronzо, Drivsholm, Stumvoll early, Philips, Wareham and Stumvoll late. Results. Patients with concomitant MALS differed significantly from individuals with an intact liver by reliably higher values of glucose levels at 30´, 60´, 120´, lower Cederholm and Gutt indices of peripheral insulin sensitivity of tissues, and higher values of the area under the glucose curve and the increasing areas together, both early and late phases of glycemia. Indices of carbohydrate metabolism correlated with parameters of liver functional tests, lipid metabolism, glomerular filtration rate. An increase in the indices of liver insulin resistance and a decrease in the insulin sensitivity indices of peripheral tissues and total secretion of insulin were accompanied by signs of dilatation of ventricular cavities, hypertrophy of their walls, and impaired systolic and diastolic functions. Conclusions. Patients with concomitant MALS had significantly worse parameters of carbohydrate metabolism according to the oral glucose tolerance test and the indices of insulin sensitivity and resistance. An increase in the indices of liver insulin resistance and a decrease in the insulin sensitivity indices of peripheral tissues were accompanied by structural and functional changes in the heart.
метаболічно‑асоційована жирова хвороба печінки, пероральний глюкозотолерантний тест, індекси інсуліночутливості, індекс Cederholm, індекс Gutt
metabolic dysfunction-associated fatty liver disease; oral glucose tolerance test; insulin sensitivity indices; Cederholm index; Gutt index
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Boccatonda A, Andreetto L, D’Ardes D, Cocco G, Rossi I, Vicari S, et al. From NAFLD to MAFLD: Definition, Pathophysiological Basis and Cardiovascular Implications. Biomedicines. 2023 Mar 13;11(3):883. doi: 10.3390/biomedicines11030883. PMID: 36979861; PMCID: PMC10046146.
- Habibullah M, Jemmieh K, Ouda A, Haider MZ, Malki MI, Elzouki AN. Metabolic-associated fatty liver disease: a selective review of pathogenesis, diagnostic approaches, and therapeutic strategies. Front Med (Lausanne). 2024 Jan 23;11:1291501. doi: 10.3389/fmed.2024.1291501. PMID: 38323033; PMCID: PMC10845138.
- Bhat N, Mani A. Dysregulation of Lipid and Glucose Metabolism in Nonalcoholic Fatty Liver Disease. Nutrients. 2023 May 16;15(10):2323. doi: 10.3390/nu15102323. PMID: 37242206; PMCID: PMC10222271.
- Komarytsia О, Radchenko О, Borovets М, Strilchuk L, Stadnik S. Changes in the cytokine profile in patients with a combination of type 2 diabetes mellitus, hypertension, coronary heart disease and hepatic steatosis under conditions of obesity. Rom J Diabetes Nutr Metab Dis. 2023;30(4):460-465. https://doi.org/10.46389/rjd-2023-1373.
- Uehara K, Santoleri D, Whitlock AEG, Titchenell PM. Insulin Regulation of Hepatic Lipid Homeostasis. Compr Physiol. 2023 Jun 26;13(3):4785-4809. doi: 10.1002/cphy.c220015. PMID: 37358513; PMCID: PMC10760932.
- Semova I, Biddinger SB. Triglycerides in Nonalcoholic Fatty Liver Disease: Guilty Until Proven Innocent. Trends Pharmacol Sci. 2021 Mar;42(3):183-190. doi: 10.1016/j.tips.2020.12.001. Epub 2021 Jan 16. PMID: 33468321; PMCID: PMC10065162.
- Albareda M, Rodríguez-Espinosa J, Murugo M, de Leiva A, Corcoy R. Assessment of insulin sensitivity and beta-cell function from measurements in the fasting state and during an oral glucose tolerance test. Diabetologia. 2000 Dec;43(12):1507-11. doi: 10.1007/s001250051561. PMID: 11151759.
- Maldonado-Rojas ADC, Zuarth-Vázquez JM, Uribe M, Barbero-Becerra VJ. Insulin resistance and Metabolic dysfunction-associated steatotic liver disease (MASLD): Pathways of action of hypoglycemic agents. Ann Hepatol. 2024 Mar-Apr;29(2):101182. doi: 10.1016/j.aohep.2023.101182. Epub 2023 Dec 1. PMID: 38042482.
- Yanai H, Adachi H, Hakoshima M, Iida S, Katsuyama H. Metabolic-Dysfunction-Associated Steatotic Liver Disease-Its Pathophysiology, Association with Atherosclerosis and Cardiovascular Di–sease, and Treatments. Int J Mol Sci. 2023 Oct 23;24(20):15473. doi: 10.3390/ijms242015473. PMID: 37895151; PMCID: PMC10607514.
- Grandt J, Jensen AH, Werge MP, Rashu EB, Møller A, Jun–ker AE, et al. Postprandial dysfunction in fatty liver disease. Phy–siol Rep. 2023 Apr;11(8):e15653. doi: 10.14814/phy2.15653. PMID: 37078380; PMCID: PMC10116394.
- Lee J, van Es N, Takada T, Klok FA, Geersing GJ, Blume J, Bossuyt PM; IPD study team. Covariate-specific ROC curve analysis can accommodate differences between covariate subgroups in the eva–luation of diagnostic accuracy. J Clin Epidemiol. 2023 Aug;160:14-23. doi: 10.1016/j.jclinepi.2023.06.001. Epub 2023 Jun 8. PMID: 37295733.
- Lee SH, Park SY, Choi CS. Insulin Resistance: From Mechanisms to Therapeutic Strategies. Diabetes Metab J. 2022 Jan;46(1):15-37. doi: 10.4093/dmj.2021.0280. Epub 2021 Dec 30. PMID: 34965646; PMCID: PMC8831809.
- Sakurai Y, Kubota N, Yamauchi T, Kadowaki T. Role of Insulin Resistance in MAFLD. Int J Mol Sci. 2021 Apr 16;22(8):4156. doi: 10.3390/ijms22084156. PMID: 33923817; PMCID: PMC8072900.
- Heeren J, Scheja L. Metabolic-associated fatty liver disease and lipoprotein metabolism. Mol Metab. 2021 Aug;50:101238. doi: 10.1016/j.molmet.2021.101238. Epub 2021 Apr 20. PMID: 33892169; PMCID: PMC8324684.
- Paquin J, St-Martin P, Lord SÈ, Gendron P, Brochu M, Dionne IJ. Acute Glucose Tolerance in Response to Lower- and Hig–her-Load Resistance Exercise in Postmenopausal Women: Contribution of Aerobic Capacity and Body Composition. J Strength Cond Res. 2025 Jun 1;39(6):e749-e757. doi: 10.1519/JSC.0000000000005096. PMID: 40403187.
- Gutch M, Kumar S, Razi SM, Gupta KK, Gupta A. Assessment of insulin sensitivity/resistance. Indian J Endocrinol Metab. 2015 Jan-Feb;19(1):160-4. doi: 10.4103/2230-8210.146874. PMID: 25593845; PMCID: PMC4287763.
- Long XX, Liu D, Wu L, Qian LL, Fang QC, Li HT, Jia WP. [Correlation between intrahepatic triglyceride content quantified by proton magnetic resonance spectroscopy and glucose metabolism]. Zhonghua Nei Ke Za Zhi. 2021 Dec 1;60(12):1157-1164. Chinese. doi: 10.3760/cma.j.cn112138-20210308-00191. PMID: 34856688.
- Huang H, Zheng X, Wen X, Zhong J, Zhou Y, Xu L. Visceral fat correlates with insulin secretion and sensitivity independent of BMI and subcutaneous fat in Chinese with type 2 diabetes. Front Endocrinol (Lausanne). 2023 Feb 27;14:1144834. doi: 10.3389/fendo.2023.1144834. PMID: 36909323; PMCID: PMC9999013.
- Erqou S, Adler AI, Challa AA, Fonarow GC, Echouffo-Tcheugui JB. Insulin resistance and incident heart failure: a meta-analysis. Eur J Heart Fail. 2022 Jun;24(6):1139-1141. doi: 10.1002/ejhf.2531. Epub 2022 May 16. PMID: 35502564; PMCID: PMC9262840.
- Bjelakovic L, Vukovic V, Stankovic S, Ciric M, Lukic S, Bra–tic M, et al. Insulin resistance surrogates and left ventricular hypertrophy in normotensive obese children. Cardiol Young. 2021 Dec;31(12):1901-1906. doi: 10.1017/S1047951121001049. Epub 2021 Mar 22. PMID: 33745468.
- Serhiyenkо V, Chemerys O, Pankiv V, Serhiyenko A. Type 2 Diabetes Mellitus, Cerebral Small Vessel Disease and Depressive Disorders. International Neurological Journal. 2025;21(3):226-37. doi: 10.22141/2224-0713.21.3.2025.1178.
- Zhai Y, Fu H, Li Y, Li S, Zhang W, Yue J, Wang Z. Relationship between four insulin resistance surrogates and left ventricular hypertrophy among hypertensive adults: a case-control study. Endocr Connect. 2024 Mar 18;13(4):e230476. doi: 10.1530/EC-23-0476. PMID: 38300820; PMCID: PMC10959039.