Международный эндокринологический журнал Том 21, №8, 2025
Вернуться к номеру
Морфометрична оцінка ядер тиреоцитів при вузловому колоїдному зобі, фолікулярній аденомі, хворобі Грейвса та автоімунному тиреоїдиті в пацієнтів Полтавського регіону
Авторы: O.M. Liulka, M.I. Kravtsiv, V.I. Lyakhovskyi, O.G. Krasnov, T.V. Horodova-Andrieieva, N.V. Boruta, M.V. Rud, Y.V. Stetsuk
Poltava State Medical University, Poltava, Ukraine
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
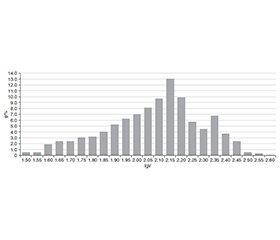
Актуальність. На сьогодні найбільш поширеним, доступним та інформативним методом диференціальної діагностики вузлових уражень щитоподібної залози (ЩЗ) вважається тонкоголкова аспіраційна пункційна біопсія (ТАПБ) із подальшим цитологічним дослідженням пунктату. Основними критеріями морфологічної диференціальної діагностики є капсулярні та ядерні ознаки. Найменш вивчені ядерні ознаки злоякісності і доброякісності процесу, а каріометрія тиреоцитів для цих цілей не застосовується достатньо широко. Мета: встановити особливості цитологічної картини ядер тиреоцитів (каріовакометрії) та можливості її використання для диференціальної діагностики вузлових утворень у ЩЗ із подальшим удосконаленням передопераційної діагностики й визначення показань до оперативного втручання. Матеріали та методи. Обстежено 40 пацієнтів із гістологічно встановленим діагнозом вогнищевих утворень у залозі: 10 хворих на вузловий колоїдний зоб (1-ша група), 10 — на фолікулярну аденому (2-га група), 10 — на автоімунний тиреоїдит (3-тя група) та 10 осіб із хворобою Грейвса (4-та група). Морфометричні дослідження ядер фолікулярного епітелію проводили на основі цитологічних препаратів, отриманих шляхом ТАПБ. Для вивчення гістологічних структур та мікрофотозйомки з морфометрією клітин використовували мікроскоп KONUS Biorex-3. Він був оснащений цифровою камерою DCM 900 та адаптованим до неї програмним забезпеченням. Для морфометричного дослідження використовували програму AimImageExaminer. Результати. Вивчено каріометричні показники пацієнтів із вузловим колоїдним зобом, фолікулярною аденомою, автоімунним тиреоїдитом, хворобою Грейвса порівняно зі здоровими особами. Оцінювали кількість ядерцевих організаторів, їх ексцентричність, розраховували десятинні логарифми об’єму ядер тиреоцитів. Для кожного частотного розподілу визначали коефіцієнт надлишковості R. Висновки. Ідентифіковано три діапазони рівня організації розподілу цитології ядер тиреоцитів за коефіцієнтом R у нормі, при вузловому колоїдному зобі, фолікулярній аденомі, хворобі Грейвса та автоімунному тиреоїдиті: імовірний, квазідетермінований та жорсткодетермінований. Жорсткодетермінований (R > 0,3): здорова залоза, фолікулярна аденома. Це вказує на більш стабільний, чітко організований розподіл ядер клітин. Квазідетермінований тип характерний (R ≤ 0,3) для вузлового колоїдного зоба, хвороби Грейвса та автоімунного тиреоїдиту.
Background. The most common, accessible and informative method of differential diagnosis for nodular thyroid gland lesions is currently fine-needle aspiration biopsy, followed by cytological examination of the puncture. The main morphological differential diagnostic criteria are capsular and nuclear features. Nuclear markers of malignancy and benignity are the least studied, and thyroid karyometry is not widely used for these purposes. The objective of the study was to determine the characteristics of the cytological picture of thyrocytes (karyovacometry) and the possibility of its use for the differential diagnosis of nodular formations in the thyroid gland with subsequent improvement of preoperative diagnosis and determination of indications for surgical intervention. Materials and methods. Forty patients with histologically confirmed diagnosis of focal lesions in the gland were examined: 10 with nodular colloid goitre (NCG; group 1), 10 with follicular adenoma (FA; group 2), 10 with autoimmune thyroiditis (AIT; group 3) and 10 with diffuse toxic goitre (DTG; group 4). Morphometric studies of follicular epithelial nuclei were performed on the basis of cytological preparations obtained by fine-needle aspiration biopsy. A KONUS Biorex-3 microscope was used to study histological structures and perform microphotography with cell morphometry. The microscope was equipped with a DCM 900 digital camera and adapted software. The AimImageExaminer programme was chosen for the morphometric study. Results. We examined the karyometric parameters of patients with nodular colloid goitre, follicular adenoma, autoimmune thyroiditis and diffuse toxic goitre, comparing them with healthy glands. Also, the number of nucleolar organisers and their eccentricity was assessed, and the decimal logarithms of thyrocyte volume was calculated. For each frequency distribution, we determined the redundancy coefficient R. Conclusions. Three ranges of the level of organisation of thyrocytes’ nuclei distribution by the R coefficient have been determined for normal thyroid, NCG, FA, DTG and AIT: probable, quasi-determined and strictly determined. Strictly determined (R > 0.3): healthy gland, FA. This indicates a more stable, clearly organised distribution of cell nuclei. Quasi-determined is characteristic (R ≤ 0.3) for NCG, DTG and AIT.
щитоподібна залоза; вузловий колоїдний зоб; фолікулярна аденома; автоімунний тиреоїдит; хвороба Грейвса; тиреоцит; морфометрія; ядро; lgV; десятинний логарифм об’єму ядер
thyroid gland; nodular colloid goitre; follicular adenoma; autoimmune thyroiditis; Graves’ disease; thyrocyte; morphometry; nucleus; lgV; decimal logarithm of nuclear volume
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Capozzi A, Jansen FA, Smetsers SE, Bakhuizen JJ, Hiemcke-Jiwa LS, et al. The Histological Spectrum of DICER1-Associated Neoplasms. Pediatr Dev Pathol. 2025 Jul-Aug;28(4):231-243. doi: 10.1177/10935266251329752.
- Boiko DI, Shyrai PO, Mats OV, Karpik ZI, Rahman MH, Khan AA, et al. Mental health and sleep disturbances among Ukrainian refugees in the context of Russian-Ukrainian war: A preliminary result from online-survey. Sleep Med. 2024;113:342-348. doi: 10.1016/j.sleep.2023.12.004.
- Haque U, Bukhari MH, Fiedler N, Wang S, Korzh O, Espinoza J, et al. A comparison of Ukrainian hospital services and functions before and during the Russia-Ukraine war. JAMA Health Forum. 2024;5(5):e240901. doi: 10.1001/jamahealthforum.2024.0901.
- Abilash SC, Devi SSL, Pammy S. Efficacy of Follicular Cell Pattern Analysis in Thyroid Fine-Needle Aspiration Cytology Evaluation. Ann Afr Med. 2024 Oct 1;23(4):623-627. doi: 10.4103/aam.aam_67_24.
- Tsuber V, Kadamov Y, Brautigam L, Berglund UW, Helleday T. Mutations in cancer cause gain of cysteine, histidine, and tryptophan at the expense of a net loss of arginine on the proteome level. Biomolecules. 2017;7(3):49. doi: 10.3390/biom7030049.
- Chambers M, Sadow PM, Kerr DA. Squamous Differentiation in the Thyroid: Metaplasia, Neoplasia, or Bystander? Int J Surg Pathol. 2022 Jun;30(4):385-392. doi: 10.1177/10668969211065126.
- Abdelhakam DA, Mojica RE, Huenerberg KA, Nassar A. Impact of a genomic classifier on indeterminate thyroid nodules: an institutional experience. J Am Soc Cytopathol. 2021 Mar-Apr;10(2):155-163. doi: 10.1016/j.jasc.2020.09.005.
- Asya O, Yumuşakhuylu AC, Enver N, Gündoğdu Y, Abuzaid G, et al. A single-center multidisciplinary study analyzing thyroid nodule risk stratification by comparing the thyroid imaging reporting and data system (TI-RADS) and American thyroid association (ATA) risk of malignancy for thyroid nodules. Auris Nasus Larynx. 2023 Jun;50(3):410-414. doi: 10.1016/j.anl.2022.08.006.
- Chmurska M, Galuszka A, Pawlicki P, Zarzycka M, Sechman A, et al. Effect of indoxyl sulfate on the morphology and function of the thyroid gland — ex vivo studies in rabbits. J Physiol Pharmacol. 2023 Dec;74(6). doi: 10.26402/jpp.2023.6.10.
- Chen Y, Lian Z, Zhang G, Lin Y, Zhang G, et al. CircRNA ITCH Inhibits Epithelial-Mesenchymal Transformation and Promotes Apoptosis in Papillary Thyroid Carcinoma via miR-106a-5p/JAZF1 Axis. Biochem Genet. 2024 Dec;62(6):4755-4769. doi: 10.1007/s10528-024-10672-1.
- Ahn HS, Kim HS, Hong MJ. Ultrasonographic and cytologic assessments of follicular neoplasms of the thyroid: Predictive features differentiating follicular carcinoma from follicular adenoma. PLoS One. 2022 Jul 21;17(7):e0271437. doi: 10.1371/journal.pone.0271437.
- Doghish AS, El-Mahdy HA, Ismail A, Hegazy M, Mokh–tar MM, et al. Significance of miRNAs on the thyroid cancer progression and resistance to treatment with special attention to the role of cross-talk between signaling pathways. Pathol Res Pract. 2023 Mar;243:154371. doi: 10.1016/j.prp.2023.154371.
- Hayakawa M, Taylor JN, Nakao R, Mochizuki K, Sawai Y, et al. Lipid droplet accumulation and adipophilin expression in follicular thyroid carcinoma. Biochem Biophys Res Commun. 2023 Jan 15;640:192-201. doi: 10.1016/j.bbrc.2022.12.007.
- El Hag IA, Al-Subaie S, Asiri SM, Alotaibi FZ, Alabashi SM, et al. What Is a Significant Nuclear Groove in Thyroid Fine Needle Aspiration Cytology? Diagn Cytopathol. 2025 Sep;53(9):437-446. doi: 10.1002/dc.25491.
- Rojo-Pardillo M, Godefroid L, Dom G, Lefort A, Libert F, et al. Understanding the Dosage-Dependent Role of Dicer1 in Thyroid Tumorige–nesis. Int J Mol Sci. 2024 Oct 4;25(19):10701. doi: 10.3390/ijms251910701.
- Lebrun L, Salmon I. Pathology and new insights in thyroid neoplasms in the 2022 WHO classification. Curr Opin Oncol. 2024 Jan 1;36(1):13-21. doi: 10.1097/CCO.0000000000001012.
- Hsiao WY, Saba NF, Lubin D, Chen A, Shi Q. Risk stratification of ThyroSeq results in indeterminate thyroid lesions: A single-institution experience of clinicopathologic correlation with cytologic findings. Cancer Cytopathol. 2025 Jan;133(1):e22905. doi: 10.1002/cncy.22905.
- Huang CY, Xie RH, Li PH, Chen CY, You BH, et al. Environmental Exposure to Bisphenol A Enhances Invasiveness in Papillary Thyroid Cancer. Int J Mol Sci. 2025 Jan 19;26(2):814. doi: 10.3390/ijms26020814.
- Huang H, Li L, Liu X, Zhao L, Cui Z, et al. Papillary thyroid carcinoma with desmoid-type fibromatosis: the clinicopathological features with characteristic imaging and molecular correlation requiring comprehensive treatment. Hum Pathol. 2023 Jun;136:84-95. doi: 10.1016/j.humpath.2023.03.019.
- Rogers E, Breathwaite EK, Nguyen-Jones T, Anderson SM, Odanga JJ, et al. Characterization of a human thyroid microtissue model for testing thyroid disrupting chemicals. Front Toxicol. 2024 Jul 24;6:1408808. doi: 10.3389/ftox.2024.1408808.
- Bahriy MM, Dibrova VA, Popadynets OH, Hryshchuk MI. Methods of morphological research: monograph. Vinnytsya: Nova knyha; 2016 (in Ukrainian).
- Norimatsu Y, Irino S, Maeda Y, Yanoh K, Kurokawa T, et al. Nuclear morphometry as an adjunct to cytopathologic examination of endometrial brushings on LBC samples: A prospective approach to combined evaluation in endometrial neoplasms and look alikes. Cytopathology. 2021 Jan;32(1):65-74. doi: 10.1111/cyt.12902.
- Saini T, Kundu R, Rohilla M, Gupta P, Gupta N, et al. Gray zone Bethesda category III — atypia of undetermined significance lesions of the thyroid: Potential diagnostic issues and image morphometry as a useful adjunct to cytomorphology. Cytojournal. 2024 Oct 17;21:38. doi: 10.25259/Cytojournal_86_2023.
- Yu HW, Park E, Lee JK, Kim W, Kong JH, et al. Analyzing circulating tumor cells and epithelial-mesenchymal transition status of papillary thyroid carcinoma patients following thyroidectomy: a prospective cohort study. Int J Surg. 2024 Jun 1;110(6):3357-3364. doi: 10.1097/JS9.0000000000001284.
- Pérez-Fernández B, Vázquez-Román V, Fernández-Santos JM, Martín-Lacave I. Characterization of primary cilia in different epithelial cells of thyroid gland. Histochem Cell Biol. 2024 Nov 18;163(1):4. doi: 10.1007/s00418-024-02328-3.
- Lametti A, Brimo F, Kanber Y, Caglar D, Auger M. Cytopathology of follicular and oncocytic follicular thyroid neoplasms: A Bethesda System perspective. Cancer Cytopathol. 2025 May;133(5):e70016. doi: 10.1002/cncy.70016.
- Schwock J, Starova B, Khan ZF, Mirkovic J, Parra-Herran C, et al. Cytomorphologic Features of Gastric-Type Endocervical Adenocarcinoma in Liquid-Based Preparations. Acta Cytol. 2021;65(1):56-66. doi: 10.1159/000511003.
- Chen W, Song YS, Lee HS, Lin CW, Lee J, et al. Estrogen-related receptor alpha promotes thyroid tumor cell survival via a tumor subtype-specific regulation of target gene networks. Oncogene. 2024 Jul;43(31):2431-2446. doi: 10.1038/s41388-024-03078-1.