Журнал «Здоровье ребенка» Том 20, №8, 2025
Вернуться к номеру
Сучасні стратегії збереження здоров’я кісток у дітей і підлітків: що повинен знати лікар?
Авторы: Бекетова Г.В. (1), Бабій А.Е. (2)
(1) - Національний університет охорони здоров’я України імені П.Л. Шупика, м. Київ, Україна
(2) - ТОВ «Здраво», м. Київ, Україна
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
Актуальність. Здоров’я кісток — це детермінований генетичними, екологічними, гормональними, харчовими і механічними впливами стан кісткової тканини, що забезпечує її стійкість до переломів, є основою для ефективної реалізації позаскелетної та механічної функцій скелета, важливою складовою гармонійного розвитку дітей і підлітків та їхнього загального фізичного благополуччя протягом усього життя. Мета: здійснити огляд наукових досліджень щодо впливу мікронутрієнтів і фізичної активності на мінеральну щільність кісткової тканини в дітей і підлітків і визначити стратегії профілактики порушень здоров’я кісток. Матеріали та методи. Огляд літературних джерел базувався на аналізі результатів наукових досліджень, що опубліковані у відкритому доступі, з використанням інформаційно-пошукових систем PubMed, Web of Science, Scopus, Google Scholar і ResearchGate. Розглянутo 109 наукових робіт, переважно за останні 5 років, відповідно до обраної теми й мети дослідження. Результати. Дані проведеного огляду літератури свідчать, що здоров’я кісток залежить від низки факторів. Серед керованих факторів важлива роль належить дотриманню здорового способу життя, зокрема достатній фізичній активності, відсутності шкідливих звичок та оптимальному харчуванню, збалансованому передусім за такими есенціальними мікронутрієнтами, як кальцій і вітаміни D та К. Недостатнє споживання кальцію та вітаміну D у дитячому й особливо підлітковому віці (критичний період для росту і розвитку кісток) супроводжується зниженням ефективності формування кісткової тканини й досягнення оптимального піку її мінеральної щільності, що підвищує ризик розвитку низки хронічних захворювань, остеопорозу й переломів кісток у дорослих. Висновки. Для запобігання порушенням здоров’я кісток і зменшення глобального впливу захворювань, пов’язаних з ними, розроблені сучасні стратегії, що включають освітньо-інформаційні технології, програми збагачення основних продуктів есенціальними мікронутрієнтами, зміни способу життя, раннє виявлення, своєчасне втручання і моніторинг дефіциту кальцію й вітаміну D, створення відповідних цифрових інструментів охорони здоров’я і персоналізованих підходів до харчування.
Background. Bone health is the condition of bone tissue determined by genetic, environmental, hormonal, nutritional and mechanical influences, which ensures its resistance to fractures; it is the basis of the effective implementation of extraskeletal and mechanical functions of the skeleton, an important component of the harmonious development of children and adolescents and their overall physical well-being throughout life. The purpose was to review scientific research on the effects of micronutrients and physical activity on bone mineral density in children and adolescents and identify strategies for preventing bone health disorders. Materials and methods. The literature review was based on the analysis of the results of scientific research published in the open access using the information search systems PubMed, Web of Science, Scopus, Google Scholar and ResearchGate. One hundred and nine scientific papers published mostly in the last 5 years were reviewed in accordance with the chosen topic and research objective. Results. The literature review suggests that bone health depends on a number of factors. Among the controllable factors, an important role belongs to maintaining a healthy lifestyle, in particular, sufficient physical activity, the absence of bad habits, optimal nutrition, balanced primarily in terms of essential micronutrients such as calcium and vitamin D and К. Insufficient calcium and vitamin D intake in childhood and, especially, in adolescence (a critical period for bone growth and development) is accompanied by a decrease in the efficiency of bone mineral density formation and reaching its optimal peak, which increases the risk of developing a number of chronic diseases, osteoporosis, and bone fractures in adults. Conclusions. To prevent bone health disorders and reduce the global impact of diseases related to them, modern strategies have been developed, including educational and information technologies, programs to enrich staple foods with essential micronutrients, lifestyle changes, early detection, timely intervention and monitoring of calcium and vitamin D and К deficiency, creation of appropriate digital health tools and personalized approaches to nutrition.
здоров’я кісток; мінеральна щільність; здоровий спосіб життя; діти; підлітки; кальцій; вітамін D; вітамін К; харчування; фізична активність; ожиріння; ІНОС® (К2+D3+Са)
bone health; mineral density; healthy lifestyle; children; adolescents; calcium; vitamin D; vitamin К; nutrition; physical activity; obesity; INOS® (К2+D3+Са)
Вступ
Матеріали та методи
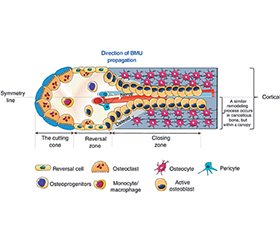
Результати
/15.jpg)
Висновки
- Baronio F, Baptista F. Editorial: Bone health and development in children and adolescents. Front Endocrinol (Lausanne). 2022 Dec 12;13:1101403. doi: 10.3389/fendo.2022.1101403. PMID: 36578952; PMCID: PMC9791941.
- Tabaie SA, O’Mara AE, Sheppard ED, Tosi LL. A Comprehensive Review of Bone Health in a Child: From Birth to Adulthood. J Am Acad Orthop Surg. 2024 May 1;32(9):363-372. doi: 10.5435/JAAOS-D-23-00853. Epub 2024 Jan 23. PMID: 38261781.
- Zhang Y, Wang X, Huo S, Hong L, Li F. The association between dietary inflammatory index and bone health in US adolescents: Analysis of the NHANES data. Bone Rep. 2025 Jan 3;24:101823. doi: 10.1016/j.bonr.2024.101823. PMID: 39866531; PMCID: PMC11758120.
- Beketova G, Savinova K, Mozgova G, Beketova N. A healthy lifestyle is the base of maintaining the health of schoolchildren. Сhild`s health. 2022;16(8):509-514. DOI: 10.22141/2224-0551.16.8.2021.248705.
- Liu X, Wu Y, Bennett S, Zou J, Xu J, Zhang L. The Effects of Diffe–rent Dietary Patterns on Bone Health. Nutrients. 2024 Jul 17;16(14):2289. doi: 10.3390/nu16142289. PMID: 39064732; PMCID: PMC11280484.
- Cormick G, Betrán AP, Metz F, Palacios C, Beltrán-Velazquez F, García-Casal MLN, et al. Regulatory and Policy-Related Aspects of Calcium Fortification of Foods. Implications for Implementing National Strategies of Calcium Fortification. Nutrients. 2020 Apr 8;12(4):1022. doi: 10.3390/nu12041022. PMID: 32276435; PMCID: PMC7230677.
- Bourassa MW, Abrams SA, Belizán JM, Boy E, Cormick G, Quijano CD, et al. Interventions to improve calcium intake through foods in populations with low intake. Ann N Y Acad Sci. 2022 May;1511(1):40-58. doi: 10.1111/nyas.14743. Epub 2022 Jan 31. PMID: 35103316; PMCID: PMC9306636.
- Wang F, Zheng J, Cheng J, Zou H, Li M, Deng B, et al. Personalized nutrition: A review of genotype-based nutritional supplementation. Front Nutr. 2022 Sep 9;9:992986. doi: 10.3389/fnut.2022.992986. PMID: 36159456; PMCID: PMC9500586.
- Vera-Ponce VJ, Ballena-Caicedo J, Zuzunaga-Montoya FE, Loayza-Castro JA, Valladolid-Sandoval LAM, Vásquez-Romero LEM, et al. Prevalence of osteoporosis in chronic diseases: an umbrella review of 283 observational studies from 13 systematic reviews. BMC Rheumatol. 2025 Jun 6;9(1):66. doi: 10.1186/s41927-025-00520-z. PMID: 40481555; PMCID: PMC12142958.
- Weivoda MM, Chew CK, Monroe DG, Farr JN, Atkinson EJ, Geske JR, et al. Identification of osteoclast-osteoblast coupling factors in humans reveals links between bone and energy metabolism. Nat Commun. 2020 Jan 7;11(1):87. doi: 10.1038/s41467-019-14003-6. PMID: 31911667; PMCID: PMC6946812.
- Hart NH, Newton RU, Tan J, Rantalainen T, Chivers P, Siafarikas A, Nimphius S. Biological basis of bone strength: anatomy, physiology and measurement. J Musculoskelet Neuronal Interact. 2020 Sep 1;20(3):347-371. PMID: 32877972; PMCID: PMC7493450.
- Lin X, Patil S, Gao YG, Qian A. The Bone Extracellular Matrix in Bone Formation and Regeneration. Front Pharmacol. 2020 May 26;11:757. doi: 10.3389/fphar.2020.00757. PMID: 32528290; PMCID: PMC7264100.
- Choi JA, Kijas AW, Lauko J, Rowan AE. The Mechanosensory Role of Osteocytes and Implications for Bone Health and Disease States. Front. Cell Dev. Biol. 2022;9:770143. doi: 10.3389/fcell.2021.770143.
- Sims NA, Martin TJ. Osteoclasts Provide Coupling Signals to Osteoblast Lineage Cells Through Multiple Mechanisms. Annu Rev Physiol. 2020 Feb 10;82:507-529. doi: 10.1146/annurev-physiol-021119-034425. Epub 2019 Sep 25. PMID: 31553686.
- McDonald MM, Khoo WH, Ng PY, Xiao Y, Zamerli J, That–cher P, et al. Osteoclasts recycle via osteomorphs during RANKL-stimu–lated bone resorption. Cell. 2021 Mar 4;184(5):1330-1347.e13. doi: 10.1016/j.cell.2021.02.002. Epub 2021 Feb 25. Erratum in: Cell. 2021 Apr 1;184(7):1940. doi: 10.1016/j.cell.2021.03.010. PMID: 33636130; PMCID: PMC7938889.
- Ma Q, Liang M, Wu Y, Luo F, Ma Z, Dong S, Xu J, Dou C. Osteoclast-derived apoptotic bodies couple bone resorption and formation in bone remodeling. Bone Res. 2021 Jan 11;9(1):5. doi: 10.1038/s41413-020-00121-1. PMID: 33431863; PMCID: PMC7801485.
- Yashiro M, Ohya M, Mima T, Nakashima Y, Kawakami K, Yamamoto S, et al. Active vitamin D and vitamin D analogs stimulate fibroblast growth factor 23 production in osteocyte-like cells via the vitamin D receptor. J Pharm Biomed Anal. 2020 Apr 15;182:113139. doi: 10.1016/j.jpba.2020.113139. Epub 2020 Jan 31. PMID: 32045827.
- Palumbo C, Ferretti M. The Osteocyte: From “Prisoner” to “Orchestrator”. J Funct Morphol Kinesiol. 2021 Mar 17;6(1):28. doi: 10.3390/jfmk6010028. PMID: 33802907; PMCID: PMC8006231.
- Wang JS, Kamath T, Mazur CM, Mirzamohammadi F, Rotter D, Hojo H, et al. Control of osteocyte dendrite formation by Sp7 and its target gene osteocrin. Nat Commun. 2021 Nov 1;12(1):6271. doi: 10.1038/s41467-021-26571-7. PMID: 34725346; PMCID: PMC8560803.
- Mallorie A, Shine B. Normal bone physiology, remodelling and its hormonal regulation. Surgery (Oxford). 2022;40(3):163-168. doi.org/10.1016/j.mpsur.2021.12.001.
- Bolamperti S, Villa I, Rubinacci A. Bone remodeling: an operational process ensuring survival and bone mechanical competence. Bone Res. 2022;10(1):48. doi: 10.1038/s41413-022-00219-8. PMID: 35851054; PMCID: PMC9293977.
- Gunay A, Turan S. Pediatric osteoporosis: An update. Trends in Pediatrics. 2024;5(4):105-115. DOI: 10.59213/TP.2024.202.
- Magallares B, Cerdá D, Betancourt J, Fraga G, Park H, Codes-Méndez H. Risk factors associated with low bone mineral density and childhood osteoporosis in a population undergoing skeletal growth: a cross-sectional analytic study. Front. Endocrinol. 2025;16:1587985. doi: 10.3389/fendo.2025.1587985.
- Yeum KJ, Ju S, Choe U. Strategies for preventing bone loss in populations with insufficient calcium and vitamin D intake. Nutr Res Pract. 2025 Apr;19(2):155-169. doi: 10.4162/nrp.2025.19.2.155. Epub 2025 Mar 13. PMID: 40226767; PMCID: PMC11982687.
- Akaike A, Suzuki D, Okuyama S, Kudo Y, Shimizu H, Takanashi S, et al. Associations between physical physique/fitness in children and bone development during puberty: a 4-year longitudinal study. Sci Rep. 2022 Aug 4;12(1):13427. doi: 10.1038/s41598-022-17623-z. PMID: 35927458; PMCID: PMC9352704.
- Donohue P, Kujath AS. Influences on Skeletal Health and Bone Mineralization in Children. Orthop Nurs. 2022 Jul-Aug 01;41(4):252-257. doi: 10.1097/NOR.0000000000000861. PMID: 35869910.
- Proia P, Amato A, Drid P, Korovljev D, Vasto S, Baldassano S. The Impact of Diet and Physical Activity on Bone Health in Children and Adolescents. Front Endocrinol (Lausanne). 2021 Sep 13;12:704647. doi: 10.3389/fendo.2021.704647. PMID: 34589054; PMCID: PMC8473684.
- Devulapalli CS. Physical activity and vitamin D in children: a review of impacts on bone health and fitness. J Pediatr Endocrinol Metab. 2025;38(7):671-678. Published 2025 Mar 4. doi: 10.1515/jpem-2024-0527.
- Przytula A, Popiolek-Kalisz J. The Impact of Physical Education Attendance and Diet on Bone Mineralization in Adolescents. Nutrients. 2025;17(18):3016. doi: 10.3390/nu17183016. PMID: 41010541; –PMCID: PMC12472207.
- Brennan M, Kalsi T. Management of Bone Health Considera–tions in Patients with Cancer. Cancers. 2025;17(17):2878. doi: 10.3390/cancers17172878. PMID: 40940974; PMCID: PMC12427312.
- Ratajczak AE, Rychter AM, Zawada A, Dobrowolska A, Krela-Kaźmierczak I. Nutrients in the Prevention of Osteoporosis in Patients with Inflammatory Bowel Diseases. Nutrients. 2020 Jun 6;12(6):1702. doi: 10.3390/nu12061702. PMID: 32517239; PMCID: PMC7352179.
- Li GF, Zhao PP, Xiao WJ, Karasik D, Xu YJ, Zheng HF. The paradox of bone mineral density and fracture risk in type 2 diabetes. Endocrine. 2024 Sep;85(3):1100-1103. doi: 10.1007/s12020-024-03926-w. Epub 2024 Jun 26. PMID: 38922479.
- Terashima A, Ono K, Omata Y, et al. Inflammatory diseases causing joint and bone destruction: rheumatoid arthritis and hemophilic arthropathy. J Bone Miner Metab. 2024;42(4):455-462. doi: 10.1007/s00774-024-01520-8. Epub 2024 Jun 10. PMID: 38856919; PMCID: PMC11415468.
- Xie R, Liu M. Relationship Between Non-Alcoholic Fatty Li–ver Disease and Degree of Hepatic Steatosis and Bone Mineral Density. Front Endocrinol (Lausanne). 2022 Mar 14;13:857110. doi: 10.3389/fendo.2022.857110. PMID: 35360054; PMCID: PMC8964007.
- Nishiura M, Watanabe H, Nakanishi-Kimura A, Hoshi-Numahata M, Nishimoto S, Ueno F, et al. Bone Metabolic Changes and Osteoporosis During Pregnancy and Lactation: A View from Dental Medicine. Int J Mol Sci. 2025 Oct 28;26(21):10476. doi: 10.3390/ijms262110476. PMID: 41226515; PMCID: PMC12609550.
- Ayers C, Ward R, Kansagara D. Update Alert: Effectiveness and Safety of Treatments to Prevent Fractures in People With Low Bone Mass or Primary Osteoporosis: A Living Systematic Review and Network Meta-analysis for the American College of Physicians. Ann Intern Med. 2024 Jun;177(6):eL230118. doi: 10.7326/L24-0118. Epub 2024 May 7. PMID: 38710084.
- Martins LM, Arrepia BF, Jural L, Vicente-Gomila JM, Masterson D, et al. Implications of Vitamin D Status for Children’s Bone Health: A Data Mining Analyses of Observational Studies. Pesquisa Brasileira em Odontopediatria e Clinica Integrada (Online). 2024;24(e230054). DOI: 10.1590/pboci.2024.048.
- Ciosek Ż, Kot K, Kosik-Bogacka D, Łanocha-Arendarczyk N, Rotter I. The Effects of Calcium, Magnesium, Phosphorus, Fluoride, and Lead on Bone Tissue. Biomolecules. 2021;11(4):506. doi: 10.3390/biom11040506. PMID: 33800689; PMCID: PMC8066206.
- Abrams SA. Bone Health in School Age Children: Effects of Nutritional Intake on Outcomes. Front Nutr. 2021 Nov 19;8:773425. doi: 10.3389/fnut.2021.773425. PMID: 34869539; PMCID: PMC8640096.
- Shlisky J, Mandlik R, Askari S, Abrams S, Belizan JM, Bourassa MW, et al. Calcium deficiency worldwide: prevalence of ina–dequate intakes and associated health outcomes. Ann N Y Acad Sci. 2022 Jun;1512(1):10-28. doi: 10.1111/nyas.14758. Epub 2022 Mar 5. PMID: 35247225; PMCID: PMC9311836.
- Palacios C, Hofmeyr GJ, Cormick G, Garcia-Casal MN, Peña-Rosas JP, Betrán AP. Current calcium fortification experiences: a review. Ann N Y Acad Sci. 2021 Jan;1484(1):55-73. doi: 10.1111/nyas.14481. Epub 2020 Sep 18. PMID: 32949062; PMCID: PMC8246751.
- Minkowitz B, Spingarn CM. Effective counseling for children’s bone health. Journal of the Pediatric Orthopaedic Society of North Ame–rica. 2024 May;(7):100032.. doi: 10.1016/j.jposna.2024.100032. PMID: 40433273; PMCID: PMC12088366.
- Sempos CT, Durazo-Arvizu RA, Fischer PR, Munns CF, Pettifor JM, Thacher TD. Serum 25-hydroxyvitamin D requirements to prevent nutritional rickets in Nigerian children on a low-calcium diet — a multivariable reanalysis. Am J Clin Nutr. 2021 Jul 1;114(1):231-237. doi: 10.1093/ajcn/nqab048. PMID: 33742199.
- Wolf CA, Malone T, McFadden BR. Beverage milk consumption patterns in the United States: Who is substituting from dairy to plant-based beverages? J Dairy Sci. 2020 Dec;103(12):11209-11217. doi: 10.3168/jds.2020-18741. Epub 2020 Oct 23. PMID: 33222851.
- Muleya M, Bailey FE, H Bailey НE. A comparison of the bioaccessible calcium supplies of various plant-based products relative to bovine milk. Food Res Int. 2024 Jan;175:113795. doi: 10.1016/j.foodres.2023.113795. Epub 2023 Dec 3. PMID: 38129068.
- Shkembi B, Huppertz T. Calcium absorption from food products: food matrix effects. Nutrients. 2021;14(1):180. doi: 10.3390/nu14010180. PMID: 35011055; PMCID: PMC8746734.
- Gómez AL, Kraemer WJ, Maresh CM, Lee EC, Szivak TK, Caldwell LK, et al. Resistance Training and Milk-Substitution Enhance Body Composition and Bone Health in Adolescent Girls. J Am Coll Nutr. 2021 Mar-Apr;40(3):193-210. doi: 10.1080/07315724.2020.1770636. Epub 2020 Jun 10. PMID: 32521207.
- Mazess RB, Bischoff-Ferrari HA, Dawson-Hughes B. Vitamin D: bolus is bogus — a narrative review. JBMR. 2021;5(12):e105677. doi: 10.1002/jbm4.10567. PMID: 34950828; PMCID: PMC8674779.
- Reid IR, Bristow SM. Calcium and Bone. Handb Exp Pharmacol. 2020;262:259-280. doi: 10.1007/164_2019_324. PMID: 31792679.
- Karimian P, Ebrahimi HK, Jafarnejad S, Delavar MA. Effects of vitamin D on bone density in healthy children: A systematic review. J Family Med Prim Care. 2022 Mar;11(3):870-878. doi: 10.4103/jfmpc.jfmpc_2411_20. Epub 2022 Mar 10. PMID: 35495788; PMCID: PMC9051716.
- Voltan G, Cannito M, Ferrarese M, Ceccato F, Camozzi V. Vitamin D: An Overview of Gene Regulation, Ranging from Metabolism to Genomic Effects. Genes (Basel). 2023 Aug 25;14(9):1691. doi: 10.3390/genes14091691. PMID: 37761831; PMCID: PMC10531002.
- Institute of Medicine (US) Committee to Review Dietary Reference Intakes for Vitamin D and Calcium. Dietary Reference Intakes for Calcium and Vitamin D. Ross AC, Taylor CL, Yaktine AL, Del Valle HB, editors. Washington (DC): National Academies Press (US); 2011. PMID: 21796828.
- Płudowski P, Karczmarewicz E, Bayer M, Carter G, Chlebna-Sokół D, Czech-Kowalska J, et al. Practical guidelines for the supplementation of vitamin D and the treatment of deficits in Central Europe — recommended vitamin D intakes in the general population and groups at risk of vitamin D deficiency. Endokrynol Pol. 2013;64(4):319-27. doi: 10.5603/ep.2013.0012.
- Grossman Z, Hadjipanayis A, Stiris T, Del Torso S, Mercier JC, Valiulis A, Shamir R. Vitamin D in European children-statement from the European Academy of Paediatrics (EAP). Eur J Pediatr. 2017 Jun;176(6):829-831. doi: 10.1007/s00431-017-2903-2.
- Rebelos E, Tentolouris N, Jude E. The Role of Vitamin D in Health and Disease: A Narrative Review on the Mechanisms Linking Vitamin D with Disease and the Effects of Supplementation. Drugs. 2023 Jun;83(8):665-685. doi: 10.1007/s40265-023-01875-8. Epub 2023 May 6. PMID: 37148471; PMCID: PMC10163584.
- Grant WB, Al Anouti F, Boucher BJ, Dursun E, Gezen-Ak D, Jude EB, Karonova T, Pludowski P. A Narrative Review of the Evidence for Variations in Serum 25-Hydroxyvitamin D Concentration Thre–sholds for Optimal Health. Nutrients. 2022 Feb 2;14(3):639. doi: 10.3390/nu14030639. PMID: 35276999; PMCID: PMC8838864.
- Hereford T, Kellish A, Samora JB, Nichols LR. Understanding the importance of peak bone mass. Journal of the Pediatric Orthopaedic Society of North America. 2024 May;(7):100031. doi: 10.1016/j.jposna.2024.100031. PMID: 40433296; PMCID: PMC12088333.
- Marushko YuV, Hyshchak TV. Prevention of vitamin D deficiency in children. The state of the problem in the world and in Ukraine. Modern Pediatrics. Ukraine. 2021;4(116):36-45. doi: 10.15574/SP.2021.116.36
- Shatylo S, Bogomaz V, Babych O. Vitamin D deficiency in Ukraine: A multicentre cross-sectional study. Glob Epidemiol. 2024 Oct 10;8:100170. doi: 10.1016/j.gloepi.2024.100170. PMID: 39483738; –PMCID: PMC11525160.
- Povorozniuk VV, Beketova GV, Klymova YV, Musiienko AS. 25(OH)D level, deficiency and insufficiency in the Kyiv city schoolchildren. World of Medicine and Biology. 2021;1(75):135-139. DOI: 10.26724/2079-8334-2021-1-75-135-138.
- Wang B, Gao S, Zhu Z. Vitamin D deficiency and adverse body composition in adolescents. J Orthop Surg Res. 2025 Jul 10;20(1):637. doi: 10.1186/s13018-025-06091-6. PMID: 40640884; PMCID: PMC12247196.
- Snetselaar LG, de Jesus JM, DeSilva DM, Stoody EE. Dietary Guidelines for Americans, 2020–2025: Understanding the Scientific Process, Guidelines, and Key Recommendations. Nutr Today. 2021 Nov-Dec;56(6):287-295. doi: 10.1097/NT.0000000000000512. Epub 2021 Nov 12. PMID: 34987271; PMCID: PMC8713704.
- Vieth R. Vitamin D supplementation: cholecalciferol, calcifediol, and calcitriol. Eur J Clin Nutr. 2020 Nov;74(11):1493-1497. doi: 10.1038/s41430-020-0697-1. Epub 2020 Jul 23. PMID: 32704098.
- Azhar M, Yasin R, Hanif S, Bughio SA, Das JK, Bhutta ZA. Nutritional Management of Low Birth Weight and Preterm Infants in Low- and Low Middle-Income Countries. Neonatology. 2025;122 –(Suppl 1):209-223. doi: 10.1159/000542154. Epub 2024 Nov 26. PMID: 39591949; PMCID: PMC11875417.
- Tobias DK, Luttmann-Gibson H, Mora S, Danik J, Bubes V, Copeland T, et al. Association of Body Weight With Response to Vitamin D Supplementation and Metabolism. JAMA Netw Open. 2023 Jan 3;6(1):e2250681. doi: 10.1001/jamanetworkopen.2022.50681. PMID: 36648947; PMCID: PMC9856931.
- Herdea A, Ionescu A, Dragomirescu MC, Ulici A. Vitamin D — A Risk Factor for Bone Fractures in Children: A Population-Based Prospective Case-Control Randomized Cross-Sectional Study. Int J Environ Res Public Health. 2023 Feb 13;20(4):3300. doi: 10.3390/ijerph20043300. PMID: 36833994; PMCID: PMC9963378.
- Maglietta G, Puntoni M, Caminiti C, Ghi T, Street ME, Perrone S, Wasniewska M. Challenges in assessing bone health in early infancy: a narrative review of existing technologies. Front Endocrinol (Lausanne). 2025 Oct 21;16:1651094. doi: 10.3389/fendo.2025.1651094. PMID: 41195209; PMCID: PMC12583111.
- Ling L. Association between serum vitamin A and bone mineral density in adolescents. Sci Rep. 2025 Feb 26;15(1):6892. doi: 10.1038/s41598-025-91367-4. PMID: 40011496; PMCID: PMC11865262.
- Shen Y, Shi G, Wen Sh, Luo W, Wang K. Vitamin K2 deficiency associated with short stature in children: a cross-sectional study. BMC Pediatrics. 2025;25(1):348. doi: 10.1186/s12887-025-05699-1. PMID: 40312299; PMCID: PMC12044740.
- Maresz K. Growing Evidence of a Proven Mechanism Shows Vitamin K2 Can Impact Health Conditions Beyond Bone and Cardiovascular. Integr Med (Encinitas). 2021 Aug;20(4):34-38. PMID: 34602875; PMCID: PMC8483258.
- Popescu A, German M. Vitamin K2 Holds Promise for Alzhei–mer’s Prevention and Treatment. Nutrients. 2021 Jun 27;13(7):2206. doi: 10.3390/nu13072206. PMID: 34199021; PMCID: PMC8308377.
- Kozioł-Kozakowska A, Maresz K. The Impact of Vitamin K2 (Menaquionones) in Children’s Health and Diseases: A Review of the Literature. Children (Basel). 2022 Jan 5;9(1):78. doi: 10.3390/children9010078. PMID: 35053702; PMCID: PMC8774117.
- Akbulut AC, Pavlic A, Petsophonsakul P, Halder M, Maresz K, Kramann R, Schurgers L. Vitamin K2 Needs an RDI Separate from Vitamin K1. Nutrients. 2020 Jun 21;12(6):1852. doi: 10.3390/nu12061852. PMID: 32575901; PMCID: PMC7353270.
- Tsugawa N, Shiraki M. Vitamin K Nutrition and Bone Health. Nutrients. 2020 Jun 27;12(7):1909. doi: 10.3390/nu12071909. PMID: 32605143; PMCID: PMC7399911.
- Zhang Y, Liu Z, Duan L, Ji Y, Yang S, Zhang Y, et al. Effect of Low-Dose Vitamin K2 Supplementation on Bone Mineral Density in Middle-Aged and Elderly Chinese: A Randomized Controlled Study. Calcif Tissue Int. 2020 May;106(5):476-485. doi: 10.1007/s00223-020-00669-4. Epub 2020 Feb 14. PMID: 32060566.
- Wang BZ, Xie ZJ, Wu ZY, Yang L. Vitamin K2 Can Rescue the Dexamethasone-Induced Downregulation of Osteoblast Autophagy and Mitophagy Thereby Restoring Osteoblast Function In Vitro and In Vivo. Front Pharmacol. 2020 Aug 11;11:1209. doi: 10.3389/fphar.2020.01209. PMID: 32848799; PMCID: PMC7431688.
- Mandatori D, Pelusi L, Schiavone V, Pipino C, Di Pietro N, Pandolfi A. The Dual Role of Vitamin K2 in “Bone-Vascular Crosstalk”: Opposite Effects on Bone Loss and Vascular Calcification. Nutrients. 2021 Apr 7;13(4):1222. doi: 10.3390/nu13041222. PMID: 33917175; –PMCID: PMC8067793.
- Solmaz I, Ozdemir MA, Unal E, Abdurrezzak U, Muhtaroglu S, Karakukcu M. Effect of vitamin K2 and vitamin D3 on bone mineral density in children with acute lymphoblastic leukemia: a prospective cohort study. J Pediatr Endocrinol Metab. 2021 Feb 25;34(4):441-447. doi: 10.1515/jpem-2020-0637. PMID: 33639045.
- Gong H, Jiang J, Choi S, Huang S. Sex differences in the association between dietary choline intake and total bone mineral density among adolescents aged 12–19 in the United States. Front Nutr. 2024 Nov 20;11:1459117. doi: 10.3389/fnut.2024.1459117. PMID: 39634554; PMCID: PMC11614608.
- Kiely ME. Risks and benefits of vegan and vegetarian diets in children. Proc Nutr Soc. 2021 May;80(2):159-164. doi: 10.1017/S002966512100001X. Epub 2021 Jan 28. PMID: 33504371.
- Desmond MA, Sobiecki JG, Jaworski M, Płudowski P, Antoniewicz J, Shirley MK, et al. Growth, body composition, and cardiovascular and nutritional risk of 5- to 10-y-old children consuming vegetarian, vegan, or omnivore diets. Am J Clin Nutr. 2021 Jun 1;113(6):1565-1577. doi: 10.1093/ajcn/nqaa445. PMID: 33740036; PMCID: PMC8176147.
- Anguita-Ruiz A, Aguilera CM, Gil Á. Genetics of Lactose Intole–rance: An Updated Review and Online Interactive World Maps of Phenotype and Genotype Frequencies. Nutrients. 2020 Sep 3;12(9):2689. doi: 10.3390/nu12092689. PMID: 32899182; PMCID: PMC7551416.
- Kwon S, Baptista F, Levy SM, Guha I, Saha PK, Janz KF. Associations Between Youth Sport Participation and Bone, Muscle, and Fat in Adulthood: Iowa Bone Development Study. Int J Environ Res Public Health. 2025 Mar 12;22(3):416. doi: 10.3390/ijerph22030416. PMID: 40238574; PMCID: PMC11942570.
- Kongsvold A, Skarpsno ES, Flaaten M, Logacjov A, Bach K, Nilsen TIL, Mork PJ. Associations of sport and exercise participation in adolescence with body composition and device-measured physical activity in adulthood: longitudinal data from the Norwegian HUNT study. Int J Behav Nutr Phys Act. 2025 Mar 5;22(1):29. doi: 10.1186/s12966-025-01726-7. PMID: 40045311; PMCID: PMC11883909.
- Marusic U, Narici M, Simunic B, Pisot R, Ritzmann R. Nonuniform loss of muscle strength and atrophy during bed rest: a systematic review. J Appl Physiol. 2021 Jul 1;131(1):194-206. doi: 10.1152/japplphysiol.00363.2020. Epub 2021 Mar 11. PMID: 33703945; PMCID: PMC8325614.
- Kouda K, Iki M, Fujita Y, Nakamura H, Uenishi K, Ohara K, Nishiyama T. Calcium Intake and Bone Mineral Acquisition during the Pubertal Growth Spurt: Three-Year Follow-Up of the Kitakata Kids Health Study in Japan. J Nutr Sci Vitaminol (Tokyo). 2020;66(2):158-167. doi: 10.3177/jnsv.66.158. PMID: 32350177.
- Xu B, Anderson DB, Park ES, Chen L, Lee JH. The influence of smoking and alcohol on bone healing: Systematic review and meta-analysis of non-pathological fractures. EClinicalMedicine. 2021 Oct 31;(42):101179. doi: 10.1016/j.eclinm.2021.101179. PMID: 34765953; PMCID: PMC8571530.
- Patel H, Patel M, Clark L, Denison H, Teesdale-Spittle P, Dennison EM. Posted Date: 29 May 2025 doi: 10.20944/preprints202505.2317.v1.
- Roizen JD, Levine MA. Vitamin D Therapy and the Era of Precision Medicine. J Clin Endocrinol Metab. 2020 Mar 1;105(3):e891-3. doi: 10.1210/clinem/dgz120. PMID: 31665328; PMCID: PMC7112971.
- Clarke J, Peyre H, Alison M, Bargiacchi A, Stordeur C, Boizeau P, et al. Abnormal bone mineral density and content in girls with early-onset anorexia nervosa. J Eat Disord. 2021 Jan 10;9(1):9. doi: 10.1186/s40337-020-00365-6. PMID: 33423687; PMCID: PMC7798269.
- Fintini D, Cianfarani S, Cofini M, Andreoletti A, Ubertini GM, Cappa M, Manco M. The Bones of Children With Obesity. Front Endocrinol (Lausanne). 2020 Apr 24;11:200. doi: 10.3389/fendo.2020.00200. PMID: 32390939; PMCID: PMC7193990.
- Juhász MF, Varannai O, Németh D, Szakács Z, Kiss S, Izsák VD, et al. Vitamin D supplementation in patients with cystic fibrosis: A systematic review and meta-analysis. J Cyst Fibros. 2021 Sep;20(5):729-736. doi: 10.1016/j.jcf.2020.12.008. Epub 2020 Dec 19. PMID: 33349585.
- Nisha Y, Dubashi B, Bobby Z, Sahoo JP, Kayal S, Ananthakrishnan R, Ganesan P. Cytotoxic chemotherapy is associated with decreased bone mineral density in postmenopausal women with early and locally advanced breast cancer. Arch Osteoporos. 2023 Mar 10;18(1):41. doi: 10.1007/s11657-023-01231-z. PMID: 36899284; PMCID: PMC10004442.
- Ward LM. Glucocorticoid-Induced Osteoporosis: Why Kids Are Different. Front Endocrinol (Lausanne). 2020 Dec 16;11:576. doi: 10.3389/fendo.2020.00576. PMID: 33391179; PMCID: PMC7772619.
- Cipriani F, Gnessi L, Watanabe M, Baldelli R. Inositols and Bone Health: Potential Therapeutic Applications in Osteoporosis Prevention and Treatment. Nutrients. 2025;17(12):1999. doi: 10.3390/nu17121999. PMID: 40573111; PMCID: PMC12195919.
- Castellani C, De Martino E, Scapato P. Osteoporosis: Focus on Bone Remodeling and Disease Types. BioChem. September 2025;5(3):31. DOI: 10.3390/biochem5030031.
- Gaete PV, Cuellar-Rodríguez V, Mendivil CO. Antiseizure Medications and Bone Health. Neurol Ther. 2025;(14):1827-1844. https://doi.org/10.1007/s40120-025-00805-y.
- Farella I, Chiarito M, Vitale R, D’Amato G, Faienza MF. The “Burden” of Childhood Obesity on Bone Health: A Look at Prevention and Treatment. Nutrients. 2025;17(3):491. DOI: 10.3390/nu17030491.
- Lee JY, Finlayson C, Olson-Kennedy J, Garofalo R, Chan YM, Glidden DV, Rosenthal SM. Low Bone Mineral Density in Early Pubertal Transgender/Gender Diverse Youth: Findings From the Trans Youth Care Study. J Endocr Soc. 2020 Jul 2;4(9):bvaa065. doi: 10.1210/jendso/bvaa065. PMID: 32832823; PMCID: PMC7433770.
- Schagen SEE, Wouters FM, Cohen-Kettenis PT, Gooren LJ, Hannema SE. Bone Development in Transgender Adolescents Treated With GnRH Analogues and Subsequent Gender-Affirming Hormones. J Clin Endocrinol Metab. 2020 Dec 1;105(12):e4252-63. doi: 10.1210/clinem/dgaa604. PMID: 32909025; PMCID: PMC7524308.
- Oh YT, Goh TX, Chong JC, Yang WY, Arasu K. Knowledge, attitude regarding osteoporosis, dietary calcium intake and food sources of calcium among Chinese young adults in Klang Valley, Malaysia. Discov Public Health. 2024;(21):58. DOI: 10.1186/s12982-024-00179-w.
- Saleem S, Khan Z, Hussain I, Khan F, Al-Asmari F, Khan FA, et al. Evaluating the effect of vitamin D3 fortification on physicochemical and sensory properties of yogurt. Cogent Food Agric. 2024;(10):2350145. DOI: 10.1080/23311932.2024.2350145.
- Shea MK, Strath L, Kim M, Ðoàn LN, Booth SL, Brinkley TE, Kritchevsky SB. Perspective: Promoting Healthy Aging through Nutrition: A Research Centers Collaborative Network Workshop Report. Adv Nutr. 2024 Apr;15(4):100199. doi: 10.1016/j.advnut.2024.100199. Epub 2024 Mar 1. PMID: 38432592; PMCID: PMC10965474.
- Gobbo LA, Júdice PB, Hetherington-Rauth M, Sardinha LB, Dos Santos VR. Sedentary Patterns Are Associated with Bone Mineral Density and Physical Function in Older Adults: Cross-Sectional and Prospective Data. Int J Environ Res Public Health. 2020 Nov 6;17(21):8198. doi: 10.3390/ijerph17218198. PMID: 33171963; PMCID: PMC7664175.
- Lin Z, Shi G, Liao X, Huang J, Yu M, Liu W, Luo X, Zhan H, Cai X. Correlation between sedentary activity, physical activity and bone mine–ral density and fat in America: National Health and Nutrition Exa–mination Survey, 2011–2018. Sci Rep. 2023 Jun 21;13(1):10054. doi: 10.1038/s41598-023-35742-z. PMID: 37344579; PMCID: PMC10284806.
- Sosa-Holwerda A, Park OH, Albracht-Schulte K, Niraula S, Thompson L, Oldewage-Theron W. The Role of Artificial Intelligence in Nutrition Research: A Scoping Review. Nutrients. 2024 Jun 28;16(13):2066. doi: 10.3390/nu16132066. PMID: 38999814; PMCID: PMC11243505.
- Saag JL, Danila MI. Remote Management of Osteoporosis. Curr Treatm Opt Rheumatol. 2022;8(4):143-151. doi: 10.1007/s40674-022-00195-4. Epub 2022 Sep 2. PMID: 36068838; PMCID: PMC9438367.
- Alhussein G, Hadjileontiadis L. Digital Health Technologies for Long-term Self-management of Osteoporosis: Systematic Review and Meta-analysis. JMIR Mhealth Uhealth. 2022 Apr 21;10(4):e32557. doi: 10.2196/32557. PMID: 35451968; PMCID: PMC9073608.
- Webster J, Dalla Via J, Langley C, Smith C, Sale C, Sim M. Nutritional strategies to optimise musculoskeletal health for fall and fracture prevention: Looking beyond calcium, vitamin D and protein. Bone Rep. 2023 May 5;19:101684. doi: 10.1016/j.bonr.2023.101684. PMID: 38163013; PMCID: PMC10757289.

/16.jpg)
/17.jpg)
/18.jpg)