Вступ
Проблема лікування хронічних дифузних захворювань печінки залишається однією з найактуальніших у сучасній гастроентерології. Спостерігається їх значна поширеність, зростає захворюваність на печінкову патологію. Хронічний гепатит різного генезу, як правило, має тенденцію до прогресування в напрямку фіброзу й цирозу печінки. З огляду на малосимптомний перебіг гепатозу й гепатиту виявлення даної патології у таких хворих не завжди може бути своєчасним. За останні десятиліття певних змін зазнав етіологічний склад хронічних дифузних захворювань печінки. Окрім традиційно поширених алкогольних і вірусних уражень, збільшується частота метаболічних уражень печінки.
До 2023 року дана група захворювань мала назву «неалкогольна жирова хвороба печінки», куди включали стеатоз, стеатогепатит, цироз печінки внаслідок стеатогепатиту. Але у 2023 році змінилася назва цієї патології, яка робить акцент не на відсутності зловживання алкоголем, а саме на наявності метаболічних порушень як основи патологічних процесів. Тепер ця патологія називається «метаболічно-асоційована стеатотична хвороба печінки» (МАСХП) [1].
Для встановлення діагнозу МАСХП необхідна наявність у пацієнта стеатозу печінки (за даними інструментальних досліджень або результатами біопсії) та принаймні одного з п’яти кардіометаболічних критеріїв, які включають:
— індекс маси тіла ≥ 25 кг/м2 або окружність талії > 94 см у чоловіків і > 80 см у жінок або етнічні еквіваленти;
— глюкоза натще ≥ 5,6 ммоль/л, або глюкоза через 2 години після глюкозного навантаження ≥ 7,8 ммоль/л, або глікований гемоглобін HbA1c ≥ 5,7 %, або цукровий діабет 2 типу, або лікування цукрового діабету 2 типу;
— артеріальний тиск ≥ 130/85 мм рт.ст. або специфічне антигіпертензивне медикаментозне лікування;
— тригліцериди ≥ 1,7 ммоль/л або ліпідознижувальна терапія;
— холестерин ліпопротеїнів високої щільності ≤ 1,0 ммоль/л у чоловіків і ≤ 1,3 ммоль/л у жінок або ліпідознижувальна терапія [2].
Зрозуміло, що існує тісний зв’язок між збільшенням ваги, надлишковим вживанням висококалорійних продуктів, малорухомим способом життя і розвитком МАСХП. Так, метааналіз 2023 року, що включав понад 150 досліджень і понад 100 тисяч осіб, вказав, що неалкогольна жирова хвороба печінки спостерігалась у 69,99 % осіб з підвищеною масою тіла і 75,27 % осіб з ожирінням. При цьому поширеність стеатогепатиту становила 33,50 % в осіб з підвищеною масою тіла та 33,67 % в осіб з ожирінням, фіброзу F3-F4 — 6,65 % в осіб з підвищеною масою тіла та 6,85 % в осіб з ожирінням [3].
Проте накопичено чимало даних про те, що МАСХП може спостерігатися не лише в осіб з ожирінням і надлишковою масою тіла. Стеатотичні зміни в печінці можуть спостерігатись і в струнких пацієнтів. Навіть з’явився такий термін: МАСХП у струнких пацієнтів (lean liver disease) [4].
Відповідно до цього виникають певні питання. З якої причини виникає МАСХП? Чому вона може спостерігатися не лише в пацієнтів з підвищеним індексом маси тіла? Чому в частини хворих МАСХП перебігає лише зі стеатозом, а в іншої частини — зі стеатогепатитом і фіброзом? Яким чином розвивається та прогресує МАСХП? Адже добре відомо, що для того, щоб успішно лікувати ту чи іншу патологію, важливо розуміти її патогенез і спрямовувати зусилля на усунення або гальмування патофізіологічних чинників.
Наприкінці минулого сторіччя з’явилася гіпотеза подвійного удару в патогенезі МАСХП: накопичення жиру в печінці — стеатоз (перший удар) і вплив додаткових факторів, наприклад кишкових ендотоксинів, що викликають розвиток запалення печінки, — стеатогепатит (другий удар) [5]. Однак подальші дослідження показали, що, імовірно, існують паралельні удари — вплив прозапальних факторів, особливо кишечника та жирової тканини, що призводять до розвитку стеатогепатиту [6]. У 2016 році гіпотезу подвійного удару вже вважали застарілою, натомість пропонувалася гіпотеза множинного удару, що розглядала одночасно множинне ураження як результат дії різноманітних факторів інсулінорезистентності, дії гормонів жирової тканини, харчових факторів, кишкової мікробіоти, генетичних та епігенетичних факторів [7].
Безперечно, ожиріння, інсулінорезистентність, артеріальна гіпертензія та гіпертригліцеридемія залишаються основними факторами ризику МАСХП [8]. Відповідно стеатоз печінки — це результат надлишкового надходження калорій і надмірного накопичення великої кількості тригліцеридів у гепатоцитах. Вільні жирні кислоти, які є субстратом для формування тригліцеридів, накопичуються в печінці або за рахунок надходження з їжею, або в процесі ліпогенезу в печінці [8].
Надлишкове накопичення жиру в печінці може провокувати розвиток ліпотоксичності [8]. Ліпотоксичність здатна викликати стрес ендоплазматичного ретикулуму й оксидативний стрес [9]. Окрім того, ліпотоксичність сприяє розвитку мітохондріального порушення й лізосомальної дисфункції [8]. Усе це призводить до пошкодження гепатоцитів, розвитку стеатогепатиту й можливого фіброзу печінки.
Іншим патогенетичним фактором розвитку стеатогепатиту є фероптоз — це форма регульованої модальності клітинної смерті, пов’язана з порушенням гомеостазу заліза й необмеженим перекисним окисненням ліпідів [10]. Фактори, що викликають фероптоз, впливають на глутатіонпероксидазу, що призводить до зниження антиоксидантної здатності й накопичення ліпідних активних форм кисню [11]. Зібрано дані, що доводять внесок фероптозу в прогресування стеатогепатиту [12].
Ще одним дуже важливим фактором розвитку МАСХП та інших метаболічних порушень є дисбіоз кишкової мікрофлори. З одного боку, дисбіоз кишечника підвищує проникність кишкового бар’єра, що призводить до підвищеної абсорбції жирних кислот. З іншого боку, дисбіоз підвищує продукцію та всмоктування ендотоксинів, які потрапляють у печінку й пошкоджують її. Провокуючий вплив на розвиток МАСХП також може здійснюватися через негативну дію дисбіозу кишечника на метаболізм жовчних кислот [8]. Дослідження показали, що у хворих на МАСХП менше різноманіття кишкової мікрофлори, ніж у здорових осіб [8]. Натомість має місце посилення окремих видів мікрофлори, що можуть мати негативний вплив на печінку. Так, в одному з досліджень збільшення бактероїдів корелювало зі стеатогепатитом, збільшення румінококів — зі значним фіброзом [13]. Доведено, що синдром надлишкового бактеріального росту й ендотоксемія мають також вплив на жирову хворобу печінки [14].
Подальше вивчення патогенезу МАСХП триває. Постійно з’являються нові факти. Але вже сьогодні видно, що в патогенезі даного захворювання провідну роль відіграють не лише метаболічні порушення, але й прозапальні чинники.
Лікування МАСХП має бути комплексним і повинно насамперед включати комплекс заходів, що спрямовані на модифікацію стилю життя пацієнта, корекцію його харчування. Проте також важливим є застосування медикаментозних засобів для зменшення метаболічних порушень у печінці.
Серед засобів, що можуть застосовуватись у лікуванні МАСХП, дуже корисними є ті, що спрямовані, з одного боку, на корекцію метаболічних порушень у печінці та загалом в організмі, з іншого боку — на зменшення запальних і дистрофічних змін у гепатоцитах.
З огляду на вищесказане перспективним засобом для успішної корекції зазначених порушень є біологічно активна добавка Гепавіста Детокс, яка складається з двох основних елементів — S-адеметіоніну та глутатіону. Одна таблетка засобу містить 400 мг S-адеметіоніну та 250 мг глутатіону.
S-аденозил-L-метіонін (адеметіонін) — біологічна речовина, що бере участь у понад 40 біохімічних реакціях. Серед них слід насамперед відзначити транс–метилювання — перенос метильних груп для синтезу фосфоліпідів, гормонів, нейромедіаторів; транссульфурування — участь у синтезі цистеїну, таурину, глутатіону; амінопропілювання — участь у синтезі поліамінів, що стимулюють регенерацію та проліферацію гепатоцитів. Зрозуміло, що вказані ефекти адеметіоніну чинять дезінтоксикаційний, антиоксидантний, протизапальний і регенеруючий вплив на печінку. Адеметіоніну властива певна ліпотропна дія. Адеметіонін впливає не лише на стан печінки, але й на головний мозок: він бере участь у реакціях синтезу біологічних речовин, що відіграють важливу роль у передачі нейрогуморальних сигналів, стимулює утворення нейромедіаторів. Завдяки цьому адеметіонін забезпечує швидкість реакції, активізацію розумової діяльності, поліпшення настрою, отже, проявляє антидепресантну активність.
Глутатіон — це трипептид, що містить 3 важливі амінокислоти (глутамін, цистеїн і гліцин), він є природним компонентом клітин усіх тканин організму. Добре відомо, що глутатіон є одним з головних внутрішньоклітинних антиоксидантів з потужною детоксикаційною дією: він зв’язує вільні радикали, відновлює продукти перекисного окиснення ліпідів, фосфоліпідів мембран, білків, нуклеїнових кислот і виводить їх з організму у вигляді нетоксичних кон’югатів, відновлює інші антиоксиданти (вітаміни С і Е). Глутатіон також має імуномодуюючі властивості: він активує природні кілери (NK-клітини) і модулює функціональну активність Т-лімфоцитів.
Отже, така комбінація (S-адеметіонін + глутатіон) здатна вплинути на основні патогенетичні фактори розвитку МАСХП і допомогти покращити функціональний і структурний стан печінки.
Проте вимоги доказової медицини потребують оцінки ефективності таких засобів і конкретизації показань до призначення, що і є метою даного дослідження.
Метою дослідження була оцінка ефективності лікування комплексним засобом Гепавіста Детокс у хворих на МАСХП з урахуванням динаміки лабораторних (печінкові проби) та інструментальних (стеатоз, фіброз) показників у печінці.
Матеріали та методи
Дослідження проведено в 45 хворих на МАСХП. Діаг–ноз МАСХП встановлювався за критеріями EASL 2023 року. Для встановлення діагнозу МАСХП необхідна наявність у пацієнта стеатотичної хвороби печінки та принаймні одного з п’яти кардіометаболічних факторів ризику, які включають: збільшення індексу маси тіла або окружності талії; порушення метаболізму глюкози; високий артеріальний тиск; високий рівень тригліцеридів; низький рівень холестерину ліпопротеїнів високої щільності [2].
До даного дослідження залучили лише тих пацієнтів, хто підписав інформовану згоду, відповідав критеріям включення і не мав критеріїв виключення.
Критерії включення: вік хворого від 18 до 65 років; наявність МАСХП; ознаки стеатозу печінки за даними зсувнохвильової еластографії (ЗХЕ) печінки; згода хворого на участь в обстеженні й можливість виконувати процедури.
Критерії виключення: конкуруючі захворювання печінки (вірусні, алкогольні, автоімунні, біліарні тощо); тяжкі ураження інших органів і систем; ендокринна патологія, включно з інсулінозалежним і некомпенсованим інсулінонезалежним цукровим діабетом І і ІІ типу.
Серед досліджених пацієнтів чоловіків було 25 (55,6 %), жінок — 20 (44,4 %). Середній вік становив (51,53 ± 1,93) року. Анамнестично середня тривалість МАСХП становила (8,91 ± 1,45) року, отже, для більшості хворих властивий був доволі тривалий перебіг захворювання. З них 8 хворих мали стеатогепатоз і 37 — стеатогепатит. Індекс маси тіла в пацієнтів був від 23,42 до 53,26, становлячи в середньому (33,50 ± 0,94) кг/м2.
Серед супутньої патології найчастіше спостерігалися: артеріальна гіпертензія — 23 (51,1 %), компенсований цукровий діабет 2 типу — 4 (18,9 %), ішемічна хвороба серця — 5 (11,1 %) пацієнтів; 7 хворих (15,6 %) палять.
Хворі отримували комплексний засіб Гепавіста Детокс по 1 таблетці 2 рази на добу протягом 45 днів.
Усім хворим проводилося клінічне, лабораторне й інструментальне обстеження згідно з протоколом дослідження до та після прийому комплексного засобу. Вираженість клінічних симптомів оцінювалась у балах (0 балів — відсутній, 1 бал — мінімальний, 2 бали — помірний, 3 бали — виражений).
Для оцінки цитолітичного синдрому вимірювали активність аланінамінотрансферази (АЛТ), аспартат–амінотрансферази (АСТ), уміст загального білірубіну і співвідношення його фракцій у сироватці крові. Холестатичний синдром характеризував уміст лужної фосфатази (ЛФ), γ-глутамілтранспептидази (ГГТ) і білірубіну. Активність АЛТ, АСТ, ЛФ, ГГТ сироватки крові визначали методом ультрафіолетової кінетики, рекомендованим Міжнародною федерацією клінічної хімії (IFCC), згідно з інструкціями до наборів фірми EliTech (Франція). Активність АЛТ визначали методом ALT/GPT, АСТ — AST/GOT. Концентрацію загального білірубіну і його фракцій у сироватці крові досліджували фотоколориметричним діазометодом за Єндрашиком, Клеггорном, Грофом.
З метою неінвазивної оцінки ступеня стеатозу та стадії фіброзу печінки у хворих виконано стеатометрію — дослідження коефіцієнта затухання амплітуди ультразвуку (КЗАУ), а також зсувнохвильову еластографію з визначенням показника жорсткості паренхіми печінки — модуля Юнга.
Для виконання ЗХЕ та стеатометрії використовувався ультразвуковий сканер Soneus P7 (Ultrasign, Україна, Швейцарія). Для оцінки стадії фіброзу застосовувався конвексний датчик 3,5–7,0 МГц, інформація оброблялась у режимі реального часу. Аналіз стадіювання фіброзу проводили за шкалою Metavir (Castera et al., 2008), результат оцінювали так: відсутній фіброз (F0) — до 5,8 кПа, 1 стадія фіброзу (F1) — 5,9–7,0 кПа, 2 стадія (F2) — 7,1–9,5 кПа, при 9,6–12,5 кПа діагностували 3 стадію фіброзу печінки (F3), понад 12,5 — 4 стадію фіброзу печінки (F4), тобто цироз печінки [15]. Оцінку ступеня стеатозу печінки за результатами стеатометрії виконували за шкалою САР (Sasso M. et al., 2012), яка валідизована з морфологічною шкалою: показник S0 відповідав нормі (частка гепатоцитів із жиром становить від 0 до 5 %: від 1,0 до 2,19 дБ/см), S1 вказував на легкий ступінь стеатозу (частка гепатоцитів із жиром становить від 5,1 до 33 %: від 2,20 до 2,29 дБ/см), S2 відповідав помірному ступеню стеатозу (частка гепатоцитів із жиром становить від 33,1 до 66 %: від 2,30 до 2,90 дБ/см), S3 свідчив про тяжкий ступінь стеатозу (частка гепатоцитів із жиром становить понад 66 %: > 2,90 дБ/см) [16].
Статистичну обробку проводили за допомогою програмного забезпечення Statistica 6.1. Перевірка відповідності розподілу кількісних ознак нормальному закону проводилася за критерієм Шапіро — Уїлка, перевірка гіпотези про рівність дисперсій — за тестом Левена. Для опису кількісних даних використовувалися середня арифметична (M) і стандартна похибка середньої величини (m). Для порівняння безперервних даних до та після лікування використовували критерій Стьюдента (t) для залежних вибірок, для якісних показників — критерій Мак-Немара. Для аналізу взаємозв’язку між ознаками використовували кореляційний аналіз із розрахунком коефіцієнтів кореляції Пірсона (r).
Результати та обговорення
При оцінці клінічної симптоматики встановлено, що у хворих до лікування домінувала локалізація болю в правому підребер’ї (46,7 % пацієнтів). Приблизно в кожного четвертого-п’ятого пацієнта спостерігався біль в епігастрії та лівому підребер’ї (табл. 1). У процесі лікування в переважної більшості пацієнтів больовий синдром був усунений. Наприкінці лікування лише у 2 пацієнтів був наявний больовий синдром (в 1 — в епігастрії та правому підребер’ї, в 1 — у лівому підребер’ї).
Хоча вираженість больових відчуттів у хворих на МАСХП до лікування була незначною, становлячи в середньому від 1,70 до 1,88 бала, більшість з тих, хто скаржився на біль, визначали його як помірний, що відповідав 2 балам (рис. 1).
Після лікування в середньому больовий синдром минав у пацієнтів через 7–11 днів від початку лікування (табл. 2).
При аналізі диспептичного синдрому встановлено, що до початку лікування найчастіше хворі скаржилися на здуття живота (64,4 %), сухість у роті (42,2 %), гіркоту в роті (35,6 %), печію (33,3 %). На фоні лікування препаратом Гепавіста Детокс відзначалася суттєва позитивна динаміка: лише в 1 пацієнта залишилася гіркота в роті, решту симптомів хворі після лікування не відзначали. Виняток становила лише непереносимість молочних продуктів — цей симптом, звісно, залишився і після лікування (рис. 2).
Вираженість диспептичних симптомів у балах у хворих на МАСХП до лікування була незначною (в діапазоні 1,33–1,82). Після лікування диспептичні прояви в середньому зникали в пацієнтів через 5–14 днів після початку лікування (табл. 3).
Печінка була збільшена до лікування на 1 см у 29 (64,4 %) хворих, після лікування в 10 пацієнтів печінка повернулася до нормальних розмірів, у 19 залишилася збільшеною на 1 см. У 8 (17,8 %) хворих до лікування печінка була збільшена на 2 см, після лікування у 3 відзначено зменшення її розмірів до нормальних, у 5 пацієн–тів вона була збільшена на 1 см.
При аналізі лабораторних показників встановлено, що до початку лікування в пацієнтів з МАСХП спостерігалося статистично значуще підвищення активності трансаміназ: активність АЛТ становила (50,04 ± 3,75) од/л, що значно перевищувало показник контрольної групи (29,80 ± 5,73 од/л, p < 0,05); рівень АСТ становив (35,33 ± 2,69) од/л проти контрольного значення (23,44 ± 3,15) од/л, p < 0,05 (табл. 4). Отже, синдром цитолізу був загалом наявний у групі хворих на МАСХП, які були залучені до дослідження.
Після курсу лікування комплексним засобом Гепавіста Детокс було зафіксовано статистично значуще зниження активності як АЛТ — до (33,73 ± 3,60) од/л (p < 0,001), так і АСТ — до (23,93 ± 1,58) од/л (p < 0,001). При цьому рівні активності АЛТ та АСТ після лікування наблизилися до показників контрольної групи.
Рівень АЛТ понад 40 од/л до лікування діагностовано в 33 (73,3 %) хворих, після лікування — в 11 (24,4 %). У 22 з 33 (66,7 %) пацієнтів після лікування цей показник відповідав нормі. Загалом у 34 (75,6 %) пацієнтів мало місце зниження АЛТ у динаміці лікування.
Рівень АСТ понад 35 од/л до лікування діагностовано у 21 (46,7 %) хворого, після лікування — у 5 (11,1 %). У 16 з 21 (76,2 %) пацієнта цей показник після лікування був у діапазоні норми. Загалом у 30 (66,7 %) пацієнтів мало місце зниження АСТ у динаміці лікування.
Синдром холестазу був суттєво менше виражений у залучених хворих, ніж синдром цитолізу. Середній рівень ЛФ до лікування ((86,84 ± 3,69) од/л) був у межах норми. Середній рівень ГГТ до лікування ((51,00 ± 3,44) од/л) був вірогідно вищим від показників контрольної групи, але все ж таки не був суттєво підвищеним.
У підсумку лікування середній рівень ГГТ вірогідно знизився до (39,32 ± 2,57) од/л. До лікування в 11 (24,4 %) хворих відзначалося перевищення нормальних показників ГГТ, після лікування — у 5 з 11 (45,5 %) цей показник повернувся до нормальних значень. Загалом у 31 (68,9 %) пацієнта мало місце зниження ГГТ у динаміці лікування.
Рівень ЛФ суттєво не змінювався в процесі лікування ((88,29 ± 3,66) од/л) і залишився в межах нормального діапазону. Підвищення ЛФ понад референтні значення до лікування спостерігали в 7 (15,6 %) випадках, після лікування — у 6 (13,3 %) випадках.
На рис. 3 показана частота випадків перевищення референтних значень показників цитолізу і холестазу у хворих на МАСХП у динаміці лікування. Як видно з рисунка, у підсумку лікування підвищення печінкових показників понад норму спостерігалося лише в 11,1–24,4 % хворих, тобто менше ніж у кожного четвертого пацієнта.
Рівень загального білірубіну в пацієнтів як до лікування ((10,85±0,81) мкмоль/л), так і після нього ((10,88 ± 0,79) мкмоль/л) знаходився в межах норми і не демонстрував статистично значущих змін (p > 0,05).
Загалом зниження рівнів АЛТ та АСТ є одним з найважливіших показників ефективності лікування МАСХП: зменшення АЛТ (p < 0,001) та АСТ (p < 0,001) після лікування до рівнів, порівнянних з даними контрольної групи, може свідчити про зменшення активності некрозапального процесу в печінці. Це є ключовим терапевтичним досягненням, що вказує на регресування пошкодження гепатоцитів.
Для оцінки ступеня стеатозу та стадії фіброзу печінки у хворих виконано стеатометрію з визначенням КЗАУ, а також ЗХЕ з оцінкою показника жорсткості паренхіми печінки — модуля Юнга.
На початку лікування ступені стеатозу розподілилися таким чином: S2 і S3 були відповідно у 24 (53,3 %) і 21 (46,7 %). Отже, у всіх пацієнтів, залучених до дослідження, на початку виявлявся щонайменше другий ступінь стеатозу печінки.
Вираженість ступеня стеатозу після лікування знизилась. Максимальний ступінь стеатозу S3 після лікування спостерігався лише в 4 (8,9 %) пацієнтів, що на 37,8 % нижче, ніж до лікування (рис. 4). У 35 (77,8 %) пацієнтів після лікування визначено ступінь стеатозу S2, отже, на 24,5 % збільшилася кількість пацієнтів з менш тяжкими формами стеатозу, а в 6 (13,3%) пацієнтів після лікування було виявлено вже перший ступінь стеатозу S1 (рис. 4).
Значення КЗАУ — показника стеатометрії — мало вірогідну позитивну динаміку, а саме: спостерігали зниження КЗАУ в середньому на 6 % (р < 0,001) — з (2,85 ± 0,03) дБ/см до (2,68 ± 0,03) дБ/см (табл. 5).
За результатами кореляційного аналізу встановлено прямий зв’язок між рівнем АЛТ і КЗАУ (r = 0,492; р = 0,0007), що подано на рис. 5.
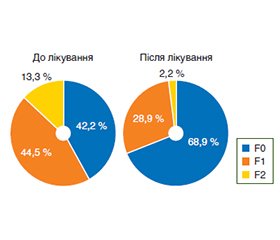
За даними зсувнохвильової еластографії печінки до лікування майже з однаковою частотою відзначено відсутність фіброзу (F0) в 19 (42,2 %) випадках і першу стадію фіброзу (F1) у 20 (44,5 %) випадках (рис. 6). Друга стадія фіброзу (F2) діагностована в 6 (13,3%) хворих, F3 і F4 у жодному випадку не реєструвалися.
Проте після лікування вже в переважної більшості — 31 (68,9 %) пацієнта — фіброз був відсутній; перша стадія фіброзу (F1) реєструвалась у 13 (28,9 %) пацієнтів, друга (F2) виявлена лише в одного хворого (2,2 %).
При аналізі показника жорсткості паренхіми печінки спостерігали зменшення модуля Юнга в середньому на 7,4 % (р < 0,05) — з (5,97 ± 0,16) кПа до (5,53 ± 0,11) кПа (табл. 5).
Встановлено пряму кореляцію між рівнем АСТ і модулем Юнга — показником жорсткості печінки за даними ЗХЕ (r = 0,519; р = 0,0003), що подано на рис. 7.
Отже, як показали результати ЗХЕ печінки, призначення комплексного засобу Гепавіста Детокс в обстежуваних хворих приводить до зменшення КЗАУ і жорсткості печінки. Максимальний ступінь стеатозу S3 після лікування спостерігався лише в 4 (8,9 %) пацієнтів, що на 37,8 % нижче, ніж у групі до лікування. У 57,8 % хворих на МАСХП до терапії був діагностований фіброз печінки, у той час як після лікування він спостерігався лише в третини хворих.
Висновки
1. На фоні лікування комплексним засобом Гепавіста Детокс відзначається позитивна динаміка клінічної симптоматики, особливо це може стосуватися таких ознак, як біль у правому підребер’ї, гіркота й сухість у роті, гепатомегалія.
2. Застосування комплексного засобу Гепавіста Детокс зменшило показники ураження клітин печінки та прояви цитолізу. Після курсу лікування комплексним засобом Гепавіста Детокс було зафіксовано статистично значуще зниження як АЛТ — до (33,73 ± 3,60) од/л (p < 0,001), так і АСТ — до (23,93 ± 1,58) од/л (p < 0,001); у процесі лікування зниження АЛТ спостерігалось у 75,6 % пацієнтів, а зниження АСТ — у 66,7 %. У підсумку лікування середній рівень ГГТ вірогідно знизився до (39,32 ± 2,57) од/л (p < 0,05).
3. Після курсу лікування засобом Гепавіста Детокс відзначена позитивна динаміка нормалізації структури печінки. Оцінка стану печінки відповідно до даних зсувнохвильової еластографії та стеатометрії на фоні терапії виявила, що показник жорсткості (модуль Юнга) зменшився на 7,0 % — з (5,97 ± 0,16) кПа до (5,53 ± 0,11) кПа (р < 0,05), показник накопичення жиру (КЗАУ) знизився в середньому на 6,0 % — з (2,85 ± 0,03) дБ/см до (2,68 ± 0,03) дБ/см (р < 0,001).
Підсумовуючи, слід наголосити, що МАСХП є поширеною патологією, що має складний патогенетичний механізм, у якому задіяні дисрегуляторні метаболічні, токсичні й оксидативні впливи на клітини печінки. Застосування комплексних гепатопротекторних препаратів, що містять природні амінокислоти, зокрема аденозилметіонін і глутатіон, з можливим впливом на патогенетичні складові є важливим і перспективним у лікуванні даної патології.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів і власної фінансової зацікавленості при підготовці даної статті.
Внесок авторів. Степанов Ю.М. — концепція та дизайн дослідження; Будзак І.Я. — аналіз та обговорення отриманих даних, оформлення статті; Горбунцова В.І. — клінічний відбір і ведення хворих; Бочаров Г.І. — аналіз та обговорення отриманих даних; Кленіна І.А. — виконання лабораторних досліджень; Кислова Р.М. — виконання інструментальних досліджень; Петішко О.П. — створення електронної бази даних, статистична обробка матеріалу.
Отримано/Received 23.09.2025
Рецензовано/Revised 07.11.2025
Прийнято до друку/Accepted 20.11.2025
/13.jpg)
/14_2.jpg)
/15_2.jpg)

/12.jpg)
/13_2.jpg)
/14.jpg)
/15.jpg)