Журнал "Гастроэнтерология" Том 59, №4, 2025
Вернуться к номеру
Мікробіота кишечника та коротколанцюгові жирні кислоти у хворих із постковідною імунною відповіддю
Авторы: V.I. Didenko, I.A. Klenina, O.M. Tatarchuk, O.P. Petishko
State Institution “Institute of Gastroenterology of the National Academy of Medical Sciences of Ukraine”, Dnipro, Ukraine
Рубрики: Гастроэнтерология
Разделы: Клинические исследования
Версия для печати
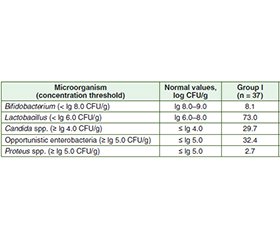
Актуальність. Кишкова мікробіота та її метаболіти істотно впливають на перебіг захворювань печінки. Пандемія COVID-19 зумовила зростання кількості пацієнтів із метаболічно-асоційованою стеатотичною хворобою печінки (МАСХП), перебіг якої ускладнюється дисбалансом мікробіоти. Мета: оцінити особливості кількісного та якісного складу товстокишкової мікробіоти та її метаболітів при МАСХП в осіб з імунною відповіддю до SARS-CoV-2. Матеріали та методи. У дослідження було включено 112 пацієнтів — 75 (66,9 %) чоловіків та 37 (33,1 %) жінок із МАСХП віком від 18 до 73 років (середній показник (46,4 ± 1,5) року). В усіх хворих за допомогою імуноферментного методу оцінювали рівні IgG, специфічного до SARS-CoV-2. Визначення коротколанцюгових жирних кислот у калі проводили на хроматографі за методикою Guohua Zhao. Видовий та кількісний склад мікрофлори товстої кишки досліджували методом посіву десятикратних розведень (10–¹–10–⁹) на стандартний набір елективних і диференційно-діагностичних поживних середовищ для виділення аеробних та анаеробних мікроорганізмів. Результати. В осіб із МАСХП з імунною відповіддю на SARS-CоV-2 спостерігаються зміни якісного й кількісного складу мікрофлори товстої кишки з переважанням дисбіозу ІІ ступеня в групі пацієнтів з імунною відповіддю, які хворіли на CОVID-19, та І ступеня в тих, у кого не було CОVID-19. У пацієнтів, які перехворіли на CОVID-19, встановлено більш глибокі зміни: зниження концентрації біфідо- (у 28,3 %) і лактобактерій (у 71,7 % випадків), підвищення частоти виявлення умовно-патогенних ентеробактерій. Висновки. В осіб із метаболічно-асоційованою стеатотичною хворобою печінки та імунною відповіддю до SARS-CoV-2 виявлено суттєві порушення кишкового мікробіоценозу й дисбаланс коротколанцюгових жирних кислот. Отримані результати підкреслюють важливість ранньої діагностики та корекції мікробіоти кишечника як складової терапевтичної стратегії в цій категорії хворих.
Background. The intestinal microbiota and its metabolites play a pivotal role in the progression of liver diseases. The COVID-19 pandemic has led to a growing number of patients with metabolic-associated steatotic liver disease (MASLD), the course of which is often complicated by microbiota imbalance, acting as a key factor in hepatic metabolic and inflammatory alterations. The purpose was to assess the quantitative and qualitative composition of colonic microbiota and its metabolites in patients with metabolic-associated steatotic liver disease and immune response to SARS-CoV-2. Materials and methods. A total of 112 patients, 75 men (66.9 %) and 37 women (33.1 %), with MASLD aged 18–73 years (mean age (46.4 ± 1.5) years) were examined. The serum level of SARS-CoV-2-specific IgG antibodies was determined using the enzyme-linked immunosorbent assay. The concentration of short-chain fatty acids in feces was measured by gas chromatography. The quantitative and species composition of colonic microbiota was studied by tenfold serial dilution (10–1–10–9) using standard elective and differential diagnostic media for the isolation of aerobic and anaerobic microorganisms. Results. Patients with MASLD and immune response to SARS-CoV-2 demonstrated pronounced alterations in the intestinal microbiota profile. Grade II dysbiosis predominated in patients who had COVID-19 and grade I dysbiosis predominated in those without a history of infection. In post-COVID-19 patients, deeper disturbances were revealed, including a decrease in Bifidobacterium (28.3 %) and Lactobacillus (70.0 %) concentrations and a higher detection rate of conditionally pathogenic Enterobacteriaceae. Conclusions. Patients with MASLD and immune response to SARS-CoV-2 exhibit significant intestinal microbiota dysbiosis and imbalance of short-chain fatty acids. These findings emphasize the importance of early diagnosis and targeted correction of gut microbiota as an integral component of therapeutic strategies in this patient population.
метаболічно-асоційована стеатотична хвороба печінки; мікробіом кишечника; коротколанцюгові жирні кислоти; дисбіоз; SARS-CoV-2
metabolic-associated steatotic liver disease; intestinal microbiome; short-chain fatty acids; dysbiosis; SARS-CoV-2
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Wang L, Cao ZM, Zhang LL, Li JM, Lv WL. The Role of Gut Microbiota in Some Liver Diseases: From an Immunological Perspective. Front Immunol. 2022 Jul 13;13:923599. doi: 10.3389/fimmu.2022.923599.
- Jaworska K, Koper M, Ufnal M. Gut microbiota and renin-angiotensin system: a complex interplay at local and systemic levels. Am J Physiol Gastrointest Liver Physiol. 2021 Oct 1;321(4):G355-G366. doi: 10.1152/ajpgi.00099.2021.
- Scarlata GGM, Morano D, Ismaiel A, Spagnuolo R, Luzza F, et al. Gut Microbiota Changes in Metabolic Dysfunction-Associated Steatohepatitis and Inflammatory Bowel Disease: Common Pathogenic Features. Curr Issues Mol Biol. 2025 Oct 15;47(10):847. doi: 10.3390/cimb47100847.
- Ohtani N, Kamiya T, Kawada N. Recent updates on the role of the gut-liver axis in the pathogenesis of NAFLD/NASH, HCC, and beyond. Hepatol Commun. 2023 Aug 28;7(9):e0241. doi: 10.1097/HC9.0000000000000241.
- Stepanov Y, Didenko V, Klenina I, Tatarchuk O, Petishko O. Metabolic abnormalities in patients with non-alcoholic fatty liver disease with immune response to SARS-CoV-2. Gastroenterology. 2024;58(1):25-30. doi: 10.22141/2308-2097.58.1.2024.583.
- Gudan A, Kozłowska-Petriczko K, Wunsch E, Bodnarczuk T, Stachowska E. Small Intestinal Bacterial Overgrowth and Non-Alcoholic Fatty Liver Disease: What Do We Know in 2023? Nutrients. 2023 Mar 8;15(6):1323. doi: 10.3390/nu15061323.
- Gudan A, Jamioł-Milc D, Hawryłkowicz V, Skonieczna-Żydecka K, Stachowska E. The Prevalence of Small Intestinal Bacterial Overgrowth in Patients with Non-Alcoholic Liver Diseases: NAFLD, NASH, Fibrosis, Cirrhosis — A Systematic Review, Meta-Analysis and Meta-Regression. Nutrients. 2022 Dec 9;14(24):5261. doi: 10.3390/nu14245261.
- Durairajan SSK, Singh AK, Saravanan UB, Namachivayam M, Radhakrishnan M, et al. Gastrointestinal Manifestations of SARS-CoV-2: Transmission, Pathogenesis, Immunomodulation, Microflora Dysbiosis, and Clinical Implications. Viruses. 2023 May 24;15(6):1231. doi: 10.3390/v15061231.
- Didenko V, Klenina I, Tatarchuk O, Petishko O. Correlation of immunological and biochemical parameters in patients with chronic diffuse liver diseases depending on the etiological factors of steatosis and liver fibrosis. Gastroenterology. 2021;53(2):115-122. doi: 10.22141/2308-2097.53.2.2019.168985.
- Arab JP, Arrese M, Shah VH. Gut microbiota in non-alcoholic fatty liver disease and alcohol-related liver disease: Current concepts and perspectives. Hepatol Res. 2020 Apr;50(4):407-418. doi: 10.1111/hepr.13473.
- Assimakopoulos SF, Eleftheriotis G, Lagadinou M, Karamouzos V, Dousdampanis P, et al. SARS CoV-2-Induced Viral Sepsis: The Role of Gut Barrier Dysfunction. Microorganisms. 2022 May 19;10(5):1050. doi: 10.3390/microorganisms10051050.
- Guo GJ, Yao F, Lu WP, Xu HM. Gut microbiome and metabolic-associated fatty liver disease: Current status and potential applications. World J Hepatol. 2023 Jul 27;15(7):867-882. doi: 10.4254/wjh.v15.i7.867.
- Vasques-Monteiro IML, Souza-Mello V. Coronavirus di–sease 2019 severity in obesity: Metabolic dysfunction-associated fatty liver disease in the spotlight. World J Gastroenterol. 2021 Apr 28;27(16):1738-1750. doi: 10.3748/wjg.v27.i16.1738.
- Sharma S, Tiwari N, Tanwar SS. The current findings on the gut-liver axis and the molecular basis of NAFLD/NASH associated with gut microbiome dysbiosis. Naunyn Schmiedebergs Arch Pharmacol. 2025 Sep;398(9):11541-11579. doi: 10.1007/s00210-025-04069-z.
- Caliman-Sturdza OA, Hamamah S, Iatcu OC, Lobiuc A, Bosancu A, Covasa M. Microbiome and Long COVID-19: Current Evidence and Insights. Int J Mol Sci. 2025 Oct 17;26(20):10120. doi: 10.3390/ijms262010120.
- Alves MCS, Rego MS, Silva RCCD, Silva RA, Arruda IES, et al. Gut Microbiota and COVID-19: Unraveling the Gut-Lung Axis and Immunomodulatory Therapies. ACS Infect Dis. 2025 Jul 11;11(7):1844-1853. doi: 10.1021/acsinfecdis.5c00250.
- Zhou B, Pang X, Wu J, Liu T, Wang B, Cao H. Gut microbiota in COVID-19: new insights from inside. Gut Microbes. 2023 Jan-Dec;15(1):2201157. doi: 10.1080/19490976.2023.2201157.
- Sencio V, Machelart A, Robil C, Benech N, Hoffmann E, et al. Alteration of the gut microbiota following SARS-CoV-2 infection correlates with disease severity in hamsters. Gut Microbes. 2022 Jan-Dec;14(1):2018900. doi: 10.1080/19490976.2021.2018900.
- Zhang F, Wan Y, Zuo T, Yeoh YK, Liu Q, et al. Prolonged Impairment of Short-Chain Fatty Acid and L-Isoleucine Biosynthesis in Gut Microbiome in Patients With COVID-19. Gastroenterology. 2022 Feb;162(2):548-561.e4. doi: 10.1053/j.gastro.2021.10.013.
- Sajdel-Sulkowska EM. Neuropsychiatric Ramifications of COVID-19: Short-Chain Fatty Acid Deficiency and Disturbance of Microbiota-Gut-Brain Axis Signaling. Biomed Res Int. 2021 Oct 5;2021:7880448. doi: 10.1155/2021/7880448.
- Włodarczyk J, Czerwiński B, Fichna J. Short-chain fatty acids-microbiota crosstalk in the coronavirus disease (COVID-19). Pharmacol Rep. 2022 Dec;74(6):1198-1207. doi: 10.1007/s43440-022-00415-7.
- Mussabay K, Kozhakhmetov S, Dusmagambetov M, Mynzhanova A, Nurgaziyev M, et al. Gut Microbiome and Cytokine Profiles in Post-COVID Syndrome. Viruses. 2024 May 2;16(5):722. doi: 10.3390/v16050722.
- Syrchak ES, Gryga VI, Petrychko OI, Pichkar YI. Effectiveness of Bifidobacterium infantis 35624 in the treatment of patients with non-alcoholic fatty liver disease. Gastroenterology. 2020;54(1):8-17. doi: 10.22141/2308-2097.54.1.2020.199136.
- Xu Y, Yang X, Bian H, Xia M. Metabolic dysfunction associa–ted fatty liver disease and coronavirus disease 2019: clinical relationship and current management. Lipids Health Dis. 2021 Oct 3;20(1):126. doi: 10.1186/s12944-021-01564-z.