Журнал «Травма» Том 27, №1, 2026
Вернуться к номеру
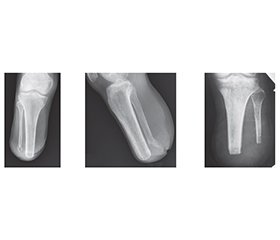
Стресові переломи кісток ампутаційних кукс нижніх кінцівок: клініко-рентгенологічні та морфологічні особливості
Авторы: Безсмертний Ю.О., Бондаренко Д.В., Шевчук В.І., Безсмертна Г.В., Браніцький О.Ю.
Університетська клініка, Вінницький національний медичний університет імені М.І. Пирогова,
м. Вінниця, Україна
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
Актуальність. Стресові переломи кісток ампутаційних кукс нижніх кінцівок є недостатньо вивченим ускладненням протезування, що розвивається на тлі порушеного кісткового ремоделювання та повторюваного механічного навантаження. Мета роботи: дослідити клінічні, рентгенологічні й морфологічні особливості стресових переломів кісток ампутаційних кукс нижніх кінцівок і визначити їх зв’язок із термінами й характером протезування. Матеріали та методи. Обстежено 23 пацієнти віком 21–49 років зі стресовими переломами кісток ампутаційних кукс нижніх кінцівок у різні терміни після протезування. Проведено клінічну оцінку больового синдрому й функції ходи, рентгенологічне дослідження з аналізом стану кортикального шару та трабекулярної архітектоніки, а також морфологічне дослідження кісткової тканини за матеріалами ревізійних оперативних втручань; додатково здійснено аналіз системних і локальних факторів ризику розвитку стресових переломів. Статистичну обробку результатів виконували з використанням параметричних методів, рівень статистичної значущості становив p < 0,05. Результати. Встановлено, що ранні стресові переломи (≤ 4 міс. після протезування) формуються на фоні незавершеного структурно-функціонального формування кукси й активного репаративного остеогенезу та у 72 % випадків виникають протягом перших 2,5 місяця, супроводжуючись помірними порушеннями кортикальної та трабекулярної архітектоніки. Переломи цієї групи локалізувалися переважно в зонах максимального механічного навантаження й анатомічної васкулярної вразливості. Пізні стресові переломи (> 4 міс. після протезування) характеризувалися вираженим остеопорозом, гіперостозом, кістоподібною перебудовою медулярного каналу та грубим порушенням трабекулярної структури, що відображало хронічне патологічне ремоделювання кісткової тканини. Двобічна ампутація асоціювалася з прискореним формуванням стресових переломів незалежно від термінів протезування. Висновки. Стресові переломи ампутаційних кукс нижніх кінцівок є наслідком дисбалансу між процесами кісткового ремоделювання й повторюваним механічним навантаженням. Терміни та якість протезування, біомеханіка ходи, а також поєднання системних і локальних факторів визначають характер і темпи розвитку ушкоджень, що обґрунтовує необхідність індивідуалізованого підходу до протезування та поетапного дозування навантаження.
Background. Stress fractures of amputation stumps of the lower extremities are an understudied complication of prosthesis use that develops against the background of impaired bone remodeling and repeated mechanical stress. Aim: to investigate the clinical, radiological, and morphological features of stress fractures of lower limb amputation stumps and to determine their relationship with the timing and nature of prosthetic rehabilitation. Materials and methods. Twenty-three patients aged 21–49 years with stress fractures of lower limb amputation stumps were examined at various times after prosthetic fitting. A clinical assessment of pain syndrome and gait function was performed, as well as an X-ray examination with analysis of the condition of the cortical layer and trabecular architectonics, morphological examination of bone tissue based on materials from revision surgical interventions. Additionally, an analysis of systemic and local risk factors for stress fractures was performed. Statistical processing of the results was made using parametric methods, with a statistical significance level of p < 0.05. Results. It was found that early stress fractures (≤ 4 months after prosthetic fitting) form against the background of incomplete structural and functional formation of the stump and active reparative osteogenesis; in 72 % of cases, they occur within the first 2.5 months and are accompanied by moderate disturbances in cortical and trabecular architectonics. Fractures in this group were localized mainly in areas of maximum mechanical stress and anatomical vascular vulnerability. Late stress fractures (> 4 months after prosthetic fitting) were characterized by severe osteoporosis, hyperostosis, cystic remodeling of the medullary canal, and gross disruption of the trabecular structure, reflecting chronic pathological remodeling of bone tissue. Bilateral amputation was associated with accelerated formation of stress fractures regardless of the timing of prosthetic replacement. Conclusions. Stress fractures of lower limb amputation stumps are the result of an imbalance between bone remodeling processes and repeated mechanical stress. The timing and quality of prosthesis use, gait biomechanics, and a combination of systemic and local factors determine the nature and rate of damage development, which justifies the need for an individualized approach to prosthetic rehabilitation and a phased load dosage.
стресові переломи; ампутаційна кукса; кісткове ремоделювання; рентгенологічна діагностика; морфологічні зміни; протезування
stress fractures; amputation stump; bone remodeling; radiological diagnosis; morphological changes; prosthesis use