Международный эндокринологический журнал Том 22, №1, 2026
Вернуться к номеру
Метаболізмзалежна ендокринна регуляція експресії гена TMPRSS2 (rs12329760): протеомні мережі та функціональні шляхи взаємодії при COVID-19
Авторы: L. Sydorchuk (1), M. Sokolenko (1), V. Vasiuk (1), V. Dzhuryak (1), A. Gutnitska (2), L. Honcharuk (1), D. Sobko (3), Y. Karavan (1)
(1) - Bukovinian State Medical University, Chernivtsi, Ukraine
(2) - Chernivtsi Medical College, Chernivtsi, Ukraine
(3) - Yuriy Fedkovich Chernivtsi National University, Chernivtsi, Ukraine
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
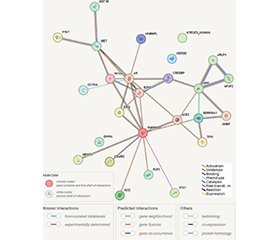
Актуальність. Ген TMPRSS2 кодує трансмембранну серинову протеазу 2, яка відіграє ключову роль у проникненні SARS-CoV-2 у клітину, індивідуальній сприйнятливості до COVID-19 та формуванні клінічних наслідків захворювання. Мета: дослідити протеомну активність, функціональні мережі й основні регуляторні шляхи, пов’язані з поліморфізмом TMPRSS2 rs12329760 у пацієнтів із COVID-19, з акцентом на гормонозалежні та ендокринно-пов’язані регуляторні механізми. Матеріали та методи. У дослідження включено 197 пацієнтів із лабораторно підтвердженим COVID-19, які перебували на стаціонарному лікуванні в закладах центральної України у 2021–2023 роках. Генотипування поліморфізму гена TMPRSS2 (rs12329760) проводили методом полімеразної ланцюгової реакції в реальному часі. Кумулятивну частоту алелів Val160Met C/T поліморфізму TMPRSS2 (rs12329760) у п’яти популяціях визначали на основі даних проєкту 1000 Genomes Project Phase 3 (EMBL-EBI rs12329760). Генотипування виконували з використанням TaqMan®-зондів (FAM — T-алель; VIC — C-алель) на системі CFX96™ Real-Time PCR (Bio-Rad, США). Функціональні зв’язки гена TMPRSS2 (rs12329760) будували за допомогою програми STRING Interaction Network (www.genecards.org). Результати. Встановлено, що частота мутантного C-алеля гена TMPRSS2 (rs12329760) була дещо вищою, ніж у північноамериканських i південноазійських субпопуляціях (p > 0,05), та вірогідно вищою — у 1,5–6 разів — порівняно з південноамериканськими субпопуляціями (p < 0,001). Найтісніші взаємодії та найбільшу кількість зв’язків гена TMPRSS2 (rs12329760) встановлено з такими генами: ACE2, ERG, SPINT2, AR, MYCN. Ідентифіковано п’ять супершляхів взаємодії гена TMPRSS2: ранні етапи інфікування SARS-CoV-2 у взаємодії з 38 генами, основними з яких є ACE2, AGRN, BECN1, CHMP2A, CHMP2B (F = 0,33–0,75); SuperPath-мережу шляхів інфекційних захворювань (F = 0,81); SuperPath-мережу шляхів поширення інфекції SARS-CoV-2 (F = 0,72); мережу шляхів трансляції структурних білків (F = 0,81); SuperPath-мережу шляхів взаємодії між SARS-CoV-1 та організмом хазяїна (F = 0,68). Висновки. Загалом інтеграція популяційно-генетичних даних із протеомними та системно-біологічними підходами підтверджує ключову роль TMPRSS2 як важливого молекулярного чинника патогенезу COVID-19 і обґрунтовує доцільність його подальшого вивчення як потенційного біомаркера та терапевтичної мішені.
Background. The TMPRSS2 gene encodes a transmembrane serine protease 2, which plays a key role in SARS-CoV-2 entry, individual susceptibility to COVID-19, and its clinical outcome. The purpose of this study was to investigate the proteomic activity, functional networks, and major regulatory pathways associated with the TMPRSS2 rs12329760 polymorphism in patients with COVID-19, with emphasis on hormone-dependent and endocrine-related regulatory mechanisms. Materials and methods. We included 197 patients with COVID-19 with confirmed COVID-19, recruited from hospital in central Ukraine from 2021 to 2023. Real-time polymerase chain reaction was used to genotype the polymorphism of the TMPRSS2 (rs12329760) gene. The cumulative frequency of Val160Met C/T alleles of the TMPRSS2 gene polymorphism (rs12329760) in five populations was determined based on data from the 1000 Genomes Project Phase 3 (EMBL-EBI rs12329760). Genotyping was performed using Taqman® probes (FAM — T allele; VIC — C allele) of the CFX96™ Real-Time PCR system (Bio-Rad, USA). Functional linkage of the TMPRSS2 gene (rs12329760) were constructed using the STRING Interaction Network program (www.genecards.org). Results. It was found that the frequency of the mutational C allele of the TMPRSS2 gene (rs12329760) was slightly higher than in the North American and South Asian subpopulations (p > 0.05) and significantly higher — 1.5–6 times — than in South American subpopulations (p < 0.001). The closest interaction and the largest number of linkage of the TMPRSS2 gene (rs12329760) were established with the following genes: ACE2, ERG, SPINT2, AR, MYCN. Five superpathways of TMPRSS2 gene interaction have been identified: early cases of SARS-CoV-2 infection in interaction with 38 genes, the main ones being ACE2, AGRN, BECN1, CHMP2A, CHMP2B (F = 0.33–0.75); SuperPath network of pathways for infectious diseases (F = 0.81); the SuperPath network of SARS-CoV-2 infection spread pathways (F = 0.72); the network of pathways for the translation of structural proteins (F = 0.81); the SuperPath network of interaction pathways between SARS-CoV-1 and the host (F = 0.68). Conclusions. Overall, the integration of population genetics with proteomic and systems biology approaches reinforces the relevance of TMPRSS2 as a critical molecular player in COVID-19 pathogenesis and supports its further exploration as a biomarker and therapeutic target.
метаболізм; ендокринна регуляція; експресія гена TMPRSS2; COVID-19; SARS-CoV-2; протеомна активність; функціональні зв’язки; шляхи взаємодії
metabolism; endocrine regulation; TMPRSS2 gene expression; COVID-19; SARS-CoV-2; proteomic activity; functional relationships; pathways of interaction
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Asselta R, Paraboschi EM, Mantovani A, Duga S. ACE2 and TMPRSS2 variants and expression as candidates to sex and country differences in COVID-19 severity in Italy. Aging (Albany NY). 2020 Jun 5;12(11):10087-10098. doi: 10.18632/aging.103415.
- Paniri A, Hosseini MM, Akhavan-Niaki H. First comprehensive computational analysis of functional consequences of TMPRSS2 SNPs in susceptibility to SARS-CoV-2 among different populations. J Biomol Struct Dyn. 2021 Jul;39(10):3576-3593. doi: 10.1080/07391102.2020.1767690.
- David A, Parkinson N, Peacock TP, Pairo-Castineira E, Khanna T, Cobat A, et al.; GenOMICC Consortium; ISARIC4C Investigators; Casanova JL, Abel L, Barclay WS, Baillie JK, Sternberg MJ. A common TMPRSS2 variant has a protective effect against severe COVID-19. Curr Res Transl Med. 2022 May;70(2):103333. doi: 10.1016/j.retram.2022.103333.
- Irham LM, Chou WH, Calkins MJ, Adikusuma W, Hsieh SL, Chang WC. Genetic variants that influence SARS-CoV-2 receptor TMPRSS2 expression among population cohorts from multiple continents. Biochem Biophys Res Commun. 2020 Aug 20;529(2):263-269. doi: 10.1016/j.bbrc.2020.05.179.
- Sokolenko MO, Sydorchuk LP, Sokolenko LS, Sokolenko AA. General immunologic reactivity of patients with COVID-19 and its relation to gene polymorphism, severity of clinical course of the disease and combination with comorbidities. Medicni Perspektivi. 2024;29(3);108. doi: 10.26641/2307-0404.2024.3.313570 (in Ukrainian).
- De Andrade CC, Silva ATP, Vasconcelos LRS, Oliveira PRS, de Souza CDF, da Costa Armstrong A, do Carmo RF. A Polymorphism in the TMPRSS2 Gene Increases the Risk of Death in Older Patients Hospitalized with COVID-19. Viruses. 2022 Nov 18;14(11):2557. doi: 10.3390/v14112557.
- Hoseinnezhad T, Soltani N, Ziarati S, Behboudi E, Mousavi MJ. The role of HLA genetic variants in COVID-19 susceptibi–lity, severity, and mortality: A global review. J Clin Lab Anal. 2024 Jan;38(1–2):e25005. doi: 10.1002/jcla.25005.
- Sydorchuk L, Sokolenko M, Škoda M, Lajcin D, Vyklyuk Y, Sydorchuk R, et al. Management of Severe COVID-19 Diagnosis Using Machine Learning. Computation. 2025;13:238. doi: 10.3390/computation13100238.
- Wu C, Chen X, Cai Y, Xia J, Zhou X, Xu S, et al. Risk Factors Associated With Acute Respiratory Distress Syndrome and Death in Patients With Corowithrus Disease 2019 Pneumonia in Wuhan, China. JAMA Intern Med. 2020 Jul 1;180(7):934-943. doi: 10.1001/jamainternmed.2020.0994.
- Zguro K, Fallerini C, Fava F, Furini S, Renieri A. Host genetic basis of COVID-19: from methodologies to genes. Eur J Hum Genet. 2022 Aug;30(8):899-907. doi: 10.1038/s41431-022-01121-x.
- Karlsen TH. Understanding COVID-19 through genome-wide association studies. Nat Genet. 2022 Apr;54(4):368-369. doi: 10.1038/s41588-021-00985-x.
- Velavan TP, Pallerla SR, Rüter J, Augustin Y, Kremsner PG, Krishna S, Meyer CG. Host genetic factors determining COVID-19 susceptibility and severity. EBioMedicine. 2021 Oct;72:103629. doi: 10.1016/j.ebiom.2021.103629.
- Davidson AM, Wysocki J, Batlle D. Interaction of SARS-CoV-2 and Other Coronavirus with ACE (Angiotensin-Converting Enzyme)-2 as Their Main Receptor: Therapeutic Implications. Hypertension. 2020 Nov;76(5):1339-1349. doi: 10.1161/HYPERTENSIONAHA.120.15256.
- Mitra P. Inhibiting fusion with cellular membrane system: therapeutic options to prevent severe acute respiratory syndrome coronavirus-2 infection. Am J Physiol Cell Physiol. 2020 Sep 1;319(3):C500-C509. doi: 10.1152/ajpcell.00260.2020.
- Heurich A, Hofmann-Winkler H, Gierer S, Liepold T, Jahn O, Pöhlmann S. TMPRSS2 and ADAM17 cleave ACE2 diffe–rentially and only proteolysis by TMPRSS2 augments entry driven by the severe acute respiratory syndrome coronavirus spike protein. J Virol. 2014 Jan;88(2):1293-307. doi: 10.1128/JVI.02202-13.
- Yaghoobi A, Lord JS, Rezaiezadeh JS, Yekaninejad MS, Amini M, Izadi P. TMPRSS2 polymorphism (rs12329760) and the severity of the COVID-19 in Iranian population. PLoS One. 2023 Feb 16;18(2):e0281750. doi: 10.1371/journal.pone.0281750.
- Monticelli M, Hay Mele B, Benetti E, Fallerini C, Baldassarri M, Furini S, et al.; Gen-Covid Multicenter Study. Protective Role of a TMPRSS2 Variant on Severe COVID-19 Outcome in Young Males and Elderly Women. Genes (Basel). 2021 Apr 19;12(4):596. doi: 10.3390/genes12040596.
- Kim TS, Heinlein C, Hackman RC, Nelson PS. Phenotypic analysis of mice lacking the Tmprss2-encoded protease. Mol Cell Biol. 2006 Feb;26(3):965-75. doi: 10.1128/MCB.26.3.965-975.2006.
- Dong M, Zhang J, Ma X, Tan J, Chen L, Liu S, et al. ACE2, TMPRSS2 distribution and extrapulmonary organ injury in patients with COVID-19. Biomed Pharmacother. 2020 Nov;131:110678. doi: 10.1016/j.biopha.2020.110678.
- Schuler BA, Habermann AC, Plosa EJ, Taylor CJ, Jetter C, Negretti NM, et al.; Vanderbilt COVID-19 Consortium Cohort; Human Cell Atlas Biological Network; Kropski JA, Sucre JM. Age-determined expression of priming protease TMPRSS2 and localization of SARS-CoV-2 in lung epithelium. J Clin Invest. 2021 Jan 4;131(1):e140766. doi: 10.1172/JCI140766.
- Protocol “Provision of medical assistance for the treatment of coronavirus disease (COVID-19)”. Approved by the Order of the Mini–stry of Health of Ukraine of April 2, 2020, No. 762 (as amended by the Order of the Ministry of Health of Ukraine of May 17, 2023, No. 913). Available from: https://www.dec.gov.ua/wp-content/uploads/2023/05/protokol-covid2023.pdf (in Ukrainian).
- Medical care standards “Coronavirus disease (COVID-19)”. Approved by Order No. 722 of the Ministry of Health of Ukraine dated March 28, 2020. Available from: https://www.dec.gov.ua/wp-content/uploads/2021/10/2020_722_standart_covid_19.pdf (in Ukrainian).
- Pashkovska N, Pankiv V, Pashkovska O. COVID-19 and dia–betes mellitus: management of patients during the pandemic. International Journal of Endocrinology (Ukraine). 2020;16(3):180-184. doi: 10.22141/2224-0721.16.3.2020.205264.
- Sokolenko M, Sydorchuk L, Sokolenko A, Sydorchuk R, Kamyshna I, et al. Antiviral Intervention of COVID-19: Linkage of Disease Severity with Genetic Markers FGB (rs1800790), NOS3 (rs2070744) and TMPRSS2 (rs12329760). Viruses. 2025;17(6):792. doi: 10.3390/v17060792.
- Calcagnile M, Damiano F, Lobreglio G, Siculella L, Bozzetti MP, Forgez P, et al. In silico evidence that substitution of glycine for valine (p.G8V) in a common variant of TMPRSS2 isoform 1 increases accessibility to an endocytic signal: Implication for SARS-CoV-2 entry into host cells and susceptibility to COVID-19. Biochimie. 2024 Oct;225:89-98. doi: 10.1016/j.biochi.2024.05.004.
- Lee IH, Lee JW, Kong SW. A survey of genetic variants in SARS-CoV-2 interacting domains of ACE2, TMPRSS2 and TLR3/7/8 across populations. Infect Genet Evol. 2020 Nov;85:104507. doi: 10.1016/j.meegid.2020.104507.
- Hoffmann M, Kleine-Weber H, Schroeder S, et al. SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor. Cell. 2020;181(2):271-280.e8. doi: 10.1016/j.cell.2020.02.052.
- Glowacka I, Bertram S, Müller MA, et al. Evidence that TMPRSS2 activates the SARS-CoV spike protein for membrane fusion and reduces viral control by the humoral immune response. J Virol. 2011;85(9):4122-4134. doi: 10.1128/JVI.02232-10.
- Stopsack KH, Mucci LA, Antonarakis ES, Nelson PS, Kantoff PW. TMPRSS2 and COVID-19: Serine Proteases as Potential Targets for Treatment and Prevention. J Clin Oncol. 2020;38(33):3717-3719. doi: 10.1200/JCO.20.00994.
- Wambier CG, Goren A. SARS-COV-2 infection is likely to be androgen mediated. J Am Acad Dermatol. 2020;83(1):308-309. doi: 10.1016/j.jaad.2020.04.032.