Международный эндокринологический журнал Том 22, №1, 2026
Вернуться к номеру
Можливість нутрицевтичної корекції функціонального стану нирок у пацієнтів з цукровим діабетом 2-го типу
Авторы: Жердьова Н.М. (1), Костіцька І.О. (2), Михальченко В.Г. (1)
(1) - ДНУ «Центр інноваційних медичних технологій НАН України», м. Київ, Україна
(2) - Івано-Франківський національний медичний університет, м. Івано-Франківськ, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
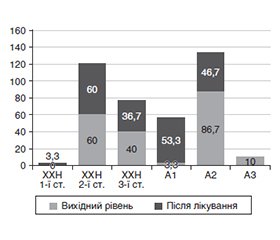
Актуальність. У статті наведені дані щодо можливостей використання нутрицевтичної підтримки у лікуванні хронічної хвороби нирок (ХХН) у пацієнтів з цукровим діабетом 2-го типу, а саме леспедези головчастої та артишоку. Метою нашого дослідження було з’ясувати можливість корекції функціонального стану нирок у пацієнтів з цукровим діабетом 2-го типу за допомогою комбінованого препарату леспедези головчастої та артишоку. Матеріали та методи. У дослідженні взяли участь 30 пацієнтів, із них 18 жінок та 12 чоловіків. Тривалість цукрового діабету 2-го типу — 9,03 ± 1,51 року. Середній рівень глікованого гемоглобіну становив 7,16 ± 0,23 %. Усім пацієнтам проведена оцінка функціонального стану нирок за допомогою розрахункової швидкості клубочкової фільтрації (рШКФ) за рівнем креатиніну (формула CKD-EPI Createnine), а також визначення альбумінурії як співвідношення альбуміну та креатиніну (САК). Як терапію призначили комбінований препарат леспедези головчастої та артишоку по 1 капсулі 2 рази на добу, курс лікування 2 місяці. Результати. Через 2 місяці лікування препаратом Лібера форте відмітили вірогідне поліпшення показника альбумінурії з 212,17 ± 23,20 мг/г до 62,0 ± 14,6 мг/г (р = 0,036), відсутність діагностування стадії А3 і збільшення відсотка пацієнтів зі стадією А1. Також відмітили поліпшення рівня рШКФ з 61,63 ± 2,55 мл/хв/1,73 м2 до 64,57 ± 2,77 мл/хв/1,73 м2 (р = 0,43), але ці дані суттєво не значущі, хоча після лікування у 3,3 % обстежених фіксували нормальні показники рШКФ. Висновки. Вірогідне зниження САК і стабільні показники рШКФ у пацієнтів з цукровим діабетом 2-го типу та ХХН 2-го та 3-го ступеня дають змогу розглядати додавання комбінованого препарату Лібера форте в комплексну терапію як потенційного нефропротектора.
Background. The article presents data on the possibilities of using nutraceutical assistance in the treatment of chronic kidney disease (CKD) in patients with type 2 diabetes mellitus, namely Lespedeza capitata and artichoke. The purpose of our study was to determine the possibility of correcting the functional state of the kidneys in patients with type 2 diabetes mellitus using a combined preparation of Lespedeza capitata and artichoke. Materials and methods. The study involved 30 patients, 18 women and 12 men. The duration of type 2 diabetes mellitus was 9.03 ± 1.51 years. The average level of glycated hemoglobin was 7.16 ± 0.23 %. All patients underwent an assessment of the functional state of the kidneys using the estimated glomerular filtration rate (eGFR) by creatinine level according to the CKD-EPI creatinine equation, as well as the determination of albuminuria as albumin to creatinine ratio (ACR). As a therapy, a 2-month course was prescribed with a combined preparation of Lespedeza capitata and artichoke, 1 capsule 2 times a day. Results. After 2 months of treatment with Libera forte, a significant improvement in albuminuria was noted from 212.17 ± 23.20 mg/g to 62.0 ± 14.6 mg/g (p = 0.036), with no diagnosis of stage A3 after treatment, and an increase in the percentage of patients with stage A1. An improvement in eGFR was also noted from 61.63 ± 2.55 ml/min/1.73 m2 to 64.57 ± 2.77 ml/min/1.73 m2 (p = 0.43), but the data were not significant, although after treatment, 3.3 % of the examined patients had normal eGFR. Conclusions. A significant decrease in ACR and stable eGFR in patients with type 2 diabetes and CKD stages 2 and 3 allow us to consider the inclusion of the combined drug Libera forte in the comprehensive therapy as a potential nephroprotector.
леспедеза головчаста; артишок; альбумінурія; рШКФ; цукровий діабет
Lespedeza capitata; artichoke; albuminuria; estimated glomerular filtration rate; diabetes mellitus
Вступ
Матеріали та методи
Результати та обговорення
/23_2.jpg)
Висновки
- Kovesdy CP. Epidemiology of chronic kidney disease: an update 2022. Kidney Int Suppl (2011). 2022 Apr;12(1):7-11. doi: 10.1016/j.kisu.2021.11.003.
- Prasad R, Jha RK, Keerti A. Chronic Kidney Disease: Its Relationship with Obesity. Cureus. 2022 Oct 21;14(10):e30535. doi: 10.7759/cureus.30535.
- Жердьова Н., Тодуров І., Плегуца О., Степура О., Кирик В. Поширеність хронічної хвороби нирок у пацієнтів із метаболічним синдромом в Україні. Сімейна медицина. Європейські практики. 2025;(3):100-105. https://doi.org/10.30841/2786-720X.3.2025.339915.
- Жердьова Н., Тодуров І., Орлик О., Степура О., Косюхно С., Зенькіна Л. Епідеміологія хронічної хвороби нирок у пацієнтів з цукровим діабетом 2-го типу в Україні. Проблеми ендокринної патології. 2024;81(1):15-20. https://doi.org/10.21856/j-PEP.2024.1.02.
- American Diabetes Association Professional Practice Committee for Diabetes. 9. Pharmacologic Approaches to Glycemic Treatment: Standards of Care in Diabetes-2026. Diabetes Care. 2026 Jan 1;49(Suppl_1):S183-S215. https://doi.org/10.2337/dc26-S009.
- Khan MA, Kassianos AJ, Hoy WE, Alam AK, Healy HG, Gobe GC. Promoting Plant-Based Therapies for Chronic Kidney Di–sease. J Evid Based Integr Med. 2022 Jan-Dec;27:2515690X221079688. doi: 10.1177/2515690X221079688.
- Correction of azotemia in patients with chronic kidney disease. Available from: https://www.researchgate.net/publication/376996981_Correction_of_azotemia_in_patients_with_chronic_kidney_disease [accessed Dec 29 2025].
- Tarbeeva DV, Pislyagin EA, Menchinskaya ES, Berdyshev DV, Kalinovskiy AI, Grigorchuk VP, et al. Polyphenolic Compounds from Lespedeza bicolor Protect Neuronal Cells from Oxidative Stress. Antioxidants (Basel). 2022 Apr 3;11(4):709. doi: 10.3390/antiox11040709.
- Sokolova LK, Belchina JuB, Cymbal TS, Chervjakova SA, Sokolova AM. Use of Lespedeza capitula extract in the complex treatment of chronic kidney disease. Mìžnarodnij endokrinologìčnij žurnal. 2023;19(5):26-32. Ukrainian.
- Kushnirenko SV, Savytska LM, Tykhonenko NO, Markotenko OO. Prospects for the use of standardized Lespedeza capitata extract in children with chronic kidney disease. Modern Рediatrics Ukraine. 2025;6(150):7-12. doi: 10.15574/SP.2025.6(150).712.
- Serebrovska Z, Tolstun D, Sykalo N, Farkhidinov I, Kropyva V, Myhovan S, et al. Synergistic effects of Lespedeza and artichoke extracts in the therapy of chronic kidney disease: mechanisms and perspectives. Kidneys. 2025 Mar 25;14(1):63-70. doi: 10.22141/2307-1257.14.1.2025.499.
- Khaled A, Ahmed E, Mamdouh M, Saad H, Mohamed A, Sobhy M, et al. Natural angiotensin converting enzyme inhibitors: A safeguard against hypertension, respiratory distress syndrome, and chronic kidney diseases. Phytother Res. 2023 Dec;37(12):5464-5472. doi: 10.1002/ptr.7987.
- Kim DB, Unenkhuu B, Kim GJ, Kim SW, Kim HS. Cynarin attenuates LPS-induced endothelial inflammation via upregulation of the negative regulator MKP-3. Anim Cells Syst (Seoul). 2022 May 20;26(3):119-128. doi: 10.1080/19768354.2022.2077438.
- Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2024 Clinical Practice Guideline for the Evalua–tion and Management of Chronic Kidney Disease. Kidney Int. 2024 Apr;105(4S):S117-S314. doi: 10.1016/j.kint.2023.10.018.
- Ko K, Kwon MJ, Ryu S, Woo HY, Park H. Performance Eva–luation of Three URiSCAN Devices for Routine Urinalysis. J Clin Lab Anal. 2016 Sep;30(5):424-30. doi: 10.1002/jcla.21874.

/23.jpg)