Международный эндокринологический журнал Том 22, №1, 2026
Вернуться к номеру
GAS6 як індикатор порушень вуглеводного обміну в пацієнтів з ішемічною серцевою недостатністю та коморбідними метаболічними розладами
Авторы: K.M. Borovyk
Kharkiv National Medical University, Kharkiv, Ukraine
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
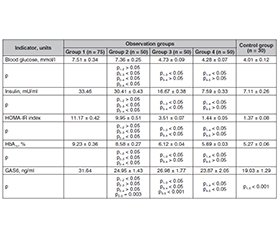
Актуальність. Коморбідний перебіг ожиріння та цукрового діабету 2-го типу (ЦД2) значно погіршує загальний тягар хронічної серцевої недостатності з ішемічною хворобою серця, пришвидшуючи дисфункцію міокарда й дифузний фіброз через хронічне системне запалення. Білок GAS6 виступає ключовим ланцюгом у цьому складному кардіометаболічному континуумі, активно призводячи до інсулінорезистентності шляхом зміни сигналінгу інсулінових рецепторів. Його участь у запаленні та профібротичному каскаді робить оцінку GAS6 значущою для стратифікації ризику. Мета: оцінити та перевірити рівень циркулюючого GAS6 як незалежного показника тяжкості порушень вуглеводного обміну і предиктора несприятливого перебігу хронічної серцевої недостатності в осіб з ішемічною хворобою серця на тлі супутнього цукрового діабету 2-го типу й ожиріння. Матеріали та методи. До дослідження були залучені 225 пацієнтів з ішемічною серцевою недостатністю, розділені на чотири основні групи залежно від поєднання ЦД2 та/або ожиріння, а також контрольна група здорових осіб (n = 30). Рівень GAS6 у сироватці крові визначали імуноферментним методом. Вуглеводний обмін оцінювали за вмістом глюкози, інсуліну, HbA1c та індексом HOMA-IR. Для статистичного аналізу використовували коефіцієнти кореляції (r) із rcrit = 0,39 для оцінки взаємозв’язків. Результати. Пацієнти групи 1 (із супутнім ЦД2 та ожирінням) мали найсерйозніші порушення вуглеводного профілю, включаючи гіперінсулінемію та високий індекс HOMA-IR. Рівень GAS6 також був найвищим у групі 1 (32,03 ± 2,06 нг/мл) та групі 3 (із супутнім ожирінням), значно перевищуючи показник контрольної групи (19,03 ± 1,29 нг/мл) (p < 0,05). Кореляційний аналіз у групі 1 продемонстрував найсильніший позитивний зв’язок між GAS6 та індексом маси тіла (r = 0,68; p < 0,05). Також було виявлено значущі кореляції з рівнем інсуліну (r = 0,49; p < 0,05) та HbA1c (r = 0,43; p < 0,05). Висновки. Наявність ожиріння є ключовим фактором, який активує циркуляцію GAS6 у пацієнтів із хронічною серцевою недостатністю ішемічного генезу. GAS6 діє як потенційний інтегрований біомаркер, що відображає ступінь метаболічного запалення й профібротичної активності. Сильний зв’язок між високим рівнем GAS6 та індексом маси тіла свідчить про його корисність для стратифікації ризику, особливо в пацієнтів з ожирінням.
Background. Comorbid obesity and type 2 diabetes mellitus significantly worsen the global burden of chronic heart failure with coronary artery disease, accelerating myocardial dysfunction and diffuse fibrosis via chronic systemic inflammation. The growth arrest-specific protein 6 (GAS6) acts as a key link in this complex cardiometabolic continuum, actively contributing to insulin resistance by altering insulin receptor signaling. Its involvement in inflammation and the fibrotic cascade makes evaluating GAS6 crucial for risk stratification. The purpose was to evaluate and verify the level of circulating GAS6 as an independent indicator of the severity of carbohydrate metabolism disorders and a predictor of unfavourable course of heart failure in patients with coronary artery disease against the background of concomitant type 2 diabetes mellitus and obesity. Materials and methods. A clinical study was conducted on 225 patients with ischaemic chronic heart failure, divided into four main groups based on the combination of type 2 diabetes and/or obesity, and a healthy control group (n = 30). Serum GAS6 levels were measured using ELISA. Carbohydrate metabolism was assessed by glucose, insulin, HbA1c, and the HOMA-IR index. Statistical analysis utilised correlation coefficients (r) with rcrit = 0.39 to assess relationships. Results. Patients in group 1 (with comorbid type 2 diabetes mellitus and obesity) exhibited the most severe abnormalities in the carbohydrate profile, including hyperinsulinemia and high HOMA-IR. GAS6 levels were highest in group 1 (32.03 ± 2.06 ng/ml) and group 3 (with concomitant obesity), significantly exceeding the control group (19.03 ± 1.29 ng/ml) (p < 0.05). Correlation analysis in group 1 revealed the strongest positive link between GAS6 and body mass index (r = 0.68; p < 0.05). Significant correlations were also found with insulin (r = 0.49; p < 0.05) and HbA1c (r = 0.43; p < 0.05). Conclusions. The presence of obesity is the key factor activating circulating GAS6 in patients with ischaemic chronic heart failure. GAS6 acts as a potential integral biomarker reflecting the degree of metabolic inflammation and profibrotic activity. The strong association between high GAS6 levels, body mass index suggests its utility for risk stratification, particularly in patients with obesity.
хронічна серцева недостатність; ішемічна хвороба серця; цукровий діабет 2-го типу; ожиріння; білок GAS6; вуглеводний обмін
chronic heart failure; coronary artery disease; type 2 diabetes mellitus; obesity; growth arrest-specific protein 6; carbohydrate metabolism
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Shahim B, Kapelios CJ, Savarese G, Lund LH. Global Public Health Burden of Heart Failure: An Updated Review. Card Fail Rev. 2023 Jul 27;9:e11. doi: 10.15420/cfr.2023.05.
- Kang K, Wang Q, Li Y, Liu C, Yu H, Li N. Global and Chinese perspectives on the growing burden of heart failure: trends, gender, and age-related differences (1990–2021) based on GBD 2021 data. BMC Cardiovasc Disord. 2025 Jul 15;25(1):510. doi: 10.1186/s12872-025-04954-8.
- Sulaieva O, Yerokhovych V, Zemskov S, Komisarenko I, Gurianov V, Pankiv V, et al. The impact of war on people with type 2 diabetes in Ukraine: a survey study. EClinicalMedicine. 2024 Dec 15;79:103008. doi: 10.1016/j.eclinm.2024.103008.
- Giraldo-Gonzalez GC, Roman-Gonzalez A, Cañas F, Garcia A. Molecular Mechanisms of Type 2 Diabetes-Related Heart Disease and Therapeutic Insights. Int J Mol Sci. 2025 May 9;26(10):4548. doi: 10.3390/ijms26104548.
- Li Z, Zhao H, Wang J. Metabolism and Chronic Inflammation: The Links Between Chronic Heart Failure and Comorbidi–ties. Front Cardiovasc Med. 2021 May 5;8:650278. doi: 10.3389/fcvm.2021.650278.
- Heidenreich PA, Bozkurt B, Aguilar D, Allen LA, Byun JJ, Colvin MM, et al.; ACC/AHA Joint Committee Members. 2022 AHA/ACC/HFSA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2022 May 3;145(18):e895-e1032. doi: 10.1161/CIR.0000000000001063.
- Rizzi M, Tonello S, D’Onghia D, Sainaghi PP. Gas6/TAM Axis Involvement in Modulating Inflammation and Fibrosis in COVID-19 Patients. Int J Mol Sci. 2023 Jan 4;24(2):951. doi: 10.3390/ijms24020951.
- Law LA, Graham DK, Di Paola J, Branchford BR. GAS6/TAM Pathway Signaling in Hemostasis and Thrombosis. Front Med (Lausanne). 2018 May 9;5:137. doi: 10.3389/fmed.2018.00137.
- Apostolo D, D’Onghia D, Nerviani A, Ghirardi GM, Sola D, Perazzi M, et al. Could Gas6/TAM Axis Provide Valuable Insights into the Pathogenesis of Systemic Sclerosis? Curr Issues Mol Biol. 2024 Jul 15;46(7):7486-7504. doi: 10.3390/cimb46070444.
- Schott C, Germain A, Lacombe J, Pata M, Faubert D, Boulais J, et al. GAS6 and AXL Promote Insulin Resistance by Rewiring Insulin Signaling and Increasing Insulin Receptor Trafficking to Endosomes. Diabetes. 2024 Oct 1;73(10):1648-1661. doi: 10.2337/db23-0802.
- DeBerge M, Glinton K, Subramanian M, Wilsbacher LD, Rothlin CV, Tabas I, Thorp EB. Macrophage AXL receptor tyrosine kinase inflames the heart after reperfused myocardial infarction. J Clin Invest. 2021 Mar 15;131(6):e139576. doi: 10.1172/JCI139576.
- McShane L, Tabas I, Lemke G, Kurowska-Stolarska M, Maffia P. TAM receptors in cardiovascular disease. Cardiovasc Res. 2019 Jul 1;115(8):1286-1295. doi: 10.1093/cvr/cvz100.
- Bellan M, Cittone MG, Tonello S, Rigamonti C, Castello LM, Gavelli F, et al. Gas6/TAM System: A Key Modulator of the Interplay between Inflammation and Fibrosis. Int J Mol Sci. 2019 Oct 12;20(20):5070. doi: 10.3390/ijms20205070.
- Lu B, Huang L, Cao J, Li L, Wu W, Chen X, Ding C. Adipose tissue macrophages in aging-associated adipose tissue function. J Physiol Sci. 2021 Dec 4;71(1):38. doi: 10.1186/s12576-021-00820-2.
- Sahu P, Bestepe F, Vehbi S, Ghanem GF, Blanton RM, Icli B. Obesity and Heart Failure: Mechanistic Insights and the Regulatory Role of MicroRNAs. Genes (Basel). 2025 May 28;16(6):647. doi: 10.3390/genes16060647.
- Chylikova J, Dvorackova J, Tauber Z, Kamarad V. M1/M2 macrophage polarization in human obese adipose tissue. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub. 2018 Jun;162(2):79-82. doi: 10.5507/bp.2018.015.
- Larsen TS, Jansen KM. Impact of Obesity-Related Inflammation on Cardiac Metabolism and Function. J Lipid Atheroscler. 2021 Jan;10(1):8-23. doi: 10.12997/jla.2021.10.1.8.
- John S, Bhowmick K, Park A, Huang H, Yang X, Mishra L. Recent advances in targeting obesity, with a focus on TGF-β signaling and vagus nerve innervation. Bioelectron Med. 2025 Apr 30;11(1):10. doi: 10.1186/s42234-025-00172-x.
- Hsiao FC, Lin YF, Hsieh PS, Chu NF, Shieh YS, Hsieh CH, et al. Circulating growth arrest-specific 6 protein is associated with adiposity, systemic inflammation, and insulin resistance among overweight and obese adolescents. J Clin Endocrinol Metab. 2013 Feb;98(2):E267-74. doi: 10.1210/jc.2012-3179.
- Koval SM, Yushko KO, Snihurska IO, Starchenko TG, Pankiv VI, Lytvynova OM, Mysnychenko OV. Relations of angiotensin-(1–7) with hemodynamic and cardiac structural and functional parameters in patients with hypertension and type 2 diabetes. Arterial Hypertension. 2019;23(3):183-189. doi: 10.5603/AH.a2019.0012.
- Su SC, Chiang CF, Hsieh CH, Lu GH, Liu JS, Shieh YS, et al. Growth arrest-specific 6 modulates adiponectin expression and insulin resistance in adipose tissue. J Diabetes Investig. 2021 Apr;12(4):485-492. doi: 10.1111/jdi.13412.
- Ma T, Huang R, Xu Y, Lv Y, Liu Y, Pan X, et al. Plasma GAS6 predicts mortality risk in acute heart failure patients: insights from the DRAGON-HF trial. J Transl Med. 2023 Jan 12;21(1):21. doi: 10.1186/s12967-022-03859-w.
- Liu H, Lyu YN, Li D, Cui Y, Dai W, Li Y. Association of circulating growth differentiation factor-15, Krüppel-like factor 4 and growth arrest-specific 6 with coronary artery disease. Clin Chim Acta. 2019 Aug;495:630-636. doi: 10.1016/j.cca.2019.05.029.
- Wang X, Chen L, Wei J, Zheng H, Zhou N, Xu X, et al. The immune system in cardiovascular diseases: from basic mechanisms to therapeutic implications. Signal Transduct Target Ther. 2025 May 23;10(1):166. doi: 10.1038/s41392-025-02220-z.
- Petsophonsakul P, Furmanik M, Forsythe R, Dweck M, Schurink GW, Natour E, et al. Role of Vascular Smooth Muscle Cell Phenotypic Switching and Calcification in Aortic Aneurysm Formation. Arterioscler Thromb Vasc Biol. 2019 Jul;39(7):1351-1368. doi: 10.1161/ATVBAHA.119.312787.