Международный эндокринологический журнал Том 22, №1, 2026
Вернуться к номеру
Сироваткові біомаркери (CA 15-3, CEA) та статус гормональних рецепторів як предиктори рецидиву раку молочної залози
Авторы: Muntaha Maddah Al Alouci (1), Fatima Mallallah Mohammed (2), Zainab M. Qassam (2), Osama A. Mohsein (3)
(1) - College of Medicine, University of Anbar, Iraq
(2) - College of Medicine, University of Diyala, Diyala, Iraq
(3) - Thi-Qar Health Directorate, Al-Habboubi Teaching Hospital, Thi-Qar, Iraq
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
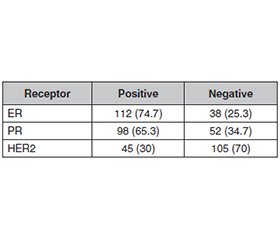
Актуальність. Рак молочної залози є гетерогенним злоякісним новоутворенням і однією з провідних причин смертності, пов’язаної з онкологічними хворобами, серед жінок у всьому світі. Рецидиви залишаються серйозною проблемою довгострокового виживання й ефективного ведення пацієнток. Мета: визначити цінність циркулюючих біомаркерів (CA 15-3 та CEA) і стан гормональних рецепторів (рецептор естрогену (ER), рецептор прогестерону (PR) та рецептор людського епідермального фактора росту-2 (HER2)) для прогнозування рецидиву раку молочної залози, що таким чином розширить можливості діагностики захворювання на ранній стадії та дозволить розробити персоналізовані плани лікування. Матеріали та методи. Вивчено цінність сироваткових біомаркерів CA 15-3 та CEA, а також статус гормональних рецепторів (ER, PR, HER2) щодо прогнозування рецидиву раку молочної залози в перехресному обсерваційному дослідженні, яке проводилося з січня по жовтень 2025 року в клініці Al-Habboubi, Ірак. У нього включені пацієнтки з первинним діагнозом раку молочної залози, підтвердженим гістологічно. Аналіз біомаркерів за допомогою ELISA проводився на зразках крові, а імуногістохімічний аналіз — на зразках пухлини та в сумнівних випадках HER2 за допомогою тесту FISH. Результати. У дослідженні брали участь пацієнтки з раком молочної залози (середній вік 52,3 ± 10,4 року) та здорові жінки контрольної групи (50,8 ± 9,8 року). Хворі мали вищий індекс маси тіла (27,8 ± 4,2 кг/м2 проти 26,5 ± 3,9 кг/м2, P = 0,045) та більше випадків раку молочної залози в родинному анамнезі (26,7 проти 4 %, P < 0,001). Рівні сироваткових CA 15-3 і CEA були вірогідно підвищені в пацієнток (45,6 ± 12,3 Од/мл; 7,8 ± 2,4 нг/мл) порівняно з контрольною групою. Переважали випадки ER+ та PR+, при цьому HER2+ траплявся рідше. Уміст CA 15-3 та CEA корелював із ризиком рецидиву захворювання (r = 0,71, P < 0,001). Висновки. Високі рівні біомаркерів CA 15-3 та CEA, а також негативний статус ER/PR пов’язані зі збільшенням рецидивів раку молочної залози. Це вказує на більш агресивну біологію пухлини й гормональну регуляцію, що може обумовити використання цих біомаркерів у моніторингу й прогнозуваннi прогресування хвороби.
Background. Breast cancer is a heterogenous malignancy and is one of the leading causes of cancer-related mortality in women worldwide. Recurrence as a barrier to long-term survivorship and effective patient management is a formidable challenge. Aim of the study was to determine the prognostic value of circulating biomarkers (CA 15-3 and CEA) and the status of hormone receptors (estrogen receptor (ER), progesterone receptor (PR), and human epidermal growth factor receptor-2 (HER2)) to predict recurrence of breast carcinoma, which will thus expand the diagnostic capacity of the disease in an early stage and guide personalized treatment plans. Materials and methods. The objectives of this study were to assess the predictive capacity of CA 15-3 and CEA serum biomarkers, as well as the hormonal receptor status (ER, PR, HER2) to predict breast cancer recurrence in this cross-sectional observational study, which was carried out in the period of January to October 2025 at Al-Habboubi Teaching Hospital, Iraq. It included female patients with a primary diagnosis of breast cancer that was confirmed by histopathology. ELISA biomarker analysis was performed on blood samples and immunohistochemistry on tumor specimens and equivocal cases of HER2 by FISH. Results. The study included female breast cancer patients (mean age 52.3 ± 10.4 years) and healthy controls (50.8 ± 9.8 years). Patients had higher body mass index (27.8 ± 4.2 vs. 26.5 ± 3.9 kg/m2, P = 0.045) and more family history of breast cancer (26.7 vs. 4 %, P < 0.001). Serum CA 15-3 and CEA levels were significantly elevated in patients (45.6 ± 12.3 U/mL, 7.8 ± 2.4 ng/mL) compared to controls. ER+ and PR+ were predominant, HER2+ was less common. CA 15-3 and CEA correlated strongly with recurrence risk, especially combined (r = 0.71, P < 0.001). Conclusions. High levels of serum CA 15-3 and CEA, as well as negativity on ER/PR are linked to increased recurrence of breast cancer. It indicates more aggressive tumor biology and hormonal regulation that may result in the usage of these biomarkers in the disease progression monitoring and prediction.
рак молочної залози; CA 15-3; CEA; гормональні рецептори; рецидив; біомаркери
breast cancer; CA 15-3; CEA; hormonal receptors; recurrence; biomarkers
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Smolarz B, Nowak AZ, Romanowicz H. Breast Cancer-Epi–demiology, Classification, Pathogenesis and Treatment (Review of Literature). Cancers (Basel). 2022 May 23;14(10):2569. doi: 10.3390/cancers14102569.
- Kim J, Harper A, McCormack V, et al. Global patterns and trends in breast cancer incidence and mortality across 185 countries. Nat Med. 2025;31:1154-1162. doi: 10.1038/s41591-025-03502-3.
- Arnold M, Morgan E, Rumgay H, Mafra A, Singh D, et al. Current and future burden of breast cancer: Global statistics for 2020 and 2040. Breast. 2022 Dec;66:15-23. doi: 10.1016/j.breast.2022.08.010.
- Dyachenko EI, Bel’skaya LV. Salivary Transmembrane Mucins of the MUC1 Family (CA 15-3, CA 27.29, MCA) in Breast Cancer: The Effect of Human Epidermal Growth Factor Receptor 2 (HER2). Cancers (Basel). 2024 Oct 12;16(20):3461. doi: 10.3390/cancers16203461.
- Pandey SN, Babu MA, Ali H, Malathi H, Maharana L, et al. MUC1 as a diagnostic biomarker and siRNA-based therapeutic target in breast cancer: A clinical chemistry perspective. Clin Chim Acta. 2025 Aug 15;576:120387. doi: 10.1016/j.cca.2025.120387.
- Terävä J, Verhassel A, Botti O, Islam MK, Leivo J, et al. Primary breast cancer biomarkers based on glycosylation and extracellular vesicles detected from human serum. Cancer Rep (Hoboken). 2022 Aug;5(8):e1540. doi: 10.1002/cnr2.1540.
- Ojha PS, Maste MM, Tubachi S, Patil VS. Human papillomavirus and cervical cancer: an insight highlighting pathogenesis and targeting strategies. Virusdisease. 2022 Jun;33(2):132-154. doi: 10.1007/s13337-022-00768-w.
- Min YL, Gong YX, Zhu PW, Lin Q, Li B, et al. CEA as a risk factor in predicting ocular metastasis from colorectal cancer. J Cancer. 2020 Jan 1;11(1):51-56. doi: 10.7150/jca.31196.
- Sahlolbei M, Dehghani M, Kheiri Yeghane Azar B, Vafaei S, Roviello G, et al. Evaluation of targetable biomarkers for chimeric antigen receptor T-cell (CAR-T) in the treatment of pancreatic cancer: a systematic review and meta-analysis of preclinical studies. Int Rev Immunol. 2020;39(5):223-232. doi: 10.1080/08830185.2020.1776274.
- Li Y, Yang D, Yin X, Zhang X, Huang J, et al. Clinicopatho–logical Characteristics and Breast Cancer-Specific Survival of Patients With Single Hormone Receptor-Positive Breast Cancer. JAMA Netw Open. 2020 Jan 3;3(1):e1918160. doi: 10.1001/jamanetworkopen.2019.18160.
- Clusan L, Ferrière F, Flouriot G, Pakdel F. A Basic Review on Estrogen Receptor Signaling Pathways in Breast Cancer. Int J Mol Sci. 2023 Apr 6;24(7):6834. doi: 10.3390/ijms24076834.
- Segovia-Mendoza M, Morales-Montor J. Immune Tumor Microenvironment in Breast Cancer and the Participation of Estrogen and Its Receptors in Cancer Physiopathology. Front Immunol. 2019 Mar 1;10:348. doi: 10.3389/fimmu.2019.00348.
- Fu Y, Li H. Assessing Clinical Significance of Serum CA15-3 and Carcinoembryonic Antigen (CEA) Levels in Breast Cancer Patients: A Meta-Analysis. Med Sci Monit. 2016 Sep 6;22:3154-62. doi: 10.12659/msm.896563.
- Ghabra S, Chang D, Sugarbaker PH. Preoperative tumor marker elevations in colorectal cancer patients with peritoneal metastases should be used to help select patients for cytoreductive surgery. Eur J Surg Oncol. 2025 Jun;51(6):109720. doi: 10.1016/j.ejso.2025.109720.
- Zaakouk M, Quinn C, Provenzano E, Boyd C, Callagy G, et al. Concordance of HER2-low scoring in breast carcinoma among expert pathologists in the United Kingdom and the republic of Ireland — on behalf of the UK national coordinating committee for breast patho–logy. Breast. 2023 Aug;70:82-91. doi: 10.1016/j.breast.2023.06.005.
- Bertozzi S, Londero AP, Diaz Nanez JA, et al. Breast cancer care for the aging population: a focus on age-related disparities in breast cancer treatment. BMC Cancer. 2025;25:492. doi: 10.1186/s12885-025-13893-8.
- Lee K, Kruper L, Dieli-Conwright CM, Mortimer JE. The Impact of Obesity on Breast Cancer Diagnosis and Treatment. Curr Oncol Rep. 2019 Mar 27;21(5):41. doi: 10.1007/s11912-019-0787-1.
- Sun L, Zhu Y, Qian Q, Tang L. Body mass index and prognosis of breast cancer: An analysis by menstruation status when breast cancer diagnosis. Medicine (Baltimore). 2018 Jun;97(26):e11220. doi: 10.1097/MD.0000000000011220.
- Durham DD, Abraham LA, Roberts MC, Khan CP, Smith RA, et al. Breast cancer incidence among women with a family history of breast cancer by relative’s age at diagnosis. Cancer. 2022 Dec 15;128(24):4232-4240. doi: 10.1002/cncr.34365.
- Braithwaite D, Miglioretti DL, Zhu W, Demb J, Trentham-–Dietz A, et al.; Breast Cancer Surveillance Consortium. Family History and Breast Cancer Risk Among Older Women in the Breast Cancer Surveillance Consortium Cohort. JAMA Intern Med. 2018 Apr 1;178(4):494-501. doi: 10.1001/jamainternmed.2017.8642.
- Ryu JM, Kang D, Cho J, Lee JE, Kim SW, et al. Prognostic Impact of Elevation of Cancer Antigen 15-3 (CA15-3) in Patients with Early Breast Cancer With Normal Serum CA15-3 Level. J Breast Cancer. 2023 Apr;26(2):126-135. doi: 10.4048/jbc.2023.26.e17.
- Fakhari A, Gharepapagh E, Dabiri S, Gilani N. Correlation of cancer antigen 15-3 (CA15-3) serum level and bony metastases in breast cancer patients. Med J Islam Repub Iran. 2019 Dec 19;33:142. doi: 10.34171/mjiri.33.142.
- Pacheco JG, Silva MSV, Freitas M, Nouws HPA, Delerue-–Matos C. Molecularly imprinted electrochemical sensor for the point-of-care detection of a breast cancer biomarker (CA 15-3). Sensors and Actuators B: Chemical. 2018;256:905-912. doi: 10.1016/j.snb.2017.10.027.
- Li J, Liu L, Feng Z, Wang X, Huang Y, et al. Tumor markers CA15-3, CA125, CEA and breast cancer survival by molecular subtype: a cohort study. Breast Cancer. 2020 Jul;27(4):621-630. doi: 10.1007/s12282-020-01058-3.
- Zhao W, Li X, Wang W, Chen B, Wang L, et al. Association of Preoperative Serum Levels of CEA and CA15-3 with Molecular Subtypes of Breast Cancer. Dis Markers. 2021 Sep 27;2021:5529106. doi: 10.1155/2021/5529106.
- Nam SE, Lim W, Jeong J. et al. The prognostic significance of preoperative tumor marker (CEA, CA15-3) elevation in breast cancer patients: data from the Korean Breast Cancer Society Registry. Breast Cancer Res Treat. 2019;177:669-678. doi: 10.1007/s10549-019-05357-y.
- Zahraa Mohammed Al-Nafakh, Arshad Noori G. Al-Dujaili, Ammar Rasoul Mohammed Rudha. Assessment of cancer embryonic antigen (CEA) biomarker in women with breast cancer disease. AIP Conference Proceedings. 2020;2290(1). doi: 10.1063/5.0029114.
- Hao C, Zhang G, Zhang L. Serum CEA levels in 49 different types of cancer and noncancer diseases. Prog Mol Biol Transl Sci. 2019;162:213-227. doi: 10.1016/bs.pmbts.2018.12.011.
- Cui Q, Dai L, Li J, Xue J. Accuracy of CEUS-guided sentinel lymph node biopsy in early-stage breast cancer: a study review and meta-analysis. World J Surg Oncol. 2020 May 29;18(1):112. doi: 10.1186/s12957-020-01890-z.
- Umadevi K, Sundeep D, Latha AM, et al. Enhancement of Diagnostic Accuracy in Endometrial Carcinoma using CW-THz Spectroscopy. Indian J Gynecol Oncolog. 2024;22:100. doi: 10.1007/s40944-024-00872-3.
- Chen H, Gui X, Zhou Z, Su F, Gong C, et al. Distinct ER and PR expression patterns significantly affect the clinical outcomes of early HER2-positive breast cancer: A real-world analysis of 871 patients treated with neoadjuvant therapy. Breast. 2024 Jun;75:103733. doi: 10.1016/j.breast.2024.103733.
- Wu X, Zhang W, Lu X, et al. Prognostic significance of ER-to-PR difference in ER+/HER2-early breast cancer. Sci Rep. 2024;14:24431. doi: 10.1038/s41598-024-74608-w.
- Arena V, Pennacchia I, Vecchio FM, Carbone A. ER-/PR+/HER2-breast cancer type shows the highest proliferative activity among all other combined phenotypes and is more common in young patients: Experience with 6643 breast cancer cases. Breast J. 2019 May;25(3):381-385. doi: 10.1111/tbj.13236.
- Uygur MM, Gümüş M. The utility of serum tumor markers CEA and CA 15-3 for breast cancer prognosis and their association with clinicopathological parameters. Cancer Treat Res Commun. 2021;28:100402. doi: 10.1016/j.ctarc.2021.100402.
- Bae SY, Lim W, Jeong J, Lee S, Choi J, et al. 276P. The prognostic significance of preoperative tumour marker (CEA, CA15-3) elevation in breast cancer patients. Annals of Oncology. 2019;30(5):mdz240.099. doi: 10.1093/annonc/mdz240.099.
- Riis CL, Bechmann T, Jensen PT, Coulter A, Steffensen KD. Are patient-reported outcomes useful in post-treatment follow-up care for women with early breast cancer? A scoping review. Patient Relat Outcome Meas. 2019 Mar 27;10:117-127. doi: 10.2147/PROM.S195296.
- Walters SJ, Jacques RM, Dos Anjos Henriques-Cadby IB, Candlish J, Totton N, Xian MTS. Sample size estimation for randomised controlled trials with repeated assessment of patient-reported outcomes: what correlation between baseline and follow-up outcomes should we assume? Trials. 2019 Sep 13;20(1):566. doi: 10.1186/s13063-019-3671-2.