Международный эндокринологический журнал Том 22, №1, 2026
Вернуться к номеру
Відмінності гормональних та імунологічних параметрів залежно від якості сперми
Авторы: Asmahan Adnan Al-Naqeeb, Suzan Ibraim Bajilan, Salwa Ghazi Turki
College of Nursing, University of Baghdad, Iraq
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
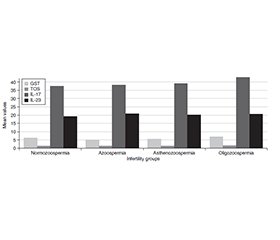
Актуальність. Надмірна кількість активних форм кисню в спермі може призвести до чоловічої безплідності. Їх певні фізіологічні концентрації необхідні для багатьох природних процесів, як-от дозрівання сперматозоїдів, реакція між акросомами та запліднення. Мета: з’ясувати, яким був рівень глутатіон-S-трансферази (GST), загального оксидантного статусу людини (TOS), інтерлейкіну (IL) 17 та IL-23 у сім’яній плазмі різних груп безплідних чоловіків, а також дослідити роль цих факторів у виникненні чоловічого безпліддя. Матеріали та методи. Дослідження було проведено для визначення деяких патофізіологічних механізмів у чоловічій репродуктивній ендокринології. У ньому взяли участь дев’яносто чоловіків віком від 20 до 60 років, які звернулися до High Institute of Infertility Diagnosis and Assisted Reproductive Technology при Al-Nahrain University (Ірак) у період з січня до листопада 2024 року. Пацієнтів було розділено на групи залежно від кількості сперматозоїдів: 9 осіб мали азооспермію, 31 — астенозооспермію, 21 — нормозооспермію та 29 — олігозооспермію. Для вимірювання рівнів GST, TOS, IL-17 та IL-23 у сім’яній рідині використовували метод імуноферментного аналізу. Результати. Концентрація GST при олігозооспермії була вірогідно вищою за таку при азооспермії та астенозооспермії. У той же час TOS в осіб з олігозооспермією показав вірогідне збільшення порівняно з іншими групами безплідних чоловіків. Що стосується інтерлейкінів, єдині статистичні відмінності спостерігалися щодо рівня IL-17 при олігозооспермії порівняно з нормозооспермією та астенозооспермією. У той же час не виявлено суттєвих відмінностей у показниках IL-23. Висновки. Оцінка активності GST у сперматозоїдах безплідних чоловіків може сприяти визначенню їхньої фертильності та встановленню ефективності антиоксидантів при цій патології. Результати показують, що IL-17 змінює властивості сім’яної рідини, що, у свою чергу, впливає на репродуктивну здатність. Він пов’язаний із запаленням та інфекцією в яєчках та інших чоловічих статевих органах і може бути мішенню для лікування в цих ситуаціях.
Background. Too many reactive oxygen species in the sperm can make men unable to have children. Certain physiological concentrations of reactive oxygen species are needed for many natural processes, such as the maturation of sperm, the response between acrosomes, and the fertilization. The purpose of this study was to find out how much glutathione S-transferase (GST), human total oxidant status (TOS), interleukin (IL) 17, and IL-23 were present in seminal plasma from different groups of infertile men and to look into the roles that these factors play in male infertility. Materials and methods. This study was done to fill in some of the gaps in male reproductive endocrinology. Ninety male patients between the ages of 20 and 60 who went to the High Institute of Infertility Diagnosis and Assisted Reproductive Technology at Al-Nahrain University between January and November 2024 were part of this study. They were divided into groups based on the number of sperm they had: 9 azoospermic men, 31 asthenozoospermic men, 21 normozoospermic men, and 29 oligozoospermic men. Enzyme-linked immunosorbent assay was used to measure the amounts of GST, human TOS, IL-17, and IL-23 in the seminal fluid. Results. The concentration of GST in oligozoospermia was significantly the highest when compared to the azoospermia and asthenozoospermia. Meanwhile, the TOS in oligozoospermia men revealed a significant increase versus other infertile groups. In respect to the interleukins, the only significant statistical changes have been observed in IL-17 level in oligozoospermia compared to normozoospermia and asthenozoospermia. At the same time, no significant differences were found in IL-23. Conclusions. Checking the activity of GST in the sperm cells of men who can’t have children may help with figuring out their fertility and seeing how well antioxidants work as a cure. The results show that IL-17 changes the properties of seminal fluid, which in turn affects a man’s ability to have children. It is linked to inflammation and infection in the testis and other male genital organs, and it could be a good target for treatment in these situations.
чоловіча репродуктивна ендокринологія; безпліддя; якість сперми; оксидантний стрес; глутатіон-S-трансфераза; вісь інтерлейкін-17/23
male reproductive endocrinology; infertility; semen quality; oxidative stress; glutathione S-transferase; interleukin-17/23 axis
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Patki A, Shelatkar R, Singh M, Agarwal S, Venugopal M, Umbardand S, et al. Impact of antioxidants in improving semen parameters like count, motility and DNA fragmentation in sub-fertile males: a randomized, double-blind, placebo-controlled clinical trial. Transl Clin Pharmacol. 2023 Mar;31(1):28-39. doi: 10.12793/tcp.2023.31.e6.
- Palani A, Alahmar A. Impact of oxidative stress on semen parameters in normozoospermic infertile men: a case-control study. Afr J Urol. 2020;26:50. doi: 10.1186/s12301-020-00061-6.
- Pahune PP, Choudhari AR, Muley PA. The total antioxidant power of semen and its correlation with the fertility potential of human male subjects. J Clin Diagn Res. 2013 Jun;7(6):991-5. doi: 10.7860/JCDR/2013/4974.3040.
- Ross C, Morriss A, Khairy M, Khalaf Y, Braude P, Coomarasamy A, El-Toukhy T. A systematic review of the effect of oral antioxidants on male infertility. Reprod Biomed Online. 2010 Jun;20(6):711-23. doi: 10.1016/j.rbmo.2010.03.008.
- Alnasser SM. The role of glutathione S-transferases in human disease pathogenesis and their current inhibitors. Genes Dis. 2024 Dec 5;12(4):101482. doi: 10.1016/j.gendis.2024.101482.
- Fafula RV, Paranyak NM, Besedina AS, Vorobets DZ, Iefremova UP, Onufrovych OK, Vorobets ZD. Biological Significance of Glutathione S-Transferases in Human Sperm Cells. J Hum Reprod Sci. 2019 Jan-Mar;12(1):24-28. doi: 10.4103/jhrs.JHRS_106_18.
- Fafula RV, Onufrovych OK, Iefremova UP, Melnyk OV, Nakonechnyi IA, Vorobets DZ, Vorobets ZD. Glutathione content in sperm cells of infertile men. Regulatory Mechanisms in Biosystems. 2017;8(2):157-161. doi: 10.15421/021725.
- Paira DA, Silvera-Ruiz S, Tissera A, Molina RI, Olmedo JJ, Rivero VE, Motrich RD. Interferon γ, IL-17, and IL-1β impair sperm motility and viability and induce sperm apoptosis. Cytokine. 2022 Apr;152:155834. doi: 10.1016/j.cyto.2022.155834.
- Elsaied AA, Ibrahim HM, Hegazy EM, Wahip MR. Serum and seminal plasma level of interleukin-17 in infertile patients. SVU Int J Med Sci. 2024;7(1):119-126. doi: 10.21608/SVUIJM.2020.47546.1017.
- García-Domínguez M. The Role of IL-23 in the Development of Inflammatory Diseases. Biology (Basel). 2025 Mar 27;14(4):347. doi: 10.3390/biology14040347.
- Scriffignano S, Perrotta FM, Lubrano E. Male Fertility in Spondyloarthritis: from Clinical Issues to Cytokines Milieu. A Narrative Review. Curr Rheumatol Rep. 2024 Sep;26(9):321-331. doi: 10.1007/s11926-024-01153-w.
- Björndahl L, Kirkman Brown J; other Editorial Board Members of the WHO Laboratory Manual for the Examination and Processing of Human Semen. The sixth edition of the WHO Laboratory Manual for the Examination and Processing of Human Semen: ensuring quality and standardization in basic examination of human ejaculates. Fertil Steril. 2022 Feb;117(2):246-251. doi: 10.1016/j.fertnstert.2021.12.012.
- Kim HY. Statistical notes for clinical researchers: post-hoc multiple comparisons. Restor Dent Endod. 2015 May;40(2):172-6. doi: 10.5395/rde.2015.40.2.172.
- Brandt JS, Cruz Ithier MA, Rosen T, Ashkinadze E. Advanced paternal age, infertility, and reproductive risks: A review of the lite–rature. Prenat Diagn. 2019 Jan;39(2):81-87. doi: 10.1002/pd.5402.
- Durairajanayagam D. Lifestyle causes of male infertility. Arab J Urol. 2018 Feb 13;16(1):10-20. doi: 10.1016/j.aju.2017.12.004.
- Anifandis G, Bounartzi T, Messini CI, Dafopoulos K, Soti–riou S, Messinis IE. The impact of cigarette smoking and alcohol consumption on sperm parameters and sperm DNA fragmentation (SDF) measured by Halosperm®. Arch Gynecol Obstet. 2014 Oct;290(4):777-82. doi: 10.1007/s00404-014-3281-x.
- Aboulmaouahib S, Madkour A, Kaarouch I, Sefrioui O, Saadani B, Copin H, et al. Impact of alcohol and cigarette smoking consumption in male fertility potential: Looks at lipid peroxidation, enzymatic antioxidant activities and sperm DNA damage. Andrologia. 2018 Apr;50(3). doi: 10.1111/and.12926.
- Hanson BM, Aston KI, Jenkins TG, Carrell DT, Hotaling JM. The impact of ejaculatory abstinence on semen analysis parameters: a systematic review. J Assist Reprod Genet. 2018 Feb;35(2):213-220. doi: 10.1007/s10815-017-1086-0.
- Ahmed A, Bello A, Mbibu NH, Maitama HY, Kalayi GD. Epidemiological and aetiological factors of male infertility in northern Nigeria. Niger J Clin Pract. 2010 Jun;13(2):205-9.
- Serour GI. Medical and socio-cultural aspects of infertility in the Middle East. ESHRE Monographs. 2008;1:34-41. doi: 10.1093/humrep/den143.
- Maduro MR, Lo KC, Chuang WW, Lamb DJ. Genes and male infertility: what can go wrong? J Androl. 2003 Jul-Aug;24(4):485-93. doi: 10.1002/j.1939-4640.2003.tb02697.x.
- Fallara G, Capogrosso P, Pozzi E, Belladelli F, Corsini C, Boeri L, et al. The Effect of Varicocele Treatment on Fertility in Adults: A Systematic Review and Meta-analysis of Published Prospective Trials. Eur Urol Focus. 2023 Jan;9(1):154-161. doi: 10.1016/j.euf.2022.08.014.
- Aydemir B, Onaran I, Kiziler AR, Alici B, Akyolcu MC. Increased oxidative damage of sperm and seminal plasma in men with idiopathic infertility is higher in patients with glutathione S-transfe–rase Mu-1 null genotype. Asian J Androl. 2007 Jan;9(1):108-15. doi: 10.1111/j.1745-7262.2007.00237.x.
- Mazari AMA, Zhang L, Ye ZW, Zhang J, Tew KD, Town–send DM. The Multifaceted Role of Glutathione S-Transferases in Health and Disease. Biomolecules. 2023 Apr 18;13(4):688. doi: 10.3390/biom13040688.
- Ebisch IM, Peters WH, Thomas CM, Wetzels AM, Peer PG, Steegers-Theunissen RP. Homocysteine, glutathione and related thiols affect fertility parameters in the (sub)fertile couple. Hum Reprod. 2006 Jul;21(7):1725-33. doi: 10.1093/humrep/del081.
- Wu W, Lu J, Tang Q, Zhang S, Yuan B, Li J, et al. GSTM1 and GSTT1 null polymorphisms and male infertility risk: an updated meta-analysis encompassing 6934 subjects. Sci Rep. 2013;3:2258. doi: 10.1038/srep02258.
- Chengyong W, Man Y, Mei L, Liping L, Xuezhen W. GSTM1 null genotype contributes to increased risk of male infertility: a meta-analysis. J Assist Reprod Genet. 2012 Aug;29(8):837-45. doi: 10.1007/s10815-012-9790-2.
- Demir M, Ozdem S. Evaluation of total antioxidant capacity in human seminal plasma. Int J Med Biochem. 2022; 5(1): 54-59. doi: 10.14744/ijmb.2021.30092.
- Imani M, Raad MV, Afsari M. et al. Effects of adverse semen parameters on total oxidation status and DNA/chromatin integrity. Afr J Urol. 2023;29:44. doi: 10.1186/s12301-023-00377-z.
- Babinets LS, Migenko BO, Borovyk IO, Halabitska IM, Lobanets NV, Onyskiv OO. The role of cytocin imbalance in the development of man infertility. Wiad Lek. 2020;73(3):525-528.
- Duan YG, Yu CF, Novak N, Bieber T, Zhu CH, Schuppe HC, et al. Immunodeviation towards a Th17 immune response associa–ted with testicular damage in azoospermic men. Int J Androl. 2011 Dec;34(6 Pt 2):e536-45. doi: 10.1111/j.1365-2605.2010.01137.x.
- Hekim N, Gure MA, Metin Mahmutoglu A, Gunes S, Asci R, Henkel R. SNP’s in xenobiotic metabolism and male infertility. Xenobiotica. 2020 Mar;50(3):363-370. doi: 10.1080/00498254.2019.1616850.
- Yu B, Huang Z. Variations in Antioxidant Genes and Male Infertility. Biomed Res Int. 2015;2015:513196. doi: 10.1155/2015/513196.