Международный эндокринологический журнал Том 22, №1, 2026
Вернуться к номеру
Зв’язок нових та класичних адипокінів сироватки з інсулінорезистентністю, вісцеральним ожирінням та метаболічним ризиком у дорослих середнього віку: перехресне дослідження
Авторы: Abeer Ameen Mustafa, Rafal Mustafa Tuama, Marwa Abdulsalam Kader
Biology Department, College of Science, Tikrit University, Tikrit, Iraq
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
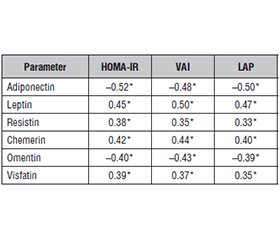
Актуальність. Адипокіни, що синтезуються жировою тканиною, визнані важливими регуляторами метаболічних процесів, включно з чутливістю до інсуліну та розподілом жиру. Хоча традиційні адипокіни (наприклад, адипонектин, лептин, резистин) ретельно досліджені, роль нових адипокінів (хемерин, оментин, вісфатин) щодо метаболічного ризику та вісцерального ожиріння залишається неясною, особливо в людей середнього віку. Мета: вивчити кореляції між концентраціями класичних і нових адипокінів у сироватці крові й інсулінорезистентністю, вісцеральним ожирінням та метаболічним ризиком у людей середнього віку. Матеріали та методи. З листопада 2024 року до вересня 2025 року в лікарні Tikrit Teaching Hospital (Ірак) проведено перехресне обсерваційне дослідження. Загалом було залучено 350 добровольців віком від 35 до 60 років: 250 осіб із метаболічними порушеннями та 100 здорових людей контрольної групи. Проводили антропометричні вимірювання, визначали артеріальний тиск, рівень глюкози натще, інсуліну, ліпідний профіль та адипокіни. Для розрахунку вісцерального жиру використовували індекс вісцерального ожиріння (VAI) та коефіцієнт накопичення ліпідів (LAP). Модель HOMA-IR застосовано для оцінки ступеня інсулінорезистентності людини. Рівень адипокінів вимірювали за допомогою імуноферментного аналізу. Результати. У пацієнтів спостерігалися вірогідно вищий індекс маси тіла, окружність талії, рівень глюкози натще, інсуліну, HOMA-IR, тригліцеридів та прозапальних адипокінів (лептин, резистин, хемерин, вісфатин), із нижчими рівнями адипонектину й оментину порівняно з контрольною групою. Адипонектин та оментин негативно корелювали з HOMA-IR, VAI та LAP, тоді як лептин, резистин, хемерин і вісфатин показали позитивну кореляцію (p < 0,05). Висновки. Як традиційні, так і нові адипокіни суттєво корелюють з інсулінорезистентністю й вісцеральним ожирінням. Ці біомаркери можуть функціонувати як значні ознаки метаболічного ризику в людей середнього віку та потенційні мішені для раннього втручання.
Background. Adipokines, synthesized by adipose tissue, are recognized as essential regulators of metabolic processes, including insulin sensitivity and fat distribution. While traditional adipokines (e.g., adiponectin, leptin, resistin) have been thoroughly investigated, the role of novel adipokines (e.g., chemerin, omentin, visfatin) concerning metabolic risk and visceral adiposity remains unclear, particularly in middle-aged populations. The purpose of the study was to examine the correlations between serum concentrations of classical and novel adipokines and insulin resistance, visceral adiposity, and metabolic risk in middle-aged individuals. Materials and methods. A cross-sectional observational investigation was conducted at Tikrit Teaching Hospital from November 2024 to September 2025. A total of 350 volunteers aged 35 to 60 years were recruited, consisting of 250 individuals with metabolic disorders and 100 healthy controls. We looked at anthropometric measurements, blood pressure, fasting glucose, insulin, lipid profile, and adipokine levels. The visceral adiposity index (VAI) and the lipid storage product (LAP) were used to measure visceral fat. The HOMA-IR model was used to figure out how insulin-resistant someone was. Enzyme-linked immunosorbent assay was utilized to measure adipokine levels. Results. Patients exhibited significantly higher body mass index, waist circumference, fasting glucose, insulin, HOMA-IR, triglycerides, and pro-inflammatory adipokines (leptin, resistin, chemerin, visfatin), with lower adiponectin and omentin compared to controls. Adiponectin and omentin negatively correlated with HOMA-IR, VAI, and LAP, while leptin, resistin, chemerin, and visfatin showed positive correlations (p < 0.05). Conclusions. Both traditional and novel adipokines significantly correlate with insulin resistance and visceral adiposity. These biomarkers may function as significant signs of metabolic risk in middle-aged adults and prospective targets for early intervention.
адипокіни; інсулінорезистентність; вісцеральне ожиріння; метаболічний синдром; люди середнього віку
adipokines; insulin resistance; visceral adiposity; metabolic syndrome; middle-aged adults
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Booth A, Magnuson A, Fouts J, Foster MT. Adipose tissue: an endocrine organ playing a role in metabolic regulation. Horm Mol Biol Clin Investig. 2016 Apr 1;26(1):25-42. doi: 10.1515/hmbci-2015-0073.
- Didushko OM, Herych PR, Cherniavska IV, Yatsyshyn RI, Pankiv VI. Influence of the complex treatment of hypothyroidism on the leptin level in patients with primary hypothyroidism. World of Medicine and Biology. 2018;3(65):59-63. doi: 10.26724/2079-8334-2018-3-65-59-63.
- Mitrovic B, Gluvic ZM, Obradovic M, Radunovic M, Rizzo M, Banach M, Isenovic ER. Non-alcoholic fatty liver disease, metabolic syndrome, and type 2 diabetes mellitus: where do we stand today? Arch Med Sci. 2022 Jun 3;19(4):884-894. doi: 10.5114/aoms/150639.
- Mongraw-Chaffin M, Hairston KG, Hanley AJG, Tooze JA, Norris JM, Palmer ND, et al. Association of Visceral Adipose Tissue and Insulin Resistance with Incident Metabolic Syndrome Independent of Obesity Status: The IRAS Family Study. Obesity (Silver Spring). 2021 Jul;29(7):1195-1202. doi: 10.1002/oby.23177.
- Hayden MR. Overview and New Insights into the Metabolic Syndrome: Risk Factors and Emerging Variables in the Development of Type 2 Diabetes and Cerebrocardiovascular Disease. Medicina (Kaunas). 2023 Mar 13;59(3):561. doi: 10.3390/medicina59030561.
- Rusdiana R, Moradi A, Widjaja SS, Daulay MH, Rusmalawaty R. The Assessment Metabolic Markers and Cardio Risk Index Among Controlled and Uncontrolled Type 2 Diabetic Patients in Primary Health Clinics in Medan City, North Sumatera, Indonesia: Cross-sectional Study. Acta Inform Med. 2022 Sep;30(3):201-204. doi: 10.5455/aim.2022.30.201-204.
- Różańska-Walędziak A, Walędziak M. Unraveling the Complexity of Metabolic Disorders Through Biomarkers: A Focus on Obesity and Type 2 Diabetes Mellitus. Biomedicines. 2025 Oct 7;13(10):2443. doi: 10.3390/biomedicines13102443.
- Luo L, Liu M. Adipose tissue in control of metabolism. J Endocrinol. 2016 Dec;231(3):R77-R99. doi: 10.1530/JOE-16-0211.
- Hemat Jouy S, Mohan S, Scichilone G, Mostafa A, Mahmoud AM. Adipokines in the Crosstalk between Adipose Tissues and Other Organs: Implications in Cardiometabolic Diseases. Biomedicines. 2024 Sep 19;12(9):2129. doi: 10.3390/biomedicines12092129.
- Zorena K, Jachimowicz-Duda O, Ślęzak D, Robakowska M, Mrugacz M. Adipokines and Obesity. Potential Link to Metabo–lic Disorders and Chronic Complications. Int J Mol Sci. 2020 May 18;21(10):3570. doi: 10.3390/ijms21103570.
- Koval SM, Yushko KO, Snihurska IO, Starchenko TG, Pankiv VI, Lytvynova OM, Mysnychenko OV. Relations of angiotensin-(1-7) with hemodynamic and cardiac structural and functional parameters in patients with hypertension and type 2 diabetes. Arterial Hypertension. 2019;23(3):183-189. doi: 10.5603/AH.a2019.0012.
- Datta S, Koka S, Boini KM. Understanding the Role of Adipokines in Cardiometabolic Dysfunction: A Review of Current Knowledge. Biomolecules. 2025 Apr 23;15(5):612. doi: 10.3390/biom15050612.
- Yoon MJ, Lee GY, Chung JJ, Ahn YH, Hong SH, Kim JB. Adiponectin increases fatty acid oxidation in skeletal muscle cells by sequential activation of AMP-activated protein kinase, p38 mitogen-activated protein kinase, and peroxisome proliferator-activated receptor alpha. Diabetes. 2006 Sep;55(9):2562-70. doi: 10.2337/db05-1322.
- Wang LH, Liu YC, Hou JS, Wu DA, Hsu BG. Hypoadiponectemia is associated with metabolic syndrome in patients with type 2 diabetes. Int J Clin Exp Pathol. 2017 Oct 1;10(10):10515-10521.
- Błażejewska W, Dąbrowska J, Michałowska J, Bogdański P. The Role of Adiponectin and ADIPOQ Variation in Metabolic Syndrome: A Narrative Review. Genes (Basel). 2025 Jun 10;16(6):699. doi: 10.3390/genes16060699.
- Kusters CD, Paul KC, Lu AT, Ferrucci L, Ritz BR, Bin–der AM, Horvath S. Higher testosterone and testosterone/estradiol ratio in men are associated with better epigenetic estimators of mortality risk. medRxiv. 2023 Jul 30:2023.02.16.23285997. doi: 10.1101/2023.02.16.23285997.
- Pataky MW, Young WF, Nair KS. Hormonal and Meta–bolic Changes of Aging and the Influence of Lifestyle Modifications. Mayo Clin Proc. 2021 Mar;96(3):788-814. doi: 10.1016/j.mayocp.2020.07.033.
- Esfahani M, Movahedian A, Baranchi M, Goodarzi MT. Adiponectin: an adipokine with protective features against metabolic syndrome. Iran J Basic Med Sci. 2015 May;18(5):430-42.
- Pedro WJS, Barbosa Júnior FV, Alves FNBR, Braga LV, Alves LR, Afonso JPR, et al. Role of Adipokines Chemerin, Visfatin, and Omentin in Obesity and Their Inflammatory and Metabolic Implications. Biomedicines. 2025 Sep 23;13(10):2321. doi: 10.3390/biomedicines13102321.
- Barth S, Klein P, Horbach T, Dötsch J, Rauh M, Rascher W, Knerr I. Expression of neuropeptide Y, omentin and visfatin in visceral and subcutaneous adipose tissues in humans: relation to endocrine and clinical parameters. Obes Facts. 2010 Aug;3(4):245-51. doi: 10.1159/000319508.
- Nway NC, Sitticharoon C, Chatree S, Maikaew P. Correlations between the expression of the insulin sensitizing hormones, adiponectin, visfatin, and omentin, and the appetite regulatory hormone, neuropeptide Y and its receptors in subcutaneous and visceral adipose tissues. Obes Res Clin Pract. 2016 May-Jun;10(3):256-63. doi: 10.1016/j.orcp.2015.05.007.
- Hu W, Zhu H, Gong F. Leptin and leptin resistance in obesity: current evidence, mechanisms and future directions. Endocr Connect. 2025 Sep 29;14(9):e250521. doi: 10.1530/EC-25-0521.
- Saad MF, Damani S, Gingerich RL, Riad-Gabriel MG, Khan A, Boyadjian R, et al. Sexual dimorphism in plasma leptin concentration. J Clin Endocrinol Metab. 1997 Feb;82(2):579-84. doi: 10.1210/jcem.82.2.3739.
- Rosenbaum M, Pietrobelli A, Vasselli JR, Heymsfield SB, Leibel RL. Sexual dimorphism in circulating leptin concentrations is not accounted for by differences in adipose tissue distribution. Int J Obes Relat Metab Disord. 2001 Sep;25(9):1365-71. doi: 10.1038/sj.ijo.0801730.
- Schwartz DR, Lazar MA. Human resistin: found in translation from mouse to man. Trends Endocrinol Metab. 2011 Jul;22(7):259-65. doi: 10.1016/j.tem.2011.03.005.
- Helfer G, Wu QF. Chemerin: a multifaceted adipokine involved in metabolic disorders. J Endocrinol. 2018 Aug;238(2):R79-R94. doi: 10.1530/JOE-18-0174.
- Imiela AM, Stępnicki J, Zawadzka PS, Bursa A, Pruszczyk P. Chemerin as a Driver of Cardiovascular Diseases: New Perspectives and Future Directions. Biomedicines. 2025 Jun 16;13(6):1481. doi: 10.3390/biomedicines13061481.
- Palomba S, Seminara G, Costanzi F, Caserta D, Aversa A. Chemerin and Polycystic Ovary Syndrome: A Comprehensive Review of Its Role as a Biomarker and Therapeutic Target. Biomedicines. 2024 Dec 16;12(12):2859. doi: 10.3390/biomedicines12122859.
- Abdalla MMI. Role of visfatin in obesity-induced insulin resistance. World J Clin Cases. 2022 Oct 26;10(30):10840-10851. doi: 10.12998/wjcc.v10.i30.10840.
- Alnowihi SM, Al Doghaither HA, Osman NN. Serum visfatin concentration and its relationship with sex hormones in obese Saudi women. Int J Health Sci (Qassim). 2020 May-Jun;14(3):9-13.
- Sitticharoon C, Nway NC, Chatree S, Churintaraphan M, Boonpuan P, Maikaew P. Interactions between adiponectin, visfatin, and omentin in subcutaneous and visceral adipose tissues and serum, and correlations with clinical and peripheral metabolic factors. Peptides. 2014 Dec;62:164-75. doi: 10.1016/j.peptides.2014.10.006.
- Martin LJ, Mahaney MC, Almasy L, MacCluer JW, Blangero J, Jaquish CE, Comuzzie AG. Leptin’s sexual dimorphism results from genotype by sex interactions mediated by testosterone. Obes Res. 2002 Jan;10(1):14-21. doi: 10.1038/oby.2002.3.