Вступ
Протягом останнього десятиріччя з’явилися переконливі докази нейропротекторних властивостей Церебролізину, що пояснюють його багаторівневий вплив як на патологічний каскад пошкодження, так і на процеси відновлення в подальшому [1, 2].
Церебролізин® — препарат з доведеною нейротрофічною дією, який використовується в клінічній практиці для відновлення неврологічних функцій пацієнтів з деменцією, які перенесли інсульт або черепно-мозкову травму [3–7]. Застосування Церебролізину вірогідно зменшує неврологічний дефіцит, покращує когнітивні здібності, зменшує об’єм зони інфаркту при інсульті [5, 8–11]. Церебролізин® чинить органоспецифічну мультимодальну дію на головний мозок, тобто забезпечує метаболічну регуляцію, нейропротекцію, функціональну нейромодуляцію та нейротрофічну активність [9, 12]. Церебролізин® захищає нейрони від пошкоджуючої дії лактацидозу, запобігає утворенню вільних радикалів [13, 14], підвищує виживання і запобігає загибелі ней–ронів в умовах гіпоксії та ішемії, послаблює пошкоджуючу нейротоксичну дію глутамату як збуджувальної амінокислоти [15].
Пластичність головного мозку, що залежить від цілісності структури і функції, базується на таких процесах, як ангіогенез, нейрогенез, гліогенез і синаптогенез [16, 17]. Рання втрата синапсів розглядається як патерн анатомічного процесу денервації та відтворюється в експериментальних умовах на тваринах. Так, можливість Церебролізину здійснювати вплив на процеси ней–ропротекції та нейропластичності була доведена серією робіт [1, 2, 18, 19] на моделі хвороби Альцгеймера (ХА) у трансгенних мишей за білком — попередником амілоїду (mThy-1-hAPP751 tg). За даними гістохімічних та імунохімічних досліджень, при ХА втрачається 20–42 % пресинаптичних зв’язків [8]. На моделі ХА показано, що Церебролізин® шляхом регуляції синтезу, транспорту білка — попередника амілоїда і відкладення -амілоїда у синапсах здійснює синаптотрофічний ефект, який відіграє першочергову роль у процесах ней–ропластичності, що вкрай важливі в набутті нових навичок і збереженні тих, які вже є [20].
Вплив Церебролізину на процеси нейрогенезу вивчався в культурі нейрональних клітин-попередників і в зубчастій звивині нормальних дорослих щурів [21]. Результати цього дослідження дали підстави вважати, що в патогенезі ХА певну роль відіграє дизрегуляція нейрогенезу в зубчастій звивині та порушення співвідношення в комплексі нейротрофічних факторів, що знаходяться в мікрооточенні клітин — попередників нейронів, тим самим визначаючи, що патологія нейрогенезу є перспективною терапевтичною мішенню при даному захворюванні, а системне введення нейротрофічних факторів може сприяти покращанню когнітивних функцій за рахунок посилення нейрогенезу [22].
З огляду на багатобічний механізм дії Церебролізину, включно з впливом на процеси нейрогенезу, ней–ропластичності та нейропротекції, препарат на даний час має три основних показання для застосування — це інсульт, деменція і травматичні пошкодження головного мозку [7, 11, 23–25].
На сьогодні експериментальна й доказова бази клінічного застосування Церебролізину як хворобомодифікуючого засобу включають результати досліджень, проведених незалежно один від одного різними колективами в багатьох країнах світу [26–28]. Так, на тлі курсового лікування Церебролізином одержано значне покращання когнітивного функціонування (понад 6 балів за шкалою ADAS-cog+ порівняно з групою плацебо на 24-му тижні терапії) і розширення повсякденної активності хворих (за шкалою CIBIC+), причому аналогічні результати спостерігались у підгрупі пацієнтів з початково тяжким когнітивним дефіцитом (≤ 20 балів за шкалою MMSE). Позитивні ефекти препарату прослідковувалися на тлі доброї переносимості лікування [29].
Хоч оксидативний стрес є одним із ключових факторів у патогенезі ХП, терапія, що базується на застосуванні екзогенних антиоксидантів, не виявилася достатньо ефективною. Альтернативною стратегією, що може протистояти пошкоджуючим ефектам вільних радикалів і відновлювати клітинний редокс-баланс, є активація ендогенних антиоксидантних ензимів, присутніх у центральній нервовій системі (ЦНС), таких як супероксиддисмутаза (СОД), каталаза, глутатіонпероксидаза тощо.
Транскрипція цих цитопротекторних білків перебуває під контролем транскрипційного фактора Nrf2, який відіграє провідну роль у регуляції клітинного редокс-статусу і є головним регулятором клітинної відповіді на оксидативний стрес шляхом індукції антиоксидантних і детоксикаційних ферментів і протеїнів [30].
Установлено, що різноманітні активатори Nrf2/ARE сигнального шляху, у тому числі пептиди, демонструють свою ефективність у моделях неврологічних розладів як in vitro, так і in vivo [31]. Ці активатори здійснюють нейропротекторний вплив при МРТР-індукованому паркінсонізмі [32].
Слід вважати, що Церебролізин®, як нейротрофічна пептидна суміш, буде діяти аналогічно, тому вивчення його впливу на експресію білка Nrf2 та антиоксидантних ферментів, які регулюються цим фактором, у хворих на ХП можна вважати вагомим внеском у доказову базу ефективності Церебролізину при хворобі Паркінсона.
Необхідно відзначити, що інтерес до застосування Церебролізину як активного нейропротекторного засобу у хворих на ХП виник лише протягом останніх декількох років. Так, у роботі E. Luchanina et al. [13] уперше в клінічній неврології показаний вплив препарату на рухову активність і м’язовий тонус хворих з ХП, які отримували лікування препаратами леводопи. Наступні роботи мали доказову базу впливу препарату, що ґрунтується на експериментальних моделях паркінсонізму. Встановлено, що Церебролізин® покращував приживлюваність ДОФА-трансплантата зі стовбурових клітин, інстальованих у чорну субстанцію [8, 9], зменшував вираженість паркінсонічних симптомів у модельних тварин [10, 12], що стало підставою для перспективної рекомендації щодо застосування Церебролізину в клінічній практиці у хворих на ХП на різних стадіях перебігу захворювання [5, 14].
Необхідно вважати, що вивчення ефективності застосування препарату Церебролізин® у комплексній патогенетичній терапії ХП з метою зменшення проявів окиснювального стресу та мітохондріальної дисфункції досить актуальне і перспективне. Дослідження механізмів дії препарату доцільно проводити комплексно, як на клінічному матеріалі (у хворих на ХП), так і в експерименті при моделюванні паркінсоноподібного синдрому у тварин.
Мета дослідження — вивчити й оцінити ефективність і переносимість препарату Церебролізин® виробництва EVER PHARMA (Австрія) у комплексному лікуванні пацієнтів із хворобою Паркінсона; дослідити механізм дії Церебролізину на клінічну симптоматику ХП у пацієнтів з когнітивними порушеннями, мітохондріальну дисфункцію та прояви оксидативного стресу.
Завдання дослідження:
— вивчити вплив препарату Церебролізин® на клініко-неврологічну симптоматику хвороби Паркінсона;
— оцінити ефективність препарату Церебролізин® при порушеннях когнітивних функцій у хворих на ХП;
— установити дію Церебролізину на показники центрального супраспінального контролю рухової активності;
— вивчити вплив Церебролізину на рівень оксидативного стресу і мітохондріальну дисфункцію за допомогою визначення в плазмі крові пацієнтів ультраструктури мітохондрій і прооксидантно-антиоксидантного балансу;
— визначити можливість впливу Церебролізину на рівні експресії генів DJ-1, PINK-1 і BDNF у клітинах крові пацієнтів з ХП.
Матеріали та методи
17 пацієнтів із хворобою Паркінсона з установленим діагнозом відповідно до критеріїв Британського банку мозку (Hughes A., 1992) віком 45–74 роки зі стадією хвороби 1,5–3,0 (за Hoehn-Yahr) приймали базисну терапію леводопавмісними препаратами. Пацієнти перебували на стаціонарному лікуванні у відділенні екстрапірамідних захворювань нервової системи ДУ «Інститут геронтології ім. Д.Ф. Чеботарьова НАМН України». Пацієнти підписували добровільну інформовану згоду на участь у дослідженні, що ґрунтується на положеннях Гельсінської декларації Всесвітньої медичної асоціації, за погодженням комісії з питань етики ДУ «Інститут геронтології ім. Д.Ф. Чеботарьова НАМН України».
Методи обстеження хворих на ХП до та після лікування Церебролізином:
1. Загальноклінічні, неврологічні.
2. Оцінка рухової активності за міжнародною шкалою MDS/UPDRS, 2015.
3. Нейропсихологічне обстеження: тестування за шкалами MMSE, MoCA, шкалою «Батарея лобної дисфункції» (FAB), шкалою тривожності Спілбергера, шкалою депресії Бека.
4. Дослідження когнітивних викликаних потенціалів Р300.
5. Дослідження біоелектричної активності м’язів (електронейроміографія).
6. Комп’ютеризована програма дослідження сенсомоторної реакції і моторного темпу.
7. Дослідження ультраструктури мітохондрій у тромбоцитах крові хворих на ХП.
8. Визначення стану перекисного окиснення ліпідів (ПОЛ) та антиоксидантного захисту в плазмі крові хворих на ХП.
9. Визначення рівня експресії генів Parkin’a в клітинах крові пацієнтів з ХП.
Призначення препарату Церебролізин® проводилося на тлі базисної протипаркінсонічної терапії (леводопавмісні препарати, агоністи дофамінових рецепторів, амантадин, інгібітори МАО-В), яка була стабільною протягом 28–30 днів до початку прийому Церебролізину і протягом усього досліджуваного періоду. Режим прийому препарату — 20 мл внутрішньовенно краплинно 1 раз на добу протягом 10 днів. Інфузії проводились у першій половині дня. Характеристика вибірки подана в табл. 1.
Для об’єктивного дослідження стану пацієнтів до та після курсу Церебролізину використовували набір клінічних шкал для оцінки рухових і немоторних порушень, комп’ютеризовані тести для визначення латентного періоду сенсомоторної реакції і моторного темпу, нейропсихологічні тести, електронейроміографію та реєстрацію ендогенних викликаних потенціалів головного мозку.
Перевірку гіпотези про ефективність нейропротекторної дії препарату проводили за допомогою критеріїв Вілкоксона (для пов’язаних виборок) і Манна — Уїтні (для незалежних груп). Зв’язок між досліджуваними показниками подавали у вигляді коефіцієнтів рангової кореляції Спірмена. Як значущі розглядалися відмінності, для яких p < 0,05.
Результати та обговорення
Клініко-нейрофізіологічна оцінка ефективності курсового лікування Церебролізином пацієнтів із хворобою Паркінсона
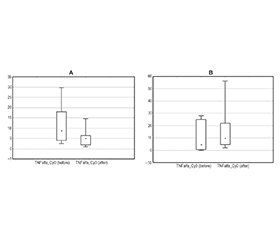
Курсове введення Церебролізину на тлі базисної протипаркінсонічної терапії мало сприятливий вплив на стан більшої частини досліджених хворих, передусім на їх активність у повсякденному житті та здатність до самообслуговування. Об’єктивно це виражалось у вірогідному зменшенні балів за усіма субшкалами UPDRS (рис. 1).
Відзначається позитивний вплив курсу Церебролізину на комплекс немоторних порушень, супутніх щодо моторних симптомів ХП. У досліджуваних виявлене статистично значуще покращання когнітивних функцій за даними спеціалізованих шкал MMSE, FAB і MoCA, зниження показників депресії за шкалою Бека і ситуаційної (реактивної) тривожності за шкалою Спілбергера — Ханіна. Показник особистісної тривожності не змінювався відносно вихідного рівня (рис. 2).
Для інструментальної оцінки впливу Церебролізину на власне рухові функції найбільш чутливим виявився тест «Моторний темп», у якому було зареєстроване значуще зменшення середнього, мінімального і максимального часу рухових реакцій (рис. 3). Цікаво, що дані зміни більшою мірою характерні для реакцій правої руки, тоді як для лівої зменшувалося тільки середнє значення моторного темпу. Можна припустити, що така асиметричність ефектів пов’язана зі стороною патологічного процесу, тому що значна частина пацієнтів (76 % досліджуваної групи) демонструвала переважно правосторонню симптоматику ХП. У той же час латентний період простої сенсомоторної реакції не змінювався на тлі курсового прийому Церебролізину. Оскільки реалізація даної реакції, на відміну від рухів у тесті «Моторний темп», включає також процеси аналізу сенсорної інформації та прийняття рішень, можна припустити переважний вплив препарату на периферичні механізми організації рухової активності (рис. 3).
/26.jpg)
На тлі курсового застосування Церебролізину було виявлено збільшення порогу виникнення Н-рефлексу m. gastrocnemius з 5 [3; 9] мА до 6 [5,8; 18] мА (табл. 2; рис. 4). Латентний період і потужнісні характеристики H-рефлексу і параметри М-відповіді при цьому не змінювалися відносно їхніх вихідних значень.
Аналіз ендогенних компонентів викликаних потенціалів показав, що в досліджуваній групі пацієнтів з ХП спостерігається уповільнення процесів формування хвилі Р3 (медіана 434 мс, інтерквартильний розмах 386–512 мс у тім’яній ділянці неокортексу) порівняно з відповідною віковою нормою 390–410 мс [41, 42]. Після курсу Церебролізину було зареєстроване статистично значуще збільшення латентного періоду компонента Р3 у центрально-парієтальному відведенні до 394 [304; 446] мс (рис. 5). Значущих змін латентного періоду компонента N2 і амплітуди компонентів N2 і P3 виявлено не було.
/27.jpg)
Уповільнення процесів формування хвилі Р3 є досить характерною особливістю низки нейродегенеративних захворювань, зокрема хвороби Альцгеймера і хвороби Паркінсона. Описаний стійкий взаємозв’язок між вираженістю когнітивних порушень та уповільненням хвилі Р3, яка розглядається як index of cognitive decline і може використовуватися для раннього виявлення деменції [43]. Для пацієнтів із ХП з помірними когнітивними порушеннями (mild cognitive impairment, PD-MCI) також описане зростання латентного періоду Р3 та обернений взаємозв’язок цього показника з об’ємом сірої речовини блідої кулі й шкаралупи, дисфункція яких веде до маніфестації таких симптомів, як брадикінезія та ригідність [44]. Покращання даного показника на тлі курсового прийому Церебролізину дозволяє припустити, що більш вираженого ефекту на стан вищих кортикальних функцій можна очікувати в пацієнтів з підвищеним ризиком розвитку або прогресування когнітивних порушень.
/27_2.jpg)
/28.jpg)
Кореляційний аналіз змін клінічних, фізіологічних характеристик стану пацієнтів і результатів курсового застосування препарату Церебролізин® дозволив виділити низку чинників, які істотно впливають на вираженість ефектів лікування. Зокрема, ступінь покращання низки немоторних характеристик (когнітивних функцій за шкалою FAB, амплітуди когнітивного викликаного потенціалу Р3 та ознак депресії за шкалою Бека) був більшим у людей, які первинно отримували більш високу добову дозу леводопи.
Для показників когнітивних функцій (MMSE, амплітуда когнітивного викликаного потенціалу Р3) був також виявлений аналогічний взаємозв’язок із часом виникнення захворювання: більш виражені позитивні ефекти лікування Церебролізином спостерігались у пацієнтів з більш раннім дебютом ХП і більшою тривалістю захворювання.
У той же час більш виражене скорочення часу реакцій було характерним для індивідів з меншими вихідними оцінками тяжкості ХП за шкалою UPDRS і меншим рівнем тривожності. Такі кореляційні взаємозв’язки виявляються як при безпосередній оцінці часу рухових реакцій у тестах «Моторний темп» і «Сенсомоторна реакція», так і при визначенні латентних періодів Н-рефлексу і М-відповіді.
Отже, курсове застосування Церебролізину покращує загальний стан пацієнтів з хворобою Паркінсона, що вірогідно проявляється в зменшенні кількісних показників усіх субшкал UPDRS, послабленні проявів афективних розладів, таких як тривога і депресія, покращанні стану когнітивних функцій. На тлі застосування Церебролізину покращуються динамічні характеристики простих рухових реакцій і зростає поріг виникнення Н-рефлексу, що свідчить про полегшення процесів супраспінального контролю за діяльністю функціональної активності мотонейронів.
Терапевтичні ефекти Церебролізину при порушенні когнітивної та афективної сфери при ХП більш виражені в пацієнтів з раннім дебютом захворювання, більшою його тривалістю та вищою добовою дозою леводопи. Покращання часу рухових реакцій більшою мірою проявляється в пацієнтів з менш вираженою стадією хвороби і при низькому вихідному рівні тривожності.
Мітохондріальна дисфункція до та після лікування Церебролізином у пацієнтів із хворобою Паркінсона
Відповідно до фармакологічних властивостей ней–ропротективна дія Церебролізину включає суму всіх механізмів, спрямованих проти тривалих факторів і короткочасних ендо- та екзогенних нейробіологічних процесів. Ендогенна нейропротекція включає два різних типи механізмів — абсолютні й відносні. Абсолютні механізми завжди активують експресію ДНК, після чого відбувається індукція синтезу білка. Відносні механізми здійснюють нейропротекцію за рахунок впливу на попередньо експресовані білки клітинної мембрани, цитозолю й органел [45].
Нейропротективна стратегія Церебролізину пов’язана перш за все з активацією абсолютних механізмів біологічно активних олігопептидів. До того ж препарат містить амінокислоти, мікроелементи й вітаміни, які також роблять свій внесок в активацію відносних механізмів нейропротекції. Нейропротективна дія Церебролізину проявляється в зниженні ексайтотоксичності, інактивації утворення вільних радикалів, пригніченні запальної відповіді, зменшенні набряку і гальмуванні процесів апоптозу й некрозу [19, 46, 47]. Саме ці дослідження властивостей і впливів Церебролізину наближають до мети дослідження.
Щодо гіпотез патогенезу хвороби Паркінсона, то тут значна роль відводиться дисфункції мітохондрій та убіквітин-протеосомальній дисфункції, дії окиснювального стресу, запаленню, апоптозу [19, 48, 49].
Для вивчення морфофункціонального стану клітинних органел та, опосередковано, стану судинної стінки в здорових людей і пацієнтів з патологією практично єдиними об’єктами (за відсутності оперативного втручання) є клітини крові, зокрема тромбоцити. Вони беруть участь у багатьох процесах в організмі, як пов’язаних, так і не пов’язаних з ХП: у регенерації тканин, забезпеченні гемостазу та ін. Тромбоцити містять значну кількість різноманітних гранул, які включають глікопротеїни, білки, фактори росту, АДФ, АТФ, іони кальцію, серотонін, гістамін тощо, а також мітохондрії, стан яких визначає енергетичний метаболізм у тканинах і в організмі в цілому [40, 50].
Результати проведених досліджень дозволили виявити істотні відмінності в структурній організації тромбоцитів в осіб з ХП, обстежених до початку стандартного лікувального процесу. Перш ніж розглядати ультраструктуру тромбоцитів в осіб з ХП, наводимо приклад їх структури в здорових осіб контрольної групи (рис. 6).
Електронно-мікроскопічне й морфометричне вивчення тромбоцитів у пацієнтів з ХП виявило, що тромбоцити були переважно зрілими й старими клітинами. У них була знижена кількість щільних -гранул — 5,1 ± 0,4 шт. у клітині (у здорових осіб — 8,4 ± 0,5 шт. у клітині, р < 0,05). Проте кількість прозорих -гранул підвищилася з 5,3 ± 0,2 шт. до 10,3 ± 0,6 шт. у клітині. До того ж останні часто мали великі розміри (> 100 нм) і містили значну кількість білкового дебрису (рис. 7).
Одиничні мітохондрії (МХ), які виявлялись у клітинах (2–4 на клітину), були структурно досить збереженими й мали середній діаметр 0,48 ± 0,02 мкм, вірогідно не відрізняючись від тих, що визначались у контрольній групі (0,41 ± 0,04 мкм).
Однією з важливих функцій тромбоцитів є участь у метаболізмі серотоніну; встановлено, що кількість щільних -гранул залежить саме від його концентрації [39]. Окрім серотоніну -гранули містять АДФ і АТФ, а також акумулюють Са2+. Тромбоцити — практично єдині клітини крові, у яких концентруються резерви серотоніну (до 96 % серотоніну, що визначається в плазмі). Так, його кількість, накопичена у -гранулах, непрямо свідчить про обмін серотоніну, який в обстежених пацієнтів імовірно знижений, що може вказувати на дисфункцію серотонінергічної системи, яка бере участь у формуванні ХП, відповідаючи за синдром постійної втоми [51]. Оскільки тромбоцити є резервуарами серотоніну, який надходить із плазми крові, його кількість, накопичена в -гранулах, як указано вище, опосередковано свідчить про обмін серотоніну, який в обстежених пацієнтів значно знижений, що може зумовлювати наявність афективних розладів при ХП і вказувати на дисфункцію серотонінергічної системи, а також може свідчити про порушення регуляторних ефектів серотоніну відносно скоротливої здатності судинної стінки [40].
/30.jpg)
/30_2.jpg)
Великі -гранули містять різноманітні білки і глікопротеїни, що беруть участь у процесах згортання крові, фактори росту, протеолітичні ферменти. Можна припустити, що значна кількість гранул, у яких виявляється антигепариновий фактор тромбоцитів 4 — тромбо–спондин, що сприяє агрегації тромбоцитів, вказує на зростання ризику тромбоутворення в пацієнтів з ХП.
Значні порушення були виявлені в ультраструктурі МХ у тромбоцитах хворих. Крім втрати чіткості мембран МХ (зовнішньої і/або внутрішньої, кристоутворюючої), спостерігалось утворення септованих органел (сМХ). Механізми і причини утворення сМХ до цього часу є недослідженими. Припускають, що сМХ здатні акумулювати Са2+ [52]. Оскільки відомо, що акумуляція Са2+ і синтез АТФ — альтернативні процеси, пов’язані з переносом електронів, то посилення Са-акумулюючої здатності МХ може вказувати на зменшення синтезу АТФ у них. До того ж поява сМХ може свідчити про парціальний некроз клітини. Указані зміни ультраструктури МХ є свідченням формування у тромбоцитах мітохондріальної дисфункції.
Застосування Церебролізину в комплексній терапії пацієнтів з ХП супроводжувалося вірогідною динамікою морфофункціонального стану тромбоцитів (табл. 3).
Застосування Церебролізину приводило до вірогідного (на 45 %) збільшення кількості -гранул. На цю зміну необхідно звернути увагу, тому що серотонін абсорбується тромбоцитами, а саме -гранулами, які забезпечують його зберігання і транспортування. Відносна і/або абсолютна серотонінова недостатність тією чи іншою мірою порушує функції ЦНС [51]. Отже, зменшення кількості депонованого в тромбоцитах серотоніну може сприяти негативним змінам у ЦНС. Зростання ж кількості -гранул свідчить про збільшення запасів серотоніну. Імовірно, таким шляхом реалізується один з можливих механізмів нейропротекторної дії Церебролізину. До того ж відносно зменшується Са2+-акумулююча здатність тромбоцитів, що повинно сприяти покращанню синтезу АТФ, в усякому разі — у цих клітинах крові.
Вірогідних змін кількості -гранул не було виявлено; спостерігалася лише тенденція до її зменшення (0,1 < Р < 0,2). Така тенденція має також позитивну спрямованість, у першу чергу, на наш погляд, відносно тромботичної здатності, яка часто є підвищеною в пацієнтів з ХП [53].
Що стосується МХ, то, незважаючи на невелику кількість органел у тромбоцитах, можна допускати деяке збільшення їх кількості — з 2–4 органел до лікування до 5–7 органел після лікування Церебролізином, що в поєднанні з відсутністю сМХ може свідчити про зменшення вираженості мітохондріальної дисфункції.
Отже, лікування Церебролізином сприяє покращанню морфофункціонального стану тромбоцитів у пацієнтів з ХП, а саме збільшує запаси серотоніну, знижує Са2+-акумулюючу здатність, зменшує прояви мітохондріальної дисфункції, дає слабковиражений антитромботичний ефект.
Вплив курсового лікування Церебролізином на експресію генів PARKIN’a в пацієнтів із хворобою Паркінсона
У всій групі протестованих осіб, узятих разом (без контролю), за допомогою тесту Спірмена не було виявлено кореляції експресії виміряних генів. Разом з тим при розподілі за статтю були виявлені різноспрямовані відмінності в експресії генів до та після терапії препаратом Церебролізин® (табл. 4).
Зокрема, група чоловіків характеризувалася зниженням експресії гена BDNF — p = 0,025, а в жінок після застосування препарату експресія збільшувалась — p = 0,046 (рис. 8).
Важливо відзначити, що при порівнянні результатів експресії генів з когнітивними параметрами підвищення BDNF у жінок (але не в чоловіків) також супроводжувалося підвищенням показника за шкалою MMSE (рис. 9).
На кореляційних матрицях показаний взаємозв’язок окремих виміряних параметрів для чоловіків (табл. 5) і жінок (табл. 6) при р < 0,05.
Слід вважати, що відмінності можуть бути більш істотними при зниженні p-value до 0,1, що може мати певне значення для планування подальших досліджень.
Вплив курсового лікування Церебролізином на стан оксидантно-прооксидантної системи в пацієнтів із хворобою Паркінсона
Показано, що у хворих на ХП у крові відбувається значне зростання маркерів окиснювального стресу. Так, рівень ТБК-АП у плазмі крові збільшувався на 74 % (P < 0,05), вміст Н2О2 в еритроцитах крові — на 42 % (P < 0,05) на відміну від здорових людей. Відомо, що окиснювальний стрес відіграє ключову роль у патогенезі ХП і є тригером процесу нейродегенерації. Основною причиною окиснювального стресу за цих умов є надмірна генерація активних форм кисню (АФК), які утворюються як результат метаболізму дофаміну, мітохондріальної дисфункції та нейрозапалення [33]. Відомо, що надмірне утворення продуктів ПОЛ має цитотоксичну дію, яка може проявлятися пошкодженням мембран клітин, у тому числі еритроцитів, збільшенням в’язкості білок-ліпідного шару, зниженням активності мембранозв’язаних ферментів, рецепторів тощо [53].
У хворих на ХП активація прооксидантних процесів пов’язана не тільки з надвиробленням АФК, але й зі змінами в ефективності антиоксидантного захисту [34, 54]. Тому паралельно з маркерами окиснювального стресу ми досліджували активність антиоксидантних ферментів — СОД і каталази, які становлять першу лінію антиоксидантного захисту в плазмі крові хворих на ХП. Відомо, що СОД і каталаза діють як взаємопов’язані ланки антиоксидантної системи, які забезпечують детоксикацію первинних АФК — супероксиданіону й подальшого продукту його дисмутації — Н2О2 [55].
Відзначалось підвищення активності СОД на 29 % (P < 0,05), каталази — на 205 % (P < 0,05) порівняно з показниками контролю (табл. 7). Така активація СОД і каталази свідчить про наявність у крові хворих на ХП надмірної генерації супероксиданіону, який є субстратом для СОД, і пероксиду водню, який є субстратом для антиперекисного фермента каталази [54], що створює передумови для генерації не менш цитотоксичного гідроксильного радикалу. Декілька досліджень показали зростання активності мітохондріальної СОД у передній корі півкуль мозку пацієнтів з ХП [35, 56]. Було встановлене підвищення активності СОД у плазмі крові вже на безсимптомній фазі захворювання [57, 58]. З іншого боку, показано появу характерних ознак окиснювального стресу в пацієнтів з ХП, незважаючи на компенсаторну активацію СОД, якщо це відбувається на тлі мітохондріальної дисфункції [36].
Проте інформація відносно статусу антиоксидантів та активності антиоксидантних ферментів у хворих на ХП у сучасній літературі досить контраверсійна. Є багато даних як про активізацію системи антиоксидантного захисту у відповідь на підвищений рівень утворення вільних радикалів та органічних і гідропероксидів, так і про можливість виснаження адаптивної здатності ендогенної антиоксидантної системи захисту [33].
Поряд з антирадикальними ферментами система глутатіону є однією з активних складових антиоксидантного захисту організму, яка відіграє велику роль у послабленні патологічного процесу, особливо в захисті еритроцитів, оскільки не лише запобігає розвитку вільнорадикальних реакцій, але й забезпечує ефективну елімінацію кінцевих метаболітів ПОЛ [59].
Глутатіон належить до основних ланок антиоксидантного захисту, що бере участь у детоксикації ксенобіотиків і токсичних продуктів метаболізму, впливає на активність ферментів, регулює обмін ейкозаноїдів і простагландинів, впливає на біосинтез нуклеїнових кислот, бере участь у процесі апоптозу, а також виконує інші, не менш важливі функції [60]. Дефіцит цього трипептиду в еритроцитах свідчить про напруженість антиоксидантного захисту, зміни в редокс-системі клітин, а також може бути найбільш раннім показником посилення окиснювальних процесів і дисбалансу в про-/антиоксидантній системі. Результати різноманітних досліджень показують тісний взаємозв’язок між рівнем відновленого глутатіону як у ЦНС, так і у крові пацієнтів з ХП і ступенем тяжкості нейродегенеративних процесів [37].
Результати досліджень показали зниження рівня глутатіону на 66 % (P < 0,05) і активності глутатіонпероксидази — на 15 % (P > 0,05) в еритроцитах крові хворих на ХП на відміну від контрольних показників (табл. 8). Зменшення активності глутатіонпероксидази, встановлене в нашому дослідженні, можна пояснити виснаженням рівня відновлення глутатіону, який в умовах окиснювального стресу в глутатіонпероксидазній реакції виступає як субстрат для цього фермента [59].
Застосування Церебролізину приводило до зниження інтенсивності прооксидантних процесів в організмі пацієнтів з ХП, про що свідчить зменшення в плазмі крові цих хворих вмісту вторинних продуктів ПОЛ (ТБК-АП) на 17 % (P > 0,05), в еритроцитах крові — вмісту Н2О2 на 12 % (P > 0,05) порівняно з аналогічними показниками до лікування. Підтвердженням уповільнення окиснювальних процесів у хворих на ХП може бути зниження активності антиперекисного фермента каталази — на 20 % (P < 0,05) та антирадикального фермента СОД — на 11 % (P > 0,05). Відомо, що зміни активності СОД залежать від інтенсивності утворення токсичного для клітин супероксиданіону, оскільки він є субстратом для цього антирадикального фермента [61]. Тенденція до зниження активності СОД, встановлена при введенні Церебролізину, може бути підтвердженням ефективності процесів дисмутації зі зниженням рівня агресивного радикалу в крові хворих на ХП. Застосування вищевказаного препарату посилювало антиоксидантний захист клітин крові, перш за все еритроцитів, про що свідчить збільшення вмісту відновленого глутатіону на 30 % (P < 0,05) та активності глутатіонпероксидази на 15 % (P > 0,05) в еритроцитах крові порівняно із цими показниками до лікування.
Отже, застосування Церебролізину потенціює антиоксидантний захист і зменшує напруженість окиснювального стресу, а також інтенсивність перекисних процесів у крові пацієнтів з ХП.
Висновки
1. Курсове використання Церебролізину покращує загальний стан пацієнтів з ХП, що вірогідно проявляється в зменшенні кількісних показників усіх субшкал UPDRS, послабленні проявів афективних розладів, таких як тривога і депресія, покращанні стану когнітивних функцій. На фоні застосування Церебролізину покращуються динамічні характеристики простих рухових реакцій і зростає поріг виникнення Н-рефлексу, що свідчить про полегшення процесів супраспінального контролю за діяльністю функціональної активності мотонейронів.
2. Терапевтичні ефекти Церебролізину при порушенні когнітивної та афективної сфер при ХП більш виражені в пацієнтів з раннім дебютом захворювання, більшою його тривалістю та вищою добовою дозою леводопи. Покращання часу рухових реакцій більшою мірою проявляється в пацієнтів з менш вираженою стадією захворювання і при низькому вихідному рівні тривожності.
3. Унаслідок курсового лікування препаратом Церебролізин® відбувається зменшення латентного періоду когнітивного потенціалу Р300 і зниження його амплітуди, що вказує на активацію ролі передньофронтальних нейрональних генераторів у регуляції когнітивних функцій.
4. Під впливом препарату Церебролізин® вірогідно знижуються прояви мітохондріальної дисфункції та оксидативного стресу в лабораторних тварин (щурів) з моделлю паркінсонізму, що проявляється в нормалізації ультраструктури в тканинах довгастого мозку і стріатуму, зниженні гіпергідратації біологічних бар’єрів, оновленні антиоксидантного захисту мозку.
5. У хворих на ХП препарат Церебролізин® викликав інтенсифікацію морфогенезу мітохондрій і процесу їх поздовжньої асоціації, що свідчить про нарощування енергетичних можливостей мозку і збільшення інтенсивності автофагії цієї структури та здатності клітин протидіяти метаболічному стресу як результату нейродегенерації.
6. Курсове лікування Церебролізином супроводжується збільшенням експресії гена BDNF, що клінічно корелює з вірогідним покращанням когнітивних функцій у пацієнтів з ХП.
7. Результати комплексного дослідження ефективності Церебролізину в пацієнтів з ХП з когнітивними порушеннями показали, що включення препарату Церебролізин® до патогенетичної терапії хворих на ХП сприяє зниженню вираженості рівня оксидативного стресу — ключового механізму розвитку захворювання, зменшенню ступеня мітохондріальної дисфункції, що дає підстави рекомендувати Церебролізин® у неврологічній практиці як нейротрофічний засіб для фармакотерапії нейродегенеративного процесу на всіх стадіях перебігу хвороби Паркінсона.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 10.01.2026
Рецензовано/Revised 16.02.2026
Прийнято до друку/Accepted 01.03.2026
Список литературы
1. Stepanichev M, Onufriev M, Aniol V et al. Effects of cerebrolysin on nerve growth factor system in the aging rat brain. Restor Neurol Neurosci. 2017;35( 6):571-581.
2. Alvarez XA, Fernndez-Novoa L, Sampedro C, Lombardi V, Windisch M, Cacabelos C. Neuroimmunotrophic effects of cerebrolysin in an animal model of hippocampal degeneration induced by -amyloid. In: Korczyn A.D., ed. International Congress on Vascular Dementia 2017. Bologna, Italy: Monduzzi Editore, 1999. P. 233-237.
3. Abdel-Salam Omar ME et al. Cerebrolysin protects against rotenone induced oxidative stress and neurodegeneration. Journal of Neurorestoratology, Open Access. 2014. Doi: org|10.2147|JN.S50114.
4. Muresanu Dafin F et al. Persistence of the effects of Cerebrolysin on cognition and qEEG slowing in vascular dementia patients: Results of a 3-month extension study. Journal of the Neurological Sciences. 2010;299:179-183.
5. Gao Ju, Wong Luwen, Liu Jingyi et al. Abnormalities of Mitochondrial dynamics in neurodegenerative diseases a likely novel therapeutic strategy for neurodegenerative disease. Antioxidants. 2017;6:25.
6. Xing S, Zhang J, Dang C et al. Cerebrolysin reduces amyloid- deposits, apoptosis and autophagy in the thalamus and improves functional recovery after cortical infarction. J Neurol Sci. 2014;337(1–2):104-111.
7. Chen CC, Wei ST, Tsaia SC, Chen XX, Cho DY. Cerebrolysin enhances cognitive recovery of mild traumatic brain injury patients: double-blind, placebo-controlled, randomized study. Br J Neurosurg. 2013;27(6);803-807.
8. Rochenstein E et al. Neuropeptide Treatment with Cerebrolysin Enhances the Survival of Grafted neural stem cell in a synuclein transgenic model of Parkinson’s disease. Suppl. issue: molecular and cellular mechanisms of neurodegeneration. Journal of Experimental Neuroscience. 2015;9(S2):131-140.
9. Pantcheva P et al. Treating non-motor symptoms of Parkinson’s disease with transplantation of stem cells. Expert Rev Neurother. 2015 Oct;15(10):1231-1240. Doi: 10/1586|14737175.2015.1091727.
10. Requeejoe C, et al. Nanodelivery of Cerebrolysin and rearing enriched environment induce neuroprotective effects in a Preclinical Rat model of Parkinson’s disease. Springer Science+Business Media, LLC, 2017. Doi: 10.07|s12035-017-0741-x.
11. Brainin M. Cerebrolysin: a multi-target drug for recovery after stroke. Expert Rev Neurother. 2018;18(8):681-687.
12. Noor Neveen A et al. A promissing therapeutic potential of cerebrolysin in 6-OHDA rat model of Parkinson’s disease. Life Sciences. 2016. Doi: 10.1016|j.Lfs 2016.05.022.
13. Luchanina E, Karaban I, Berezetskaya N. Diagnosis of Parkinson’s Disease by Electrophysiological Methods. In: Diagnostics and Rehabilitation of Parkinson’s disease Edited by Juliana Dushanova. 2011. P. 27-58.
14. Young Wise, Keck WM. Cerebrolysin review. In: Effects of Botox on Motoneurons Analysis of 2009 NIH Human Stem Cell Research Policy, 2009.
15. Eder P, Reinprecht I, Schreiner E, Skofitsch G, Windisch M. Increased density of glutamate receptor subunit 1 due to Cerebrolysin treatment: an immunohistochemical study on aged rats. Histochem J. 2001;33(11–12):605-612.
16. Ginsberg SD, Malek-Ahmadi MH, Alldred MJ et al. Selective decline of neurotrophin and neurotrophin receptor genes within CA1 pyramidal neurons and hippocampus proper: Correlation with cognitive performance and neuropathology in mild cognitive impairment and Alzheimer’s disease. Hippocampus. 2019;29(5):422-439.
17. Gomazkov OA. Apoptosis in neuronal structures and the role of neurotrophic growth factors. Biochemical mechanisms of brain derived peptide preparations. Korsakov Journal of Neurology and Psychiatry. 2002;Suppl 7;17-21.
18. Veinbergs I, Mante M, Mallory M, Masliah E. Neurotrophic effects of Cerebrolysin in animal models of excitotoxicity. J Neural Transm Suppl. 2000;59:273-280.
19. Zhang С, Chopp M, Cui Y, Wang L, Zhang R. Cerebrolysin enhances neurogenesis in the ischemic brain and improves functional outcome after stroke. J Neurosci Res. 2010;88(15):3275-3281.
20. Gavrilova SI, Avlvarez A. Cerebrolysin in the therapy of mild cognitive impairment and dementia due to Alzheimer’s disease: 30 years of clinical use. Med Res Rev. 2020;1:29. Doi: 10.1002|med 21722.
21. Tatebayashi Y, Lee MH, Li L et al. The dentate gyrus neurogenesis: a therapeutic target for Alzheimer’s disease. Acta Neuropathol. 2003:105(3);225-232.
22. Plosker GL, Gauthier S. Cerebrolysin: a review of its use in dementia. Drugs Aging. 2009;26(11);893-915.
23. Guekht AB, Moessler H, Novak PH, Gusev EI. Cerebrolysin Investigators. Cerebrolysin in vascular dementia: improvement of clinical outcome in a randomized, double-blind, placebo-controlled multicenter trial. J Stroke Cerebrovasc Dis. 2011;20(4):310-318.
24. Cui S, Chen N, Yang M et al. Cerebrolysin for vascular dementia. Cochrane Database Syst Rev. 2019;11:CD008900.
25. Fiani B, Covarrubias C, Wong A, Doan T, Reardon T, Nikolaidis D, Sarno E. Cerebrolysin for stroke, neurodegeneration, and traumatic brain injury: review of the literature and outcomes. Neurol Sci. 2021;42(4):1345-1353. Doi: 10.1007/s10072-021-05089-2. Epub 2021 Jan 30. PMID: 33515100.
26. Cummings J, Ritter A, Zhong K. Clinical trials for disease-modifying therapies in Alzheimer’s disease: a primer, lessons learned, and a blueprint for the future. J Alzheimers Dis. 2018;64(s1);S3-S22.
27. Gray SC, Kinghorn KJ, Woodling NS. Shifting equilibriums in Alzheimer’s disease: the complex roles of microglia in neuroinflammation, neuronal survival and neurogenesis. Neural Regen Res. 2020;15(7);1208-1219.
28. Medina M. An Overview on the clinical development of tau-based therapeutics. Int J Mol Sci. 2018;19(4);1160.
29. Alvarez XA, Alvarez I, Iglesias O et al. Synergistic increase of serum BDNF in Alzheimer patients treated with Cerebrolysin and donepezil: association with cognitive improvement in ApoE4 cases. Int J Neuropsychopharmacol. 2016;19(6):pyw024.
30. Mauricio R, Benn C, Davis J et al. Tackling gaps in developing life-changing treatments for dementia. Alzheimers Dement;2019;5:241-253.
31. Schneider-Garces NJ, Gordon BA, Brumback-Peltz CR, Shin E, Lee Y, et al. Span, CRUNCH, and beyond: working memory capacity and the aging brain. J Cogn Neurosci. 2010;22:655-669.
32. Li GD, Bi R, Zhang DF et al. Female-specific effect of the BDNF gene on Alzheimer’s disease. Neurobiol Aging. 2017;53:192.e11-192.e19.
33. Васенина Е.Е., Левин О.С. Окислительный стресс в патогенезе нейродегенеративных заболеваний: возможности терапии. Современная терапия в психиатрии и неврологии. 2013;3–4:39-46.
34. De Farias C et al. Highly specific changes in antioxidant le–vels and lipid peroxidation in Parkinson’s disease and its progression: Disease and staging biomarkers and new drug targets. Neuroscience letters. 2016;617:66-71.
35. Masaldan S, Bush AI, Devos D. Striking while the iron is hot: Iron metabolism and ferroptosis in neurodegeneration. Free Radic Biol Med. 2019;133:221-233.
36. Surmeier DJ, Guzman JN, Sanchez-Padilla J, Schumac–ker PT. The role of calcium and mitochondrial oxidant stress in the loss of substantia nigra pars compacta dopaminergic neurons in Parkinson’s disease. Neuroscience. 2011;198:221-231.
37. Liddell JR, et al. Nexus between mitochondrial function, iron, copper and glutathione in PD. Neurochemistry Internat. 2018;117:126-138.
38. Симоненков А.П., Клюжев В.М. Синдром серотониновой недостаточности. М.: Бином, 2013. 96 с.
39. Clauser S, Cramer-Borde E. Role of platelet electron microscopy in the diagnosis of platelet disorders. Semin Thromb Hemost. 2009;35(2):213-223.
40. Филиппова О.И., Колосков А.В., Столица А.А. Методы исследования функциональной активности тромбоцитов (обзор литературы). Трансфузиология. 2012;13(2):493-514.
41. Гнездицкий В.В., Корепина О.С. Атлас по вызванным потенциалам мозга. Иваново: ПресСто, 2011. 532 с.
42. Van Dinteren R, Arns M, Jongsma ML., Kessels RP. P300 development across the lifespan: a systematic review and meta-analysis. PLoS One. 2014;9(2):e87347. Doi: 10.1371/journal.pone.0087347.
43. Papadaniil CD, Kosmidou VE, Tsolaki A, Tsolaki M, Kompatsiaris IY, Hadjileontiadis LJ. Cognitive MMN and P300 in mild cognitive impairment and Alzheimer’s disease: A high density EEG-3D vector field tomography approach. Brain Res. 2016;1648(Pt A):425-433. Doi: 10.1016/j.brainres.2016.07.043. Epub 2016 Jul 30. PMID: 27485659.
44. Hnerli D, Emek-Sava DD, avuolu B, Dnmez olakolu B, Ada E, Yener GG. Mild cognitive impairment in Parkinson’s disease is associated with decreased P300 amplitude and reduced putamen volume. Clin Neurophysiol. 2019;130(8);1208-1217. Doi: 10.1016/j.clinph.2019.04.314. Epub 2019 May 4. PMID: 31163365.
45. Muresanu DF, Buzoianu A, Florian SI, von Wild T. Towards a roadmap in brain protection and recovery. J Cell Molec Med. 2012;16(12):2861-2871.
46. Gonzlez ME, Francis L, Castellano O. Antioxidant systemic effect of short-term Cerebrolysin administration. J Neural Transmission. 1998;53(suppl):333-341.
47. Alvarez XA, Lombardi VR, Fernndez-Novoa L, Garca M, Sampedro C. Cerebrolysin reduces microglial activation in vivo and in vitro: a potential mechanism of neuroprotection. J Neural Transmission. 2000;59:281-292.
48. Gao J, Wang L, Liu J, Xie F, Su B. Wang X. Abnormalities of Mitochondrial Dynamics in Neurodegenerative Diseases. Antioxidants (Basel). 2017;6(2):25.
49. Alzoubi KH, Al-Jamal FF, Mahasneh AF. Cerebrolysin prevents sleep deprivation induced memory impairment and oxidative stress. Physiol Behav. 2020;217:11282.
50. Колосова Е.Н., Василенко И.А., Ковалева Л.Г. Оценка морфофункционального состояния тромбоцитов у больных идиопатической тромбоцитопенической пурпурой методом витальной компьютерной морфометрии. Бюлл. СО РАМН. 2011; 31(2):58-63.
51. Титова Н.В., Чаудури К.Р. Немоторные симптомы болезни Паркинсона: подводная часть айсберга. Анналы клин. и эксперимент. неврологии. 2017;11(4):5-18.
52. Mansur A, Rabiner EA, Comley RA et al. Characterization of 3 PET tracers for quantification of mitochondrial andsynaptic function in healthy human brain:18F-BCPP-EF, 11C-SA-4503, and 11C-UCB-J. J Nucl Med. 2020;61(1):96-103.
53. Tana С, Lauretani F, Ticinesi A, Prati B, Nouvenne A, Meschi T. Molecular and Clinical Issues about the Risk of Venous Thromboembolism in Older Patients: A Focus on Parkinson’s Disease and Parkinsonism. Int J Mol Sci. 2018;19(5):1299.
54. Lvy E, El Banna N, Balle D et al. Causative links between protein aggregation and oxidative stress: a review. Int J Mol Sci. 2019;20(16):3896.
55. Butterfield DA, Halliwell B. Oxidative stress, dysfunctional glucose metabolism and Alzheimer disease. Nat Rev Neurosci. 2019;20(3):148-160.
56. Ferrer I, Perez E, Dalfo E. Abnormal levels of prohibitin and ATP synthase in the substantia nigra and frontal cortex in Parkinson’s disease. Neurosci Lett. 2007;415:205-209.
57. Ihara Y, Chuda M, Kuroda S, Hayabara T. Hydroxyl radical and superoxide dismutase in blood of patients with Parkinson’s disease: relationship to clinical data. J Neurol Sci. 1999;170:90-95.
58. Do Van B, Gouel F, Jonneaux A. Ferroptosis, a newly characterized form of cell death in Parkinson’s disease that is regulated by PKC. Neurobiol Dis. 2016;94:169-178.
59. Кулинский В.И., Колесниченко Л.С. Система глутатиона. I. Синтез, транспорт, глутатионтрансферазы, глутатион-пероксидазы. Биомед. химия. 2009;55(3):255-277.
60. Sies H. Glutathione and its role in cellular functions. Free Radicals Biol Med. 1999;27(9–10):916-921.
61. Зенков Н.К., Ланкин В.З., Меньшикова Е.Б. Окислительный стресс: Биохимический и патофизиологический аспекты. М.: Наука/Интерпериодика, 2001. 343 с.
/25.jpg)
/28.jpg)

/26.jpg)
/27.jpg)
/27_2.jpg)
/29.jpg)
/30.jpg)
/30_2.jpg)
/31.jpg)
/31_2.jpg)
/32.jpg)
/32_2.jpg)
/33.jpg)
/33_2.jpg)