Международный неврологический журнал Том 22, №1, 2026
Вернуться к номеру
Три варіанти впливу симпатичного тонусу на діастолічний артеріальний тиск та їх супутні фактори і предиктори
Авторы: N.V. Kozyavkina (1, 2), I.L. Popovych (1), D.V. Popovych (2), T.B. Voloshyn (1), W.A. Zukow (3)
(1) - Kozyavkin International Rehabilitation Clinic, Truskavets, Ukraine
(2) - I. Horbachevsky Ternopil National Medical University, Ternopil, Ukraine
(3) - Nicolaus Copernicus University, Toruń, Poland
Рубрики: Неврология
Разделы: Клинические исследования
Версия для печати
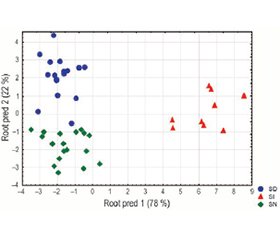
Актуальність. У попередньому дослідженні, проведеному відповідно до концепції тензіорегулому, виявлено, що, по-перше, кореляція між змінами систолічного та діастолічного артеріального тиску (АТ) під впливом бальнеотерапії має лише помірну силу, по-друге, кореляції між змінами обох компонентів АТ з одного боку та маркерами варіабельності серцевого ритму (ВСР) як симпатичного, так і вагусного тонусу — з іншого знаходяться на межі значущості або навіть є незначущими. Було припущено, що спрямованість та вираженість впливу вегетативної нервової системи на АТ визначається супутніми змінами констеляції параметрів нейроендокринно-імунного комплексу та метаболізму і може бути передбачена тією ж або іншою комбінацією. Мета: перевірити ці гіпотези. Матеріали та методи. Під спостереженням перебувало 44 пацієнти з хронічним пієлонефритом і холециститом у фазі ремісії. Тестування проводилося двічі — при госпіталізації та через 7–10 днів стандартної бальнеотерапії на курорті Трускавець. Об’єктами дослідження були АТ та ВСР, електроенцефалографічні, ендокринні, імунні й метаболічні показники. Результати. На першому етапі аналізу інформаційне поле, здавалося б, хаотичних (r = 0,25) взаємозв’язків між симпатичним тонусом і діастолічним АТ фрагментовано на три кластери. Перший кластер (n = 16; 36,3 %) продемонстрував класичний прямий зв’язок (r = +0,91): зміни симпатичного тонусу (LFnu) від –17 до +14 % були пов’язані зі змінами діастолічного АТ від –13 до +22 мм рт.ст. Другий кластер (n = 19; 43,1 %) показав ареактивність (r = 0,24): незважаючи на значні коливання симпатичного тонусу (від –44 до +46 %), діастолічний АТ залишався відносно стабільним (зміни від –4 до +8 мм рт.ст.). Третій кластер (n = 9; 20,5 %) виявив парадоксальну обернену залежність: зміни симпатичного тонусу від –19 до +10 % були тісно та обернено (r = –0,91) пов’язані зі змінами діастолічного АТ від +17 до –7 мм рт.ст. Дискримінантний аналіз ідентифікував 24 супутні змінні (Wilks’ = 0,025; F = 3,48; p < 10–5) та 24 предиктори (Wilks’ = 0,019; F = 4,70; p < 10–6), які диференціюють ці кластери. Точність класифікації становила 97,7 % (100 % для парадоксального кластера). Парадоксальна реакція АТ на зміни LFnu супроводжувалася такою ж інверсійною кореляцією зі змінами IgM сироватки (r = –0,85), інтенсивності фагоцитозу E.coli нейтрофілами (r = –0,72), активності каталази сироватки (r = –0,68) і урикозурії (r = –0,61), натомість позитивною кореляцією зі змінами амплітуди -ритму (r = 0,75) і щільності спектра потужності (ЩСП) в локусах F7 (r = 0,74), C4 (r = 0,71) і P4 (r = 0,70), а також ЩСП -ритму в локусі F7 (r = 0,73) і -ритму в локусі F8 (r = 0,70). Парадоксальна реакція була передбачена: підвищеним початковим симпатичним тонусом (маркери: LFnu та LF/HF),
зниженим вагусним тонусом (маркер: HF); підвищеною реакцією систолічного АТ на оклюзію плечової артерії під час його реєстрації (маркери: співвідношення Ps3/Ps1 та Ps2/Ps1); нормальними базальними рівнями каталази й кальцитоніну сироватки; зниженими базальними рівнями ентропії ЩСП у локусах F3 та C3, а також ЩСП -ритму в локусах F3 та C4 та -ритму в локусах F8 та T4. Висновки. Дослідження демонструє, що очевидна слабка кореляція між симпатичним тонусом та діастолічним АТ на рівні популяції маскує три якісно різні моделі реакції, включно з парадоксальною оберненою залежністю у 20,5 % пацієнтів. Ця парадоксальна реакція пов’язана зі специфічними нейроендокринно-імунометаболічними профілями та може бути передбачена з високою точністю (97,7 %) при використанні початкових параметрів. Результати дослідження ставлять під сумнів універсальність класичної парадигми симпатичної регуляції АТ і забезпечують наукову основу для персоналізованих підходів до оцінки та терапії серцево-судинної системи в бальнеологічній
практиці.
Background. In a previous study in line with the tensioregulome concept, we found that, firstly, the correlation between changes in systolic and diastolic blood pressure (BP) under the influence of balneotherapy is only of moderate strength; secondly, the correlations between changes in both components of BP, on the one hand, and heart rate variability (HRV) markers of both sympathetic and vagal tones, on the other hand, are on the verge of significance or even insignificant. We assumed that the directionality and severity of the autonomic nervous system influence on BP are determined by concomitant changes in the constellation of parameters of the neuro-endocrine-immune complex and metabolism, and can be predicted by the same or a different combination. The purpose of this study is to test these hypotheses. Materials and methods. Under observation, there were 44 patients with chronic pyelonephritis and cholecystitis in the phase of remission. Testing was performed twice — on admission and after 7–10 days of standard balneotherapy on the Truskavets Spa. The objects of the study were BP and HRV, electroencephalographic, endocrine, immune, and metabolic variables. Results. In the first stage of analysis, the information field of seemingly chaotic (r = 0.25) sympathetic tone/BP diastolic relationships was fragmented into three clusters. The first cluster (n = 16; 36.3 %) demonstrated a classic direct relationship (r = +0.91): changes in sympathetic tone (LFnu) from –17 to +14 % were associated with changes in diastolic BP from –13 to +22 mmHg. The second cluster (n = 19; 43.1 %) showed areactivity (r = 0.24): despite significant fluctuations in sympathetic tone (from –44 to +46 %), diastolic BP remained relatively stable (changes from –4 to +8 mmHg). The third cluster (n = 9; 20.5 %) revealed a paradoxical inverse relationship: changes in sympathetic tone from –19 to +10 % were closely and inverse (r = –0.91) associated with changes in diastolic BP from +17 to –7 mmHg. Discriminant analysis identified 24 concomitant variables (Wilks’ = 0.025; F = 3.48; p < 10–5) and 24 predictors (Wilks’ = 0.019; F = 4.70; p < 10–6) that differentiate these clusters. Classification accuracy reached 97.7 % (100 % for paradoxical cluster). The paradoxical response of BP to changes in LFnu was accompanied by the same inverse correlation with changes in serum IgM (r = –0.85), intensity of E.coli phagocytosis by neutrophils (r = –0.72), serum catalase activity (r = –0.68) and uricosuria (r = –0.61), but with a positive correlation with changes in the amplitude of the -rhythm (r = 0.75) and its spectral power density (SPD) in loci F7 (r = 0.74), C4 (r = 0.71) and P4 (r = 0.70), as well as in the SPD of the -rhythm in locus F7 (r = 0.73) and -rhythm in locus F8 (r = 0.70). The paradoxical reaction was predicted by elevated baseline sympathetic tone (markers: LFnu and LF/HF), decreased vagal tone (marker: HF); increased systolic BP response to brachial artery occlusion during BP registration (markers: Ps3/Ps1 and Ps2/Ps1 ratio); normal basal levels of catalase and calcitonin; reduced basal levels of SPD entropy in loci F3 and C3, as well as SPD of the -rhythm in loci F3 and C4 and -rhythm in loci F8 and T4. Conclusions. The study demonstrates that the apparent weak correlation between sympathetic tone and diastolic BP at the population level masks three qualitatively distinct response patterns, including a paradoxical inverse relationship in 20.5 % of patients. This paradoxical reaction is associated with specific neuro-endocrine-immuno-metabolic profiles and can be predicted with high accuracy (97.7 %) using baseline parameters. The findings challenge the universality of the classical paradigm of sympathetic BP regulation and provide a scientific basis for personalized approaches to cardiovascular assessment and therapy in balneological practice.
діастолічний артеріальний тиск; симпатичний тонус; варіабельність серцевого ритму; парадоксальна реакція; електроенцефалографія; гормони адаптації; імунітет; метаболіти; нейроімуно-ендокринні взаємодії; персоналізована медицина; бальнеотерапія; курорт Трускавець; тензіорегулом
diastolic blood pressure; sympathetic tone; heart rate variability; paradoxical reaction; electroencephalography; adaptation hormones; immunity; metabolites; neuro-immuno-endocrine interactions; personalized medicine; balneotherapy; Truskavets Spa; tensioregulome