Вступ
Гострий мозковий інсульт залишається однією з провідних причин смертності, довготривалої інвалідизації та втрати працездатності у світі, формуючи суттєвий медико-соціальний та економічний тягар [1]. Попри значний прогрес у розвитку реперфузійних технологій, оптимізації інтенсивної терапії та впровадженні стандартизованих протоколів лікування, ішемічний інсульт і надалі характеризується високою варіабельністю клінічного перебігу та результатів відновлення. У зв’язку з цим особливої актуальності набуває пошук модифікуючих факторів, що впливають на тяжкість первинного ушкодження мозкової тканини та подальший функціональний прогноз.
Одним із таких факторів є порушення вуглеводного обміну [2]. Цукровий діабет 2-го типу (ЦД2) розглядається як незалежний фактор ризику розвитку інсульту та асоціюється з більш ніж дворазовим підвищенням імовірності його виникнення. Крім того, наявність ЦД2 обумовлює більш тяжкий клінічний перебіг, більший об’єм ішемічного ураження, підвищений ризик геморагічної трансформації та вищу летальність як у гострому періоді, так і в довгостроковій перспективі [3]. Хронічна гіперглікемія сприяє розвитку діабетичної макро- та мікроангіопатії, ремоделюванню судинної стінки, зниженню ендотелійзалежної вазодилатації та порушенню авторегуляції мозкового кровотоку, що зменшує цереброваскулярний резерв і обмежує адаптаційні можливості мозку в умовах ішемії.
Водночас підвищення рівня глюкози крові в гострому періоді інсульту реєструється у значної частки пацієнтів, у тому числі без попередньо встановленого діабету. Стресіндукована гіперглікемія є складною нейроендокринною реакцією на гостре церебральне ушкодження, що реалізується через активацію гіпоталамо-гіпофізарно-наднирникової осі та симпатоадреналової системи [4]. Надлишкова секреція кортизолу, катехоламінів і глюкагону, підвищення рівня вільних жирних кислот та формування інсулінорезистентності сприяють гіперглікемії, яка, у свою чергу, потенціює оксидативний стрес, посилює системну запальну відповідь і поглиблює метаболічну дисфункцію ішемізованої тканини мозку [5]. Активація прооксидантних механізмів, підвищення проникності гематоенцефалічного бар’єра, ендотеліальна дисфункція та формування протромботичного стану створюють умови для розширення інфарктної зони та прогресування неврологічного дефіциту [6, 7].
Таким чином, як хронічна гіперглікемія при ЦД2, так і транзиторне підвищення глікемії в гострому періоді інсульту можуть розглядатися як потенційні детермінанти несприятливого перебігу та відновлення. Водночас механізми їх впливу не є ідентичними: у випадку ЦД2 домінують структурні судинні зміни та тривала метаболічна дисфункція, тоді як при стресовій гіперглікемії провідну роль відіграють гострі нейроендокринні та запальні реакції [8‒10]. Це зумовлює необхідність диференційованого підходу до оцінки клінічних результатів залежно від глікемічного профілю пацієнта.
Ключовим елементом об’єктивізації клінічного стану при ішемічному інсульті є застосування валідизованих кількісних шкал. NIHSS забезпечує стандартизовану оцінку вираженості неврологічного дефіциту та дає змогу стратифікувати тяжкість інсульту в динаміці [11]. Модифікована шкала Ренкіна (mRS) використовується для інтегральної оцінки ступеня інвалідизації та функціонального прогнозу, тоді як індекс Бартел характеризує рівень автономності пацієнта у виконанні базових повсякденних активностей і відображає ступінь залежності від сторонньої допомоги. Комплексне застосування цих інструментів створює можливість багатовимірної оцінки клінічних наслідків інсульту, поєднуючи аналіз неврологічного дефіциту, соціальної адаптації та функціональної незалежності [12].
Попри наявність значної кількості досліджень, присвячених ролі гіперглікемії при ішемічному інсульті, результати щодо її впливу на ранню динаміку неврологічного дефіциту та функціональну незалежність залишаються неоднозначними [13]. Недостатньо уніфікованою залишається порівняльна оцінка пацієнтів із нормоглікемією, транзиторною гіперглікемією та ЦД2 з позицій стандартизованих клінічних шкал у перші дні госпіталізації. Саме ранній період має принципове значення для прогнозування подальшого відновлення, стратифікації ризику ускладнень та оптимізації лікувально-реабілітаційної тактики [14].
У цьому контексті інтегративний аналіз показників неврологічного дефіциту та функціональної незалежності з урахуванням глікемічного статусу дає змогу не лише поглибити розуміння патофізіологічних механізмів церебрального ушкодження, але й уточнити клінічні предиктори несприятливого перебігу, що є підґрунтям для персоналізованого підходу до ведення пацієнтів з ішемічним інсультом.
Мета роботи: провести поглиблений порівняльний аналіз показників неврологічного дефіциту та функціональної незалежності у пацієнтів з ішемічним інсультом залежно від стану вуглеводного обміну (нормоглікемія, транзиторна гіперглікемія, цукровий діабет 2-го типу) за даними шкал NIHSS, модифікованої шкали Ренкіна (mRS) та індексу Бартел з оцінкою їх динаміки в ранньому госпітальному періоді.
Матеріали та методи
Нами було проведено клініко-інструментальне обстеження 124 пацієнтів з ішемічним інсультом (59 жінок, 65 чоловіків; вік 43–80 років). Середній вік жінок становив 69,5 ± 1,3 року, чоловіків — 66,3 ± 1,25 року (медіана 73 та 69 років відповідно, р = 0,041).
Інсульт верифіковано у таких басейнах головного мозку: права середня мозкова артерія — 27,4 %, ліва середня мозкова артерія — 57,25 %, ліва задня мозкова артерія — 7,25 %, права задня мозкова артерія — 8,06 %. Переважали ураження середніх мозкових артерій (> 84 %).
Серед коморбідної патології: цукровий діабет 2-го типу — 50,8 %, транзиторна гіперглікемія — 25 %, фібриляція передсердь — 33,9 %, артеріальна гіпертензія — 87,9 %, ожиріння — 30,6 %, хронічна хвороба нирок — 21 %, серцева недостатність — 36,3 %, дихальна недостатність — 12,9 %.
Пацієнти розподілені на групи:
1. Контрольна (І; n = 30): гострий мозковий інсульт без супутніх метаболічних порушень.
2. Основна група:
2.1. Підгрупа II (n = 31): гострий мозковий інсульт + транзиторна гіперглікемія.
2.2. Підгрупа III (n = 63): гострий мозковий інсульт + цукровий діабет 2-го типу.
Результати
Порівняльна оцінка показників за шкалами NIHSS, Ренкіна та індексу Бартел у пацієнтів з гострим мозковим інсультом та транзиторною гіперглікемією
До цієї групи входив 31 пацієнт з гострим мозковим інсультом та транзиторною гіперглікемією. Пацієнти групи мали транзиторне підвищення рівня глюкози крові в середньому до 11 ммоль і в середньому на 3 доби.
Середній вік пацієнтів з транзиторною гіперглікемією становив 68,51 ± 1,28 року, Me [Q1–Q3]: 70 [62–77] років. Порівняно з іншими групами пацієнти з транзиторною гіперглікемією були дещо старшими (пацієнти з цукровим діабетом 2-го типу — 65,1 ± 1,91 року, Me [Q1–Q3]: 67 [58–75] років).
Вираженість неврологічного дефіциту на момент госпіталізації та виписки (через 5–7 діб після госпіталізації) була оцінена за шкалою Національного інституту здоров’я США (шкала NIHSS). При госпіталізації: середнє значення становило 8,13 ± 4,16, Me [Q1–Q3]: 7 [6–9,5]. При виписці: середнє значення було 3,7 ± 2,9, Me [Q1–Q3]: 2 [2–4] (p < 0,001).
На момент виписки ступені інвалідизації за шкалою Ренкіна у пацієнтів з транзиторною гіперглікемією розподілилися так: 1 бал — 32,3 % (10/31), 2 бали — 32,3 % (10/31), 3 бали — 16,1 % (5/31), 4 бали — 9,7 % (3/31), 5 балів — 3,2 % (1/31), 6 балів — 6,5 % (2/31). Таким чином, сприятливий функціональний результат (0–2 бали) на момент виписки отримали 64,6 % пацієнтів цієї групи (табл. 1).
Оцінка функціонального стану пацієнтів з транзиторною гіперглікемією на момент виписки за шкалою Ренкіна показала переважання сприятливого результату. Найбільшими були частки пацієнтів з 1 та 2 балами за шкалою Ренкіна — по 32,3 %, що відповідає відсутності значних обмежень у повсякденній активності. Загалом сприятливий функціональний результат (0–2 бали) спостерігався у 64,6 % обстежених. Помірна інвалідизація (3 бали) фіксувалася у 16,1 % пацієнтів, а несприятливі результати (4–6 балів) — у 19,4 % випадків, що свідчить про потребу в сторонній допомозі лише у цієї меншої частини когорти.
Клінічно стресова гіперглікемія негативно впливає на функціональний результат, але меншою мірою, ніж хронічні порушення вуглеводного обміну. Одним із підтверджень цього є дані нашого спостереження — середнє значення індексу Бартел: 75,8 ± 33,42, Me [Q1–Q3]: 90 [75–100]. Тобто пацієнти з транзиторною гіперглікемією мали високий індекс Бартел, що свідчить про незначну залежність від сторонньої допомоги.
Порівняльна оцінка показників за шкалами NIHSS, Ренкіна та індексу Бартел у пацієнтів з гострим мозковим інсультом та цукровим діабетом 2-го типу
У цю групу було включено 63 пацієнти з гострим мозковим інсультом та цукровим діабетом 2-го типу. Середній вік пацієнтів із ЦД2 становив 65,26 ± 1,07 року, Me [Q1–Q3]: 66 [58–73] років; тоді як без цього захворювання пацієнти в середньому мали інсульт у віці 68,51 ± 1,28 року, Me [Q1–Q3]: 70 [62–77] років. Отже, пацієнти з ЦД2 були молодшими за тих, хто не мав цукрового діабету в анамнезі. Серед усіх пацієнтів цієї групи у 42,85 % (27/63) пацієнтів стаж цукрового діабету становив від 7 до 10 років, у 12,09 % (15/63) — від 2 до 5 років, у 16,93 % (21/63) пацієнтів цукровий діабет був уперше виявлений.
Вираженість неврологічного дефіциту на момент госпіталізації та виписки у хворих була оцінена за шкалою NIHSS. При госпіталізації: середнє значення бала за шкалою NIHSS становило 10,41 ± 7,16, Me [Q1–Q3]: 7 [5–14]. При виписці середній бал становив 4,8 ± 3,7, Me [Q1–Q3]: 4 [2–6] (p < 0,001).
На момент виписки ступені інвалідизації за шкалою Ренкіна у пацієнтів із цукровим діабетом 2-го типу розподілилися так: 1 бал — 9,5 % (n = 6/63), 2 бали — 28,6 % (n = 18/63), 3 бали — 27,0 % (n = 17/63), 4 бали — 12,7 % (n = 8/63), 5 балів — 9,5 % (n = 6/63), 6 балів — 12,7 % (n = 8/63) пацієнтів (табл. 2).
Аналіз розподілу пацієнтів за шкалою Ренкіна на момент виписки показав, що помірна інвалідизація (3 бали) та несприятливі результати (4–6 балів) разом становили переважну більшість — 61,9 % — пацієнтів (39 з 63). Зокрема, на частку несприятливого результату припало 34,9 % випадків (22 пацієнти, бали 4–6), що свідчить про значне обмеження функціональної самостійності та потребу в сторонній допомозі. Частка хворих із помірною інвалідизацією (3 бали) становила 27,0 % (17 пацієнтів). Сприятливий результат (самостійні пацієнти з балами 0–2) спостерігався у 38,1 % пацієнтів (24 людини).
Отримані дані вказують на незадовільні функціональні результати лікування на момент виписки та підкреслюють потребу в подальшій реабілітації, а також оптимізації ранніх лікувально-реабілітаційних заходів у цієї категорії хворих.
Середнє значення індексу Бартел на момент виписки становило 64,67 ± 36,3, Me [Q1–Q3]: 80 [50–95]. Це вказує на значне зниження функціональних можливостей пацієнтів з ГМІ та ЦД2.
Порівняльна оцінка показників за шкалами NIHSS, Ренкіна та індексу Бартел у пацієнтів з гострим мозковим інсультом (контрольна група, 30 пацієнтів)
У цю групу було включено 30 пацієнтів. Середній вік хворих — 65,26 ± 1,07 року, Me [Q1–Q3]: 66 [58–73] років.
Вираженість неврологічного дефіциту за шкалою Національного інституту здоров’я США (шкала NIHSS) при госпіталізації: середнє значення 8,73 ± 5,86, Me [Q1–Q3]: 7,5 [4–13], при виписці: 4,7 ± 3,9, Me [Q1–Q3]: 2 [2–6,7] (p < 0,001). Контрольна група та хворі з транзиторною гіперглікемією мали схожі показники за NIHSS при госпіталізації, однак показники останніх при виписці значно поліпшилися.
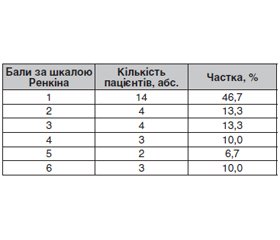
На момент виписки в контрольній групі переважало низьке значення шкали Ренкіна — 1 бал, яке спостерігалося у 46,7 % (n = 14/30) пацієнтів. Інші показники розподілилися так: 2 бали — 13,3 % (n = 4/30), 3 бали — 13,3 % (n = 4/30), 4 бали — 10,0 % (n = 3/30), 5 балів — 6,7 % (n = 2/30), 6 балів — 10,0 % (n = 3/30). Таким чином, сприятливий результат (0–2 бали) отримали 60,0 % пацієнтів. Нормоглікемія асоціюється з кращим функціональним відновленням та сприятливим прогнозом за шкалою Ренкіна (табл. 3).
Результати оцінки неврологічного дефіциту за шкалою NIHSS демонструють подібну тяжкість стану на момент госпіталізації в усіх трьох групах, що підтверджується близькими значеннями медіани: 7 балів у групі цукрового діабету (ЦД), 7 балів у групі з гіперглікемією (ГГ) та 7,5 бала у контрольній групі. Однак група ЦД виділялася найбільшим розкидом значень та найвищим середнім балом (10,41 ± 7,16), що вказує на більшу нерівномірність тяжкості інсульту серед цих пацієнтів — від легких до дуже тяжких форм. Після проведеного лікування у всіх групах спостерігалося вірогідне зменшення неврологічного дефіциту, проте група ЦД, незважаючи на поліпшення, продовжувала мати найбільший розкид значень (4,8 ± 3,7) та найвищу медіану (4 бали) після лікування, що може свідчити про менш прогнозований та менш сприятливий відновлювальний потенціал у пацієнтів із супутнім цукровим діабетом 2-го типу порівняно з іншими групами (р = 0,03).
На момент виписки у пацієнтів контрольної групи (нормоглікемія) найбільш поширеним було низьке значення шкали Ренкіна, що відображає відносно сприятливий функціональний результат. У 60,0 % хворих показники становили 1–2 бали, що відповідає відсутності значних обмежень у повсякденній активності. Частка пацієнтів з помірною інвалідизацією (3 бали) становила 13,3 %, а з несприятливим результатом (4–6 балів) — 26,7 %. При цьому тяжкі функціональні обмеження (5–6 балів) фіксувалися у 16,7 % випадків.
Отримані дані свідчать, що нормоглікемія асоціюється з більш сприятливим функціональним відновленням і кращим прогнозом за шкалою Ренкіна на момент виписки, що підкреслює важливу роль глікемічного контролю у перебігу та наслідках гострого інсульту.
Середнє значення індексу Бартел: 72,7 ± 35,2, Me [Q1–Q3]: 90 [42–100]. Пацієнти контрольної групи мали високий рівень функціональної незалежності.
Таким чином, група пацієнтів з транзиторною гіперглікемією демонструє тенденцію до найкращих усереднених функціональних результатів (найвища медіана та найнижчий квартиль) порівняно з іншими групами. Однак статистично значущої переваги групи ГГ над контрольною групою не виявлено — їхні медіанні значення ідентичні (90 балів), а середні значення близькі. Група пацієнтів з цукровим діабетом 2-го типу мала найгірші усередненні показники (найнижча медіана та середнє значення) порівняно з групою контролю (р = 0,045), що може свідчити про негативний вплив хронічного метаболічного порушення на відновлення функціональної самостійності після інсульту.
Обговорення
Результати нашого дослідження корелюють із даними літератури, згідно з якими порушення вуглеводного обміну є значущим прогностичним фактором функціонального відновлення після гострого мозкового інсульту [7]. Попри подібну початкову тяжкість неврологічного дефіциту за шкалою NIHSS у всіх трьох групах — Me 7,0 [Q1–Q3], подальші результати відновлення суттєво відрізнялися.
Пацієнти з транзиторною (стресіндукованою) гіперглікемією продемонстрували позитивну динаміку неврологічного дефіциту та високий рівень функціональної незалежності на момент виписки. Більшість з них досягли сприятливого результату за шкалою Ренкіна, а медіанне значення індексу Бартел становило 90 балів, що відповідає мінімальній залежності від сторонньої допомоги.
Ймовірно, транзиторна гіперглікемія відображає реакцію організму на гострий стрес та активацію контр–інсулярних гормонів, а не хронічне судинне ушкодження. За відсутності тривалих метаболічних змін та діабетичної ангіопатії компенсаторні можливості мозкової тканини залишаються відносно збереженими. Це пояснює подібність функціональних результатів цієї групи до контрольної.
Водночас транзиторна гіперглікемія не може розглядатися як повністю нейтральний фактор, оскільки гіперглікемія в гострому періоді інсульту здатна посилювати ішемічне ушкодження через підвищення лактат-ацидозу, оксидативного стресу та порушення гематоенцефалічного бар’єра [15]. Проте за умови своєчасної корекції її вплив є менш вираженим порівняно з хронічними метаболічними порушеннями.
Найгірші показники функціонального відновлення продемонстрували пацієнти з цукровим діабетом 2-го типу. Незважаючи на вірогідне поліпшення неврологічного статусу в динаміці лікування, вони зберігали вищі показники залишкового дефіциту та більшу частку несприятливих результатів за шкалою Ренкіна. Крім того, їхній індекс Бартел був вірогідно нижчим порівняно з контрольною групою (p = 0,045).
Це може бути зумовлено низкою патофізіологічних механізмів: хронічною ендотеліальною дисфункцією, мікро- та макроангіопатією, зниженням колатерального кровообігу, підвищеним рівнем системного запалення, порушенням нейропластичності [16].
Висновки
1. У пацієнтів із гострим ішемічним інсультом стан вуглеводного обміну є значущим предиктором клінічного перебігу та функціонального відновлення у ранньому госпітальному періоді.
2. У всіх досліджуваних групах спостерігалося статистично значуще зменшення неврологічного дефіциту за шкалою NIHSS у динаміці лікування (p < 0,001), що підтверджує ефективність базисної терапії інсульту. Водночас ступінь залишкового неврологічного дефіциту був вищим у пацієнтів із цукровим діабетом 2-го типу.
3. Найбільш сприятливі функціональні результати за шкалами mRS та індексом Бартел спостерігалися у пацієнтів з нормоглікемією, що характеризувалося більш високим рівнем функціональної незалежності та нижчим ступенем інвалідизації.
4. Транзиторна гіперглікемія асоціювалася з проміжними функціональними результатами: більшість пацієнтів досягали задовільного функціонального відновлення, однак гіперглікемія в гострому періоді інсульту потенційно могла посилювати ішемічне ушко–дження за рахунок метаболічного та оксидативного стресу.
5. Хронічна гіперглікемія при цукровому діабеті 2-го типу асоціювалася з найгіршими функціональними наслідками, що проявлялося більшою часткою пацієнтів із помірною та тяжкою інвалідизацією та нижчими показниками індексу Бартел (p = 0,045).
6. Отримані результати підтверджують роль порушень вуглеводного обміну як важливого модифікуючого фактора прогнозу ішемічного інсульту та обґрунтовують потребу в ранньому індивідуалізованому глікемічному контролі як складовій лікувально-реабілітаційної стратегії.
7. Перспективним напрямком подальших досліджень є вивчення довгострокових клінічних наслідків інсульту залежно від типу гіперглікемії та оцінка їх взаємозв’язку з нейровізуалізаційними маркерами ішемічного ушкодження.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 01.12.2025
Рецензовано/Revised 17.02.2026
Прийнято до друку/Accepted 24.02.2026
/74.jpg)

/73.jpg)