Международный эндокринологический журнал Том 22, №2, 2026
Вернуться к номеру
Мультифакторний вплив клініко-метаболічних чинників на рівень лептину у пацієнтів з артеріальною гіпертензією та цукровим діабетом 2-го типу
Авторы: Кравчун Н.О., Дунаєва І.П., Кравчун П.П., Яковенко О.Л.
Харківський національний медичний університет, м. Харків, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
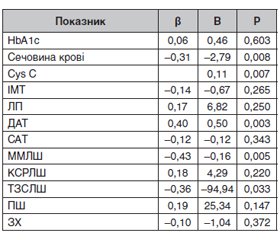
Актуальність. Артеріальна гіпертензія (АГ) у поєднанні з цукровим діабетом 2-го типу (ЦД2) є однією з провідних форм кардіометаболічної коморбідності, що супроводжується високим ризиком серцево-судинних і кардіоренальних ускладнень. Важливу роль у патогенезі цих порушень відіграють адипокіни, зокрема лептин, який інтегрує метаболічні, нейроендокринні та імунозапальні механізми. Однак мультифакторні детермінанти рівня лептину у пацієнтів з АГ та супутнім ЦД2 залишаються недостатньо вивченими. Мета: визначити мультифакторний вплив клініко-метаболічних, імунологічних, біохімічних та структурно-функціональних показників серцево-судинної системи на рівень лептину у пацієнтів з артеріальною гіпертензією, зокрема за наявності супутнього цукрового діабету 2-го типу. Матеріали та методи. У дослідження залучено 136 пацієнтів з АГ, яких розподілено на групу з ізольованою АГ (n = 64) та групу з поєднаним перебігом АГ і ЦД2 (n = 72); контрольну групу становили 20 практично здорових осіб. Усім обстеженим проведено комплексне клінічне, лабораторне, імунологічне та ехокардіографічне обстеження з визначенням показників ліпідного й вуглеводного обміну, маркерів ниркової функції, адипокінів (лептин), кардіоренальних біомаркерів та параметрів ремоделювання міокарда. Незалежні предиктори рівня лептину оцінювали за допомогою багатофакторного регресійного аналізу. Результати. У пацієнтів з АГ та супутнім ЦД2 виявлено більш виражені метаболічні, імунологічні та структурно-функціональні порушення порівняно з хворими з ізольованою АГ. Рівень лептину був вірогідно вищим у групі АГ і ЦД2 та асоціювався з індексом маси тіла, показниками вуглеводного обміну, маркерами ниркової дисфункції, параметрами клітинної ланки імунітету та ехокардіографічними ознаками ремоделювання міокарда. У загальній когорті АГ незалежними предикторами рівня лептину були діастолічний артеріальний тиск, концентрація цистатину C, маса міокарда лівого шлуночка та товщина його задньої стінки. У пацієнтів з АГ і ЦД2 рівень лептину додатково асоціювався з рівнем глікованого гемоглобіну, показниками ниркової функції, індексом маси тіла та показниками діастолічної функції серця. Висновки. Лептин у пацієнтів з АГ, особливо за наявності супутнього ЦД2, є інтегральним маркером кардіометаболічних, імунних та структурно-функціональних порушень. Виявлені мультифакторні асоціації підтверджують його значущу роль у формуванні кардіометаболічного ризику та обґрунтовують доцільність використання лептину для персоналізованої оцінки пацієнтів з коморбідною патологією.
Background. Arterial hypertension (AH) combined with type 2 diabetes mellitus (T2DM) is one of major cardiometabolic comorbidities associated with a high risk of cardiovascular and cardiorenal complications. Adipokines, particularly leptin, play a key role in integrating metabolic, neuroendocrine, and immune-inflammatory mechanisms. However, the multifactorial determinants of leptin levels in patients with AH and concomitant T2DM remain insufficiently elucidated. The purpose was to assess the multifactorial impact of clinical, metabolic, immunological, biochemical, structural and functional cardiovascular parameters on leptin levels in patients with arterial hypertension, particularly in the presence of type 2 diabetes mellitus. Materials and methods. The study included 136 patients with AH divided into groups with isolated AH (n = 64) and AH combined with T2DM (n = 72); 20 apparently healthy individuals constituted the control group. All participants underwent comprehensive clinical, laboratory, immunological, and echocardiographic assessment, including evaluation of lipid and carbohydrate metabolism, renal function markers, adipokines (leptin), cardiorenal biomarkers, and myocardial remodeling parameters. Independent predictors of leptin levels were identified using multivariate regression analysis. Results. Patients with AH and T2DM demonstrated more pronounced metabolic, immunological, structural and functional abnormalities compared to those with isolated AH. Leptin levels were significantly higher in the AH and T2DM group and were associated with body mass index, carbohydrate metabolism parameters, renal dysfunction markers, immune cell profiles, and echocardiographic indicators of myocardial remodeling. In the overall AH cohort, diastolic blood pressure, cystatin C concentration, left ventricular myocardial mass, and posterior wall thickness were independent predictors of leptin levels. In patients with AH and T2DM, leptin levels were additionally associated with HbA1c, renal function parameters, body mass index, and indices of diastolic dysfunction. Conclusions. In patients with arterial hypertension, especially those with concomitant type 2 diabetes mellitus, leptin serves as an integrative biomarker reflecting cardiometabolic, immune, structural and functional alterations. The identified multifactorial associations support its potential prognostic value in cardiometabolic risk stratification and personalized assessment of patients with comorbidity.
артеріальна гіпертензія; цукровий діабет 2-го типу; лептин; кардіометаболічний ризик; ремоделювання міокарда; імунні порушення
arterial hypertension; type 2 diabetes mellitus; leptin; cardiometabolic risk; myocardial remodeling; immune dysfunction
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- McEvoy JW, McCarthy CP, Bruno RM, Brouwers S, Cana–van MD, Ceconi C, et al.; ESC Scientific Document Group. 2024 ESC Guidelines for the management of elevated blood pressure and hypertension. Eur Heart J. 2024 Oct 7;45(38):3912-4018. doi: 10.1093/eurheartj/ehae178. Erratum in: Eur Heart J. 2025 Apr 7;46(14):1300. doi: 10.1093/eurheartj/ehaf031. Erratum in: Eur Heart J. 2025 Dec 1;46(45):4949. doi: 10.1093/eurheartj/ehaf659. PMID: 39210715.
- American Diabetes Association Professional Practice Committee. 2. Diagnosis and Classification of Diabetes: Standards of Care in Diabetes-2025. Diabetes Care. 2025 Jan 1;48(1 Suppl 1):S27-S49. doi: 10.2337/dc25-S002. PMID: 39651986; PMCID: PMC11635041.
- Obradovic M, Sudar-Milovanovic E, Soskic S, Essack M, Arya S, Stewart AJ, et al. Leptin and Obesity: Role and Clinical Implication. Front Endocrinol (Lausanne). 2021 May 18;12:585887. doi: 10.3389/fendo.2021.585887. PMID: 34084149; PMCID: PMC8167040.
- Pereira S, Cline DL, Glavas MM, Covey SD, Kieffer TJ. Tissue-Specific Effects of Leptin on Glucose and Lipid Metabolism. Endocr Rev. 2021 Jan 28;42(1):1-28. doi: 10.1210/endrev/bnaa027. PMID: 33150398; PMCID: PMC7846142.
- Perakakis N, Farr OM, Mantzoros CS. Leptin in Leanness and Obesity: JACC State-of-the-Art Review. J Am Coll Cardiol. 2021 Feb 16;77(6):745-760. doi: 10.1016/j.jacc.2020.11.069. PMID: 33573745; PMCID: PMC8483570.
- Stephan J. Guyenet, Michael W. Schwartz, Regulation of Food Intake, Energy Balance, and Body Fat Mass: Implications for the Pathogenesis and Treatment of Obesity, The Journal of Clinical Endocrinology & Metabolism. 2012 Mar 1;97(3):745-755. https://doi.org/10.1210/jc.2011-2525.
- Vilariño-García T, Polonio-González ML, Pérez-Pérez A, Ribalta J, Arrieta F, Aguilar M, et al. Role of Leptin in Obesity, Cardiovascular Disease, and Type 2 Diabetes. Int J Mol Sci. 2024 Feb 16;25(4):2338. doi: 10.3390/ijms25042338. PMID: 38397015; PMCID: PMC10888594.
- Wu XY, Song HB, Wang JW. The association between leptin and diabetes: A meta-analysis. J Obstet Gynaecol Res. 2024 Jul;50(7):1126-1131. doi: 10.1111/jog.15942. Epub 2024 Apr 9. PMID: 38594218.
- Tsuchiya H, Fujio K. Emerging role of leptin in joint inflammation and destruction. Immunol Med. 2022 Mar;45(1):27-34. doi: 10.1080/25785826.2021.1948689. Epub 2021 Aug 6. PMID: 34362290.
- Liu C, Li X. Role of leptin and adiponectin in immune response and inflammation. Int Immunopharmacol. 2025 Aug 28;161:115082. doi: 10.1016/j.intimp.2025.115082. Epub 2025 Jun 13. PMID: 40516255.
- Szumilas K, Wilk A, Szumilas P, Dziedziejko V, Pawlik A. Role of leptin and adiponectin in the pathogenesis of post-transplant diabetes mellitus. Prostaglandins Other Lipid Mediat. 2024 Oct;174:106876. doi: 10.1016/j.prostaglandins.2024.106876. Epub 2024 Jul 18. PMID: 39032860.
- Laule C, Rahmouni K. Leptin and Associated Neural Pathways Underlying Obesity-Induced Hypertension. Compr Physiol. 2025 Feb;15(1):e8. doi: 10.1002/cph4.8. PMID: 40293220; PMCID: PMC12038170.
- Dunaieva IP. Leptin as a marker of metabolic disorders in comorbid patients with arterial hypertension. Ukrainian Medical Journal. 2025;5(171):1-6. https://doi.org/10.32471/umj.1680-3051.267923.
- Sinha S, Haque M. Insulin Resistance Is Cheerfully Hitched with Hypertension. Life. 2022;12(4):564. https://doi.org/10.3390/life12040564.
- Didushko OM, Herych PR, Cherniavska IV, Yatsyshyn RI, Pankiv VI. Influence of the complex treatment of hypothyroidism on the leptin level in patients with primary hypothyroidism. World of Medicine and Biology. 2018;3(65):59-63. doi: 10.26724/2079-8334-2018-3-65-59-63.
- Mancusi C, Izzo R, di Gioia G, Losi MA, Barbato E, Morisco C. Insulin Resistance the Hinge Between Hypertension and Type 2 Diabetes. High Blood Press Cardiovasc Prev. 2020 Dec;27(6):515-526. doi: 10.1007/s40292-020-00408-8. Epub 2020 Sep 22. PMID: 32964344; PMCID: PMC7661395.
- Koval SM, Yushko KO, Snihurska IO, Starchenko TG, Pankiv VI, et al. Relations of angiotensin-(1-7) with hemodynamic and cardiac structural and functional parameters in patients with hypertension and type 2 diabetes. Arterial Hypertension. 2019;23(3):183-189. doi: 10.5603/AH.a2019.0012.
- Libby P, Hansson GK. From Focal Lipid Storage to Systemic Inflammation: JACC Review Topic of the Week. J Am Coll Cardiol. 2019 Sep 24;74(12):1594-1607. doi: 10.1016/j.jacc.2019.07.061. PMID: 31537270; PMCID: PMC6910128.
- Lee SH, Park SY, Choi CS. Insulin Resistance: From Mechanisms to Therapeutic Strategies. Diabetes Metab J. 2022 Jan;46(1):15-37. doi: 10.4093/dmj.2021.0280. Epub 2021 Dec 30. PMID: 34965646; PMCID: PMC8831809.
- Sharifi-Rad M, Anil Kumar NV, Zucca P, Varoni EM, Dini L, Panzarini E, et al. Oxidative stress, and antioxidants: back and forth in the pathophysiology of chronic diseases. Front Physiol. 2020 Jul;11:694. doi: 10.3389/fphys.2020.00694.