Международный эндокринологический журнал Том 22, №2, 2026
Вернуться к номеру
Метаболічні гормони та адипокіни як медіатори інсулінорезистентності, індукованої ожирінням
Авторы: Zina Lafta Hassan
College of Applied Sciences, University of Samarra, Samarra, Iraq
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
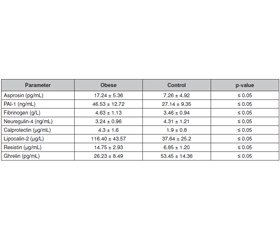
Актуальність. Ожиріння — це комплексне метаболічне захворювання, тісно пов’язане з інсулінорезистентністю, головним фактором розвитку цукрового діабету 2-го типу i серцево-судинних захворювань. Мета: оцінка рівнів ключових метаболічних гормонів та адипокінів в осіб з ожирінням і вивчення їх ролі як медіаторів у розвитку інсулінорезистентності порівняно зі здоровими людьми контрольної групи. Матеріали та методи. Дослідження типу «випадок — контроль» проведено в м. Самарра (Ірак) упродовж січня — квітня 2024 року за участю 55 чоловіків з ожирінням і 35 здорових чоловіків контрольної групи. Критерії включення: індекс маси тіла (ІМТ) ≥ 30 кг/м2 для досліджуваної групи та 18,5–24,9 кг/м2 — для контрольної. Після схвалення комісією з етики та отримання інформаційної згоди було зібрано зразки крові натще (10 мл). Рівень адипокінів, інсуліну та метаболічних маркерів у сироватці крові вимірювали за допомогою імуноферментного аналізу. Результати. Дослідження виявило вірогідні відмінності (р ≤ 0,05) між пацієнтами з ожирінням та контрольною групою за ІМТ і показниками ліпідного профілю, причому в осіб з ожирінням спостерігалися вищі ІМТ, концентрації загального холестерину, тригліцеридів, ліпопротеїнів низької та дуже низької щільності, а також нижчий уміст захисних ліпопротеїнів високої щільності, що свідчить про порушення ліпідного обміну й підвищений ризик серцево-судинних захворювань. Маркери глікемічного контролю (глюкоза в крові натще, глікований гемоглобін, інсулін, HOMA-IR) були підвищені при ожирінні, тоді як індекс QUICKI знижувався, що підтверджує інсулінорезистентність. Запальні маркери (аспрозин, інгібітор активатора плазміногену-1, фібриноген, кальпротектин, ліпокалін-2, резистин) були вищими, тоді як нейрeгулін-4 та грелін — нижчими, що відображає гормональну й запальну дисрегуляцію, пов’язану з ожирінням. Висновки. Ожиріння викликає інсулінорезистентність через гормональний і запальний дисбаланс, включно з підвищеним рівнем адипокінів та метаболічних гормонів, що порушує метаболізм глюкози й ліпідів. Хронічне запалення та змінений рівень гормонів погіршують передачу сигналів інсуліну, збільшуючи ризик метаболічних захворювань, як-от цукровий діабет 2-го типу, й серцево-судинних ускладнень.
Background. Obesity is a complex metabolic disorder strongly associated with insulin resistance, a key factor in the development of type 2 diabetes mellitus and cardiovascular diseases. The purpose of this study is to evaluate the levels of key metabolic hormones and adipokines in obese individuals and investigate their role as mediators in the development of insulin resistance compared to healthy controls. Materials and methods. This case-control study was conducted in Samarra, Iraq (January-April 2024) on 55 obese males and 35 healthy male controls. Inclusion required body mass index (BMI) ≥ 30 kg/m2 for cases and 18.5–24.9 kg/m2 for controls, excluding chronic diseases. After ethical approval and consent, fasting blood samples (10 mL) were collected, centrifuged, and stored at –20 °C. Serum levels of adipokines, insulin, and metabolic markers were measured using enzyme-linked immunosorbent assay. Results. The study revealed significant differences (p ≤ 0.05) between obese and control groups in BMI and lipid profiles, with higher BMI, total cholesterol, triglycerides, low-density lipoprotein, and very-low-density lipoprotein, and lower protective high-density lipoprotein in obese individuals, indicating disrupted lipid metabolism and increased cardiovascular risk. Glycemic control markers (fasting blood glucose, glycated hemoglobin, insulin, HOMA-IR) were elevated in obesity, while quantitative insulin sensitivity check index decreased, confirming insulin resistance. Inflammatory markers (asprosin, plasminogen activator inhibitor-1, fibrinogen, calprotectin, lipocalin-2, resistin) were higher, whereas neuregulin-4 and ghrelin were lower, reflecting hormonal and inflammatory dysregulation linked to obesity. Conclusions. Obesity induces insulin resistance through hormonal and inflammatory imbalances, including elevated adipokines and metabolic hormones that disrupt glucose and lipid metabolism. Chronic inflammation and altered hormone levels impair insulin signaling, increasing the risk of metabolic diseases such as type 2 diabetes mellitus and cardiovascular complications.
ожиріння; інсулінорезистентність; адипокіни; метаболічні гормони; запалення; ліпідний обмін
obesity; insulin resistance; adipokines; metabolic hormones; inflammation; lipid metabolism
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Zhang H, Zhou XD, Shapiro MD, Lip GYH, Tilg H, et al. Global burden of metabolic diseases, 1990-2021. Metabolism. 2024 Nov;160:155999. doi: 10.1016/j.metabol.2024.155999.
- Ruze R, Liu T, Zou X, Song J, Chen Y, et al. Obesity and type 2 diabetes mellitus: connections in epidemiology, pathogenesis, and treatments. Front Endocrinol (Lausanne). 2023 Apr 21;14:1161521. doi: 10.3389/fendo.2023.1161521.
- Hayden MR. Overview and New Insights into the Metabolic Syndrome: Risk Factors and Emerging Variables in the Development of Type 2 Diabetes and Cerebrocardiovascular Disease. Medicina (Kaunas). 2023 Mar 13;59(3):561. doi: 10.3390/medicina59030561.
- Pogodziński D, Ostrowska L, Smarkusz-Zarzecka J, Zyśk B. Secretome of Adipose Tissue as the Key to Understanding the Endocrine Function of Adipose Tissue. Int J Mol Sci. 2022 Feb 19;23(4):2309. doi: 10.3390/ijms23042309.
- Martins FF, Souza-Mello V, Aguila MB, Mandarim-de-La–cerda CA. Brown adipose tissue as an endocrine organ: updates on the emerging role of batokines. Horm Mol Biol Clin Investig. 2022 Oct 26;44(2):219-227. doi: 10.1515/hmbci-2022-0044.
- Püschel GP, Klauder J, Henkel J. Macrophages, Low-Grade Inflammation, Insulin Resistance and Hyperinsulinemia: A Mutual Ambiguous Relationship in the Development of Metabolic Diseases. J Clin Med. 2022 Jul 27;11(15):4358. doi: 10.3390/jcm11154358.
- Ashour MA, Wadea FM, Hussein NM, Elnagar AE. Insulin resistance, resistin hormone and hepatocellular carcinoma interplay: a review article. Egypt J Hosp Med. 2023 Jan 1;90(2):2041-2044. doi: 10.21608/EJHM.2023.285028.
- Didushko OM, Herych PR, Cherniavska IV, Yatsyshyn RI, Pankiv VI. Influence of the complex treatment of hypothyroidism on the leptin level in patients with primary hypothyroidism. World of Medicine and Biology. 2018;3(65):59-63. doi: 10.26724/2079-8334-2018-3-65-59-63.
- Wang Y, Wu Q, Zhou Q, Chen Y, Lei X, et al. Circulating acyl and des-acyl ghrelin levels in obese adults: a systematic review and meta-analysis. Sci Rep. 2022 Feb 17;12(1):2679. doi: 10.1038/s41598-022-06636-3.
- Mitoiu BI, Nartea R, Miclaus RS. Impact of Resistance and Endurance Training on Ghrelin and Plasma Leptin Levels in Overweight and Obese Subjects. Int J Mol Sci. 2024 Jul 24;25(15):8067. doi: 10.3390/ijms25158067.
- Sitar-Tut AV, Cozma A, Fodor A, Coste SC, Orasan OH, et al. New Insights on the Relationship between Leptin, Ghrelin, and Leptin/Ghrelin Ratio Enforced by Body Mass Index in Obesity and Diabetes. Biomedicines. 2021 Nov 10;9(11):1657. doi: 10.3390/biomedicines9111657.
- Roy PK, Islam J, Lalhlenmawia H. Prospects of potential adipokines as therapeutic agents in obesity-linked atherogenic dyslipi–demia and insulin resistance. Egypt Heart J. 2023 Apr 4;75(1):24. doi: 10.1186/s43044-023-00352-7.
- Koval SM, Yushko KO, Snihurska IO, Starchenko TG, Pankiv VI, et al. Relations of angiotensin-(1–7) with hemodynamic and cardiac structural and functional parameters in patients with hypertension and type 2 diabetes. Arterial Hypertension. 2019;23(3):183-189. doi: 10.5603/AH.a2019.0012.
- Gołacki J, Matuszek M, Matyjaszek-Matuszek B. Link between Insulin Resistance and Obesity — From Diagnosis to Treatment. Diagnostics (Basel). 2022 Jul 10;12(7):1681. doi: 10.3390/diagnostics12071681.
- Berberich AJ, Hegele RA. A Modern Approach to Dyslipi–demia. Endocr Rev. 2022 Jul 13;43(4):611-653. doi: 10.1210/endrev/bnab037.
- Kong L, Zhao Q, Han Z, Xue W, Hu Z, et al. Prognostic signi–ficance of TG/HDL-C and non-HDL-C/HDL-C ratios in patients with non-small cell lung cancer: a retrospective study. J Int Med Res. 2022 Aug;50(8):3000605221117211. doi: 10.1177/03000605221117211.
- Nagarajan SR, Cross E, Sanna F, Hodson L. Dysregulation of hepatic metabolism with obesity: factors influencing glucose and lipid metabolism. Proc Nutr Soc. 2022 Mar;81(1):1-11. doi: 10.1017/S0029665121003761.
- Lee-Rueckert M, Canyelles M, Tondo M, Rotllan N, Kovanen PT, et al. Obesity-induced changes in cancer cells and their microenvironment: Mechanisms and therapeutic perspectives to manage dysregulated lipid metabolism. Semin Cancer Biol. 2023 Aug;93:36-51. doi: 10.1016/j.semcancer.2023.05.002.
- Kleiboeker B, Lodhi IJ. Peroxisomal regulation of energy homeostasis: Effect on obesity and related metabolic disorders. Mol Metab. 2022 Nov;65:101577. doi: 10.1016/j.molmet.2022.101577.
- Tahapary DL, Pratisthita LB, Fitri NA, Marcella C, Wafa S, et al. Challenges in the diagnosis of insulin resistance: focusing on the role of HOMA-IR and triglyceride/glucose index. Diabetes Metab Syndr. 2022 Aug 1;16(8):102581. doi: 10.1016/j.dsx.2022.102581.
- Biernacka-Bartnik A, Kocełak P, Owczarek AJ, Choręza PS, Markuszewski L, et al. The cut-off value for HOMA-IR discriminating the insulin resistance based on the SHBG level in women with polycystic ovary syndrome. Front Med (Lausanne). 2023 Mar 10;10:1100547. doi: 10.3389/fmed.2023.1100547.
- Paracha AI, Haroon ZH, Aamir M, Bibi A. Diagnostic Accuracy of Markers of Insulin Resistance (HOMA-IR) and Insulin Sensitivity (QUICKI) in Gestational Diabetes. J Coll Physicians Surg Pak. 2021 Sep;31(9):1015-1019. doi: 10.29271/jcpsp.2021.09.1015.
- Farrag M, Ait Eldjoudi D, González-Rodríguez M, Cordero-Barreal A, Ruiz-Fernández C, et al. Asprosin in health and disease, a new glucose sensor with central and peripheral metabolic effects. Front Endocrinol (Lausanne). 2023 Jan 5;13:1101091. doi: 10.3389/fendo.2022.1101091.
- Corica D, Pepe G, Aversa T, Currò M, Curatola S, et al. Meal-Related Asprosin Serum Levels Are Affected by Insulin Resistance and Impaired Fasting Glucose in Children with Obesity. Front Endocrinol (Lausanne). 2022 Jan 6;12:805700. doi: 10.3389/fendo.2021.805700.
- Goodarzi G, Setayesh L, Fadaei R, Khamseh ME, Aliakbari F, et al. Circulating levels of asprosin and its association with insulin resistance and renal function in patients with type 2 diabetes mellitus and diabetic nephropathy. Mol Biol Rep. 2021 Jul;48(7):5443-5450. doi: 10.1007/s11033-021-06551-2.
- Saenz-Pipaon G, Ravassa S, Larsen KL, Martinez-Aguilar E, Orbe J, et al. Lipocalin-2 and Calprotectin Potential Prognosis Biomarkers in Peripheral Arterial Disease. Eur J Vasc Endovasc Surg. 2022 Apr;63(4):648-656. doi: 10.1016/j.ejvs.2022.01.012.
- Zollner A, Schmiderer A, Reider SJ, Oberhuber G, Pfister A, et al. Faecal Biomarkers in Inflammatory Bowel Diseases: Calprotectin Versus Lipocalin-2 — a Comparative Study. J Crohns Colitis. 2021 Jan 13;15(1):43-54. doi: 10.1093/ecco-jcc/jjaa124.
- Deng M, Aberle MR, van Bijnen AAJHM, van der Kroft G, Lenaerts K, et al. Lipocalin-2 and neutrophil activation in pancrea–tic cancer cachexia. Front Immunol. 2023 Mar 15;14:1159411. doi: 10.3389/fimmu.2023.1159411.
- Aukan MI, Nymo S, Haagensli Ollestad K, Akersveen Boye–sen G, DeBenedictis JN, et al. Differences in gastrointestinal hormones and appetite ratings among obesity classes. Appetite. 2022 Apr 1;171:105940. doi: 10.1016/j.appet.2022.105940.
- Martínez-García MÁ, Moncayo S, Insenser M, Álvarez-Blasco F, Luque-Ramírez M, Escobar-Morreale HF. Postprandial respon–ses of circulating energy homeostasis mediators to single macronutrient challenges: influence of obesity and sex hormones. Food Funct. 2021;12(3):1051-1062. doi: 10.1039/D0FO02305A.