Международный эндокринологический журнал Том 22, №3, 2026
Вернуться к номеру
Біохімічні та метаболічні зміни функції печінки, пов’язані з дисфункцією щитоподібної залози: порівняльне клінічне дослідження
Авторы: Hala Mahdi Hamad, Fiham Jassim Al-Obaidi, Hind Younis Khalaf
Department of Biology, College of Science, University of Anbar, Anbar, Iraq
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
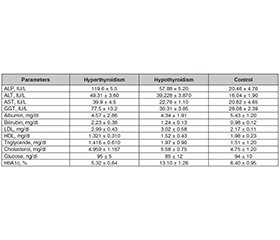
Актуальність. Гормони щитоподібної залози є важливими регуляторами системного метаболічного гомеостазу, зокрема ліпідного обміну та функції печінки. Дисфункція щитоподібної залози, включаючи гіпертиреоз і гіпотиреоз, зазвичай пов’язана з біохімічними й метаболічними порушеннями, які можуть збільшити ризик дисфункції печінки та дисліпідемії. Незважаючи на клінічну значущість цих змін, їх патогенез і ступінь вираженості залишаються недостатньо вивченими, особливо в популяціях із високою поширеністю захворювань щитоподібної залози. Мета: оцінити біохімічні й метаболічні зміни функції печінки та ліпідного профілю, пов’язані з дисфункцією щитоподібної залози, і порівняти їх у пацієнтів із гіпертиреозом, гіпотиреозом та здорових людей. Матеріали та методи. Було проведено дослідження типу «випадок — контроль» за участю 120 осіб, розділених на дві групи: пацієнти з гіпертиреозом (n = 60), хворі з гіпотиреозом (n = 60). Контрольну групу становили 30 практично здорових людей. Функцію щитоподібної залози визначали шляхом вимірювання сироваткових концентрацій тиреотропного гормону, трийодтироніну й тироксину. Стан печінки оцінювали за показниками аланінамінотрансферази (АЛТ), аспартатамінотрансферази (АСТ), лужної фосфатази (ЛФ) і гамма-глутамілтрансферази (ГГТ). Також аналізували параметри ліпідного профілю, включаючи загальний холестерин, тригліцериди, ліпопротеїни низької та високої щільності. Статистичний аналіз проводили з порогом значущості P ≤ 0,05. Результати. У досліджуваних групах виявлено різні профілі гормонів щитоподібної залози. У пацієнтів із гіпертиреозом спостерігалися вірогідно підвищені рівні ЛФ, АЛТ і ГГТ порівняно з особами з гіпотиреозом та контрольною групою (P ≤ 0,05), що свідчить про більше ураження печінки. Показники АСТ були вищими при гіпертиреозі, але без статистичної значущості. Навпаки, у пацієнтів із гіпотиреозом вірогідно зростали рівні загального холестерину й тригліцеридів, що відображає порушення ліпідного обміну. Висновки. Дисфункція щитоподібної залози супроводжується значними біохімічними й метаболічними змінами, які впливають на ферменти печінки та ліпідний гомеостаз. Для зниження ризику метаболічних і печінкових ускладнень у пацієнтів із захворюваннями щитоподібної залози рекомендується рутинний моніторинг печінкових та ліпідних параметрів.
Background. Thyroid hormones are essential regulators of systemic metabolic homeostasis, particularly lipid metabolism and hepatic function. Thyroid dysfunction, including hyperthyroidism and hypothyroidism, is commonly associated with biochemical and metabolic disturbances that may increase the risk of liver dysfunction and dyslipidemia. Despite the clinical relevance of these alterations, their patterns and extent remain insufficiently characterized, especially in populations with a high prevalence of thyroid disorders. The purpose was to evaluate biochemical and metabolic alterations in liver function and lipid profile associated with thyroid dysfunction and to compare these changes among hyperthyroid, hypothyroid, and healthy individuals. Materials and methods. A case-control study was conducted on 120 participants divided into two groups: hyperthyroid patients (n = 60), hypothyroid patients (n = 60); also, there was a group of apparently healthy controls (n = 30). Thyroid function was assessed by measuring serum levels of thyroid-stimulating hormone, triiodothyronine, and thyroxine. Liver function was evaluated using alanine aminotransferase (ALT), aspartate aminotransferase (AST), alkaline phosphatase (ALP), and gamma-glutamyl transferase (GGT). Lipid profile parameters, including total cholesterol, triglycerides, low- and high-density lipoprotein, were also analyzed. Statistical analysis was performed with a significance threshold of P ≤ 0.05. Results. Distinct thyroid hormone profiles were observed among the study groups. Hyperthyroid patients showed significantly elevated ALP, ALT, and GGT levels compared to hypothyroid and control groups (P ≤ 0.05), indicating increased hepatic involvement. AST levels were higher in hyperthyroidism but without statistical significance. In contrast, hypothyroid patients exhibited significantly increased total cholesterol and triglyceride levels, reflecting impaired lipid metabolism. Conclusions. Thyroid dysfunction is associated with significant biochemical and metabolic alterations affecting liver enzymes and lipid homeostasis. Routine monitoring of hepatic and lipid parameters in patients with thyroid disorders is recommended to reduce the risk of metabolic and hepatic complications.
дисфункція щитоподібної залози; гіпертиреоз; гіпотиреоз; ферменти печінки; ліпідний профіль
thyroid dysfunction; hyperthyroidism; hypothyroidism; liver enzymes; lipid profile
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Marino L, Kim A, Ni B, Celi FS. Thyroid hormone action and liver disease: a complex interplay. Hepatology (Baltimore, Md.). 2025;81(2):651-669. doi: 10.1097/HEP.0000000000000551.
- Punekar P, Sharma AK, Jain A. A study of thyroid dysfunction in cirrhosis of liver and correlation with severity of liver disease. Indian J Endocrinol Metab. 2018;22(5):645-650. doi: 10.4103/ijem.IJEM_25_18.
- Raj A, Pillai G, Divakar A, Shivam V, Nair A. Association of thyroid function and severity of illness in liver cirrhosis as measured by Child-Pugh score. Cureus. 2023;15(3):e36618. doi: 10.7759/cureus.36618.
- Sinha RA, Bruinstroop E, Singh BK, Yen PM. Thyroid hormones and thyromimetics: a new approach to nonalcoholic steatohepatitis? Hepatology (Baltimore, Md.). 2020;72(2):770-771. doi: 10.1002/hep.31204.
- Yorke E. Co-morbid hypothyroidism and liver dysfunction: a review. Clin Med Insights Endocrinol Diabetes. 2024;17:11795514241231533. doi: 10.1177/11795514241231533.
- Soares De Oliveira L, Ritter MJ. Thyroid hormone and the liver. Hepatol Commun. 2024;9(1):e0596. doi: 10.1097/HC9.0000000000000596.
- Levy SB, Bribiescas RG. Hierarchies in the energy budget: thyroid hormones and the evolution of human life history patterns. Evol Anthropol. 2023;32(5):275-292. doi: 10.1002/evan.22000.
- Sabatino L, Vassalle C. Thyroid hormones and metabolism regulation: which role on brown adipose tissue and browning process? Biomolecules. 2025;15(3):361. doi: 10.3390/biom15030361.
- Janota B, Szczepańska E, Adamek B, Janczewska E. Hypothyroidism and non-alcoholic fatty liver disease: a coincidence or a causal relationship? World J Hepatol. 2023;15(5):641-648. doi: 10.4254/wjh.v15.i5.641.
- Piantanida E, Ippolito S, Gallo D, et al. The interplay between thyroid and liver: implications for clinical practice. J Endocrinol Invest. 2020;43(7):885-899. doi: 10.1007/s40618-020-01208-6.
- Di Sessa A, Cembalo Sambiase Sanseverino N, De Simo–ne RF, et al. Association between non-alcoholic fatty liver disease and subclinical hypothyroidism in children with obesity. J Endocrinol Invest. 2023;46(9):1835-1842. doi: 10.1007/s40618-023-02041-3.
- Borges-Canha M, Neves JS, Mendonça F, et al. Thyroid function and the risk of non-alcoholic fatty liver disease in morbid obesity. Front Endocrinol (Lausanne). 2020;11:572128. doi: 10.3389/fendo.2020.572128.
- Liu Y, Wang W, Yu X, Qi X. Thyroid function and risk of non-alcoholic fatty liver disease in euthyroid subjects. Ann Hepatol. 2018;17(5):779-788. doi: 10.5604/01.3001.0012.3136.
- Van den Berg EH, van Tienhoven-Wind LJA, Amini M, et al. Higher free triiodothyronine is associated with non-alcoholic fatty liver disease in euthyroid subjects: the Lifelines Cohort Study. Metabolism. 2017;67:62-71. doi: 10.1016/j.metabol.2016.11.002.
- Nie Q, Jiang Y, Liang Q, et al. Exploring causal links between autoimmune liver diseases, chronic hepatitis C, and thyroid disorders: evidence from NHANES and GWAS studies. Medicine (Baltimore). 2025;104(35):e44112. doi: 10.1097/MD.0000000000044112.
- Khan R, Sikanderkhel S, Gui J, et al. Thyroid and cardiovascular disease: a focused review on the impact of hyperthyroidism in heart failure. Cardiol Res. 2020;11(2):68-75. doi: 10.14740/cr1034.
- Wang MT, Lee WJ, Huang TY, Chu CL, Hsieh CH. Antithyroid drug-related hepatotoxicity in hyperthyroidism patients: a population-based cohort study. Br J Clin Pharmacol. 2014;78(3):619-629. doi: 10.1111/bcp.12336.
- Hegde SV, Bhattam ASK, Sequeira A, et al. Effect of hypothyroi–dism on lipid profile and liver enzymes: implications in non-alcoholic fatty liver disease. Clin Ter. 2025;176(5):609-615. doi: 10.7417/CT.2025.5272.
- Bassi R, Rayamajhi S, Essilfie-Quaye K, Randhawa J, Pa–dam S. Uncontrolled primary hypothyroidism precipitating non-cirrho–tic hyperammonemia: a unique interplay between the liver and thyroid. Cureus. 2024;16(4):e57861. doi: 10.7759/cureus.57861.
- Pouwels S, Sakran N, Graham Y, et al. Non-alcoholic fatty liver disease (NAFLD): a review of pathophysiology, clinical management and effects of weight loss. BMC Endocr Disord. 2022;22(1):63. doi: 10.1186/s12902-022-00980-1.