Международный эндокринологический журнал Том 22, №3, 2026
Вернуться к номеру
Оцінка впливу окремих модифікованих факторів ризику на стан когнітивних функцій та рівень олігомерів амілоїду бета в лікворі у пацієнтів з метаболічним синдромом
Авторы: Жердьова Н.М. (1), Копчак О.О. (1, 2), Тодуров І.М. (1), Перехрестенко О.В. (1), Гриневич К.О. (1), Степура О.А. (1), Орлик О.С. (1)
(1) - Державна наукова установа «Центр інноваційних медичних технологій НАН України», м. Київ, Україна
(2) - ПВНЗ «Київський медичний університет», м. Київ, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
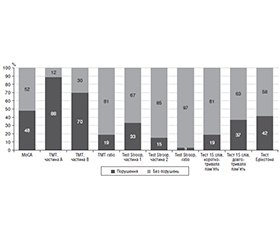
Актуальність. Метаболічний синдром асоціюється з підвищеним ризиком когнітивних порушень і деменції. Хронічна гіперглікемія, глікемічна варіабельність та інсулінорезистентність сприяють нейрозапаленню, накопиченню амілоїдного β-білка та порушенню когнітивних функцій, однак традиційний показник глікованого гемоглобіну (HbA1c) не відображає коливання глікемії та епізоди гіпоглікемії. Мета: оцінити вплив глікемічної варіабельності на рівень олігомерів β-амілоїду (Aβ), стан когнітивних функцій та порушення сну у пацієнтів із метаболічним синдромом. Матеріали та методи. У дослідження включено 100 пацієнтів із метаболічним синдромом (50 чоловіків і 50 жінок) віком 18–79 років (середній вік 55,27 ± 1,26 року), із середнім ІМТ 33,34 ± 0,62 кг/м2. Проведено клінічне та антропометричне обстеження, розширене лабораторне дослідження крові з оцінкою вуглеводного і ліпідного обміну, функції печінки та нирок, запальних маркерів і гормонального профілю. Глікемічну варіабельність оцінювали за даними безперервного моніторингу глюкози з розрахунком показника Time in Range. Визначали рівні олігомерів β-амілоїду в спинномозковій рідині та співвідношення Aβ42/Aβ40. Когнітивні функції та показники сну оцінювали із застосуванням стандартизованих нейропсихологічних тестів і валідованих опитувальників. Результати. Когнітивні порушення у пацієнтів з метаболічним синдромом виявлено у 48,0 % випадків за шкалою MoCA, з переважним ураженням пам’яті (19,0–37,0 %), виконавчих функцій (до 42,0 %) та швидкості обробки інформації (70,0–88,0 %). Зниження пам’яті в учасників дослідження було вірогідно асоційоване з вищими рівнями С-реактивного білка, глікемії натще (РГН) та HbA1c, тоді як порушення виконавчих функцій — з рівнями гонадотропних гормонів. Крім того, порушення сну супроводжувалися зниженням швидкості обробки інформації. Водночас у загальній когорті пацієнтів з метаболічним синдромом порушення амілоїдного обміну характеризувалось зниженням рівня Aβ1–42 у 35,0 % та патологічним співвідношенням Aβ42/Aβ40 у 8,0 % випадків; за наявності цукрового діабету 2-го типу частота цих змін зростала до 44,6 та 12,5 % відповідно. Зниження рівня Aβ1–42 асоціювалося з порушеннями сну, підвищенням рівнів печінкових ферментів та кортизолу, тоді як вищі показники ФСГ і ЛГ відповідали вищим рівням олігомерів Aβ. Глікемічна варіабельність та епізоди гіпоглікемії асоціювалися зі зниженням рівня Aβ1–42 і співвідношення Aβ42/Aβ40. Висновки. У пацієнтів з метаболічним синдромом виявлено високу поширеність легких когнітивних порушень. Порушення пам’яті асоціювалися з показниками запалення та глікемічного контролю, тоді як зміни показників олігомерів Aβ — з порушеннями сну, функціонального стану печінки та гормонального балансу.
Background. Metabolic syndrome is associated with an increased risk of cognitive impairment and dementia. Chronic hyperglycemia, glycemic variability, and insulin resistance contribute to neuroinflammation, accumulation of amyloid-β (Aβ) protein, and cognitive dysfunction; however, the traditional marker HbA1c does not reflect glycemic fluctuations or episodes of hypoglycemia. The purpose of the study was to assess the impact of glycemic variability on Aβ oligomer levels, cognitive function, and sleep disturbances in patients with metabolic syndrome. Materials and methods. The study included 100 patients with metabolic syndrome (50 men and 50 women) aged 18–79 (mean of 55.27 ± 1.26) years with a mean body mass index of 33.34 ± 0.62 kg/m2. All participants underwent clinical and anthropometric examination, as well as extended laboratory blood testing with evaluation of carbohydrate and lipid levels, hepatic and renal function, inflammatory and hormonal parameters. Glycemic variability was assessed using the Time in range index. Levels of amyloid-β oligomers in cerebrospinal fluid were determined, as well as Aβ42/Aβ40 ratio. Cognitive function and sleep parameters were evaluated using standardized neuropsychological tests and validated questionnaires. Results. The study detected cognitive impairment in 48.0 % of patients with metabolic syndrome according to the Montreal Cognitive Assessment, with predominant involvement of memory (19.0–37.0 %), executive functions (up to 42.0 %), and information processing speed (70.0–88.0 %). Higher levels of C-reactive protein, fasting plasma glucose, and HbA1c correlated with memory decline, whereas gonadotropic hormone levels correlated with executive dysfunction. Sleep disturbances contributed to reduced information processing speed. The study revealed disturbances of amyloid metabolism in the overall cohort of patients with metabolic syndrome, including reduced Aβ1–42 levels in 35.0 % and a pathological Aβ42/Aβ40 ratio in 8.0 % of cases; in type 2 diabetes mellitus, the prevalence of these changes increased to 44.6 and 12.5 %, respectively. Lower Aβ1–42 levels correlated with sleep disturbances, increased liver enzyme activity, and cortisol levels, whereas higher follicle-stimulating and luteinizing hormones corresponded to higher Aβ oligomer levels. Glycemic variability and hypoglycemic episodes were associated with reduced Aβ1–42 levels and a lower Aβ42/Aβ40 ratio. Conclusions. The study demonstrated a high prevalence of mild cognitive impairment in patients with metabolic syndrome. Memory impairment was associated with markers of inflammation and glycemic control, whereas alterations in Aβ oligomer profiles were linked to sleep disturbances, liver function parameters, and hormonal balance.
метаболічний синдром; когнітивні порушення; β-амілоїд; цукровий діабет 2-го типу; порушення сну
metabolic syndrome; cognitive impairment; β-amyloid; type 2 diabetes mellitus; sleep disturbances
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Qiu SD, Zhang DD, Ma LY, Li QY, Wang LY, Wang YD, et al. Associations of metabolic syndrome with risks of dementia and cognitive impairment: A systematic review and meta-analysis. J Alzheimers Dis. 2025 May;105(1):15-27. doi: 10.1177/13872877251326553. Epub 2025 Mar 20. PMID: 40111916.
- Tahmi M, Palta P, Luchsinger JA. Metabolic Syndrome and Cognitive Function. Curr Cardiol Rep. 2021 Oct 19;23(12):180. doi: 10.1007/s11886-021-01615-y. PMID: 34668083.
- Yates KF, Sweat V, Yau PL, Turchiano MM, Convit A. Impact of metabolic syndrome on cognition and brain: a selected review of the literature. Arterioscler Thromb Vasc Biol. 2012 Sep;32(9):2060-7. doi: 10.1161/ATVBAHA.112.252759. PMID: 22895667; PMCID: PMC3442257.
- Livingston G, Huntley J, Liu KY, Costafreda SG, Selbæk G, Alladi S, et al. Dementia prevention, intervention, and care: 2024 report of the Lancet standing Commission. Lancet. 2024 Aug 10;404(10452):572-628. doi: 10.1016/S0140-6736(24)01296-0. Epub 2024 Jul 31. PMID: 39096926.
- Xue M, Xu W, Ou YN, Cao XP, Tan MS, et al. Diabetes mellitus and risks of cognitive impairment and dementia: A systematic review and meta-analysis of 144 prospective studies. Ageing Res Rev. 2019 Nov;55:100944. doi: 10.1016/j.arr.2019.100944. Epub 2019 Aug 17. PMID: 31430566.
- Rawlings AM, Sharrett AR, Albert MS, Coresh J, Windham BG, Power MC, et al. The Association of Late-Life Diabetes Status and Hyperglycemia with Incident Mild Cognitive Impairment and Dementia: The ARIC Study. Diabetes Care. 2019 Jul;42(7):1248-1254. doi: 10.2337/dc19-0120. Epub 2019 May 21. PMID: 31221696; PMCID: PMC6609963.
- Liu Y, Liu Y, Qiu H, Haghbin N, Li J, Li Y, et al. Association of time in range with cognitive impairment in middle-aged type 2 diabe–tic patients. BMC Endocr Disord. 2024 Nov 8;24(1):241. doi: 10.1186/s12902-024-01772-5. PMID: 39516758; PMCID: PMC11546570.
- Xia W, Luo Y, Chen YC, Chen H, Ma J, Yin X. Glucose Fluctuations Are Linked to Disrupted Brain Functional Architecture and Cognitive Impairment. J Alzheimers Dis. 2020;74(2):603-613. doi: 10.3233/JAD-191217. PMID: 32065795.
- Zhong Y, Zhang XY, Miao Y, Zhu JH, Yan H, Wang BY, et al. The relationship between glucose excursion and cognitive function in aged type 2 diabetes patients. Biomed Environ Sci. 2012 Feb;25(1):1-7. doi: 10.3967/0895-3988.2012.01.001. PMID: 22424620.
- Rukadikar C, Shah CJ, Raju A, Popat S, Josekutty R. The Influence of Obesity on Cognitive Functioning Among Healthcare Professionals: A Comprehensive Analysis. Cureus. 2023 Aug 3;15(8):e42926. doi: 10.7759/cureus.42926. PMID: 37667717; PMCID: PMC10475152.
- Cui Y, Tang TY, Lu CQ, Ju S. Insulin Resistance and Cognitive Impairment: Evidence From Neuroimaging. J Magn Reson Imaging. 2022 Dec;56(6):1621-1649. doi: 10.1002/jmri.28358. Epub 2022 Jul 19. PMID: 35852470.
- Wei Z, Koya J, Reznik SE. Insulin Resistance Exacerbates Alzheimer Disease via Multiple Mechanisms. Front Neurosci. 2021 Jul 19;15:687157. doi: 10.3389/fnins.2021.687157. PMID: 34349617; PMCID: PMC8326507.
- Tolar M, Hey J, Power A, Abushakra S. Neurotoxic Soluble Amyloid Oligomers Drive Alzheimer’s Pathogenesis and Represent a Clinically Validated Target for Slowing Disease Progression. Int J Mol Sci. 2021 Jun 14;22(12):6355. doi: 10.3390/ijms22126355. PMID: 34198582; PMCID: PMC8231952.
- Brinkmalm G, Hong W, Wang Z, Liu W, O’Malley TT, Sun X, et al. Identification of neurotoxic cross-linked amyloid-β dimers in the Alzheimer’s brain. Brain. 2019 May 1;142(5):1441-1457. doi: 10.1093/brain/awz066. PMID: 31032851; PMCID: PMC6487330.
- Gaspar RC, Villarreal SA, Bowles N, Hepler RW, Joyce JG, Shughrue PJ. Oligomers of beta-amyloid are sequestered into and seed new plaques in the brains of an AD mouse model. Exp Neurol. 2010 Jun;223(2):394-400. doi: 10.1016/j.expneurol.2009.09.001. Epub 2009 Sep 8. PMID: 19744481.
- Iljina M, Garcia GA, Dear AJ, Flint J, Narayan P, Michaels TC, et al. Quantitative analysis of co-oligomer formation by amyloid-beta peptide isoforms. Sci Rep. 2016 Jun 27;6:28658. doi: 10.1038/srep28658. PMID: 27346247; PMCID: PMC4921824.
- O’Brien RJ, Wong PC. Amyloid precursor protein processing and Alzheimer’s disease. Annu Rev Neurosci. 2011;34:185-204. doi: 10.1146/annurev-neuro-061010-113613. PMID: 21456963; PMCID: PMC3174086.
- Olsson B, Lautner R, Andreasson U, Öhrfelt A, Portelius E, Bjerke M, et al. CSF and blood biomarkers for the diagnosis of Alzheimer’s disease: a systematic review and meta-analysis. Lancet Neurol. 2016 Jun;15(7):673-684. doi: 10.1016/S1474-4422(16)00070-3. Epub 2016 Apr 8. PMID: 27068280.
- Lewczuk P, Łukaszewicz-Zając M, Mroczko P, Kornhuber J. Clinical significance of fluid biomarkers in Alzheimer’s Disease. Pharmacol Rep. 2020 Jun;72(3):528-542. doi: 10.1007/s43440-020-00107-0. Epub 2020 May 8. PMID: 32385624; PMCID: PMC7329803.
- Zhao D, Wang J, Zhu Y, Zhang H, Ni C, Zhao Z, et al. Targeting the glymphatic system: Aβ accumulation and phototherapy strategies across different stages of Alzheimer’s disease. Transl Neurodegener. 2025 Sep 24;14(1):49. doi: 10.1186/s40035-025-00510-8. PMID: 40993746; PMCID: PMC12459067.
- Moon C, Schneider A, Cho YE, Zhang M, Dang H, Vu K. Sleep duration, sleep efficiency, and amyloid β among cognitively healthy later-life adults: a systematic review and meta-analysis. BMC Geriatr. 2024 May 8;24(1):408. doi: 10.1186/s12877-024-05010-4. PMID: 38714912; PMCID: PMC11076214.
- Ju YS, Ooms SJ, Sutphen C, Macauley SL, Zangrilli MA, Jerome G, et al. Slow wave sleep disruption increases cerebrospinal fluid amyloid-β levels. Brain. 2017 Aug 1;140(8):2104-2111. doi: 10.1093/brain/awx148. PMID: 28899014; PMCID: PMC5790144.
- Blattner MS, Panigrahi SK, Toedebusch CD, Hicks TJ, McLeland JS, Banks IR, et al. Increased Cerebrospinal Fluid Amy–loid-β During Sleep Deprivation in Healthy Middle-Aged Adults Is Not Due to Stress or Circadian Disruption. J Alzheimers Dis. 2020;75(2):471-482. doi: 10.3233/JAD-191122. PMID: 32250301; PMCID: PMC7246155.
- Ooms S, Overeem S, Besse K, Rikkert MO, Verbeek M, Claassen JA. Effect of 1 night of total sleep deprivation on cerebrospinal fluid β-amyloid 42 in healthy middle-aged men: a randomized clinical trial. JAMA Neurol. 2014 Aug;71(8):971-7. doi: 10.1001/jamaneurol.2014.1173. PMID: 24887018.
- Lucey BP, Hicks TJ, McLeland JS, Toedebusch CD, Boyd J, Elbert DL, et al. Effect of sleep on overnight cerebrospinal fluid amyloid β kinetics. Ann Neurol. 2018 Jan;83(1):197-204. doi: 10.1002/ana.25117. PMID: 29220873; PMCID: PMC5876097.
- Stickgold R, Walker MP. Sleep-dependent memory consolidation and reconsolidation. Sleep Med. 2007 Jun;8(4):331-43. doi: 10.1016/j.sleep.2007.03.011. Epub 2007 Apr 30. PMID: 17470412; PMCID: PMC2680680.
- Bellesi M, Pfister-Genskow M, Maret S, Keles S, Tononi G, Cirelli C. Effects of sleep and wake on oligodendrocytes and their precursors. J Neurosci. 2013 Sep 4;33(36):14288-300. doi: 10.1523/JNEUROSCI.5102-12.2013. PMID: 24005282; PMCID: PMC3874087.
- Durmer JS, Dinges DF. Neurocognitive consequences of sleep deprivation. Semin Neurol. 2005 Mar;25(1):117-29. doi: 10.1055/s-2005-867080. PMID: 15798944.
- Tononi G, Cirelli C. Sleep and the price of plasticity: from synaptic and cellular homeostasis to memory consolidation and integration. Neuron. 2014 Jan 8;81(1):12-34. doi: 10.1016/j.neuron.2013.12.025. PMID: 24411729; PMCID: PMC3921176.
- Wu L, Sun D, Tan Y. A systematic review and dose-response meta-analysis of sleep duration and the occurrence of cognitive disorders. Sleep Breath. 2018 Sep;22(3):805-814. doi: 10.1007/s11325-017-1527-0. Epub 2017 Jun 6. PMID: 28589251.
- Lucey BP, Wisch J, Boerwinkle AH, Landsness EC, Toedebusch CD, McLeland JS, et al. Sleep and longitudinal cognitive performance in preclinical and early symptomatic Alzheimer’s disease. Brain. 2021 Oct 22;144(9):2852-2862. doi: 10.1093/brain/awab272. PMID: 34668959; PMCID: PMC8536939.
- Baril AA, Beiser AS, Mysliwiec V, Sanchez E, DeCarli CS, Redline S, et al. Slow-Wave Sleep and MRI Markers of Brain Aging in a Community-Based Sample. Neurology. 2021 Mar 9;96(10):e1462-e1469. doi: 10.1212/WNL.0000000000011377. Epub 2020 Dec 22. PMID: 33361258; PMCID: PMC8055313.
- De Looze C, Feeney JC, Scarlett S, Hirst R, Knight SP, Carey D, et al. Sleep duration, sleep problems, and perceived stress are associated with hippocampal subfield volumes in later life: findings from The Irish Longitudinal Study on Ageing. Sleep. 2022 Jan 11;45(1):zsab241. doi: 10.1093/sleep/zsab241. PMID: 34558630.
- Ali NH, Al-Kuraishy HM, Al-Gareeb AI, Hadi NR, Assiri AA, Alrouji M, et al. Hypoglycemia and Alzheimer Disease Risk: The Possible Role of Dasiglucagon. Cell Mol Neurobiol. 2024 Jul 8;44(1):55. doi: 10.1007/s10571-024-01489-y. PMID: 38977507; PMCID: PMC11230952.
- Konda M, Lingutla C, Eruvuri V, Gatla SR, Vityala Y. Hypoglycemia as a risk factor for dementia in diabetes: a systema–tic review. Adv Neurol. 2025; Online ahead of print. doi: 10.36922/AN025270077.