Международный эндокринологический журнал Том 22, №3, 2026
Вернуться к номеру
Klotho та FGF23: ендокринна регуляція результатів хвороби нирок
Авторы: O.I. Nishkumay (1, 2), Mike K.S. Chan (2), O.B. Iaremenko (1), V.E. Kondratiuk (1), I.V. Rudenko (1), O.E. Zaytseva (1), O.I. Rokyta (1), G.M. Mykytenko (1)
(1) - Bogomolets National Medical University, Kyiv, Ukraine
(2) - European Wellness Academy, Malaysia
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
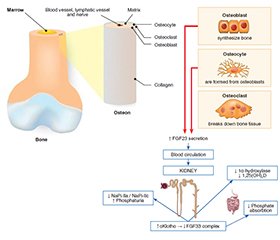
Ендокринна регуляція мінерального обміну значною мірою залежить від взаємодії між нирками, кістковою тканиною та паращитоподібними залозами. Одним із ключових регуляторів цієї осі є система Klotho — фактор росту фібробластів 23 (FGF23), яка відіграє центральну роль у контролі гомеостазу фосфату й вітаміну D. Білок α-Klotho, що переважно експресується в ниркових канальцях, функціонує як необхідний корецептор для FGF23, забезпечуючи його зв’язування з рецепторами фактора росту фібробластів і активацію подальших сигнальних шляхів у клітинах-мішенях. Порушення цієї сигнальної системи, особливо при хронічній хворобі нирок, призводить до розладів фосфорно-кальцієвого обміну, розвитку судинної кальцифікації, ниркового фіброзу і серцево-судинних ускладнень. Окрім участі в сигнальному шляху FGF23, розчинна форма Klotho має численні системні захисні властивості, включаючи антиоксидантну, протизапальну, антифібротичну та цитопротекторну дію. Зростаюча кількість експериментальних і клінічних досліджень свідчить, що зниження рівнів циркулюючого та ниркового Klotho може бути раннім біомаркером порушення функції нирок і асоціюється з несприятливими нирковими й серцево-судинними наслідками. Натомість відновлення рівня Klotho, зокрема шляхом введення рекомбінантного білка або застосування терапевтичних стратегій, спрямованих на підвищення його ендогенної експресії, демонструє перспективні рено- та кардіопротекторні ефекти в експериментальних моделях. Таким чином, вісь Klotho — FGF23 є важливим ендокринним регулятором прогресування захворювань нирок та їх системних ускладнень. Подальші дослідження необхідні для глибшого розуміння молекулярних механізмів цієї сигнальної системи і трансляції отриманих знань у нові діагностичні маркери й таргетні терапевтичні підходи при захворюваннях нирок.
Endocrine regulation of mineral metabolism largely depends on the interaction between the kidneys, bone tissue, and parathyroid glands. One of the key regulators of this axis is the Klotho-fibroblast growth factor 23 (FGF23) system, which plays a central role in the control of phosphate and vitamin D homeostasis. The α-Klotho protein, predominantly expressed in the renal tubules, functions as an essential co-receptor for FGF23, enabling its binding to fibroblast growth factor receptors and activation of downstream signaling pathways in target cells. Disruption of this signaling system, particularly in chronic kidney disease, leads to disturbances in phosphate and calcium metabolism, vascular calcification, renal fibrosis, and cardiovascular complications. In addition to its role in FGF23 signaling, soluble Klotho exhibits multiple systemic protective properties, including antioxidant, anti-inflammatory, anti-fibrotic, and cytoprotective effects. A growing body of experimental and clinical evidence suggests that reduced circulating and renal Klotho levels may serve as an early biomarker of kidney dysfunction and are associated with adverse renal and cardiovascular outcomes. Conversely, restoration of Klotho levels — either through administration of recombinant protein or therapeutic strategies aimed at enhancing endogenous expression — has demonstrated promising renoprotective and cardioprotective effects in experimental models. Overall, the Klotho-FGF23 axis represents a crucial endocrine regulator of kidney disease progression and its systemic complications. Further studies are required to better understand the molecular mechanisms underlying this pathway and to translate these findings into novel diagnostic markers and targeted therapeutic strategies for kidney diseases.
ендокринна регуляція Klotho — FGF23; хронічна хвороба нирок; фосфатний обмін; судинна кальцифікація; ренальний фіброз
endocrine regulation Klotho-FGF23; chronic kidney disease; phosphate metabolism; vascular calcification; renal fibrosis
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Kuro-O M. The Klotho proteins in health and disease. Nat Rev Nephrol. 2019;15(1):27-44. doi: 10.1038/s41581-018-0078-3.
- Nambidi S, Pallatt S, Banerjee A, Pathak S, Chan MKS. Klotho protein: a multifaceted regulator in aging and cancer dynamics. Mol Biol Rep. 2025;52(1):507. doi: 10.1007/s11033-025-10575-3.
- Hajare AD, Dagar N, Gaikwad AB. Klotho antiaging protein: molecular mechanisms and therapeutic potential in diseases. Mol Biomed. 2025;6;19. doi: 10.1186/s43556-025-00253-y.
- Tang J, Xu Z, Ren L, et al. Association of serum Klotho with the severity and mortality among adults with cardiovascular-kidney-meta–bolic syndrome. Lipids Health Dis. 2024;23(1):408. doi: 10.1186/s12944-024-02400-w.
- Chen L, Fu L, Sun J, et al. Structural basis for FGF hormone signalling. Nature. 2023;618(7966):862-870. doi: 10.1038/s41586-023-06155-9.
- Liu Z, Yoon J, Lee E, Chang AN, Miller RT. Calcium-sensing receptor- and ADAM10-mediated klotho shedding is regulated by tetraspanin 5. FEBS Lett. 2025;599(6):866-875. doi: 10.1002/1873-3468.15078.
- Erben RG, Andrukhova O. FGF23-Klotho signaling axis in the kidney. Bone. 2017;100:62-68. doi: 10.1016/j.bone.2016.09.010.
- Agoro R, White KE. Regulation of FGF23 production and phosphate metabolism by bone-kidney interactions. Nat Rev Nephrol. 2023;19(3):185-193. doi: 10.1038/s41581-022-00665-x.
- Rout P, Jialal I. Hyperphosphatemia. In: StatPearls. Treasure Island (FL): StatPearls Publishing; June 12, 2023.
- Neyra JA, Hu MC, Moe OW. Klotho in Clinical Nephrology: Diagnostic and Therapeutic Implications. Clin J Am Soc Nephrol. 2020;16(1):162-176. doi: 10.2215/CJN.02840320.
- Hu MC, Shiizaki K, Kuro-o M, Moe OW. Fibroblast growth factor 23 and Klotho: physiology and pathophysiology of an endocrine network of mineral metabolism. Annu Rev Physiol. 2013;75:503-533. doi: 10.1146/annurev-physiol-030212-183727.
- Memon F, El-Abbadi M, Nakatani T, Taguchi T, Lanske B, Razzaque MS. Does Fgf23-klotho activity influence vascular and soft tissue calcification through regulating mineral ion metabolism? Kidney Int. 2008;74(5):566-570. doi: 10.1038/ki.2008.218.
- Li L, Liu W, Mao Q, et al. Klotho Ameliorates Vascular Calcification via Promoting Autophagy. Oxid Med Cell Longev. 2022;2022:7192507. doi: 10.1155/2022/7192507.
- Wu T, Ding L, Andoh V, Zhang J, Chen L. The Mechanism of Hyperglycemia-Induced Renal Cell Injury in Diabetic Nephropathy Disease: An Update. Life (Basel). 2023;13(2):539. doi: 10.3390/life13020539.
- Wang H, Liu H, Cheng H, et al. Klotho Stabilizes the Podocyte Actin Cytoskeleton in Idiopathic Membranous Nephropathy through Regulating the TRPC6/CatL Pathway. Am J Nephrol. 2024;55(3):345-360. doi: 10.1159/000537732.
- Speer T, Schunk SJ. Klotho in diabetic kidney disease: more than dust in the Wnt. Kidney Int. 2022;102(3):469-471. doi: 10.1016/j.kint.2022.05.016.
- Chen X, Tan H, Xu J, et al. Klotho-derived peptide 6 ameliorates diabetic kidney disease by targeting Wnt/β-catenin signaling. Kidney Int. 2022;102(3):506-520. doi: 10.1016/j.kint.2022.04.028.
- Patel ML, Gupta S, Shyam R, Sachan R, Ali W. Serum Fibroblast Growth Factor 23 Levels as a Predictor of Acute Kidney Injury in Critically Ill Obstetric Women in Obstetric Intensive Care Units: A North Indian Study. Adv Biomed Res. 2025;14:66. doi: 10.4103/abr.abr_146_23.
- Muñoz-Castañeda JR, Rodelo-Haad C, Pendon-Ruiz de Mier MV, Martin-Malo A, Santamaria R, Rodriguez M. Klotho/FGF23 and Wnt Signaling as Important Players in the Comorbidities Associated with Chronic Kidney Disease. Toxins. 2020;12(3):185. doi: 10.3390/toxins12030185.
- Khan SR. Renal tubular damage/dysfunction: key to the formation of kidney stones. Urol Res. 2006;34(2):86-91. doi: 10.1007/s00240-005-0016-2.
- Nikitin O, Kordubailo I, Nishkumay O, Chan MK, Klo–kol D. Analysis of salt transport indices, calcification markers, and FGF23 in patients with nephrolithiasis and crystalluria. Kidneys. 2025;14(3):236-240. doi: 10.22141/2307-1257.14.3.2025.545.
- Xiao Y, Xiao Z. Association between Serum Klotho and Kidney Stones in US Middle-Aged and Older Individuals with Diabetes Mellitus: Results from 2007 to 2016 National Health and Nutrition Survey. Am J Nephrol. 2023;54(5-6):224-233. doi: 10.1159/000531045.
- Chen L, Xie L, Wu B, Zhao W. Assessing causal associations of FGF23 and α-Klotho with urolithiasis using Mendelian randomi–zation analysis. Urolithiasis. 2025;53(1):161. doi: 10.1007/s00240-025-01836-8.
- Rendina D, Esposito T, Mossetti G, et al. A functio–nal allelic variant of the FGF23 gene is associated with renal phosphate leak in calcium nephrolithiasis. J Clin Endocrinol Metab. 2012;97(5):E840-E844. doi: 10.1210/jc.2011-1528.
- Prud’homme GJ, Kurt M, Wang Q. Pathobiology of the Klotho Antiaging Protein and Therapeutic Considerations. Front Aging. 2022;3:931331. doi: 10.3389/fragi.2022.931331.
- Mahdavi S. Klotho, Kidneys, and Micronutrient Signaling: A Promising Paradigm for Healthy Aging. Lifestyle Genom. 2026;19(1):31-41. doi: 10.1159/000548666.
- Martín-Vírgala J, Martín-Carro B, Fernández-Villabrille S, et al. Soluble Klotho, a Potential Biomarker of Chronic Kidney Disease-Mineral Bone Disorders Involved in Healthy Ageing: Lights and Shadows. Int J Mol Sci. 2024;25(3):1843. doi: 10.3390/ijms25031843.
- Vázquez-Sánchez S, Blasco A, Fernández-Corredoira P, et al. Recombinant Klotho administration after myocardial infarction reduces ischaemic injury and arrhythmias by blocking intracellular calcium mishandling and CaMKII activation. J Pathol. 2025;265(3):342-356. doi: 10.1002/path.6388.
- Tsai KD, Lee YC, Chen BY, et al. Recombinant Klotho attenuates IFNγ receptor signaling and SAMHD1 expression through blocking NF-κB translocation in glomerular mesangial cells. Int J Med Sci. 2023;20(6):810-817. doi: 10.7150/ijms.78279.
- Typiak M, Piwkowska A. Antiinflammatory Actions of Klotho: Implications for Therapy of Diabetic Nephropathy. Int J Mol Sci. 2021;22(2):956. doi: 10.3390/ijms22020956.
- Liu X, Niu Y, Zhang X, et al. Recombinant α-Klotho Protein Alleviated Acute Cardiorenal Injury in a Mouse Model of Lipopolysaccharide-Induced Septic Cardiorenal Syndrome Type 5. Anal Cell Pathol (Amst). 2019;2019:5853426. doi: 10.1155/2019/5853426.
- Hu MC, Shi M, Gillings N, et al. Recombinant α-Klotho may be prophylactic and therapeutic for acute to chronic kidney disease progression and uremic cardiomyopathy. Kidney Int. 2017;91(5):1104-1114. doi: 10.1016/j.kint.2016.10.034.
- Park Y, Woo JS, Park YS, et al. Recombinant klotho protein protects tissues by mitigating the detrimental effects of sterile inflammation following hemorrhagic shock. Shock. doi: 10.1097/SHK.0000000000002755.