Журнал «Медицина неотложных состояний» 6 (45) 2012
Вернуться к номеру
Острая печеночная недостаточность
Авторы: Думанский Ю.В., чл.-корр. НАМН Украины, д.м.н., профессор;
Кабанова Н.В., д.м.н., профессор кафедры анестезиологии и интенсивной терапии ДонНМУ им. М. Горького;
Верхулецкий И.Е., завкафедрой хирургических болезней № 1 факультета интернатуры и последипломного образования ДонНМУ им. М. Горького, д.м.н., профессор;
Синепупов Н.А., доцент кафедры хирургических болезней № 1 факультета интернатуры и последипломного образования ДонНМУ им. М. Горького, к.м.н.;
Осипов А.Г., доцент кафедры хирургических болезней № 1 факультета интернатуры и последипломного образования ДонНМУ им. М. Горького, к.м.н.;
Синепупов Д.Н., ассистент кафедры хирургических болезней № 1 факультета интернатуры и последипломного образования ДонНМУ им. М. Горького
Рубрики: Семейная медицина/Терапия, Анестезиология-реаниматология, Медицина неотложных состояний, Гастроэнтерология, Инфекционные заболевания, Хирургия
Разделы: Медицинское образование
Версия для печати
Актуальность
По данным ВОЗ, острая печеночная недостаточность (ОПечН) занимает 3-е место в мире после сердечно-сосудистой и онкологической патологий, что связано с ухудшением экологического состояния окружающей среды, снижением уровня жизни людей, ухудшением качества пищевых продуктов, увеличением потребления некачественного алкоголя, широким распространением вирусных инфекций. Обширный спектр нарушений функции печени варьирует от умеренных до фульминантной. Особенностями течения заболеваний печени являются высокий уровень летальности в остром периоде болезни (90 %), значительная частота хронизации процесса (цирроз печени или гепатоцеллюлярная карцинома) с развитием инвалидности, ухудшение качества жизни, сокращение ее продолжительности, низкая выживаемость (17 на 100 тыс.). Фульминантная печеночная недостаточность может быть исходом вирусных гепатитов, аутоиммунных гепатитов, наследственных заболеваний, являться результатом приема лекарственных препаратов (например, парацетамола), воздействия токсических веществ (например, токсинов бледной поганки).
При выраженной печеночной недостаточности происходит накопление как водорастворимых, так и нерастворимых, связанных с альбумином веществ. Классические методы экстракорпорального очищения крови (гемодиализ и гемофильтрация) способны удалять только растворимые молекулы. Для удаления липофильных веществ и молекул, связанных с альбумином, требуются совершенно иные технологии. Эту проблему призваны решать такие системы, как MARS (Molecular Adsorbents Recirculating System) и Prometheus.
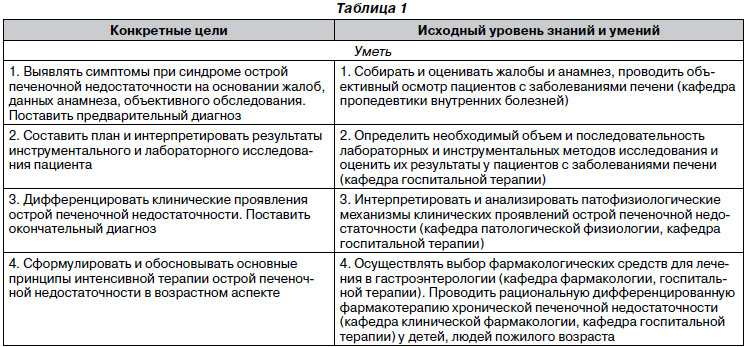
Цель занятия общая: диагностировать синдром острой печеночной недостаточности и проводить интенсивную терапию пациентов с острой печеночной недостаточностью.
Содержание обучения
I. Теоретические вопросы
1. Этиологические факторы, патофизиология развития, клиническое течение острой печеночной недостаточности. Методы интенсивной терапии острой печеночной недостаточности.
II. Основные термины и их определения
Определение
Функциональная недостаточность печени — состояние, когда орган не способен поддерживать обмен веществ и постоянство внутренней среды организма, а если поддерживает, то за счет напряжения своих компенсаторных возможностей (Гальперин Э.И.).
Актуальность проблемы ОПечН заключается в нарушении всех видов обмена веществ:
- Нарушение синтеза белка.
- Нарушение синтеза других азотсодержащих веществ: холина, глутатиона, таурина, этаноламина.
- Нарушение расщепления белков и аминокислот в реакциях дезаминирования, трансаминирования, декарбоксилирования.
- Нарушение образования мочевины.
- Нарушение обмена билирубина.
- Нарушение обезвреживания эндогенных токсинов, образовавшихся из белков (индол, скатол, ароматические углеводороды, аммиак).
- Нарушение обезвреживания экзогенных токсинов, функции детоксикации. Биохимическими признаками ОПечН являются гипопротеинемия, гипоальбуминемия, гипоглобулинемия, гипофибриногенемия, гипопротромбинемия, желтуха, гипокоагуляция, гиперферментемия.
Классификация ОПечН необходима для выбора тактики лечения и оценки его результатов в разных странах и клиниках.
1. С клинической точки зрения важно дифференцировать фульминантную и субфульминантную (развитие энцефалопатии примерно через 2 нед. после появления желтухи).
2. По скорости развития процесса, временному интервалу от появления желтухи до развития печеночной энцефалопатии (ПЭ), различают сверхострое (0–7 сут. от появления желтухи с летальностью 64 %), острое (8–28 сут. с летальностью 94 %) и подострое (29 сут. — 12 нед. с летальностью 86 %) течение ОПечН.
О поздней печеночной недостаточности говорят в тех случаях, когда энцефалопатия развивается через 8 нед. и более, но не позднее 24 нед. от момента появления первых симптомов болезни при отсутствии предшествующего заболевания печени. К тошноте, слабости и дискомфорту в области живота присоединяются асцит, энцефалопатия и поражение почек. Выживаемость без трансплантации печени составляет около 20 %. После трансплантации печени выживаемость к концу первого года достигает 55 % .
3. Различают три вида ОПечН:
1) печеночноклеточная, первичная печеночная кома, эндогенная кома, или кома распада печени. Характеризуется клиникой паренхиматозного дефицита: гипербилирубинемия, гиперферментемия, гипокоагуляция.
2) экзогенная кома, или кома выпадения функции печени, портосистемная функциональная, шунтовая, ложная. Характеризуется наличием портосистемного шунтирования крови, сбросом нейротоксинов кишечного происхождения по портосистемным шунтам.
3) смешанная, характеризующаяся развитием печеночноклеточной недостаточности на фоне коллатерального кровообращения.
Этиология ОПечН
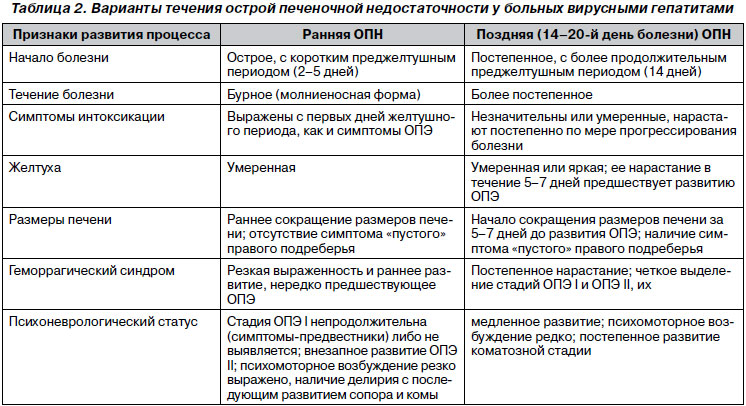
Наиболее частой причиной ОПечН являются инфекции (вирусы, бактерии, паразиты). Гепатит А в этиологии ОПечН составляет 5 %, особенно часто у пациентов старше 40 лет, с ранее диагностированными заболеваниями печени, у наркоманов. Гепатит В в структуре печеночной недостаточности занимает 47 %. Инфицирование пациентов вирусами гепатитов С, D, E также может стать причиной развития ОПечН (табл. 2). Наиболее опасен вирус гепатита Е для беременных: ОПечН развивается у 20 % пациенток. Редко к развитию ОПечН приводит вирус простого герпеса, Эпштейна — Барр, оспы, цитомегаловирус, аденовирус, а также желтая лихорадка и туберкулез.
Оценку степени тяжести пациентов с ОПечН осуществляют с помощью:
1. Коэффициента Фишера (в норме 3–3,5, при ОПечН менее 1,5).
2. Шкалы АРАСНЕ 2 и 3.
3. Шкалы SOFA.
4. Шкалы MELD.
5. Шкалы ком Глазго.
Осложнения ОПечН
Неврологическими осложнениями ОПечН являются печеночная энцефалопатия и отек головного мозга с повышением внутричерепного давления. Печеночная энцефалопатия (ПЭ) — это потенциально обратимое нарушение функции мозга, обусловленное метаболическими расстройствами и возникающее вследствие острой или хронической печеночноклеточной недостаточности и/или портосистемного шунтирования крови.
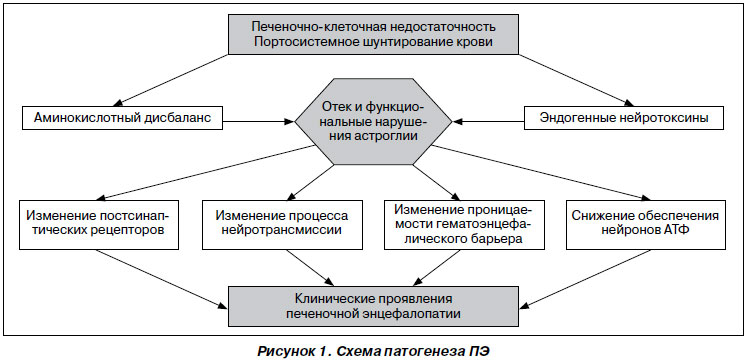
Патогенез ПЭ
Синдром ПЭ объединяет комплекс неврологических и психоэмоциональных расстройств, проявляющихся патологическими нервно-мышечными и нейрофизиологическими нарушениями, изменением сознания, поведения, снижением интеллекта, изменением личности, расстройством интеллекта и речи. ПЭ, ассоциированная с ОПН при вирусных поражениях печени, особенно при вирусных гепатитах В и D, характеризуется высокой летальностью, достигающей без трансплантации печени 80–100 % (рис. 1).
Согласно классификации, предложенной в 1998 году, ПЭ делится на типы:
A (Acute) — связана с острой печеночной недостаточностью;
B (Bypass) — связана с портосистемным шунтированием крови, заболевание печени отсутствует;
С (Cirrohosis) — связана с циррозом печени, портальной гипертензией и портосистемным шунтированием.
Классификация ПЭ основана на особенностях течения и характера нервно-психических нарушений (табл. 3). Принято выделять острую, латентную, клинически выраженную (хроническую, рецидивирующую) ПЭ. К особым формам ПЭ относятся гепатоцеребральная дегенерация и спастический парапарез. Клиническая классификация включает эпизодическую, персистирующую и минимальную ПЭ.
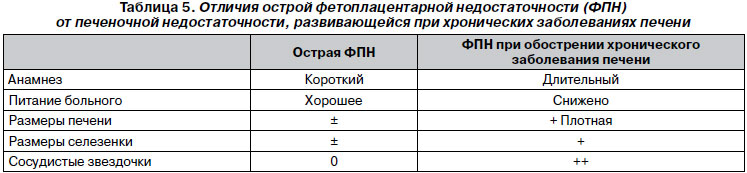
Острая ПЭ у больных острыми вирусными гепатитами при развитии ОПН имеет характерные особенности (табл. 4), отличающие ее от ОПЭ при хронических заболеваниях печени (табл. 5).
Генерализованный отек головного мозга (внутричерепная гипертензия) может привести к вклинению ствола головного мозга, которое является наиболее частой причиной смерти пациентов (81 %). Ведущими механизмами патогенеза отека мозга считают сосудистый и цитотоксический. Сосудистый механизм обусловлен нарушением гематоэнцефалического барьера с выходом плазмы в спинномозговую жидкость. В основе цитотоксического механизма лежат клеточные изменения, приводящие к переходу воды в клетки головного мозга по осмотическому градиенту. У большинства пациентов мозговой кровоток неадекватен вследствие нарушения его ауторегуляции (в норме обеспечивающей поддержание кровотока, несмотря на снижение системного артериального давления), что вызывает гипоксию головного мозга и также может провоцировать развитие его отека. Поэтому особенно высока опасность системной артериальной гипотензии у пациентов с ФПН. Повышение внутричерепного давления можно заподозрить при повышении мышечного тонуса с миоклонусом, приводящим к разгибанию и гиперпронации верхних конечностей и разгибанию ног (децеребрационная ригидность). Могут нарушиться координированные движения глазных яблок с развитием косоглазия. При прогрессировании этих симптомов наблюдают потерю зрачковых рефлексов и остановку дыхания вследствие вклинения ствола головного мозга.
Коагулопатия при ОПечН имеет сложный генез и обусловлена не только дефицитом факторов свертывания, но и повышением фибринолитической активности, наиболее вероятной причиной которой является внутрисосудистое свертывание. Количество тромбоцитов может снижаться вследствие усиленного их потребления или пониженного образования. Функция тромбоцитов также нарушена. Возникающая коагулопатия предрасполагает к кровотечению, которое может быть спонтанным и возникает из слизистых оболочек (желудочно-кишечный тракт или кровоизлияние в вещество головного мозга).
Метаболические нарушения. Стойкая гипогликемия встречается у 40 % пациентов с ОПечН. Гиперинсулинемия объясняется уменьшением его захвата печенью, сниженным глюконеогенезом. Патогенез гипокалиемии объясняют усиленным выведением калия с мочой, неадекватным восполнением его потерь, а также введением в качестве энергетического субстрата больших доз глюкозы. К другим электролитным нарушениям относят гипонатриемию, гипофосфатемию, гипокальциемию и гипомагниемию. Причиной респираторного алкалоза является усиленное дыхание, связанное с прямой стимуляцией дыхательного центра токсичными веществами. Респираторный ацидоз может быть обусловлен повышением внутричерепного давления и подавлением дыхательной деятельности, а также легочными осложнениями. Метаболический ацидоз связан с недостаточным кровоснабжением тканей на фоне артериальной гипотензии и гипоксемии. Снижение рН является при этом одним из критериев необходимости трансплантации печени.
Инфекционные осложнения наблюдают у 90 % пациентов с наличием у 25 % из них сопутствующей бактериемии, что может быть обусловлено снижением защитных сил организма, нарушением функции клеток Купффера и нейтрофилов, а также снижением содержания в крови фибронектина, опсонинов и белков системы комплемента. Чаще всего поражаются органы дыхания, может развиться спонтанный бактериальный перитонит. Типичные проявления сепсиса, например лихорадка и лейкоцитоз, могут отсутствовать. Чаще инфекционные осложнения вызывают грамположительные микроорганизмы, обычно стафилококки, реже обнаруживают стрептококки и грамотрицательные бактерии. У трети больных развивается грибковая инфекция.
Нарушение функции почек. В связи со сниженным образованием мочевины в печени концентрация ее в крови не служит адекватным критерием функции почек. Предпочтительно исследование содержания креатинина в сыворотке крови. Функциональная почечная недостаточность (гепаторенальный синдром) с острым канальцевым некрозом или без него развивается у 55 % пациентов. Сепсис, эндотоксемия, кровотечения и артериальная гипотензия приводят к острому канальцевому некрозу.
Системная артериальная гипотензия характеризуется низким общим периферическим сосудистым сопротивлением и повышением сердечного выброса, которые коррелируют со степенью поражения печени. Циркуляторные изменения сочетаются с уменьшением церебрального кровотока и спазмом почечных сосудов. Наблюдают нарушения ритма сердца, связанные с электролитными расстройствами, ацидозом, гипоксией. Подавление функции ствола головного мозга приводит к недостаточности кровообращения.
Легочные осложнения наблюдают более чем у половины пациентов в виде некардиогенного отека легких, аспирационной пневмонии, диффузного усиления легочного рисунка, ателектазов долей легких, респираторного дистресс-синдрома. Внутрилегочное артериовенозное шунтирование усугубляет гипоксию.
Острый геморрагический панкреатит и панкреонекроз. Активность амилазы сыворотки крови повышена у трети пациентов. Причинами осложнения являются дуоденит, кровоизлияние в поджелудочную железу и окружающие ее ткани, терапия кортикостероидами и шок.
Интенсивная терапия
Выживаемость пациентов зависит от интенсивной терапии этого состояния и глубокого понимания важных функций, утрачиваемых при повреждении печеночных клеток. Для ранней диагностики осложнений ОПечН мониторируют показатели (температура тела, пульс, артериальное давление, сатурация кислорода, водный баланс, диурез) с ежечасной их регистрацией. Устанавливают венозный, мочевой катетеры, назогастральный зонд. Для предотвращения эрозий и кровотечения из желудочно-кишечного тракта назначают антагонисты Н2-гистаминовых рецепторов. Ежедневно с помощью перкуссии определяют размеры печени и отмечают ее нижний край на коже передней брюшной стенки. Результаты измерения размеров печени верифицируют с помощью ультразвукового исследования.
Основными принципами интенсивной терапии ОПечН являются:
1. Этиотропная терапия при вирусных гепатитах, устранение причины.
2. Мероприятия, направленные на элиминацию триггерных, разрешающих и отягощающих факторов ОПечН:
— устранение повышенного катаболизма белка (профилактика инфекции, гематом, травмы, операции, гипоксии, дефицита альбумина);
— профилактика желудочно-кишечных кровотечений;
— устранение дополнительной интоксикации (прием алкоголя, лекарств, инфекция, запор);
— недопустимость стимуляции ГАМК-рецепторов (отказ от приема барбитуратов, фенотиазинов, бензодиазепинов);
— профилактика метаболических нарушений (гипогликемия, ацидоз);
— профилактика электролитных нарушений (дефицит натрия, калия, кальция, фосфора);
— профилактика гипоксии, гиповолемии, гипотензии;
— профилактика подавления факторов синтеза мочевины (прием диуретиков, дефицит цинка).
3. Соблюдение диеты с достаточным количеством калорий (1,5–2 тыс. кал), так как все процессы детоксикации аммиака являются энергозависимыми.
Диетотерапия должна быть направлена на ограничение поступления белка с пищей и увеличение потребления пищевых волокон. Временно ограничить количество белка в сутки: при латентной ПЭ — до 40 г/сут (0,6 г/кг массы тела), при I–II стадии ПЭ — до 30 г/сут (0,4 г/кг), при III–IV стадиях ПЭ — 20 г/сут. В рационе пациентов с ПЭ белок должен быть представлен преимущественно протеинами растительного происхождения ввиду их лучшей переносимости. Растительные белки богаты орнитином и аргинином и содержат меньше метионина и ароматических аминокислот. Однако длительное и резкое ограничение белка способствует распаду эндогенных протеинов и повышению концентрации азотсодержащих соединений в крови. После исчезновения явлений ПЭ количество белка увеличивают до 80–100 г/сут (1–1,5 г/кг). Белок можно вводить в легкоусваяемой форме в виде растворов гепастерила, гепастерила В.
4. Уменьшение образования кишечных токсинов:
— Санация кишечника. С целью уменьшения образования аммиака в кишечнике и поступления его и других токсических метаболитов в кровеносное русло, коррекции нарушения моторики тонкой кишки применяется неадсорбируемый дисахарид (1,4-0-b-D-галактопиранозил-D-фруктоза) — лактулоза. Лактулоза снижает внутрикишечный pH, ингибирует размножение бактерий-аммониепродуцентов, нарушает всасывание аммиака и аминосодержащих соединений, способствует их утилизации и быстрому выведению из кишечника с калом, а также препятствует расщеплению глутамина в слизистой оболочке кишки. Внутрь лактулозу принимают длительно в виде порошка по 20–30 г 3 раза в сутки, в виде сиропа по 15–30 мл 3–5 раз в день после еды или ректально (по 300 мл сиропа на 700 мл воды) через 2–3 ч до появления послабляющего эффекта. После выхода больного из коматозного состояния лактулозу назначают в дозе 20 г 2–3 раза в день. Препарат дозируют индивидуально, но в качестве доступного критерия оценки эффективности принимают увеличение кратности стула до 2–3 раз в сутки. Это отражает снижение pH толстой кишки < 6,0. Побочные эффекты лактулозы включают тошноту, рвоту, потерю аппетита, вздутие живота, диарею, тенезмы. Лактулоза показана для длительной терапии, может применяться при любой стадии и форме ПЭ и служит средством выбора ее профилактики. С этой же целью применяют маннит, сернокислую магнезию.
— Антибиотики, подавляющие аммониепродуцирующую кишечную микрофлору. Предпочтение отдают препаратам с минимальным побочным действием — фторсодержащим хинолонам (норфлоксацин, ципрофлоксацин), назначаемым в течение 5 сут., а также рифаксимину в суточной дозе 1200 мг с длительностью курса 1–2 нед. Показано назначение метронидазола в дозе 250 мг 4 раза в сутки.
5. Наличие повышенного уровня бензодиазепинов (стимуляторов ГАМК-рецепторов) в ткани мозга стало основанием для использования в терапии ПЭ антагониста бензодиазепиновых рецепторов — флумазенила внутривенно струйно в дозе 0,2–0,3 мг, затем капельно 5 мг/ч с последующим переходом на пероральный прием в дозе 50 мг/сут. На фоне приема препарата отмечают уменьшение выраженности церебральной дисфункции у пациентов.
6. Назначение аминокислот с разветвленной цепью (лейцин, изолейцин и валин) для предотвращения поступления ложных нейромедиаторов в ЦНС. Положительный клинический эффект инфузий аминокислот с разветвленной цепью связан с уменьшением белкового катаболизма в печени и мышцах и улучшением обменных процессов в головном мозге. Аминокислоты с разветвленной цепью являются важным источником белка для пациентов с ПЭ, ограниченных в получении пищевого белка.
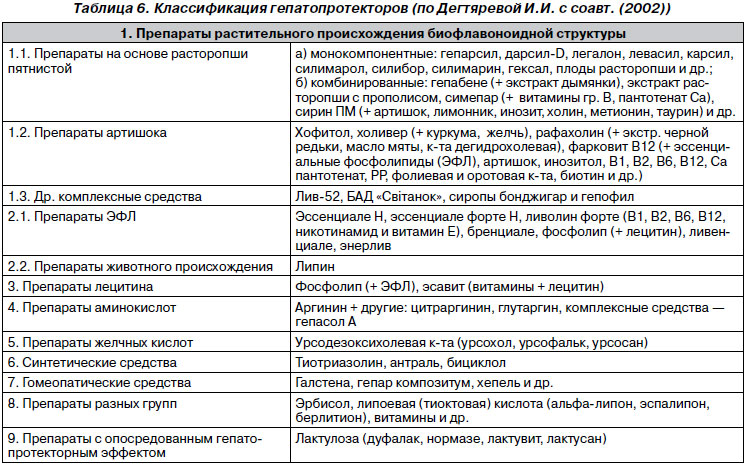
7. Гепатотропная терапия. Гепатопротекторы — группа лекарственных средств природного (растительного и животного) и синтетического происхождения, с различными механизмами действия, эффект которых заключается в повышении устойчивости печени к действию патогенных факторов, усилении процессов ее регенерации и нормализации функциональной активности (табл. 6).
Препараты расторопши пятнистой (Silybum marianum) содержат комплекс флавоноидов силимарин. В основе действия флавоноидов расторопши лежат антиоксидантный эффект, активация синтеза белков печени, антифибротическое действие.
Препараты артишока проявляют гепатопротекторный эффект благодаря антиоксидантной активности флавоноидов и органических кислот. Они улучшают дезинтоксикационную функцию печени, оказывают холеретическое действие, снижают уровень холестерина, нормализуют липидный обмен, а также обладают диуретическим эффектом, способствуют выделению из организма мочевины, токсинов (в том числе нитросоединений, алкалоидов, металлов).
Гепатопротекторный эффект глутаргина обусловлен связыванием эндогенного аммиака, повышением активности цитохрома Р-450, препарат улучшает микроциркуляцию, устраняет гипоксию, повышает резистентность гепатоцитов и способствует устранению венозного стаза в портальной системе при циррозе печени. Глутаминовая кислота повышает устойчивость к гипоксии. Это позволяет предупредить развитие печеночной прекомы и комы при ОПечН. Активатором эндогенного синтеза мочевины является также L-орнитин L-аспартат (гепа-мерц). Основной механизм действия препарата — активация образования мочевины из аммиака через стимуляцию фермента карбамоилсинтетазы орнитинового цикла и непосредственного участия аспартата в качестве субстрата цикла Кребса. Гепа-мерц принимают по 20-40 г/сут внутривенно капельно на физиологическом растворе (500 мл) со скоростью 5 г/ч. К группе промежуточных метаболитов цикла мочевины относятся орнитин-аспартат, орнитин-кетоглутарат и аргинин-малат. Механизмы действия этих соединений определяются включением в орнитиновый цикл в качестве субстратов, а также стимуляцией активности ферментов орнитинового цикла. Назначение L-орнитина-L-аспартата способствует активизации орнитинового цикла детоксикации аммиака. Для лечения ПЭ препарат выпускается как в виде раствора для внутривенной инфузии (5 г активного вещества в ампуле), так и в форме гранулята (3 г активного вещества в одном порошке) для перорального приема. Схемы введения предусматривают внутривенное капельное введение 20–30 г препарата в 500 мл изотонического раствора по 6–10 капель в минуту ежедневно в течение 7–14 дней с последующим переходом на пероральный прием по 9–18 г/сут. В лечении больных на всех стадиях ПЭ показан инфузионный препарат гепасол А, в состав которого входят L-аргинин, L-аспарагиновая кислота, L-яблочная кислота, сорбит, витамины группы В. Гепасол А обладает метаболическим, гепатопротекторным и дезинтоксикационным действием. Эффект препарата основан на введении в организм важных продуктов метаболизма, участвующих в цикле трикарбоновых кислот, в синтезе мочевины и других биохимических процессах, и прежде всего на влиянии L-аргинина на метаболические процессы. L-аргинин способствует превращению аммиака в мочевину, связыванию токсичных ионов аммония, образующихся при катаболизме белков в печени. L-яблочная кислота участвует в образовании АТФ (цикл Кребса), являясь предшественником аспартата, который активно связывает аммиак. Вместе с сорбитом L-яблочная кислота обеспечивает организм энергией. Гепасол А способствует уменьшению интоксикации за счет усиления метаболизма аммиака в печени и в головном мозге, повышает антиоксидантный потенциал сыворотки крови, нормализует показатели интерферонового статуса, обладает умеренным иммуномодулирующим действием. Данные изменения способствуют нормализации биохимической активности в ткани печени, уменьшению клинических проявлений ПЭ и повышению толерантности к белку. Гепасол А вводят внутривенно капельно в дозе 500 мл со скоростью 40 капель в минуту 2 раза в сутки. Препарат хорошо переносится больными, его побочных действий не установлено. Противопоказаниями для его введения являются непереносимость сорбита, фруктозы, дефицит фруктозо-1,6-дифосфатазы, проявления алкалоза, отравление метанолом, тяжелая почечная недостаточность.
Лецитин (и холин) требуется для нормального обмена жиров и холестерина, ему присуще липотропное (жирорастворяющее) действие.
Цитраргинин, помимо аргинина, в своем составе содержит бетаин — аминокислоту, принимающую участие в синтезе фосфолипидов, превращении гомоцистеина в метионин, способствует мобилизации жиров в печени, что обусловливает эффект при жировой инфильтрации печени.
Тиотриазолин является синтетическим гепатопротектором с антиоксидантным эффектом. Экспериментальные и клинические исследования тиотриазолина доказали, что препарат регулирует белковый, липидный, углеводный, энергетический обмен веществ, увеличивает компенсаторную активацию анаэробного гликолиза, активирует окисление в цикле Кребса, имеет выраженную антиоксидантную активность, иммуномодулирующий эффект, улучшает реологические свойства крови. Препарат имеет мембраностабилизирующий эффект, противовоспалительное и репаративное действие. Препарат уменьшает проявления жировой инфильтрации печени, тормозит образование центролобулярных некрозов.
Бициклол уменьшает выработку фактора некроза опухоли, а также обладает антиоксидантной активностью.
Галстена. В гомеопатических разведениях содержит расторопшу, одуванчик, чистотел и др., используется в лечении как острых, так и хронических заболеваний печени (острый и хронический гепатит, гепатоз).
Гепар композитум — гомеопатический препарат, оказывающий на печень гепатопротекторное (мембраностабилизирующее), антиоксидантное, желчегонное, дезинтоксикационное, регенерирующее, метаболическое, венотонизирующее действие.
Хепель содержит Lycopodium, Chelidonium, China, Myristica fragrans, Carduus marianus, Phosphorus, Veratrum, Colocynthis; обладает гепатопротективным, спазмолитическим, желчегонным, противовоспалительным действием.
8. Внутривенно глюкозо-новокаиновая смесь, растворы разветвленных аминокислот, заместительная инфузия 5% раствором альбумина.
9. Стабилизация гемодинамики (допамин), нормотония, нормоосмия 310 = 320 мосмоль/л (маннитол 0,3–0,4 г/кг).
10. Лечение полиорганной недостаточности.
11. Методы детоксикации (экстракорпоральная поддержка печени, частичное замещение функций печени) с помощью биологических (биопечень, применение гепатоцитов свиньи, обезьян, гепатомы или стволовых клеток человека в виде взвеси клеток путем прямого контакта с плазмой, кровью, через полупроницаемую мембрану, введение в брюшную полость, портальную систему, под капсулу селезенки, подкожно) или небиологических (диализ, фильтрация, сорбция) методов. Наиболее перспективным является выполнение технологии Prometeus (фракционированное сепарирование плазмы и адсорбция), альбуминового диализа-МАРС (удаление токсинов путем переноса из альбумина плазмы в альбумин диализата). Процедуры сопровождаются снижением летальности со 100 до 75 %.
12. Устройства для искусственного замещения функции печени (свиные гепатоциты в количестве 6 • 109 обеспечивают 2 % нормальной функции печени. Только у 20 % пациентов функция печени восстанавливается настолько, что они могут дождаться пересадки печени).
13. Своевременное определение показаний к трансплантации печени, так как отсутствует сколько-нибудь эффективное лечение конечных стадий заболевания печени, кроме трансплантации. Трансплантация печени может понадобиться как при острой, так и при хронической печеночной недостаточности. Показанием к пересадке печени является нехолестатический цирроз (гепатоцеллюлярная болезнь), который может быть вызван инфекцией (вирусной), аутоиммунным повреждением или возникнуть в результате злоупотребления алкоголем или передозировки лекарств.
Другим важным показанием для пересадки печени является холестатический цирроз в результате повреждающего воздействия на желчные протоки, так называемый первичный билиарный цирроз. В среднем все формы циррозов являются причиной выполнения около 70 % трансплантаций печени. В развитых странах цирроз печени стоит на третьем месте среди основных причин смерти пациентов в возрасте 45–65 лет (после сердечно-сосудистых заболеваний и опухолей), а самой частой причиной, приводящей к циррозу, является злоупотребление алкоголем. В других странах Азии и Африки более часты вирусные циррозы, обусловленные хроническим гепатитом В. Атрезии желчных протоков и врожденные нарушения метаболизма являются главными причинами выполнения пересадки печени у детей. По данным Европейского регистра трансплантации печени за 1998 г., доля билиарных атрезий в структуре пересадок печени составляет 55 %, рака печени — 10 %, острой печеночной недостаточности — 10 %, холестаза — 11 %, метаболических болезней — 6 %.
Показания к трансплантации печени при острой печеночной недостаточности, принятые в клинике Королевского колледжа (Kings College Hospital criteria for liver transplantation in acute liver failure)
Paracetamol (acetaminophen) overdose:
— H > 50 nmol/litre.
Or all of the following:
— Prothrombin time > 100 seconds.
— Creatinine > 300 &mol/litre.
— Grade III–IV encephalopathy.
Non-paracetamol (acetaminophen):
— Prothrombin time > 100 seconds.
Or three of the following:
— Age < 10 years or > 40 years.
— Prothrombin time > 50 seconds.
— Bilirubin > 300 &mol/litre.
— Time from jaundice to encephalopathy > 2 days.
— Non-А, non-B hepatitis, halothane or drug-induced acute liver failure.

1. Бунятян А.А. (ред.) Руководство по анестезиологии. — 2-е изд., стереотип. — М.: Медицина, 1997.
2. Долина О.А. Анестезиология и реаниматология. — М.: Медицина, 2004. — 544 с.
3. Дон X. Принятие решения в ИТ / Под ред. Б.Р. Гельфанда. — М.: Медицина, 1995.
4. Рябов Г.А. Синдромы критических состояний. — М., 1994.
5. Шанин В.Ю. Клиническая патофизиология. — СПб.: Фонд «Учебная литература», Специальная литература, 1998.
6. Чепкiй Л.П., Новицька-Усенко Л.В., Ткаченко Р.О. Анестезiологiя та iнтенсивна терапiя: Пiдручник для ВМНЗ 3–4 рiвня акредитацiї. — К.: Вища школа, 2003. — 399 с.
7. Невiдкладна медична допомога / За ред. Ф.С. Глумчера, В.Ф. Москаленка. — К.: Медицина, 2006. — 632 с.
8. Сумин С.А. Неотложные состояния. — М.: ООО «Медицинское информационное агентство», 2005. — 752 с.
9. Марино П.Л. Интенсивная терапия. — М.: ГЭОТАР-Медицина, 1999. — 639 с.
10. Пасечник И.Н., Кутепов Д.Е. Печеночная недостаточность: современные методы лечения. — М.: МИА, 2009. — 240 с.