Газета «Новости медицины и фармации» 18 (472) 2013
Вернуться к номеру
Артериальная гипертензия в 2014 г.: классификации, диагностика, лечение
Авторы: Дядык А.И., Багрий А.Э., Хоменко М.В., Щукина Е.В., Приколота О.А., Яровая Н.Ф., Лукашенко Л.В. Донецкий национальный медицинский университет им. М. Горького
Рубрики: Семейная медицина/Терапия, Кардиология
Версия для печати
Артериальная гипертензия (АГ) — важнейший модифицируемый фактор сердечно-сосудистого риска. Общепризнана связь повышенного артериального давления (АД) с увеличением риска развития смертельных и несмертельных инфарктов миокарда и мозговых инсультов, а также с ускорением прогрессирования хронических заболеваний почек.
В настоящем сообщении кратко обсуждаются современные представления о классификациях, диагностике и лечении АГ. Для этого использованы материалы ряда опубликованных в 2012–2013 гг. документов, включая: 1) Приказ Министерства здравоохранения Украины № 384 от 24.05.2012 и Унифицированный клинический протокол первичной, экстренной и вторичной (специализированной) медицинской помощи «Артериальная гипертензия»; 2) Постановление Кабинета министров Украины от 25.04.2012 № 340 «О реализации пилотного проекта по внедрению государственного регулирования цен на лекарственные средства для лечения лиц с гипертонической болезнью»; 3) Рекомендации Европейского общества гипертензии и Европейского общества кардиологов (ESH/ESC) по лечению АГ, 2013.
Определение
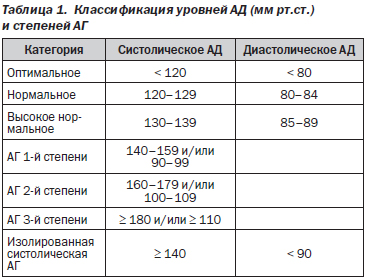
Термином «АГ» обозначают состояние, при котором имеет место устойчивое повышение уровней АД: систолического АД ≥ 140 мм рт.ст. и/или диастолического АД ≥ 90 мм рт.ст. Классификация уровней АД и степеней АГ представлена в табл. 1.
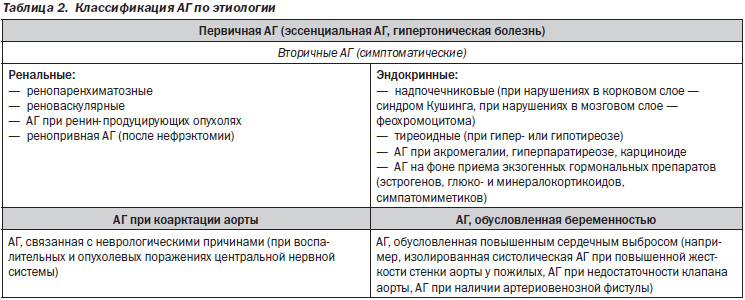
Выделяют первичную АГ (также применяется термин «эссенциальная АГ», у нас общепринято обозначение «гипертоническая болезнь»), при которой повышение АД непосредственно не связано с какими-либо органными поражениями, и вторичные (или симптоматические) АГ, при которых АГ связана с поражениями различных органов/тканей (табл. 2).
Среди всех лиц с АГ доля пациентов с гипертонической болезнью составляет около 90 %; на долю всех перечисленных в табл. 2 симптоматических АГ суммарно приходится около 10 %. Среди симптоматических АГ наиболее частыми являются ренальные (до половины случаев).
Классификации АГ по степени сердечно-сосудистого риска
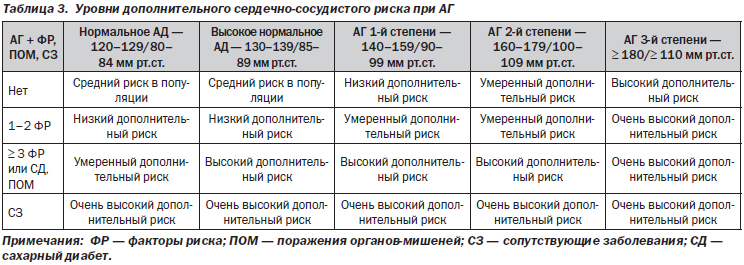
Стандартным сейчас является выделение (и указание при формулировании диагноза) степеней дополнительного сердечно-сосудистого риска при АГ (табл. 3); для этого принято учитывать наличие у пациента наряду с АГ также факторов сердечно-сосудистого риска, поражений органов-мишеней и сопутствующих заболеваний (см. далее).
В соответствии с Фремингемскими критериями термины «низкий», «средний», «высокий» и «очень высокий» риск означают 10-летнюю вероятность развития сердечно-сосудистых осложнений (смертельных и несмертельных) < 15 %, 15–20 %, 20–30 % и > 30 % соответственно.
Факторы сердечно-сосудистого риска, поражения органов-мишеней и сопутствующие заболевания при АГ
Факторы сердечно-сосудистого риска:
— возраст (мужчины ≥ 55, женщины ≥ 65 лет);
— курение;
— дислипидемия (общий холестерин (ХС) > 4,9 ммоль/л, или ХС липопротеидов низкой плотности (ЛПНП) > 3,0 ммоль/л, или ХС липопротеидов высокой плотности (ЛПВП) < 1,0 (у мужчин) и < 1,2 ммоль/л (у женщин), или триглицериды (ТГ) > 1,7 ммоль/л);
— глюкоза плазмы крови натощак ≥ чем в 2 измерениях 5,6–6,9 ммоль/л;
— нарушение толерантности к глюкозе;
— ожирение (индекс массы тела ≥ 30 кг/м2);
— абдоминальное ожирение (окружность талии ≥ 102 см — муж. и ≥ 88 см — жен.);
— сердечно-сосудистые заболевания в семейном анамнезе (< 55 лет — муж., < 65 — жен.).
Поражения органов-мишеней:
— высокое пульсовое АД у пожилых лиц (≥ 60 мм рт.ст.);
— гипертрофия левого желудочка (ЛЖ) — по данным электрокардиограммы (индекс Соколова — Лайона > 3,5 мВ или индекс Корнелл > 244) или по данным эхокардиограммы (индекс массы миокарда ЛЖ ≥ 115 г/м2 (муж.); ≥ 95 г/м2 (жен.));
— утолщение стенки сонных артерий (толщина комплекса интима-медиа > 0,9 мм) или бляшки;
— скорость пульсовой волны (на сонных — бедренных артериях) > 10 м/с;
— лодыжечно-плечевой индекс < 0,9;
— скорость клубочковой фильтрации 30–60 мл/мин;
— микроальбуминурия 30–300 мг/сут или мг/мл.
Сопутствующие заболевания:
— перенесенные инсульты, транзиторные ишемические атаки;
— ишемическая болезнь сердца;
— хроническая сердечная недостаточность при сниженной систолической функции левого желудочка, а также с сохранной его фракцией выброса;
— хроническое поражение почек (скорость клубочковой фильтрации (СКФ) < 30 мл/мин; протеинурия > 300 мг/сут);
— поражения периферических артерий с симптомами;
— тяжелая ретинопатия (геморрагии, экссудаты, отек).
Сахарный диабет:
— диагностика: гликозилированный гемоглобин ≥ 7,0 %, или глюкоза плазмы натощак (≥ 8 ч не есть, двукратно) ≥ 7,0 ммоль/л, или глюкоза через 2 ч после глюкозной нагрузки (75 г глюкозы) ≥ 11,1 ммоль/л;
— важен контроль гликозилированного гемоглобина: не реже 2 раз в году — у лиц, удерживающих целевые уровни и имеющих стабильную гликемию; 1 раз в 3 мес. — при изменении лечения, а также если нет целевого контроля гликемии;
— при нормальных анализах мочи — контроль микроальбуминурии 1 р/год;
— на начальных этапах диабетической нефропатии (микроальбуминурия) — умеренное ограничение белка в пище; при развернутой нефропатии (явная протеинурия) — значительное ограничение приема белка.
Эпидемиология
АГ является одним из наиболее распространенных хронических заболеваний. В Украине в 2011 г. было зарегистрировано более 12,1 млн больных с АГ, что составило 32,2 % взрослого населения. При анализе структуры АГ по уровням АД у 1/2 имеет место АГ 1-й степени, у 1/3 — 2-й степени и у 1/6 — 3-й степени. Распространенность АГ увеличивается с возрастом; не менее 60 % лиц в возрасте > 60–65 лет имеют повышенное АД или получают антигипертензивную терапию.
Среди лиц в возрасте 55–65 лет вероятность развития АГ, по данным Фремингемского исследования, составляет более 90 %.
Всемирная организация здравоохранения рассматривает АГ как наиболее важную из потенциально предотвратимых причин смерти в мире.
АГ ассоциирована с увеличением сердечно-сосудистой смертности и риска сердечно-сосудистых осложнений во всех возрастных группах; среди пожилых лиц степень этого риска имеет прямую связь с уровнем САД и обратную связь с уровнем ДАД.
Имеется также независимая связь между наличием АГ, с одной стороны, и риском развития сердечной недостаточности, поражений периферических артерий и снижения функции почек, с другой стороны.
По эпидемиологическим данным, в странах Запада примерно 50 % больных АГ не знают о наличии у них повышенного АД (т.е. диагноз АГ у них не установлен); среди лиц с АГ лишь около 10 % имеют контроль АД в пределах целевых цифр. Соответствующие данные по Украине в 2010–2011 гг. составляли для мужчин 40 и 10 %, для женщин — 32 и 25 %.
Изолированная систолическая АГ у пожилых
Рядом мировых экспертов рассматривается как отдельное патологическое состояние, присущее пожилым, связанное с уменьшением податливости стенки артерий; при изолированной систолической АГ (ИСАГ) увеличено САД и снижено ДАД (табл. 1). Повышение САД является важным патофизиологическим фактором, способствующим развитию гипертрофии левого желудочка сердца; снижение ДАД может приводить к ухудшению коронарного кровотока. Распространенность ИСАГ увеличивается с возрастом; у пожилых лиц это наиболее частая форма АГ (до 80–90 % всех случаев АГ).
У пожилых людей наличие ИСАГ сопряжено с более значимым увеличением степени сердечно-сосудистого риска, чем наличие систоло-диастолической АГ (при сравнимых величинах САД).
Для оценки степени дополнительного сердечно-сосудистого риска при ИСАГ следует использовать те же уровни САД, те же обозначения факторов риска, поражений органов-мишеней и сопутствующих заболеваний, что и при систоло-диастолической АГ (табл. 1, 3). При этом следует иметь в виду, что особенно низкие уровни ДАД (60–70 мм рт.ст. и ниже) ассоциированы с дополнительным повышением риска.
«АГ белого халата» («АГ в кабинете врача», «офисная АГ»)
Диагностируется, если АД, измеренное в кабинете врача, составляет ≥ 140/90 мм рт.ст. не менее чем в 3 случаях при нормальных значениях АД дома и по данным суточного мониторирования АД (см. «Диагностика АГ»). «АГ белого халата» чаще встречается у лиц пожилого возраста и у женщин. Считается, что сердечно-сосудистый риск у таких пациентов ниже, чем у больных с персистирующей АГ (т.е. с уровнями АД, которые превышают нормальные при измерении дома и при 24-ч мониторировании), но, вероятно, выше, чем у нормотензивных лиц. Подобным лицам рекомендуются изменения образа жизни, а в случае наличия высокого сердечно-сосудистого риска и/или поражения органов-мишеней — медикаментозная терапия (см. в разделе «Лечение АГ»).
Диагностика АГ
Уровни АД характеризуются спонтанной вариабельностью в течение суток, а также в течение более протяженных отрезков времени (недели-месяцы).
Диагноз АГ обычно должен базироваться на данных неоднократных измерений АД, выполненных при различных обстоятельствах; стандартно констатация АГ предусматривается по данным не менее 2–3 визитов к врачу (во время каждого из визитов АД должно быть повышено в течение не менее 2 измерений).
Если при первом визите к врачу АД лишь умеренно повышено, то повторную оценку АД следует выполнять через относительно более длительный период — через несколько месяцев (если уровень АД соответствует 1-й степени АГ — табл. 1 и нет поражений органов-мишеней).
В случае, если при первом визите уровень АД повышен более значительно (соответствует 2-й степени АГ — табл. 1), либо если имеются возможно связанные с АГ поражения органов-мишеней, либо если уровень дополнительного сердечно-сосудистого риска высокий, то повторная оценка АД должна быть сделана через относительно более короткий интервал времени (недели-дни); если же уровень АД при первом визите соответствует 3-й степени АГ, если имеется отчетливая симптоматика АГ, уровень дополнительного сердечно-сосудистого риска высокий, то диагноз АГ может базироваться на данных, полученных при единственном визите к врачу.
Рекомендуется не только контроль АД врачом/медсестрой в условиях стационара/амбулаторно, но и самостоятельный его контроль дома (больным или родственниками), а также выполнение суточного мониторирования АД.
Измерение АД
Стандартно рекомендуется измерение АД ртутным сфигмоманометром или анероидным манометром (последние получили значительное распространение в связи с тенденцией к устранению ртути из широкого использования). Независимо от вида, аппараты для измерения АД должны быть исправными, их показатели должны периодически проверяться (при сопоставлении с данными других аппаратов, обычно ртутных сфигмоманометров).
Возможно также использование полуавтоматических устройств для измерения АД; точность их работы должна быть установлена по стандартным протоколам; показания измерений АД должны периодически проверяться при сопоставлении с данными ртутных сфигмоманометров.
Рекомендации по измерению АД
Перед измерением АД пациент должен в течение 3–5 минут пребывать (обычно в положении сидя) в спокойной обстановке.
АД следует измерять по меньшей мере двукратно, с интервалом 1–2 минуты между измерениями; если полученные результаты сильно различаются, выполняют третье измерение АД. Учитывается средняя величина из 3 измерений.
При нарушении ритма (например, фибрилляции предсердий) должно выполняться несколько измерений.
Стандартные размеры манжеты — 12–13 на 35 см. При необходимости должны использоваться манжеты меньшего или большего (при окружности плеча > 32 см) размера.
Манжета должна располагаться на уровне сердца.
Для определения систолического и диастолического АД используются соответственно I (появление) и V (исчезновение) фазы тонов Короткова.
При первом визите больного следует измерить АД на обеих руках для определения возможных различий, связанных с поражением периферических артерий. Для установления степени АГ используется более высокая из полученных величин.
У пожилого больного следует измерить АД также в положении стоя, через 1, 3 и 5 минут после вставания с целью выявления ортостатической (постуральной) гипотензии.
Также в течение 30 секунд при положении пациента сидя оценивается пульс.
Суточное мониторирование АД (СМАД) по сравнению с обычным контролем АД
СМАД позволяет избежать возможных неточностей измерения, связанных с нарушением его методики, неисправностью аппарата, волнением пациента. Этот метод также обеспечивает возможность получения данных множественных измерений АД за 24-часовой период без влияния на эмоциональный статус пациента. Он считается более воспроизводимым, чем эпизодическое измерение. Данные СМАД менее подвержены влиянию «эффекта белого халата».
В целом при АГ СМАД рассматривается как более весомый критерий сердечно-сосудистого риска, однако для лиц пожилого возраста это нуждается в уточнении.
Уровни АД, регистрируемые при его суточном мониторировании, обычно ниже тех, которые выявляются при его измерении в кабинете врача. По современным представлениям, верхние границы нормы АД при его суточном мониторировании составляют 125–130/80 мм рт.ст. (130–135/85 днем и 120/70 ночью); оптимальные значения, однако, остаются неустановленными; отдельные для разных возрастов нормы не разработаны.
Показания для СМАД включают: 1) неясность диагноза АГ, предположение о наличии «эффекта белого халата»; 2) необходимость в оценке ответа АД на лечение, особенно если данные измерений в кабинете врача устойчиво превышают целевые уровни АД; 3) значительную вариабельность данных, полученных при измерении АД в кабинете врача; 4) предположение о наличии резистентности АГ к лечению; 5) предположение о наличии эпизодов гипотензии.
Измерение АД дома: преимущества и современные представления
Этот метод становится все более распространенным, особенно с расширением применения полуавтоматических аппаратов для измерения АД. Данные, полученные при измерении АД дома, менее подвержены искажениям, связанным с «эффектом белого халата», чем те, которые получены при измерении АД в присутствии врача. Измерение АД дома демонстрирует хорошую точность в определении его нормальных и повышенных уровней.
Уровни, полученные при измерении АД дома, обычно ниже тех, которые регистрируются в кабинете врача. По современным представлениям, верхняя граница нормы для АД, измеренного в домашних условиях, составляет 135/85 мм рт.ст.
Данные измерения АД дома хорошо коррелируют со среднедневными уровнями, регистрируемыми при суточном мониторировании АД. В целом у больных с АГ данные измерения АД дома лучше, чем уровни АД, измеренные в кабинете врача, коррелируют с поражением органов-мишеней и риском сердечно-сосудистой смерти. Для лиц пожилого возраста это нуждается в дополнительном изучении.
Измерение АД дома — удобный подход к его контролю. Он дает возможность неоднократно оценивать уровни АД в течение времени бодрствования пациента. Использование этого подхода повышает дисциплинированность больного и его приверженность к лечению.
Различия между уровнями АД, измеренными дома и в кабинете врача, увеличиваются с возрастом, с повышением величины САД; они выше у мужчин и у лиц, не получающих антигипертензивного лечения.
Антигипертензивная терапия обычно вызывает более значительное снижение уровня АД, измеренного в кабинете врача, чем измеренного дома (причины этого недостаточно ясны).
Рекомендации по измерению АД дома:
— использовать исправный, метрологически проверенный аппарат;
— следовать имеющимся рекомендациям по измерению АД, эти рекомендации должны быть разъяснены больному врачом/медсестрой;
— при необходимости (например, подбор дозы антигипертензивных препаратов) рекомендуется двукратное измерение АД в течение суток (утром и вечером) в течение нескольких дней (обычно не менее 3 последовательных дней);
— измерение АД дома важно для исключения «эффекта белого халата»;
— контроль АД дома также желателен для оценки ответа на антигипертензивное лечение, особенно если уровни АД в кабинете врача устойчиво превышают целевые значения;
— хотя СМАД рассматривается как предпочтительный метод оценки эффективности антигипертензивной терапии, контроль АД дома имеет определенные преимущества, а именно: он более дешев и менее некомфортен для больного.
Когда не следует рекомендовать контроль АД дома:
— при слишком большой окружности плеча, если нет манжеты подходящего размера;
— при наличии значимой нерегулярности пульса (например, в части случаев у лиц с фибрилляцией предсердий, что часто имеет место у пожилых) данные самостоятельной оценки АД могут быть неточны;
— при очень выраженном повышении жесткости стенки сосудов (все имеющиеся для измерения АД аппараты используют осциллометрический метод, который может обусловливать искажение результатов у таких больных);
— у лиц, которые не могут выполнять рекомендации (например, при когнитивных нарушениях);
— в случае, если измерение АД дома значительно повышает тревожность больного и это влияет на выбор тактики лечения.
Обследование больных с АГ
Обследование больных с АГ должно быть направлено на поиск:
— провоцирующих АГ факторов, таких как применение некоторых лекарственных средств/химических веществ (нестероидных противовоспалительных препаратов, глюкокортикоидов, эритропоэтина, циклоспорина, такролимуса, кокаина, амфетаминов, лакрицы); прием избыточных количеств поваренной соли с пищей; малоподвижный образ жизни; ожирение; синдром обструктивного апноэ во сне;
— данных о наличии поражений органов-мишеней (табл. 3);
— клинических проявлений сердечно-сосудистых осложнений (хроническая сердечная недостаточность, сосудисто-мозговые и периферические сосудистые осложнения и др.);
— сопутствующие заболевания/состояния (сахарный диабет, фибрилляция предсердий, нарушения когнитивной функции, частые падения, шаткость при ходьбе и т.д.), которые могут повлиять на выбор лечебной тактики.
Рутинные, а также рекомендуемые в части случаев исследования для лиц пожилого возраста с АГ, выполняемые перед началом лечения
Рутинные:
— глюкоза плазмы крови натощак;
— липидный профиль натощак;
— электролиты плазмы;
— мочевая кислота сыворотки;
— уровень креатинина сыворотки с подсчетом скорости клубочковой фильтрации (например, формула Кокрофта — Гаулта);
— общий анализ крови (+ оценка гематокрита);
— общий анализ мочи (возможно — оценка микроальбуминурии);
— электрокардиограмма в 12 отведениях;
— осмотр глазного дна;
— ультразвуковое исследование почек.
Рекомендуемые в части случаев:
— эхокардиографическое исследование;
— тест толерантности к глюкозе (если глюкоза плазмы натощак > 5,6 ммоль/л);
— суточное мониторирование АД, измерение АД дома.
Благоприятные эффекты контроля АД в пределах целевых уровней у лиц с АГ (по данным РКИ и метаанализов)
Показано уменьшение сердечно-сосудистой смертности и частоты сердечно-сосудистых осложнений, менее выраженный эффект на общую смертность. Также отмечается отчетливое уменьшение риска развития хронической сердечной недостаточности.
Снижение риска инсультов на фоне антигипертензивной терапии более выражено, чем уменьшение риска коронарных осложнений. Так, снижение диастолического АД всего на 5–6 мм рт.ст. приводит к уменьшению риска развития инсульта в течение 5 лет приблизительно на 40 %, а ишемической болезни сердца — примерно на 15 %.
Чем более выражена степень снижения АД (в пределах целевых уровней), тем выше благоприятное действие на прогноз.
Перечисленные благоприятные эффекты показаны также у лиц пожилого возраста, в т.ч. у имеющих изолированную систолическую АГ. Благоприятные эффекты отмечены у больных разных этнических групп (у белокожих, чернокожих, в азиатских популяциях и др.).
Цели лечения АГ
Основная цель лечения АГ — это снижение сердечно-сосудистого риска, уменьшение риска развития ХСН и хронической почечной недостаточности. Благоприятные эффекты лечения должны быть соотнесены с риском, сопряженным с возможными осложнениями лечения. Следует принять во внимание, что пожилые в сравнении с лицами среднего возраста имеют более высокую вероятность развития побочных эффектов лекарственных препаратов, нежелательных взаимодействий лекарственных средств; у них чаще имеет место применение многокомпонентных лечебных программ (при этом следует стремиться избежать полипрагмазии). В лечебной тактике важно предусмотреть меры, направленные на коррекцию выявленных у больного потенциально корригируемых факторов сердечно-сосудистого риска, включая курение, дислипидемию, абдоминальное ожирение, сахарный диабет.
До недавнего времени вопрос о необходимости применения антигипертензивных препаратов у больных с АГ в возрасте 80 лет и старше был предметом дискуссий, однако сейчас есть вполне определенные доказательства того, что антигипертензивное лечение и у этой категории пожилых лиц сопровождается благоприятными изменениями сердечно-сосудистого прогноза.
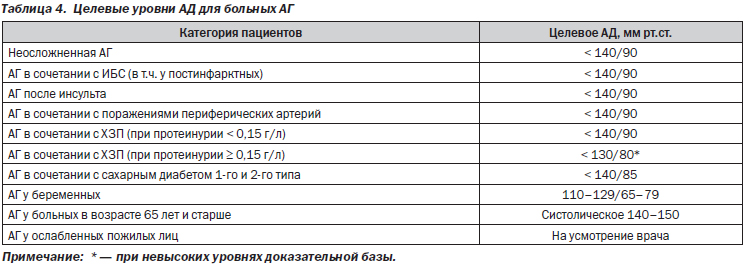
Целевые уровни АД, рекомендуемые экспертами Европы и США в ходе антигипертензивной терапии, представлены в табл. 4. Категории пожилых больных с АГ важно иметь в виду, что у них уровни АД обычно более значимо варьируют; что они более склонны к развитию эпизодов гипотензии (в т.ч. ортостатической, постуральной). Выбор целевого уровня АД для конкретного больного должен быть индивидуальным.
Лечение АГ
Нефармакологическое лечение
Перечисленные ниже изменения образа жизни способствуют снижению АД и уменьшению сердечно-сосудистого риска.
Снижение массы тела для пациентов с ожирением (если индекс массы тела более 30 кг/м2). Показано, что у подобных пациентов стойкое уменьшение массы тела на 1 кг сопровождается снижением систолического АД на 1,5–3 мм рт.ст., диастолического АД — на 1–2 мм рт.ст.
Регулярные физические нагрузки на воздухе (для гемодинамически стабильного пациента — не менее 150 (а лучше — не менее 300) минут в неделю; у многих больных достаточно быстрой ходьбы на протяжении 30–45 минут ежедневно или не реже 5 раз в неделю). Изометрические нагрузки (например, подъем тяжестей) способствуют повышению АД, их желательно исключить.
Уменьшение употребления поваренной соли. Показано, что снижение потребляемой соли до 5,0 г/сут (столько ее содержится в 1/2 чайной ложки) ассоциируется со снижением систолического АД на 4–6 мм рт.ст., диастолического АД — на 2–3 мм рт.ст. Снижение АД вследствие уменьшения употребления соли более выражено у лиц пожилого возраста. В качестве достаточно действенной меры (способствующей уменьшению употребления соли примерно на 30 %) может быть использована рекомендация убрать со стола солонку.
Уменьшение употребления алкоголя.
Уменьшение употребления насыщенных жиров (жиров животного происхождения).
Увеличение употребления свежих фруктов и овощей (суммарно желательно около 300 г/сутки).
Прекращение курения.
Фармакологическое лечение
Фармакологическое лечение требуется большинству больных с АГ, основная цель этого лечения — улучшение сердечно-сосудистого прогноза.
Медикаментозная терапия АГ (в сочетании с немедикаментозными лечебными подходами) при устойчивом поддержании уровней АД в пределах целевых значений способствует значительному улучшению сердечно-сосудистого (с уменьшением риска развития смертельных и несмертельных мозговых инсультов и инфарктов миокарда), а также почечного прогноза (со снижением темпа прогрессии почечных поражений).
Лечение (немедикаментозное и медикаментозное) необходимо начинать как можно раньше и проводить его постоянно, как правило в течение всей жизни. Понятие курсового лечения к антигипертензивной терапии неприменимо.
В соответствии с Рекомендациями по лечению АГ, представленными европейскими экспертами (ESC-ESH) в 2013 г., изменились рекомендуемые подходы к началу лечения АГ у некоторых категорий больных:
— пожилым с АГ медикаментозную антигипертензивную терапию рекомендовано начинать при уровнях систолического АД ≥ 160 мм рт.ст. (I/A). Антигипертензивные препараты могут назначаться пожилым лицам в возрасте до 80 лет и при уровнях систолического АД в пределах 140–159 мм рт.ст., если они хорошо переносятся (IIb/C);
— до получения дополнительных данных не рекомендовано начинать антигипертензивную терапию лицам с высоким нормальным АД — 130–139/85–89 мм рт.ст. (III/А). Эта рекомендация в первую очередь распространяется на лиц, не имеющих сопутствующих сердечно-сосудистых поражений;
— также пока не рекомендуется начинать антигипертензивную терапию у молодых лиц с изолированным повышением АД на плече. За ними следует тщательно наблюдать и изменить образ жизни (III/А).
В лечении больных с АГ наиболее часто используется 5 классов антигипертензивных препаратов: диуретики, блокаторы кальциевых каналов, ингибиторы АПФ, сартаны, бета-адреноблокаторы. Для препаратов этих классов имеются крупные исследования, демонстрирующие их благоприятные эффекты на прогноз. Могут также применяться и иные классы антигипертензивных средств (относящиеся ко второй линии).
Широкое распространение имеет комбинированная антигипертензивная терапия (способствует повышению эффективности и безопасности лечения). Оправданно использование фиксированных комбинированных препаратов (улучшает приверженность пациента).
Предпочтение отдается антигипертензивным препаратам продленного действия (в т.ч. ретардным формам).
После назначения антигипертензивной терапии врач должен осмотреть больного не позднее чем через 2 недели. При недостаточном снижении АД следует увеличить дозу препарата, или поменять препарат, или дополнительно назначить препарат иного фармакологического класса. В дальнейшем пациента следует регулярно осматривать (каждые 1–2 недели), пока не будет достигнут удовлетворительный контроль АД. После стабилизации АД осматривать больного следует каждые 3–6 месяцев (при удовлетворительном самочувствии).
Показано, что применение антигипертензивных препаратов у больных АГ в возрасте как до 80, так и после 80 лет сопровождается улучшением сердечно-сосудистого прогноза. Адекватное фармакологическое лечение АГ не оказывает неблагоприятного действия на когнитивную функцию у пожилых больных, не повышает риск развития деменции; более того, оно, вероятно, может такой риск снижать.
Лечение должно начинаться с малых доз, которые постепенно при необходимости можно повышать. Весьма желателен выбор препаратов с суточной продолжительностью действия.
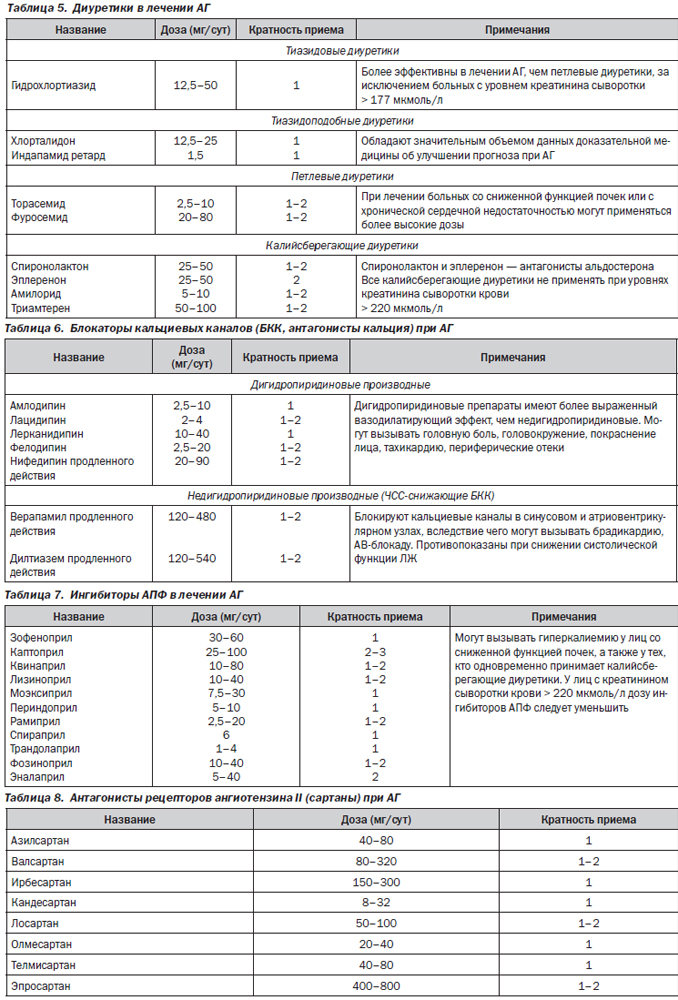
Наиболее часто для лечения АГ применяются 5 классов антигипертензивных препаратов (обозначаемых обычно как базисные): ингибиторы ангиотензинпревращающего фермента, антагонисты рецепторов ангиотензина II (сартаны), блокаторы кальциевых каналов (чаще — дигидропиридиновые), тиазидовые диуретики и b-адреноблокаторы. Также в лечении АГ могут быть использованы и дополнительные препараты (обозначаемые как лекарственные средства второй линии). В табл. 5–10 представлены классификации различных антигипертензивных препаратов и современные взгляды на их место в лечении АГ.
Место диуретиков при АГ в 2014 г.:
— сохраняют позиции одного из ведущих классов анти-АГ-препаратов;
— наиболее дешевы;
— усиливают антигипертензивный эффект любых анти-АГ-препаратов;
— ожидается расширение позиций хлорталидона и индапамида. В сравнении с гидрохлортиазидом эти препараты: 1) имеют более сильный или сравнимый антигипертензивный эффект; 2) показывают значительно меньше метаболических побочных эффектов; 3) обладают благоприятными плейотропными эффектами; 4) обладают доказательствами благоприятного влияния на сердечно-сосудистый прогноз;
— антагонисты минералокортикоидных рецепторов (антагонисты альдостерона) — спиронолактон и эплеренон — находят применение в лечении резистентной АГ (в качестве 4-го препарата, например в добавление к блокатору ренин-ангиотензиновой системы + диуретику + блокатору кальциевых каналов) при отсутствии гиперкалиемии и при СКФ > 30–60 мл/мин. Кроме того, они используются в лечении АГ при первичном гиперальдостеронизме (имеется у 10 % среди общего количества больных с АГ — N. Kaplan, 2010);
— немалой части больных с АГ для достижения целевого АД может требоваться более 1 диуретика (так называемая концепция последовательной блокады нефрона), например: 1) хлорталидон + антагонист альдостерона; 2) гидрохлортиазид + антагонист альдостерона + триамтерен; 3) петлевой диуретик + антагонист альдостерона + амилорид.
Место блокаторов кальциевых каналов при АГ в 2014 г.:
— широко применяются при АГ в целом, в особенности при сочетании АГ с хронической ишемической болезнью сердца, вазоспастическими нарушениями, наджелудочковыми нарушениями ритма, хроническим заболеванием почек;
— среди препаратов этого класса в последние годы отмечается выраженное доминирование дигидропиридиновых препаратов, а среди них — амлодипина;
— добавление амлодипина к ингибитору АПФ или сартану при хроническом заболевании почек приводит к значительному усилению ренопротекции. Но изолированное применение дигидропиридина (без блокатора ренин-ангиотензиновой системы) при ХЗП считается нежелательным;
— БКК усиливают натрийурез, вследствие чего их применение оправданно при солечувствительной АГ;
— при резистентной АГ в качестве 5–6-го шага эксперты США считают возможным использование комбинации дигидропиридинового и недигидропиридинового БКК.
Место ингибиторов АПФ при АГ в 2014 г.:
— широко применяются в лечении пациентов с АГ, ишемической болезнью сердца (как при острых, так и при хронических ее формах), хронической сердечной недостаточностью, сахарным диабетом, ХЗП;
— обладают огромной доказательной базой по разноплановой органопротекции (вазо-, кардио-, рено-, церебропротекции), по улучшению сердечно-сосудистого прогноза у больных с перечисленными выше состояниями;
— у 10–15 % лиц, получающих ингибиторы АПФ, может развиваться кашель (что рассматривается экспертами как «побочный эффект класса»);
— в лечении АГ получили распространение различные фиксированные комбинации ингибиторов АПФ (с диуретиками, БКК).
Место сартанов при АГ в 2014 г.:
— в течение последних лет существенно расширяется применение этого класса при АГ, в т.ч. как препаратов для первого назначения;
— имеют плацебоподобную переносимость;
— высокобезопасны (в том числе не увеличивают онкологический риск);
— в той же мере, что и ингибиторы АПФ, снижают риск развития инфаркта миокарда;
— обладают доказанной разноплановой органопротекцией, свидетельствами улучшения сердечно-сосудистого, цереброваскулярного и почечного прогноза;
— в сочетании с амлодипином, как и ингибиторы АПФ, способствуют уменьшению периферических отеков;
— при АГ широко используются в 2- и 3-компонентных фиксированных комбинациях (сартан + тиазидовый диуретик + блокатор кальциевых каналов);
— могут назначаться «впереди ингибиторов АПФ»: 1) при неосложненной АГ; 2) АГ у больных сахарным диабетом 2-го типа при наличии диабетической нефропатии;
— применяются «при непереносимости ингибиторов АПФ»; 1) при ишемической болезни сердца; 2) хронической сердечной недостаточности; 3) сахарном диабете 2-го типа без поражения почек; 4) сахарном диабете 1-го типа независимо от наличия поражения почек. Место сартанов «при непереносимости ингибиторов АПФ» при перечисленных состояниях связано не с тем, что они по сравнению с ингибиторами АПФ обеспечивают меньший уровень органопротекции, а лишь с тем, что сартаны у подобных больных менее изучены (имеют меньший объем данных доказательной медицины).
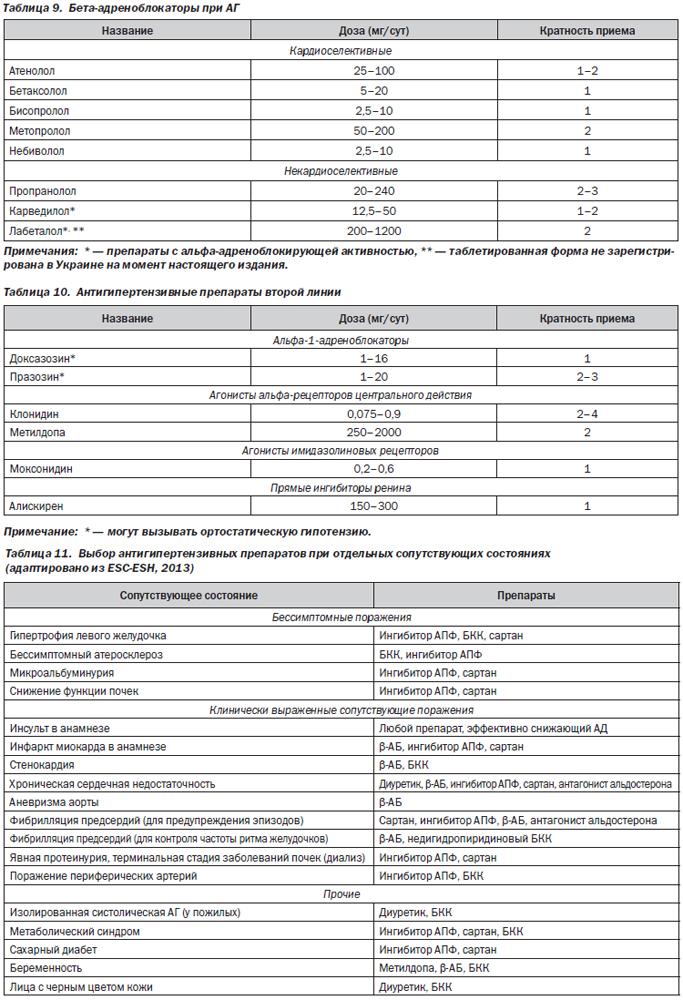
Место бета-адреноблокаторов при АГ в 2014 г.:
— бета-адреноблокаторы сохраняют позиции одного из ведущих классов лекарственных препаратов в лечении АГ;
— их выбор в особенности оправдан у лиц, перенесших инфаркт миокарда, имеющих стенокардию, хроническую сердечную недостаточность, нарушения ритма сердца, хроническое заболевание почек;
— они оказывают антигипертензивный эффект также у лиц: 1) молодого и среднего возраста; 2) с признаками гиперсимпатикотонии (тахикардия, гиперкинетический гемодинамический синдром); 3) с гипертиреозом; 4) мигренью; 5) глаукомой;
— применение бета-адреноблокаторов в лечении АГ вполне оправданно у пожилых лиц, если имеются показания к вторичной профилактике сердечно-сосудистых заболеваний (т.е. сопутствующие ишемическая болезнь сердца, хроническая сердечная недостаточность). Их место в первичной профилактике у пожилых менее ясно;
— бета-адреноблокаторы снижают активность как симпатической нервной системы, так и ренин-ангиотензин-альдостероновой системы;
— вазодилатирующие бета-адреноблокаторы (карведилол, небиволол), как и ингибиторы АПФ и сартаны, снижают центральное аортальное давление в большей степени, чем брахиальное давление. Карведилол и небиволол обладают менее выраженными метаболическими побочными эффектами в сравнении с другими представителями бета-адреноблокаторов, ввиду чего рассматриваются как препараты выбора для лиц с сахарным диабетом, которым показано применение бета-адреноблокаторов;
— как и ингибиторы АПФ и сартаны, все бета-адреноблокаторы в меньшей степени снижают АД у лиц с черным цветом кожи (в то же время блокаторы кальциевых каналов и диуретики у них более эффективны).
Место препаратов второй линии при АГ в 2014 г.:
— эти препараты обладают достаточным по выраженности антигипертензивным эффектом. Кроме того, ряду из них присущи дополнительные благоприятные свойства (например, метаболическая нейтральность или даже позитивные эффекты на липидный и гликемический профиль). Однако ввиду отсутствия данных представительных рандомизированных исследований о благоприятном влиянии на сердечно-сосудистый прогноз эти средства в лечении АГ обычно занимают вспомогательную позицию (применяются в качестве дополнения к основным классам антигипертензивных препаратов);
— альфа-1-адреноблокаторы находят более широкое применение у лиц с АГ, имеющих аденому предстательной железы;
— применение клофелина ограничено его известными побочными эффектами (седация, сухость во рту);
— метилдопа является препаратом выбора в лечении АГ при беременности;
— моксонидин преимущественно может использоваться в комбинированном антигипертензивном лечении у лиц с АГ и сопутствующими сахарным диабетом, метаболическим синдромом, а также при сниженной функции почек;
— алискирен в настоящее время применяется главным образом в лечении неосложненной АГ. Его не следует комбинировать с ингибиторами АПФ и сартанами.
У лиц с АГ в целом (и у пожилых больных в частности) могут быть использованы любые из 5 перечисленных классов базисных антигипертензивных средств. b-адреноблокаторы не рассматриваются сейчас как антигипертензивные средства выбора для пожилых пациентов с неосложненной АГ, однако они должны быть назначены лицам, перенесшим инфаркт миокарда (особенно в течение ближайших 1–3 лет), а также тем, кто имеет сопутствующую хроническую сердечную недостаточность.
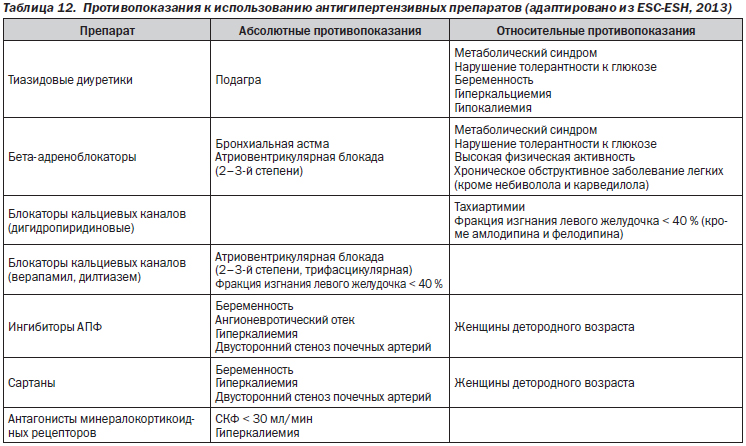
В табл. 11 представлены рекомендованные экспертами ESC-ESH в 2013 г. подходы к выбору антигипертензивных препаратов при наличии сопутствующих состояний. В табл. 12 суммированы противопоказания к использованию различных классов антигипертензивных препаратов.
Пилотный проект по внедрению государственного регулирования цен на лекарственные средства для лечения лиц с гипертонической болезнью
Кабинетом министров Украины 25.04.2012 было принято Постановление № 340 «О реализации пилотного проекта по внедрению государственного регулирования цен на лекарственные средства для лечения лиц с гипертонической болезнью». Целью этого пилотного проекта является повышение доступности препаратов, применяемых при АГ, для населения Украины, а также увеличение приверженности к лечению путем снижения цен на некоторые антигипертензивные препараты. Постановлением № 340 установлено, что препараты для лечения лиц с АГ с учетом соответствующего дозирования делятся на следующие 3 группы в зависимости от их стоимости с учетом предельных снабженческо-сбытовых и торговых (розничных) надбавок: первая группа — лекарственные средства для лечения лиц с АГ, стоимость которых подлежит частичному возмещению (90 %); вторая группа — менее 90 %; третья группа — лекарственные средства для лечения лиц с АГ, стоимость которых не возмещается.
Действие пилотного проекта распространяется на некоторые препараты и их комбинации, которые относятся к первому ряду лекарственных препаратов для лечения АГ. Вначале в проект были включены ингибиторы АПФ (эналаприл, лизиноприл), блокаторы кальциевых каналов дигидропиридинового ряда (амлодипин, ретардная форма нифедипина) и бета-адреноблокаторы (бисопролол, метопролол, небиволол). В дальнейшем добавились распространенные комбинации некоторых из перечисленных препаратов с тиазидовым диуретиком (гидрохлортиазидом) — эналаприл + гидрохлортиазид, лизиноприл + гидрохлортиазид, а также комбинация лизиноприла с амлодипином.
Предварительные результаты реализации пилотного проекта (по данным за 9 месяцев 2013 г.) состоят в снижении средневзвешенной розничной стоимости одной упаковки препарата; существенном возрастании потребления препаратов, включенных в пилотный проект; снижении средневзвешенной стоимости одной упаковки импортных антигипертензивных препаратов. Также зафиксировано улучшение показателей наличия в аптечных учреждениях полного ассортимента лекарственных средств, включенных в пилотный проект.
Выбор лечебной тактики: монотерапия или комбинированная антигипертензивная терапия?
На рис. 1 представлены подходы к выбору лечебной тактики при АГ, рекомендованные экспертами ESC-ESH в 2013 г.
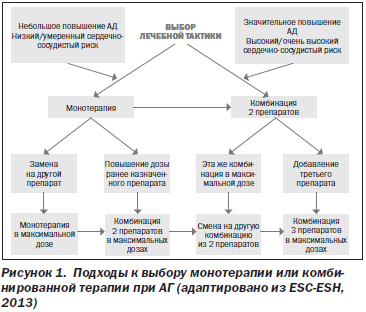
При выборе в качестве начального подхода монотерапии антигипертензивным препаратом предпочтение обычно отдают блокатору кальциевых каналов либо тиазидовому диуретику, при необходимости к ним добавляют либо ингибитор АПФ, либо сартан.
Многим больным уже на начальном этапе лечения может быть назначена комбинированная антигипертензивная терапия двумя препаратами. На рис. 2 представлены рекомендованные экспертами ESC-ESH в 2013 г. комбинации антигипертензивных препаратов. При необходимости используют трехкомпонентную антигипертензивную терапию (обычно это блокатор кальциевых каналов + тиазидовый диуретик + ингибитор АПФ/сартан). Не рекомендуется комбинировать ингибитор АПФ с сартаном.
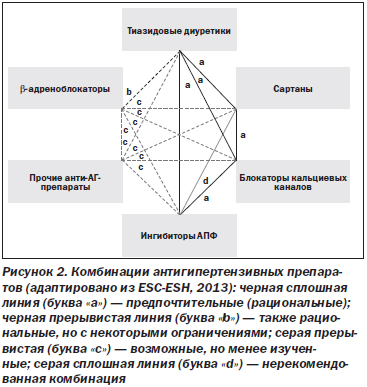
При наличии у больного высокого или очень высокого уровня дополнительного сердечно-сосудистого риска в лечебную стратегию должны быть включены статин (например, аторвастатин в дозе 10 мг/сут, при наличии сопутствующей ИБС доза должна быть выше) и аспирин (75–100 мг/сут, после достижения контроля АД, после еды вечером) — при переносимости и отсутствии противопоказаний, для постоянного приема. Основная цель назначения статина и аспирина в этом случае — уменьшение риска сердечно-сосудистых осложнений.
Плохо контролируемая и резистентная АГ
Понятия «плохо контролируемая» и «резистентная» АГ не являются синонимами. Понятием «резистентная АГ» обозначают случаи, когда уровни АД удерживаются выше целевых, несмотря на то что пациент: 1) придерживается рекомендаций по изменению образа жизни (в т.ч. по ограничению поваренной соли); 2) принимает 3 класса хорошо сочетающихся между собой антигипертензивных препаратов в полных дозах; 3) препарат одного из этих 3 классов является диуретиком. Распространенность резистентной АГ среди всех лиц с АГ в США составляет около 9 %.
В случае если предполагается наличие резистентной АГ, на начальном этапе необходимо проверить приверженность больного к лечению и адекватность выполнения им рекомендаций по изменению стиля жизни. Также необходимы поиск и лечение симптоматических АГ.
Если принято решение об использовании 4-компонентной антигипертензивной терапии, то можно к уже применяемой комбинации, включающей блокатор кальциевых каналов, тиазидовый или тиазидоподобный диуретик и ингибитор АПФ или сартан, добавить: 1) антагонист альдостерона (эплеренон или спиронолактон в небольшой дозе — 25 мг/сут) с учетом важной роли гиперальдостеронизма, в т.ч. субклинического, в развитии резистентной АГ; 2) петлевой диуретик (фуросемид или торасемид), обычно у больных с сопутствующим ХЗП; 3) калийсберегающий диуретик, не относящийся к антагонистам альдостерона (триамтерен или амилорид), в части случаев они также могут быть эффективны при резистентной АГ; 4) другой блокатор кальциевых каналов (если ранее был назначен дигидропиридиновый, то добавить недигидропиридиновый, и наоборот); 5) препарат центрального действия (моксонидин или урапидил) и/или a-адреноблокатор (доксазозин, особенно у лиц с аденомой предстательной железы); (6) нитрат (изосорбида динитрат или мононитрат).
Причины плохо контролируемой АГ (адаптировано из Ruilope L., 2013)
Факторы, зависящие от больного:
Неприверженность:
— низкий уровень информированности;
— высокая стоимость препаратов;
— сложный лекарственный режим;
— побочные эффекты лечения;
— плохие отношения с врачом;
— отсутствие социальной поддержки.
Связанные с системой здравоохранения:
— отсутствие медицинской страховки;
— отсутствие постоянного наблюдения.
Высокая распространенность АГ в отдельных группах больных:
— пожилой возраст;
— лица с ожирением.
Резистентная АГ (нечасто).
Симптоматические АГ.
Факторы, зависящие от врача:
Недостаточная информированность о современных рекомендациях:
— нет информации о целевых уровнях АД;
— нет информации об изолированной систолической АГ;
— чрезмерная приверженность к монотерапии.
Чрезмерная надежда на приверженность:
— «врачу следует отчетливо представлять себе, что большинство больных с хроническими заболеваниями имеют низкую приверженность к длительному лечению. Наша задача — постоянно и регулярно, доброжелательно и понятным образом разъяснять необходимость длительного лечения АГ, хронической ишемической болезни сердца, хронической сердечной недостаточности…»;
— «есть три основные причины резистентной АГ. Это: 1) неприверженность; 2) неприверженность и 3) неприверженность» (гипербола понятна и вполне оправданна!).
Несогласие с современными рекомендациями:
— в вопросе об изолированной систолической АГ;
— опасения в отношении J-кривой.
Вера в то, что офисное АД всегда выше домашнего.
Нежелание лечить «бессимптомное состояние».
Отсутствие времени на визите.
В качестве компонента комбинированной антигипертензивной терапии может быть также использован прямой ингибитор ренина алискирен (если нет дополнительного высокого или очень высокого сердечно-сосудистого риска — табл. 3). Не следует сочетать алискирен с ингибиторами АПФ или сартанами.
При необходимости может быть использовано лечение, включающее более 4 антигипертензивных препаратов, однако следует иметь в виду, что в этом случае: 1) какие-либо определенные рекомендации, кроме перечисленных выше, по созданию столь сложных лечебных программ отсутствуют, дальнейший выбор лечения основывается преимущественно на опыте врача; 2) дополнительно возрастает риск лекарственных взаимодействий и развития эпизодов гипотензии.
В последнее время в лечении резистентной АГ находят применение инвазивные лечебные процедуры (катетерная почечная денервация; имплантация устройств, активирующих каротидные адренорецепторы).
Направление больного на консультацию к специалисту
Значительная часть больных с АГ может находиться под наблюдением семейного врача/врача общей практики. Направление больного на консультацию к специалисту (кардиологу, нефрологу и др.) оправданно, если: 1) у больного на фоне имеющейся АГ развиваются такие осложнения, как сердечная недостаточность или снижение функции почек; 2) имеет место недостаточный ответ на применение комбинированной антигипертензивной терапии, включающей 3 и более класса антигипертензивных препаратов; 3) имеются значимые побочные эффекты лечения; 4) есть сомнения в соотношении польза/риск лечения для конкретного больного.
Наблюдение за больным с АГ
Для достижения целевых цифр АД при АГ требуются неоднократные визиты к врачу с целью своевременного изменения лечения (включая титрование доз препаратов). При наличии у больного (например, пожилого возраста) затруднений с передвижением могут требоваться визиты врача/медсестры к нему домой.
После достижения целевого АД частота визитов может быть значительно уменьшена; их кратность на этом этапе может составлять примерно 1 раз в 6 месяцев. Цели визита: 1) проверка приверженности к лечению; 2) оценка побочных эффектов, включая ортостатическую гипотензию; 3) проведение беседы с разъяснением полезности антигипертензивной терапии для здоровья и поощрением больного к продолжению лечения.
При длительном наблюдении за больным также необходимо проверять, насколько взяты под контроль такие модифицируемые факторы сердечно-сосудистого риска, как дислипидемия, диабет, курение и т.д.; следует повторно обсуждать с больным вопросы диеты и изменения образа жизни.
Ежегодно рекомендуется контролировать состояние функции почек и регистрировать электрокардиограмму с целью оценки состояния органов-мишеней при АГ. Больным, получающим комбинации ингибиторов АПФ или сартанов с антагонистами альдостерона, требуется 1 раз в 3–6 месяцев контролировать состояние функции почек и уровни электролитов крови.
Лечение АГ обычно постоянное и продолжается пожизненно.
Повышение приверженности пациентов к лечению при АГ
Информировать больного о риске, связанном с наличием АГ, и о благоприятном влиянии эффективного лечения на этот риск.
Инструкции по лечению АГ должны быть письменными и устными, максимально простыми, изложенными понятным для больного языком.
Лечебные рекомендации должны быть подобраны в соответствии с особенностями стиля жизни пациента.
Желательно упростить схему лечения путем максимального уменьшения количества применяемых лекарственных средств (для этого можно использовать комбинированные антигипертензивные препараты).
К обсуждению информации о заболевании и о планах по лечению может быть целесообразно привлечь родственников больного (и лиц, обеспечивающих уход за ним).
Во многих случаях полезно рекомендовать контроль АД на дому (в т.ч. самоконтроль).
При визитах обязательно контролировать побочные эффекты препаратов и соответственно изменять лечебные рекомендации.
Для облегчения выполнения лечебного режима препараты удобно раскладывать в разделенные по периодам приема пластмассовые контейнеры («утро — день — вечер» и др.); также применимы блистеры с календарной упаковкой (для препаратов однократного в сутки приема); в целях напоминания больному о времени приема препаратов можно использовать сигнал будильника (установленного в мобильном телефоне ежесуточно на определенное время).
Типичные проблемы, которые могут возникнуть при лечении пожилого больного с АГ
Ограничение поваренной соли в рационе у пожилых реализовать может быть сложнее, чем у более молодых пациентов, ввиду: 1) связанного с возрастом ослабления интенсивности вкусовых ощущений; 2) усложнения (из-за меньшей мобильности) приобретения свежих продуктов и приготовления пищи.
Рекомендации по ограничению калоража пищи и снижению массы тела часто оказываются неуспешными.
Наличие у больного сопутствующих заболеваний может препятствовать назначению некоторых лекарственных препаратов.
Значительно снижают приверженность к лечению когнитивные нарушения.
Необходимость применения многокомпонентного медикаментозного лечения увеличивает риск развития взаимодействий между лекарственными препаратами, возникновения побочных эффектов, снижения приверженности.
Имеется повышенный риск развития эпизодов гипотензии (в т.ч. гипотензии после еды — постпрандиальной, ортостатической гипотензии). Это увеличивает вероятность падений (и возможных переломов).