Статья опубликована на с. 106-109
На сегодняшний момент создание стабильных поливитаминных препаратов является одной из наиболее прогрессивных отраслей фармацевтической технологии. Поливитаминные лекарственные формы имеют огромное преимущество перед монокомпонентными витаминными препаратами, особенно при терапии неотложных и тяжелых состояний. Однако сегодня на фармацевтическом рынке по-прежнему лидируют витаминные монопрепараты, номенклатура которых во много раз превосходит номенклатуру поливитаминных лекарственных форм. Этот факт в первую очередь связан с тем, что из-за физико-химических свойств отдельных витаминов, включенных в пропись, очень сложно (а иногда и невозможно) добиться стабильности всех компонентов лекарственной формы. Особенно это касается жидких лекарственных форм (парентеральные, пероральные растворы), содержащих комплекс витаминов группы В. Как известно, большинство парентеральных поливитаминных препаратов содержат витамин В1 (тиамин), который при разложении (вследствие сдвига pH) способен инактивировать и дестабилизировать другие витамины, такие как цианокобаламин и др. Также витамины группы В крайне чувствительны к окислению кислородом воздуха, к солнечному свету и температуре. Эти факторы не только нивелируют биологическую активность витаминов, но и ускоряют деструктивное взаимодействие между ними.
Обычно проблема деградации витаминов в процессе производства и хранения решается добавлением в состав излишков витаминов. Однако это не является выходом, так как на определенном этапе хранения препарата количественное содержание действующих веществ может не совпадать с указанным в сертификате качества, а процесс производства становится более дорогостоящим. Поэтому стабилизация активных компонентов субстанции является необходимым комплексом мероприятий в отношении поливитаминных препаратов. Состав препарата Мильгамма® ампулы, р-р для в/м инъекций, является инновационным в плане фармацевтической технологии, так как позволил объединить в одной композиции и стабилизировать витамины В1, В6 и В12, которые в обычных условиях взаиморазрушаются. Кроме этого, в композицию удалось включить местноанестезирующий компонент, который позволил сделать препарат более удобным в применении.
1. Химико-фармацевтическая характеристика активных компонентов препарата Мильгамма
1.1. Витамин В1
/107-0.jpg)
Витамин В1 (рис. 1), или тиамин (4-метил-5-бета-оксиэтил-N-(2-метил-4-амино-5-метилпиримидил)-тиазолий), чаще всего синтезируется в форме солей гидрохлорида или гидробромида. Наряду с аминогруппой B1 содержит атом серы. В химической структуре присутствуют два кольца — пиримидиновое и тиазоловое, соединенных метиленовой связью. Температура плавления (с разложением) равна 233–234 °С. В препарате Мильгамма используется тиамина гидрохлорид с молекулярной массой 337,27. Субстанция хорошо растворяется в воде и уксусной кислоте, несколько хуже — в этиловом и метиловом спиртах и нерастворима в хлороформе, эфире, бензоле, ацетоне. Тиамина гидрохлорид может кристаллизоваться в водных растворах в виде бесцветных продолговатых кристаллов. В щелочной среде тиамин способен вступать в кислотно-восстановительные реакции, которые в зависимости от природы добавленного окислителя могут завершаться образованием тиаминдисульфида или тиохрома. Среди продуктов распада витамина в щелочной среде идентифицированы тиотиамин, сероводород, пиримидодиазепин и др. В кислой среде и при нагревании тиамин разлагается, образуя 5-гидрокси-метилпиримидин, муравьиную кислоту, 5-аминометилпиримидин, тиазоловый компонент витамина и 3-ацетил-3-меркапто-1-пропанол. Особое значение имеет эфир тиамина с фосфорной кислотой, который является активной формой витамина В1.
1.2. Витамин В6
Витамин В6 (рис. 2), или пиридоксин, распространен в виде трех оснований (пиридоксин, пиридоксаль и пиридоксамин), способных образовывать соли с сильными кислотами. В препарате Мильгамма витамин представлен в форме пиридоксина гидрохлорида (2-метил-3-окси-4,5-ди-(оксиметил)-пиридина гидрохлорид). По органолептическим свойствам представляет собой белый мелкокристаллический порошок без запаха, горьковато-кислого вкуса. В растворах субстанция способна образовывать бесцветные кристаллы в форме пластинок, температура плавления (с разложением) которых составляет 204–206 °С. Пиридоксина гидрохлорид хорошо растворим в воде, умеренно растворим в спирте и ацетоне, нерастворим в эфире и хлороформе. Все формы витамина В6 по сравнению с другими витаминами комплекса В отличаются высокой стабильностью в кислой и щелочной среде. Под влиянием света в водных растворах пиридоксин разрушается.
1.3. Витамин В12
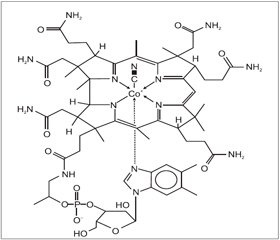
Цианокобаламин (α-(5,6-диметил-бензимидазолил)-кобамидцианид) — лекарственная форма витамина В12 (рис. 3), которая не встречается в природе и имеет молекулярную массу 1355,5. По органолептическим свойствам представляет собой кристаллический гигроскопичный порошок темно-красного цвета без запаха. При температуре от 200 до 320 °С разлагается (не плавясь). Умеренно растворяется в воде, низших спиртах, алифатических кислотах, феноле и диметилсульфоксиде. Цианокобаламин разрушается под действием окислителей, восстановителей и света. Его водные растворы устойчивы при pH 4,0–7,0. Группа CN легко замещается другими лигандами, такими как ОН, NО2, SО3, СН3. Образующиеся производные под действием цианид-иона вновь превращаются в цианокобаламин.
2. Технологические аспекты применения указанных вспомогательных веществ в препарате Мильгамма® ампулы. Стабилизация активных компонентов
Препарат Мильгамма® ампулы является сложным комплексом витаминов группы В и местного анестетика, который не может стабильно существовать в одной лекарственной форме без стабилизаторов и регуляторов кислотности. При этом в системе должны отсутствовать окислители, а ионные соединения не должны диссоциировать в растворе, так как эти факторы сразу приведут к сдвигу pH и к потере ионного равновесия в лекарственной форме.
2.1. Технологические аспекты выбора местного анестетика
В качестве компонента для местной анестезии в композиции, содержащей витамины В1, В6 и В12, можно использовать лидокаин, хлоропрокаин, артикаин, прокаин, бензокаин, тримекаин и др. Однако наиболее предпочтительным является основание лидокаина или его соль. Данный факт связан с тем, что, во-первых, лидокаин не является окислителем и не вступает в реакции с витаминами в препарате. А во-вторых, в данную лекарственную форму можно ввести от 10 до 50 мг/мл лидокаина без риска разрушения витаминов. К тому же немаловажным является тот факт, что в качестве стабилизатора лидокаина можно использовать калия гексацианоферрат (III), который является стабилизатором и цианокобаламина. При введении в лекарственную форму стабилизатора в концентрации от 0,005 до 1,0 % можно значительно повысить стабильность не только лидокаина, но и активных компонентов препарата. Эта манипуляция позволяет уменьшить количество вводимых в раствор вспомогательных веществ, что благоприятно отражается на стабильности и ионном балансе лекарственной формы.
2.2. Технологические аспекты выбора стабилизаторов и консервантов
Стабилизация цианокобаламина является основной технологической задачей в отношении лекарственной формы, которая содержит витамины В1, В6 и В12, ведь при дестабилизации цианокобаламина последний способен превращаться в оксикобаламин, а высвобожденные в среду реакции ионы кобальта способны вызывать деструкцию тиамина и пиридоксина. Для предотвращения этого процесса обычно используют цианид-ионы, добавляя в раствор цианид калия. Однако для парентеральной формы такое токсическое соединение неприемлемо. Роданид-ионы также способны стабилизировать цианокобаламин и защищать его от деструкции под влиянием солнечного света. Источником роданид-ионов может служить калия гексацианоферрат (III), который не только обеспечивает стабильность цианокобаламина и лидокаина, но и способен стабилизировать и другие витамины группы В (в несколько меньшей степени). При введении в лекарственную форму калия гексацианоферрата (III) в количестве 0,1 % возможно стабилизировать до 300 мг тиамина, до 300 мг пиридоксина и до 5000 мг цианокобаламина в одной лекарственной форме. Количественное содержание витаминов в препарате Мильгамма® ампулы соответствует устойчивой комбинации компонентов в технологическом аспекте.
Тиамин и пиридоксин имеют небольшой, однако похожий интервал кислотности — 2,7–3,6 и 2,5–3,5 соответственно. Поскольку в препарате они находятся в виде гидрохлоридов, то обеспечение постоянного pH и поддержание буфера являются основными технологическими приемами для сохранения структуры и биологической активности этих витаминов. Необходимую кислотность среды способны обеспечивать натрия гидроксид и натрия полифосфат. К тому же они способны защищать соли активных компонентов от диссоциации и обладают низкой токсичностью.
В качестве консерванта в препарате Мильгамма® ампулы был использован бензиловый спирт (40 мг/2 мл).
Этот компонент достаточно широко используется для производства инъекционных витаминов, ведь он обладает низкой токсичностью, противомикробной активностью и способен участвовать в создании депо препарата при внутримышечных инъекциях. Также он обладает слабовыраженными местноанестезирующими свойствами, а при комбинации с лидокаином способен потенцировать действие второго. Также следует отметить, что в качестве тары для инъекционного раствора использовано коричневое светозащитное гидролитическое стекло I типа, которое является не только химически инертным по отношению к компонентам данной химической системы, но и осуществляет дополнительную защиту от света чувствительных к ультрафиолету витаминов.
Выводы
Лекарственный препарат Мильгамма® ампулы содержит оптимальную комбинацию и необходимое количественное соотношение действующих и вспомогательных веществ, чтобы обеспечить фармакологическую активность каждого компонента. В данной лекарственной форме сочетаются все наиболее приемлемые токсикологические и технологические решения, направленные на поддержание раствора в стабильном состоянии и реализацию фармакодинамики препарата.
Список литературы
1. Allwood M.C., Keamey J.C. Compatibility and stability of additives in parenteral nutrition admixtures // J. Pediatric Child Health. — 2003. — 39(8). — 613-7.
2. Such A.D., Sanchez C.G., Gomis P.M., Herreros A.T. Estabilidad devitaminas en nutricion parenteral // Nutr. Hosp. — 2009. — 24(1). — 1-9.
3. US Pharmacopeia. United States Pharmacopeial Convention. — Rockville, 2008.
4. Monajjemzadeh F., Valizadeh H., Zakeri Milani P., Ebrahimi F. Stability assessment of vitamin B12 in mixed pa-renteral B complex formulations and in syringes prior to patient administration // Research in Pharmaceutical Sciences. — 2012. — 7(5).
5. Кравчун Н.А., Липсон В.В., Полторак В.В. Инновационные комплексные препараты витаминов группы В — фармакокинетические и фармакодинамические аспекты // Новая медицина тысячелетия. — 2009. — № 5.
6. Bahri Deepak, Sateesh Kumar Chauhan, Surender Kumar Kamal, Stabilization of vitamin b complex and lidocaine hydrochloride injection. — WO 2009066138 A2, 2009.
7. DATABASE WPI Derwent Publications Ltd., London, GB; AN 2004-326179 & RU 2 225 707 C1 (BRYNTSALOV A STOCK CO) 20 March 2004.
8. Dimitrov Hristov I. Medicine intended for treatment of multiple sclerosis. — WO 2002034199 A2, 2002.
9. Рабинович В.А., Хавин З.Я. Краткий химический справочник. — Л., 1991.

/107-0.jpg)
/107-1.jpg)
/107-2.jpg)