Статтю опубліковано на с. 165-169
Вступ
Пластична та енергетична перебудова головного мозку після черепно-мозкової травми (ЧМТ) відбувається шляхом поєднання двох різнонаправлених процесів: дегенеративно-деструктивного та репаративно-регенеративного. Клінічні прояви наслідків ЧМТ залежать від того, який із процесів превалює [1].
Згідно з аналізом, проведеним у роботі [2], понад третина з 50 кращих цитованих статей стосовно ЧМТ присвячені вивченню предикторів наслідків ЧМТ. Невпинна науково-дослідна робота в цьому напрямку дозволить виокремити пацієнтів, які піддаються найбільшому ризику поганого довгострокового результату, а отже, вимагають застосування конкретних стратегій діагностики та лікування. Звертається увага на той факт, що найчастіше дослідження були присвячені запобіганню розвитку когнітивного дефекту та стійкого неврологічного дефіциту, а не смертності. Зменшення уваги до встановлення предикторів прогнозування смертності після травматичного пошкодження головного мозку пояснюють як наслідками первинної профілактики, так і успіхами в лікуванні гострого періоду травми [3].
До найбільш високоцитованих належать і результати дослідження гістологічних наслідків травми. Травматична хвороба головного мозку закономірно супроводжується розвитком дегенеративно-дистрофічних процесів, проявом яких є післятравматична церебральна атрофія (ПЦА). Саме вона, на думку авторів [4, 5], є основною причиною, що веде до розвитку вентрикулодилатації, розширення субарахноїдальних просторів (САП), зниження щільності мозкової речовини, що виявляються при проведенні нейровізуалізаційних досліджень. Розширення лікворовмісних просторів після ЧМТ у більшості випадків виникає пасивно, будучи наслідком ПЦА, а не активно через порушення ліквородинаміки і ліквороциркуляції, що ведуть до посттравматичної гідроцефалії, як вважалося раніше. З впровадженням у клінічну практику сучасних неінвазивних методів нейровізуалізації (комп’ютерна томографія, магнітно-резонансна томографія) з’явилася можливість розмежування цих патологічних станів.
Мета роботи: дослідити роль ПЦА в структурі наслідків ЧМТ.
Матеріал та методи
Проведено аналіз морфометричних характеристик головного мозку у 130 хворих із наслідками ЧМТ. У 35 хворих в анамнезі — легка ЧМТ (ЛЧМТ), середній вік — 42,40 ± 1,40 року, та у 95 хворих — тяжка ЧМТ (ТЧМТ), середній вік — 41,09 ± 0,99 року. Серед обстежених переважали чоловіки: 80,55 % — у першій групі та 87,36 % — у другій групі. Середня тривалість періоду, що минув із часу перенесеної травми, становила: при ЛЧМТ — 8,46 ± 1,15 року, при ТЧМТ — 8,11 ± 0,54 року. Таким чином, за переліченими вище характеристиками досліджувані групи були репрезентативними. Оскільки під спостереженням знаходилися пацієнти з різним катамнезом травми, це дозволило нам розподілити їх на групи: І (термін травми 1–5 років), ІІ (6–10 років) та ІІІ (понад 10 років). Серед хворих із наслідками ЛЧМТ до І групи увійшли 14 пацієнтів (середній вік — 43,07 ± 2,45 року, середня тривалість посттравматичного періоду — 3,21 ± 0,29 року), до ІІ групи — 11 пацієнтів (середній вік — 40,63 ± 2,68 року, тривалість посттравматичного періоду — 7,18 ± 0,40 року), до ІІІ групи — 10 хворих (середній вік — 43,40 ± 2,11 року, тривалість посттравматичного періоду — 17,20 ± 2,26 року). У групі хворих із наслідками ТЧМТ розподіл був таким: І група — 33 хворі (середній вік 33,66 ± 1,84 року, середня тривалість посттравматичного періоду — 3,35 ± 0,18 року), ІІ група — 34 хворі (середній вік 41,53 ± 1,59 року, тривалість посттравматичного періоду — 7,29 ± 0,23 року), ІІІ група — 28 хворих (середній вік 44,61 ± 1,48 року, тривалість посттравматичного періоду — 14,71 ± 0,82 року). Клінічна характеристика наслідків ЧМТ включала оцінку провідних неврологічних синдромів, варіант перебігу посттравматичного періоду (стаціонарний, пароксизмальний), стан когнітивних функцій (за Монреальською шкалою когнітивного дефіциту — МоСА) та ступінь вираженості тривоги та депресії (за госпітальною шкалою тривоги та депресії (HADS)).
Комп’ютерну томографію головного мозку проводили на апараті Asteion Super 4 (Toshiba, Японія). Здійснювали якісну та кількісну оцінку отриманих аксіальних томограм, визначаючи такі морфометричні характеристики: ширину правого й лівого бічних шлуночків (мм), мінімальні розміри бічних шлуночків на рівні cella media, ширину третього шлуночка, розміри субарахноїдальних просторів на рівні полюса лобних часток, сильвієвої щілини та потиличної частки. Спираючись на отримані дані, обчислювали такі морфометричні індекси: фронтальних рогів, тіл бокових шлуночків (ІТБШ), бікаудатно-темпоральний (БКТІ), біфронтальний (БФІ), бікаудатний, число Хакмана (ЧХ), співвідношення Евана (СЕ) [5]. Також фіксували локалізацію та кількість посттравматичних лікворних кіст. Статистична обробка результатів виконана у відділі системних статистичних досліджень ДВНЗ «Тернопільський державний медичний університет імені І.Я. Горбачевського МОЗ України» за допомогою програмного пакета Statsoft Statistica.
Результати дослідження та обговорення
За результатами морфометрії, кількість хворих із наслідками ЛЧМТ, у яких середнє значення ширини САП виходило за межі норми, — 25,71 % (у групі з катамнезом травми 1–5 років — 21,4 %, 6–10 років — 18,2 %, понад 10 років — 40 %). За умови ТЧМТ в анамнезі — 48,42 %, причому у групі з катамнезом 1–5 років таких хворих було 36,36 %, 6–10 років — 52,94 %, понад 10 років — 50 %. Таким чином, в обох групах ми спостерігали зростання відсотка пацієнтів із поширеними САП зі збільшенням тривалості післятравматичного періоду.
У групі з наслідками ЛЧМТ кореляційний зв’язок між показниками вік/ширина САП був значним (r = +0,58), у групі з наслідками ТЧМТ — помірним (r = +0,41). Причому значення показника кореляції коливалося в групах із різною тривалістю посттравматичного періоду: від r = +0,39 у І групі до r = +0,53 у ІІІ групі. Таким чином, вплив вікового фактора на розвиток кортико-атрофічного процесу у хворих із наслідками ТЧМТ був слабшим (за винятком групи з катамнезом травми понад 10 років), ніж за умови перенесеної ЛЧМТ.
У 3 хворих (8,57 %) у віддаленому періоді ЛЧМТ встановлено збільшення розмірів ІІІ шлуночка, показники якого в рівної кількості пацієнтів (2,85 %) відповідали легкому, середньому та тяжкому ступеню внутрішньої церебральної атрофії.
У групі хворих у віддаленому періоді ТЧМТ кількість хворих із поширеним ІІІ шлуночком становила 31,57 %. Причому показники відповідали легкому ступеню церебральної атрофії у 10,5 % пацієнтів, середньому ступеню — у 5,26 %, тяжкому — у 15,79 %. Згідно з даними [5], розширення САП є одним із маркерів зовнішньої, а ІІІ шлуночка — внутрішньої церебральної атрофії. За умови поєднання цих ознак діагностують змішану церебральну атрофію. Зважаючи на вищесказане, ознаки переважно внутрішньої церебральної атрофії встановлено в 1 хворого (2,85 %), переважно зовнішньої — у 7 (20 %), змішаної — у 2 хворих (5,71 %) з наслідками ЛЧМТ.
У групі хворих із наслідками ТЧМТ отримали такі дані: переважно внутрішня церебральна атрофія — в 11 (11,57 %), переважно зовнішня — у 20 (21,05 %), змішана — у 24 (25,26 %). Таким чином, у відсотковому співвідношенні кількість хворих із морфометричними ознаками ПЦА за умови перенесеної ТМЧТ була вдвічі більшою. Серед пацієнтів обох груп, незважаючи на різні відсоткові значення, прослідковували певну закономірність — переважання хворих із зовнішньою церебральною атрофією. Детальний аналіз окремих випадків серед указаної категорії хворих показав, що розширення САП мало нерівномірний характер, у переважної більшості це був фокальний тип церебральної атрофії. Аналогічною була ситуація і в групі з наслідками ТЧМТ: у 38 хворих (40 %) — фокальний тип зовнішньої церебральної атрофії, з них у 36 хворих (37,89 %) — за рахунок поєднаного розширення САП у лобно-скроневих ділянках.
У 48 хворих (50,5 %) із наслідками ТЧМТ виявили лікворні кісти, які в переважній більшості (77 %) локалізувалися в межах однієї півкулі. У 14,5 % хворих кісти виявляли в лобній, у 25 % — у скроневій, по 16,7 % — поєднання «лоб — скроня» та обидві лобні частки. Кількість хворих із лікворними кістами в межах потиличної, обох скроневих або обох тім’яних часток коливалася від 2,1 до 4,2 %.
Середній вік пацієнтів із наслідками ТЧМТ та морфометричними ознаками зовнішньої ПЦА — 41,34 ± 1,88 року, тривалість посттравматичного періоду — 7,33 ± 0,77 року, внутрішньої ПЦА — 39,00 ± 4,14 року, з катамнезом травми 6,12 ± 1,36 року, змішаної ПЦА — 45,61 ± 2,21 року та 9,05 ± 1,24 року відповідно, р > 0,05.
Ми вирішили проаналізувати особливості гострого періоду (характер травми, оперативне втручання) у кожній із груп хворих із ТЧМТ. Відкриту ЧМТ діагностували у 43,5 % хворих із змішаною ПЦА, у 26,9 % — із зовнішньою, у 25 % — із внутрішньою та у 26,5 % — без ознак ПЦА. Поєднання удару головного мозку з суб- та епідуральними гематомами було в 42,5 % пацієнтів із зовнішньою, у 39,1 % — із змішаною ПЦА, у 12,5 % — із внутрішньою ПЦА та у 23,7 % — без ознак ПЦА. Відповідно, оперативне втручання було в анамнезі у 79 % пацієнтів із діагностованими гематомами.
Таким чином, у пацієнтів із морфометричними ознаками змішаної ПЦА в анамнезі частіше була відкрита ЧМТ, а в пацієнтів із зовнішньою ПЦА — поєднання удару головного мозку з суб- та епідуральними гематомами.
Кількість хворих із пароксизмальним варіантом перебігу захворювання становила 75 % (за умови наявності внутрішньої), 60,86 % (за умови змішаної), 53,84 % — за умови зовнішньої ПЦА та 52,63 % — без морфометричних ознак атрофічного процесу.
Розподіл хворих за типом ПЦА у групах із різним катамнезом ТЧМТ наведений у табл. 1.
Аналіз табл. 1 продемонстрував, що у відсотковому співвідношенні найбільше хворих із наслідками ТЧМТ та морфометричними ознаками ПЦА було у ІІ групі (термін травми — 6–10 років). Якщо пацієнти з різними типами ПЦА у першій групі розподілилися майже рівномірно, то серед хворих із катамнезом травми 6–10 років переважали особи з ознаками зовнішньої, а серед ІІІ групи (понад 10 років) — змішаної ПЦА.
З метою встановлення можливих клініко-морфологічних співвідношень проведено аналіз поширеності основних клінічних синдромів у хворих із різним типом ПЦА. Пацієнти сформували такі групи: І — вогнищевий синдром, ІІ — вогнищевий та лікворно-гіпертензійний синдром, ІІІ — вогнищевий та судомний, ІV — вогнищевий та психоорганічний, V — вогнищевий та вегетосудинна дистонія (ВСД), VІ — поєднання трьох та більше синдромів.
У групі хворих із морфометричними ознаками змішаної ПЦА домінуючими були прояви вогнищевого синдрому та поєднання вогнищевого й судомного синдрому. Три четвертих групи хворих із морфометричними проявами внутрішньої ПЦА клінічно були представлені вогнищевим, поєднанням вогнищевого та синдрому ВСД, а також комбінацією синдромів. Серед пацієнтів з ознаками зовнішньої ПЦА найбільше було з проявами вогнищевого та вогнищевого й лікворно-гіпертензійного синдромів.
Таким чином, найбільший відсоток хворих із вогнищевим синдромом, а також поєднання вогнищевого та судомного синдромів був у групі зі змішаною ПЦА. Найбільше хворих із комбінацією клінічних синдромів та проявами синдрому ВСД було в групі із внутрішньою ПЦА. Лікворно-гіпертензійний та психоорганічний синдроми в поєднанні з вогнищевим — у пацієнтів із зовнішньою ПЦА.
Чи можна дані, отримані під час дослідження, вважати за певну клінічну характеристику окремих видів ПЦА? За даними ранніх робіт такого плану [1], не встановлено чіткого паралелізму між клінічними проявами й морфологічними змінами головного мозку. Більш пізні роботи [4, 6, 7] вказують на наявність тенденцій в особливостях клінічних проявів та перебігу травматичної хвороби головного мозку за умови розвитку ПЦА. Так, при поширеності проявів вегетативної дисфункції у пацієнтів із морфометричними ознаками внутрішньої ПЦА та психоорганічного синдрому серед пацієнтів з ознаками змішаної ПЦА наші дані та результати літератури [4, 7] збігаються.
Подальше дослідження клінічних особливостей стосувалося аналізу результатів нейропсихологічного тестування. У групі хворих із морфометричними ознаками внутрішньої ПЦА зафіксовано такі результати: шкала МоСА — 24,25 ± 0,53 бала, рівень тривоги (НADS) — 9,62 ± 1,15 бала, рівень депресії — 8,62 ± 1,39 бала. Групи хворих з ознаками зовнішньої та змішаної церебральної атрофії продемонстрували нижчі значення МоСА-тесту — 21,35 ± 0,55 бала та 21,04 ± 0,80 бала відповідно (р > 0,05). Рівень тривоги у даних групах був 8,85 ± 0,50 бала та 9,83 ± 0,52 бала, рівень депресії — 7,57 ± 0,39 бала та 8,17 ± 0,56 бала відповідно. Середнє значення МоСА-тесту у пацієнтів без морфометричних ознак ПЦА — 22,10 ± 0,55 бала; HADS: тривога — 9,45 ± 0,47 бала, депресія — 7,87 ± 0,52 бала.
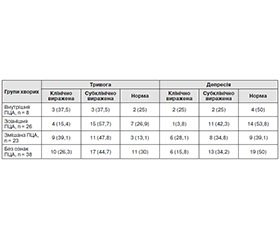
Розподіл пацієнтів за результатами HADS наведений у табл. 3.
Згідно з даними, наведеними в табл. 3, найвищий відсоток пацієнтів із клінічно вираженими тривогою та депресією був у групах з ознаками змішаної та внутрішньої ПЦА, субклінічно виражені тривога та депресія — у групах із зовнішньою ПЦА.
Встановлено кореляційні зв’язки між рівнем тривоги та окремими морфометричними показниками: ІТБШ (r = 0,57) — у групі зі змішаною ПЦА; розміром правого бокового шлуночка (r = 0,61), СЕ (r = 0,42), ІТБШ (r = 0,35), БФІ (r = 0,54) у групі із внутрішньою ПЦА. Залежність між рівнем депресії та БКТІ (r = 0,24), розміром третього шлуночка (r = 0,24) — у групі зі змішаною ПЦА та СЕ (r = 0,44), ЧХ (r = 0,53), БФІ (r = 0,62) — у групі з внутрішньою ПЦА. У групі хворих із морфометричними ознаками зовнішньої ПЦА встановлено лише слабкий кореляційний зв’язок між рівнем тривоги і БФІ (r = –0,31) та СЕ (r = –0,21), між рівнем депресії та СЕ (r = –0,2). Таким чином, найбільше кореляційних зв’язків зафіксовано у групі з морфометричними ознаками внутрішньої ПЦА.
Висновки
1. У 28,57 % хворих із наслідками ЛЧМТ та 57,89 % із наслідками ТЧМТ діагностовано морфометричні ознаки ПЦА, в обох групах переважали пацієнти з зовнішньою ПЦА. Серед хворих із катамнезом ТЧМТ протягом 6–10 років переважали особи з ознаками зовнішньої, з катамнезом 10 і більше років — змішаної ПЦА.
2. У хворих із відкритою ЧМТ в анамнезі частіше діагностували морфометричні ознаки змішаної ПЦА, а при поєднанні удару головного мозку з суб- та епідуральними гематомами — зовнішньої ПЦА.
3. У хворих зі змішаною ПЦА провідними були вогнищевий, а також поєднання вогнищевого та судомного синдромів, комбінація трьох і більше клінічних синдромів та прояви синдрому ВСД — у групі із внутрішньою ПЦА, лікворно-гіпертензійний та психоорганічний синдроми в поєднанні з вогнищевим — у пацієнтів із зовнішньою ПЦА.
4. Найвищий відсоток пацієнтів із клінічно вираженими тривогою та депресією був у групах з ознаками змішаної та внутрішньої ПЦА, субклінічно виражених тривоги та депресії — у групах із зовнішньою ПЦА.

/167.jpg)
/168.jpg)