Статтю опубліковано на с. 45-50
Цереброваскулярна патологія в більшості випадків супроводжується розвитком тяжкого порушення когнітивних функцій, що може бути провідною причиною інвалідизації хворого [7]. Проблема когнітивних розладів (КР) останніми роками набуває все більш актуального соціального значення і стає однією з основних проблем століття — хворобою століття або навіть епідемією століття [3, 4, 12]. Саме з розвитком когнітивного дефіциту пов’язують величезні соціально-економічні втрати, яких зазнає суспільство. Несвоєчасна діагностика початкових стадій КР і, відповідно, відсутність адекватної терапії призводять до їх подальшого прогресування. Виявлення КР повинно проводитися за допомогою простих методик вже на амбулаторному етапі лікарями загальної практики та неврологами. Особлива увага щодо цього має приділятися хворим, які належать до груп високого ризику розвитку КР [2].
Вивчення епідеміології судинних захворювань мозку дозволило встановити високу кореляцію між поширеністю судинних уражень мозку й серця. Кардіальна патологія є однією з найважливіших причин розвитку хронічної цереброваскулярної недостатності.
Вивченню взаємозв’язку церебральної та кардіальної патології присвячена велика кількість досліджень (Шмідт Е.В., 1963, 1975; Боголєпов Н.К., 1971; Акімов Г.А., 1971; Шхвацабая І.К., 1975; Гусєв Е.І., 1979, 2009; Чазов Е.І., 1980; Маджидов Н.М., Трошин В.Д., 1985). На I Національному конгресі «Кардіоневрологія» (Москва, 2008) був запропонований термін «кардіогенна енцефалопатія», що підкреслює актуальність вивчення церебральних розладів у хворих із хронічними формами серцевої патології.
Вивчення впливу порушень серцевого ритму та провідності на когнітивну функцію має особливе значення в кардіоневрології, оскільки саме ці розлади відіграють суттєву роль у розвитку когнітивного дефіциту. Особлива увага в літературі приділяється ролі фібриляції передсердь (ФП), яку діагностують в 1 % дорослого населення [9]. Понад 6 мільйонів європейців страждають від цієї аритмії. Поширеність ФП, за попередніми оцінками, зросте у 2 рази упродовж наступних 50 років. За своєю медико-соціальною значимістю ФП суттєво випереджає інші види кардіальних аритмій, що пов’язано не лише з її поширеністю, але й з тяжкістю обумовлених нею органних ускладнень, асоційованих зі значними моральними та матеріальними витратами. Розвиток хронічної серцевої недостатності, збільшення ризику раптової серцевої смерті, емболічні церебральні ускладнення, погіршення перебігу постінсультного періоду, стійка інвалідизація, низька виживаність — усе це є наслідком втрати синусового ритму [6]. ФП дає п’ятиразове збільшення ризику інсульту, і один з кожних п’яти інсультів пов’язаний з цією аритмією. Ішемічні інсульти при ФП часто закінчуються смертю, а пацієнти, що вижили, мають вищий відсоток інвалідизації та частіше страждають від рецидивів, ніж пацієнти з іншими причинами інсульту. Разом з тим сама специфіка хвороби (клінічні прояви, наслідки, характер лікування) визначає її істотний вплив на актуальну життєву ситуацію, інтелект та систему особистісних стосунків хворого [1]. ФП вважається чинником, асоційованим із КР, що розвиваються у результаті перенесеного інсульту, а також не пов’язаними з гострими порушеннями мозкового кровообігу [8, 10, 11].
У більшості хворих, як правило, відзначається поєднання декількох факторів ризику, окремий внесок кожного з яких досить складно оцінити. Клінічні прояви дисциркуляторної енцефалопатії (ДЕ) у хворих із ФП досить різноманітні, що обумовлено як патогенетичними особливостями судинного процесу, так і переважним ураженням тих чи інших структур головного мозку. Певне значення має й велика чутливість головного мозку до ішемії в силу інволюційних змін. Крім того, діагностика цереброваскулярної недостатності ускладнюється внаслідок частого поєднання власне судинних змін з патологічними змінами первинно-дегенеративного характеру. Це пояснює актуальність клінічного дослідження пацієнтів із КР на фоні ФП.
Мета дослідження — вивчення прогностичних критеріїв розвитку та прогресування КР у пацієнтів з дисциркуляторною енцефалопатією на фоні ФП.
Матеріал і методи дослідження
Дослідження, що проводили в період з 2013 по 2016 рік, було засноване на комплексному клініко-інструментальному обстеженні 126 пацієнтів із персистуючою (пароксизмальною) формою ФП, які спостерігалися в кардіологічній клініці Військово-медичного клінічного центру Західного регіону (м. Львів).
Критеріями включення в дослідження були наявність у хворого клінічних та електрокардіографічних ознак персистуючої або пароксизмальної форм ФП. Уніфікована лікарська терапія протягом 6 місяців спостереження не включала прийом ноотропних і психотропних препаратів. Включені в дослідження пацієнти не мали в анамнезі психічних захворювань, депресивного розладу, інсульту менше ніж за 6 місяців до початку включення в дослідження, зловживання алкоголем.
Усім хворим проводили неврологічне та нейропсихологічне обстеження з якісною й кількісною оцінкою отриманих результатів. Для виявлення найбільш значущих факторів, що визначають прогноз когнітивного зниження у хворих з ФП, через 1 рік після включення в дослідження було проведено нейропсихологічне обстеження в динаміці.
Застосовували міні-тест оцінки когнітивних функцій (MMSE) (Folstein M.F. et al., 1975), адаптований А.Н. Бєловою (2000); госпітальну шкалу тривоги та депресії (Zigmond A.S., Snaith R.P., 1983); тест запам’ятовування 5 слів (Dubois B., 2002) з оцінкою вільного й відстроченого відтворення та впізнавання; тест на зорову пам’ять; тест малювання годинника; тест на мовну активність (семантично й фонетично опосередковані асоціації).
Усім хворим проводили ультразвукову допплерографію (УЗДГ), ехокардіографію (ЕхоКГ), комп’ютерну томографію (КТ) головного мозку. При УЗДГ оцінювали стан великих екстракраніальних артерій — загальні, зовнішні та внутрішні сонні. При проведенні ЕхоКГ оцінювали показники кінцевого діастолічного розміру (КДР), кінцевого систолічного розміру лівого шлуночка, фракцію викиду (ФВ) лівого шлуночка, розміри задньої стінки лівого шлуночка (ЗСЛШ), міжшлуночкової перегородки (МШП), відзначали збільшення розмірів камер серця, патологію клапанного апарату. Проводили якісний аналіз даних КТ з оцінкою ступеня вираженості внутрішньої й зовнішньої гідроцефалії, перивентрикулярного й субкортикального лейкоареозу, лакунарних інфарктів, зазначали наявність кірковою атрофії.
Статистичний аналіз отриманих показників проводили з використанням програми Microsoft Excel для Windows ХР, IBM SPSS Statistics, version 19, 2010, і Epistat 5.01 b. 1991.
Результати дослідження та їх обговорення
У дослідження були включені 126 пацієнтів віком від 40 до 65 років (середній вік 60,8 ± 6,2 року) з персистуючою або пароксизмальною формами ФП. Було обстежено 89 (70,6 %) чоловіків та 37 (29,4 %) жінок. ДЕ I стадії діагностована в 45 (35,7 %) пацієнтів, ДЕ II — у 81 (64,3 %). У клінічній картині пацієнтів найбільш часто мали місце цефалгічний, вестибулоатактичний, пірамідний синдроми, синдром КР.
Основними захворюваннями, що призвели до розвитку ФП, були: ішемічна хвороба серця (ІХС) — 76 (60,3 %) пацієнтів, міокардитичний кардіосклероз — 32 (25,4 %) пацієнти, ревматизм — 18 (14,3 %) пацієнтів.
Найбільш значущими факторами ризику ДЕ при ФП були: артеріальна гіпертензія (АГ) (69,0 % хворих), атеросклероз (71,4 %), гіперхолестеринемія (61,1 %), надлишкова маса тіла (57,9 %), обтяжена судинна спадковість (48,4 %). Дещо рідше зустрічалися серцева недостатність (42,1 %), паління (38,9 %), цукровий діабет (20,6 %), інфаркт міокарда в анамнезі (19,0 %), вади серця (17,5 %). Простежено вірогідний взаємозв’язок наявності АГ (r = 0,32; p < 0,005) і вад серця (r = 0,44, p < 0,005; χ2 = 17,48, p < 0,005) з віком.
У хворих з ФП середній бал за шкалою MMSE становив 27,4 ± 1,2. Помірні когнітивні розлади (ПКР) були діагностовані у 46 (36,5 %), легкі (ЛКР) — у 58 (46,0 %), відсутність КР — у 22 (17,5 %).
Визначений прямий вірогідний кореляційний зв’язок між ступенем вираженості когнітивного дефіциту та ФП (r = 0,26; p < 0,05). Встановлено, що ризик розвитку КР при ФП вірогідно вищий (OR = 4,38, 95 % CI = 1,11–17,36; χ2 = 4,28, p < 0,05). У групі хворих з вищою освітою кількість ПКР була нижчою, ніж у групі хворих із середньою освітою (16,4 і 22,3 % відповідно), проте різниця не була вірогідною.
Серед хворих із ПКР АГ зустрічалася частіше (84,8 %), ніж серед хворих із ЛКР (69,0 %) (табл. 1).
Відсоток хворих з когнітивним дефіцитом серед осіб з АГ був вищим, ніж у групі хворих без АГ (54,2 і 36,8 % відповідно). У хворих із ПКР рівень діастолічного АТ був вірогідно вищим, ніж у групі пацієнтів із ЛКР (98,25 ± 5,25 мм рт.ст. і 82,60 ± 4,34 мм рт.ст. відповідно, р < 0,05). Виявлено залежність ступеня КР від рівня діастолічного АТ (r = 0,26; р < 0,05). ПКР у групі хворих з атеросклерозом судин головного мозку зустрічалися частіше (44,4 %), ніж у групі хворих без атеросклерозу (32,5 %). Отриманий вірогідний кореляційний зв’язок між атеросклерозом судин головного мозку і КР (r = 0,26; р < 0,05). Отримана кореляційна залежність між наявністю вад серця та розвитком ПКР (r = 0,44; p < 0,005). Виявлено вірогідно більш часте виникнення ПКР у пацієнтів із вадами серця (χ2 = 17,62; p < 0,05).
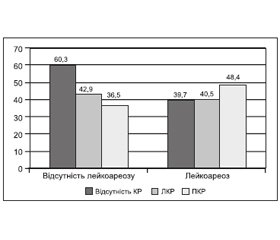
У групі пацієнтів з лейкоареозом за даними КТ хворих із ПКР було більше, ніж у групі без лейкоареозу (48,4 та 36,5 % відповідно) (рис. 1).
Було простежено кореляцію між наявністю феномена лейкоареозу й ступенем КР (r = 0,32; p < 0,05). Ризик ПКР і ЛКР вірогідно збільшувався у хворих з лейкоареозом (χ2 = 4,96; p < 0,05).
Показник ФВ у групі хворих із ПКР був нижчим (50,2 ± 2,8 %) порівняно з групою хворих із ЛКР (55,8 ± 4,2 %) (p < 0,05). Товщина МШП в групі хворих з КР була збільшеною. Збільшення розміру ЗСЛШ відзначалося серед хворих із ПКР і ЛКР, серед хворих без КР збільшення цього розміру не відзначено. Середня величина ЗСЛШ була вірогідно меншою у хворих із ЛКР (9,68 ± 2,52 мм), ніж у хворих із ПКР (11,58 ± 2,62 мм) (p < 0,05). Виявлена кореляційна залежність розмірів ЗСЛШ від рівня КР (r = 0,24; р < 0,05). Загальний бал за шкалою MMSE корелював з такими показниками, як розміри МШП (r = 0,26; р < 0,05) і розміри ЗСЛШ (r = 0,48; р < 0,005).
Показники величини комплексу інтима-медіа (КІМ) загальних сонних артерій справа й зліва у хворих із ПКР були більшими, ніж у хворих із ЛКР (р < 0,05) (табл. 2).
Виявлена кореляційна залежність між величиною КІМ зліва (r = 0,24; р < 0,05) і справа (r = 0,22; р < 0,05) та ступенем КР. У хворих з ПКР ступінь стенозу правої сонної артерії був вірогідно більшим порівняно з хворими з ЛКР (р < 0,05) (табл. 3). Виявлено кореляційний зв’язок між вираженістю стенозу сонних артерій зліва і ризиком розвитку ПКР (r = 0,26; р < 0,05).
Результати тесту безпосереднього запам’ятовування 5 слів корелювали з віком (r = 0,26; р < 0,05), розмірами ЗСЛШ (r = 0,26; р < 0,05), рівнем стенозу сонних артерій зліва (r = 0,26; р < 0,05), результатами тесту MMSE (r = 0,26; р < 0,05).
Виявлено вірогідні кореляції результатів тесту відстроченого відтворення і запам’ятовування 5 слів із віком хворого (r = 0,34; р < 0,005), частотою серцевих скорочень (ЧСС) (r = –0,36; р < 0,005). Менш виражені кореляції отримані із наявністю лейкоареозу на КТ (r = 0,24; р < 0,05), збільшенням розмірів правого шлуночка (r = 0,26; р < 0,05), величиною КІМ зліва (r = 0,26; р < 0,05).
Отримана кореляційна залежність між результатами тесту безпосереднього зорового запам’ятовування й відтворення і розмірами ЗСЛШ (r = 0,34; р < 0,005), показниками шкали MMSE (r = 0,46; р < 0,005). Менш виражені були кореляції з наявністю атеросклерозу судин головного мозку (r = 0,28; р < 0,05).
Результати тесту на зорове відстрочене запам’ятовування й відтворення були кореляційно залежні від розмірів ЗСЛШ (r = 0,36; р < 0,005). Менш значимі кореляції були отримані з віком хворого (r = 0,26; р < 0,05), результатами тесту малювання годинника (r = 0,24; р < 0,05). Отримана кореляція між результатами тесту малювання годинника і віком хворого (r = 0,38; р < 0,005), розмірами ЗСЛШ (r = 0,34; р < 0,005). Результати тесту на семантичну мовну активність корелювали зі збільшенням лівого передсердя (r = 0,22; р < 0,05). Отримані виражені кореляції результатів тесту на фонетичну мовну активність з рівнем освіти (r = 0,36; р < 0,05), ЧСС (r = 0,32; р < 0,05) та рівнем діастолічного АТ (r = 0,28; р < 0,05).
При розгляді структури когнітивного дефіциту хворі були розділені на 2 групи. До І групи (90 хворих) були віднесені пацієнти з дизрегуляторними розладами, пов’язаними з дисфункцією лобних часток, що проявлялися порушенням самостійного малювання годинника при збереженому копіюванні, а також зниженням кількості фонетично опосередкованих асоціацій при відносній збереженості семантичної мовної активності. До ІІ групи (14 хворих) були віднесені пацієнти з первинним розладом зорово-просторових функцій, пов’язаним з ураженням тім’яних часток, про що свідчить порушення спонтанного малювання й копіювання, а також зниження числа фонетично й семантично опосередкованих асоціацій.
Середнє значення КДР у групі пацієнтів з дисфункцією лобних часток було вірогідно вище (62,8 ± 2,2 мм), ніж в групі пацієнтів із первинними зорово-просторовими порушеннями (57,6 ± 1,4 мм) (p < 0,05). Середнє значення величини ЗСЛШ у групі пацієнтів з дизрегуляторними порушеннями також було вірогідно більше (11,8 ± 1,2 мм), ніж в групі пацієнтів з первинними зорово-просторовими порушеннями (10,2 ± 1,0 мм) (p < 0,05). Це підтверджує судинний характер розвитку дизрегуляторних змін.
Динаміка КР визначалася за результатами шкали MMSE через 1 рік від початку дослідження. Поліпшення або відсутність динаміки когнітивного статусу виявлено в 74 (71,2 %) пацієнтів, погіршення — у 30 (28,8 %). У віковій групі 40–49 років погіршення когнітивних функцій виявлено у 20,0 % хворих, 50–59 років — у 33,3 %, 60–65 років — у 46,7 %. Динаміка КР вірогідно залежала від віку (χ2 = 12,68; p < 0,005).
У групі хворих з погіршенням когнітивних функцій середня частота серцевих скорочень становиала 98,6 ± 4,4/хв, що було вірогідно вище (p < 0,05), ніж в групі хворих без динаміки або з поліпшенням когнітивних функцій (82,4 ± 4,2/хв). Виявлений взаємозв’язок погіршення когнітивних функцій і ЧСС (r = 0,36; p < 0,05). У пацієнтів з інфарктом міокарда в анамнезі, обтяженою судинною спадковістю, серцевими вадами відзначено більш часте погіршення когнітивних функцій.
Погіршення когнітивних функцій відмічено в 11 (36,7 %) хворих з атрофічними змінами на КТ порівняно з 4 (13,3 %) хворими без атрофічних змін. Відсутність динаміки або поліпшення виявлено в 19 (63,3 %) пацієнтів з атрофічними змінами та 15 (86,7 %) пацієнтів без атрофічних змін (рис. 2). У пацієнтів з атрофічними змінами вірогідно частіше розвивалося погіршення когнітивних функцій (χ2 = 4,12; p < 0,08). У групі з лейкоареозом погіршення когнітивних функцій виявлено у 40,0 % пацієнтів, у групі без лейкоареозу — у 10,0 % (рис. 2). Виявлено вірогідно більш часте прогресування погіршення когнітивних функцій у хворих з наявністю лейкоареозу (χ2 = 4,2; p < 0,05, OR = 3,52; 95% СІ = 0,84–14,61).
Величина КДР лівого шлуночка (63,24 ± 3,56 мм) та КІМ сонних артерій зліва (1,22 ± 0,28 мм) і справа (1,18 ± 0,20 мм) у пацієнтів з погіршенням когнітивних функцій була більшою, ніж у групі хворих без динаміки або з поліпшенням когнітивних функцій (61,15 ± 2,65 мм, p < 0,05) та (1,12 ± 0,16 мм і 1,10 ± 0,14 мм відповідно, p < 0,05) (табл. 4). Збільшення товщини КІМ вважається прогностично несприятливою ознакою прогресування ДЕ при ФП.
Отже, КР є частим і серйозним проявом цереброваскулярної патології при персистуючій та пароксизмальній формах ФП, що значною мірою погіршує прогноз і перебіг основного захворювання та вимагає проведення спеціальної терапії.
Висновки
1. У пацієнтів з персистуючою та пароксизмальною формами фібриляції передсердь ПКР було виявлено в 36,5 % випадків, ЛКР — у 46,0 %. Детальний аналіз структури когнітивного дефіциту дозволив діагностувати дизрегуляторні порушення у 86,5 % хворих з КР, первинне порушення зорово-просторових функцій — у 13,5 % хворих.
2. КР залежали від віку хворого, частоти серцевих скорочень, рівня діастолічного АТ, наявності атеросклерозу судин головного мозку, лейкоареозу за даними КТ, величини КІМ загальних сонних артерій. Основним кардіальним фактором, що визначав вираженість порушень когнітивних функцій, було зниження фракції викиду лівого шлуночка.
3. Прогресування когнітивного дефіциту протягом 1 року відмічено у 28,8 % хворих з ФП з підвищенням діастолічного АТ, лейкоареозом та атрофічними змінами головного мозку на КТ, збільшенням КДР лівого шлуночка і збільшенням розмірів КІМ загальних сонних артерій.
4. Для поліпшення прогнозу перебігу дисциркуляторної енцефалопатії на фоні ФП необхідно максимально раннє виявлення та лікування КР. Обстеження хворих з ФП повинно включати нейропсихологічне дослідження, УЗДГ магістральних артерій голови, ехокардіографію, комп’ютерну томографію головного мозку.
/47.jpg)

/47_2.jpg)
/48.jpg)
/49.jpg)