Резюме
Метою цієї роботи була валідація україномовної версії шкали Patient Determined Disease Steps (PDDS) у пацієнтів із розсіяним склерозом для застосування в щоденній практиці невролога та оцінка її зв’язку зі шкалою Expanded Disability Status Scale (EDSS). Валідаційний процес включав переклад, оцінку валідності, надійності та чутливості. Найвищі показники кореляції PDDS виявлені з пірамідною (r = 0,71, p < 0,0001), церебелярною (r = 0,51, p < 0,0001) функціональними шкалами, шкалою ходи (r = 0,8, p < 0,0001) та загальним балом за шкалою EDSS (r = 0,8, p < 0,0001). Недостатньо сильні кореляційні зв’язки виявлено із зоровою, сенсорною та тазовою функціональними шкалами. Українська версія шкали PDDS, що пропонується, є валідним, надійним та чутливим інструментом в оцінці неспроможності хворих з розсіяним склерозом, може бути використана для популяційних та наукових досліджень.
Целью данной работы была валидация украиноязычной версии шкалы Patient Determined Disease Steps (PDDS) у пациентов с рассеянным склерозом для применения в рутинной практике и оценка ее связи со шкалой Expanded Disability Status Scale (EDSS). Валидационный процесс включал перевод, оценку валидности, надежности и чувствительности. Самые высокие показатели корреляции PDDS обнаружены с пирамидной (r = 0,71, p < 0,0001), церебеллярной (r = 0,51, p < 0,0001) функциональными шкалами, шкалой походки (r = 0,8, p < 0, 0001) и общим баллом по шкале EDSS (r = 0,8, p < 0,0001). Недостаточно сильные корреляционные связи выявлены со зрительной, сенсорной и тазовой функциональными шкалами. Предлагаемая украинская версия шкалы PDDS является валидным, надежным и чувствительным инструментом в оценке несостоятельности больных с рассеянным склерозом и может быть использована для популяционных и научных исследований.
The aim of this study was to validate the Ukrainian version of the Patient Determined Disease Steps (PDDS) scale in patients with multiple sclerosis for usage in routine practice of neurologist and to evaluate its correlation with Expanded Disability Status Scale (EDSS). Validation process included translation, assessment of the validity, reliability and sensitivity. The highest parameters of PDDS correlation were found with pyramidal (r = 0.71, p < 0.0001), cerebellar (r = 0.51, p < 0.0001) functional scales, ambulation (r = 0.8, p < 0.0001) and the total EDSS score (r = 0.8, p < 0.0001). Correlations with visual, sensory and bowel and bladder scales were not strong enough. The proposed Ukrainian version of PDDS scale is a valid, reliable and sensitive instrument for assessing disability in patients with MS, it can be used for epidemiological and research studies.
Статтю опубліковано на с. 167-172
Вступ
Розсіяний склероз (РС) — найбільш поширене хронічне прогресуюче демієлінізуюче захворювання центральної нервової системи, що проявляється розсіяною неврологічною симптоматикою із залученням декількох функціональних систем, уражає осіб молодого працездатного віку та характеризується в більшості випадків ремітуючим на ранніх стадіях перебігом [1–4].
Ступінь неспроможності в пацієнтів із РС традиційно впродовж останніх 30 років оцінюється за шкалою EDSS (Expanded Disability Status Scale) [5, 6]. Динаміка за шкалою EDSS часто є первинною та кінцевою точкою клінічних досліджень. Ця шкала вимагає від лікарів дорогого тренінгового навчання, тестування для отримання сертифіката та значних витрат часу (щонайменше 20–30 хвилин) на оцінку стану пацієнта в щоденній роботі. Однак у практичній роботі невропатолога час для встановлення бала за EDSS обмежений. Тому більшість практичних спеціалістів формально не використовують шкалу EDSS, а частіше роблять приблизну оцінку інвалідизації. Для швидкої оцінки неспроможності необхідне застосування шкали, що не вимагає спеціальних вмінь, тренінгового навчання, а також не потребує значних витрат часу.
Однією з альтернатив є шкала Patient Determined Disease Steps (PDDS), розроблена в 1995 році Північно-Американським дослідницьким комітетом розсіяного склерозу (NARCOMS — North American Research Committee Multiple Sclerosis) [7–10]. Шкала PDDS — це заповнена самостійно пацієнтом шкала оцінки власного ступеня неспроможності [7–10]. PDDS має дев’ять рівнів неспроможності — від 0 (нормальний) до 8 (прикутий до ліжка) — та дає можливість оцінити легку, помірну та виражену неспроможність. Шкала PDDS не потребує спеціального тренінгу та складання іспиту лікарем. На відміну від шкали EDSS, вона може використовуватись як лікарями, так і пацієнтами для оцінки ступеня неспроможності. Слід відзначити, що шкала PDDS використовувалась як первинна та кінцева точка в ряді міжнародних мультицентрових клінічних досліджень [11, 12]. Шкала PDDS була рекомендована Американською академією неврології для використання неврологами в рутинній клінічній практиці для оцінки неспроможності пацієнтів із РС. PDDS включено як самостійний метод до переліку способів якісної оцінки РС Американської академії неврології. Підкреслено, що даний метод не потребує паралельної оцінки за шкалою EDSS [13]. Валідація українськомовної версії шкали до цього часу не здійснювалась.
Мета: валідувати україномовну версію шкали PDDS для застосування в щоденній практиці та оцінити її зв’язок зі шкалою EDSS.
Матеріали та методи
На базі Волинського обласного центру розсіяного склерозу з 2012 року постійно оновлюється електронний реєстр пацієнтів із РС. Заповнивши розроблену фахівцями анкету, пацієнти надали демографічні дані. Було обстежено 338 хворих, які надали письмову інформовану згоду на використання інформації в формі наукового звіту (51,8 % від всієї популяції хворих з вірогідним діагнозом РС за критеріями McDonald (2010) з поправкою Polman [14] станом на 01.01.2016). Усі пацієнти вільно володіють українською мовою. Пацієнти заповнювали анкету та визначали самостійно бал за шкалою PDDS. Початок захворювання визначався за датою появи перших симптомів. Час діагнозу визначався за роком, встановленим неврологом.
При визначенні варіанта перебігу захворювання використовувалось визначення F. Lublin [15]. Для оцінки ступеня неспроможності використовували шкали Functional System Scales (FSS), EDSS та PDDS. Якщо пацієнт був спроможний, для оцінки функції ходи також використовувався тест T25FW (тест 25 футів). Швидкість оцінювалася в секундах. Для оцінки швидкості когнітивної обробки інформації використовували Paced Auditory Serial Test 3 (PASAT‑3) та Symbol Digit Modalities Test (SDMT). Обидва тести є швидкими та валідними при РС [16–19]. Результат тесту PASAT‑3 визначали за кількістю правильних відповідей протягом 60 секунд. Тест PASAT‑3 оцінює сприйняття інформації на слух та оперативну пам’ять. Результат за тестом SDMT визначали за кількістю правильних відповідей письмово за 90 секунд. Тест SDMT оцінює зорове сприйняття та пов’язану з ним оперативну пам’ять. Для оцінки функції верхніх кінцівок використовувався тест з 9 луночками (9 HT). Швидкість виконання тесту оцінювали в секундах. Тест проводили двічі, домінантною та недомінантною кінцівкою.
Статистичний аналіз здійснено за допомогою програми Microsoft Excel, SPSS for Windows з використанням стандартних описових статистик. Для аналізу категоріальних даних використовували хі-квадрат Пірсона. Статистично значущими вважали результати на рівні p < 0,05.
Для оцінки величини та спрямованості кореляційної залежності використовували коефіцієнт непараметричної кореляції Спірмена.
Валідаційний процес здійснили в декілька етапів, а саме: переклад, попереднє тестування, оцінку конвергентної валідності, надійності та чутливості. Шкала PDDS не захищена авторським правом. Автор цієї статті отримала офіційний дозвіл на переклад і використання шкали PDDS (табл. 1).
Переклад українською мовою здійснювався двома незалежними перекладачами. У подальшому отриманий переклад українською інші двоє незалежних перекладачів перекладали англійською. Отримані результати порівняли та вибрали максимально точний щодо оригіналу, легкий для сприйняття текст. Фінальну версію перекладу було узгоджено з дипломованим фахівцем з медичної англійської.
Для оцінки надійності показників використовувалась оцінка їх відтворення методом тест-ретест-аналізу та визначення коефіцієнта внутрішньої постійності α Кронбаха (на рівні понад 0,70). Коефіцієнт альфа Кронбаха — це оцінка надійності, що базується на гомогенності шкали та обчислюється як сума кореляцій між відповідями на запитання в середині однієї тестової групи.
Оцінка критеріальної валідності здійснена методом порівняння з іншими шкалами і тестами. Конструктивну валідність визначали за методом «відомих груп» на основі побудови гіпотез та оцінки коефіцієнтів кореляцій із зовнішніми критеріями.
Чутливість шкали PDDS визначали за оцінкою показників через інтервали часу (6 місяців) у процесі прийому імуномодулюючої терапії методом розрахунку стандартизованих балів.
Дослідження схвалене Комісією з питань етики Волинської обласної клінічної лікарні.
Результати
Було обстежено 338 хворих на РС. Демографічні показники подані в табл. 2.
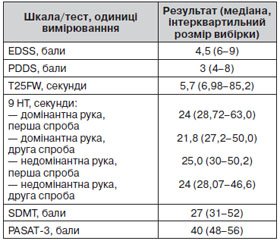
Серед обстежених переважали жінки — 65,38 %. Найбільший відсоток хворих з ремітуючо-рецидивуючим типом перебігу — 35,2 %. Результати проведених діагностичних тестів подані в табл. 3.
Здійснювалась кореляція між шкалою PDDS та балами за функціональними шкалами і шкалою EDSS (табл. 4).
Зазначені результати свідчать, що шкала PDDS чітко корелює з пірамідною, мозочковою функціональними шкалами та шкалою ходи. Вірогідно високий рівень кореляції виявлений із загальним балом за шкалами EDSS та PDDS.
Під час дослідження ми виявили недостатній кореляційний зв’язок між шкалою PDDS та T25FW (r = 0,29, χ2 = 0,001), 9HT (r = 0,33–0,42, χ2 = 0,15–0,6), PASAT (r = –0,18, χ2 = 0,6), SDMT (r = –0,31, χ2 = 0,68).
У дослідження надійності були включені 102 хворі з РС, яким було повторно проведене тестування. Не було виявлено статистично значущої різниці між первинною та повторною оцінкою за шкалою PDDS (p > 0,1).
Більше того, при повторному тестуванні 92,15 % пацієнтів надали ідентичні відповіді. Коефіцієнт кореляції між первинним та повторним тестуванням (r = 0,97) був вищим за мінімально значущий рівень, що становить 0,7. Отже, запитання шкали зрозумілі для пацієнтів, а повторна оцінка дала схожі результати. Результат оцінки внутрішньої постійності за коефіцієнтом α Кронбаха становить 0,98. Отже, результати дослідження внутрішньої постійності й відтворення підтверджують достатню надійність української версії шкали PDDS.
Конструктивна валідність шкали PDDS оцінювалась методом побудови гіпотез, в основі яких були відомі фактори та клінічні показники. Для підтвердження гіпотези, що ступінь неспроможності буде наростати з тривалістю хвороби, проаналізовано середні показники за шкалою PDDS у різних вікових групах (табл. 5). Статистичну значущість було виявлено в усіх вікових групах (p < 0,01).
Чутливість шкали PDDS оцінювали у 86 осіб з ремітуючо-рецидивуючим типом перебігу, які отримували імуномодулюючу терапію від моменту включення в дослідження (перша точка) та через 6 місяців (друга точка). Залежно від ефекту імуномодулюючої терапії пацієнтів поділили на дві групи: першу групу (n = 69) становили пацієнти, яким під час лікування стало краще, та ті, які почували себе стабільно. Другу групу становили пацієнти, у яких спостерігалось підвищення бала за шкалою PDDS (n = 17). Динаміка показників подана в табл. 6.
У групі пацієнтів з повільним прогресуванням захворювання величина ефекту становила 1,02. У групі пацієнтів, які відзначали поліпшення або стабілізацію стану, величина ефекту виявилась на рівні –0,09. Отже, шкала PDDS чутлива та здатна характеризувати мінімально значущі клінічні зміни.
Обговорення
Значних обмежень дослідження на цей час немає. Оригінал шкали PDDS створений англійською мовою. Тому мовна та культурна адаптація українського варіанта дещо відрізняється та наближена до умов пересічного пацієнта. Шкала акцентована переважно на мобільності, що проявляється її сильним кореляційним зв’язком з пірамідною, мозочковою функціональними шкалами й шкалою ходи та загальною оцінкою за шкалою EDSS. Шкала не є чутливою щодо пацієнтів з ізольованими зоровими, тазовими та сенсорними розладами. Результати нашого дослідження збігаються зі здійсненими раніше закордонними дослідженнями [10]. Сильний кореляційний зв’язок між оцінкою за шкалою PDDS та EDSS може бути зумовлений включенням в дослідження значної кількості пацієнтів з різною кількістю балів за EDSS — від 0 до 9. Одним з обмежень нашого дослідження може бути те, що ми використовували лише паперову версію шкали. Не виключено, що використання онлайн-версії могло б частково впливати на результати дослідження. Ще одним з обмежень є те, що ми не оцінювали чутливість шкали PDDS у пацієнтів з первинно-прогредієнтним перебігом через відсутність імуномодулюючої терапії в цій категорії хворих. Ми вважаємо за доцільне в перспективі оцінити за шкалою PDDS пацієнтів з доброякісним та агресивним перебігом розсіяного склерозу.
Висновки
Отже, українська версія шкали PDDS, що пропонується, є валідним, надійним та чутливим інструментом в оцінці неспроможності хворих з РС. Застосування шкали не потребує спеціальних навичок. Результати проведеного дослідження можуть використовуватись у щоденній практиці неврологами, сімейними лікарями як амбулаторно, так і в стаціонарах для моніторингу стану хворих РС на рівні району, області та країни, а також у навчальному матеріалі в навчальних закладах. Українська версія шкали PDDS може використовуватись для популяційних та наукових досліджень в Україні.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів. Автор дякує за підтримку Tuula Tyry (NARCOMS) — за дозвіл перекласти шкали PDDS українською та російською мовами. Автор висловлює подяку кандидату філологічних наук, доценту кафедри латинської та іноземних мов Львівського національного медичного університету ім. Данила Галицького Оксані Степанівні Ісаєвій за коректуру перекладу на всіх етапах роботи.
Список литературы
1. Міщенко Т.С. Розсіяний склероз: глобальні перспективи [Текст] / Т.С. Міщенко, О.Д. Шульга, Н.В. Бобрик, Л.А. Шульга // Укр. мед. часопис. — 2014. — № 3. — С. 84-87.
2. Школьник В.М. Сучасні підходи до лікування при загостренні розсіяного склерозу з позицій доказової медицини [Текст] / В.М. Школьник, О.М. Бараненко, О.В. Погорелов, О.І. Кальбус // Український медичний часопис. — 2014. — № 4. — С. 108-111.
3. Шульга О.Д. Клініко-епідеміологічна характеристика розсіяного склерозу у Волинській області [Текст] / О.Д. Шульга // Проблеми безперервної медичної освіти та науки. — 2015. — № 1. — С. 16-18.
4. Шульга О.Д. Особливості перебігу розсіяного склерозу у жителів Волині [Текст] / О.Д. Шульга // Український науково-медичний молодіжний журнал. — 2014. — № 3. — С. 120-122.
5. Kurtzke J.F. Rating Neurologic Impairment in Multiple Sclerosis an Expanded Disability Status Scale (EDSS) // Neurology. — 1983. — 33. — P. 1444-1452.
6. Шкалы в общей и детской неврологии: Науч-практ. и метод. пособие / [О.С. Евтушенко и др.]; под. ред. проф. С.К. Евтушенко. — К.: Заславский А.Ю., 2015. — С. 41-54.
7. Hohol M.J. Disease Steps in multiple sclerosis: A simple approach to evaluate disease progression / M.J. Hohol, E.J. Orav, H.L. Weiner // Neurology. — 1995. — № 45. — P. 251-255.
8. Hohol M.J. Disease steps in multiple sclerosis: A longitudinal study comparing Disease Steps and EDSS to evaluate disease progression / M.J. Hohol, E.J. Orav, H.L. Weiner // Mult. Scler. — 1999. — № 5. — P. 349-354.
9. Marrie R.A. Validity of performance scales for disability assessment in multiple sclerosis / R.A. Marrie, M. Goldman // Multiple Sclerosis. — 2007. — № 13. — P. 1176-1182.
10. Learmonth Y.C. Validation of patient determined disease steps (PDDS) scale scores in persons with multiple sclerosis / Y.C. Learmonth, R.W. Motl, B.M. Sandroff, J.H. Pula, D. Cadavid // BMC Neurology. — 2013. — 13. — P. 37. doi: 10.1186/1471-2377-13-37.
11. Jelinek G.A. Latitude, sun exposure and vitamin D supplementation: associations with quality of life and disease outcomes in a large international cohort of people with multiple sclerosis / G.A. Jelinek, C.H. Marck, T.J. Weiland, N. Pereira, D.M. van der Meer, E.J. Hadgkiss // BMC Neurol. — 2015. — 5(15). — P. 132. doi: 10.1186/s12883-015-0394-1.
12. Ezeugwu V. Mobility disability and the pattern of accelerometer-derived sedentary and physical activity behaviors in people with multiple sclerosis / V. Ezeugwu, R.E. Klaren, E. Hubbard, P. Manns (Trish), R.W. Motl // Preventive Medicine Reports. — 2015. — 2. — P. 241-246. http://doi.org/10.1016/j.pmedr.2015.03.007
13. https://www.aan.com/uploadedFiles/Website_Library_Assets/Documents/3.Practice_Management/2.Quality_Improvement/1.Quality_Measures/MS%20Measurement_set.pdf
14. Polman C.H. Diagnostic criteria for multiple sclerosis: 2010 revisions to the McDonald criteria [Text] / C.H. Polman, S.C. Reingold, B. Banwell, M. Clanet, J.A. Cohen, M. Filippi et al. // Annals of Neurology. — 2011. — Vol. 69, Issue 2. — P. 292–302. doi: 10.1002/ana.22366.
15. Lublin F.D. Defining the clinical course of multiple sclerosis: Results of an international survey [Text] / F.D. Lublin, S.C. Reingold // Neurology. — 1996. — Vol. 46, Issue 4. — P. 907-911. doi: 10.1212/wnl.46.4.907.
16. Fischer J.S. The Multiple Sclerosis Functional Composite measure (MFSC): An integrated approach to MS clinical outcome assessment. National MS Society Clinical Outcomes Assessment Task Force / J.S. Fischer, R.A. Rudick, G.R. Cutter, S.C. Reingold // Mult. Scler. — 1999. — Vol. 5. — P. 244-50.
17. Gronwall D.M. Paced auditory serial addition task: A measure of recovery from concussion // Percept. Mot. Skills. — 1977. — Vol. 44. — P. 367-373.
18. Smith A. Symbol digit modalities test: Manual. — Los Angeles: Western Psychological Services, 1982.
19. Rao S.M. Correlation of magnetic resonance imaging with neuropsychological testing in multiple sclerosis / S.M. Rao, G.J. Leo, V.M. Haughton, P.S. Aubin-Faubert, L. Bernardin // Neurology. — 1989. — Vol. 39. — P. 161-166.
/169.jpg)
/169_2.jpg)

/168.jpg)
/170.jpg)
/170_2.jpg)