Вступ
Дотепер стандартом у лікуванні ускладнень хронічного панкреатиту (ХП) та кістозних утворень підшлункової залози (ПЗ), а саме постнекротичних кіст (ПК), є відкрите оперативне втручання, що в більшості випадків передбачає виконання дренуючих (внутрішнього або зовнішнього дренування ПК ПЗ, головної панкреатичної протоки (ГПП)), резекційно-дренуючих або резекційних втручань [5]. Слід відмітити, що при використанні відкритих методів лікування спостерігається низка тяжких інтраопераційних та післяопераційних ускладнень (20,0–40,0 %), довготривале перебування хворих у стаціонарі й летальність у післяопераційному періоді при операціях внутрішнього дренування, а також її зростання при виконанні резекційних втручань на ПЗ, що досягає 12,0–15,0 % [3, 7, 8]. Лапаротомія залишається операцією вибору, але її використання не дозволяє покращити результати хірургічного лікування ускладнень ХП та ПК ПЗ [4, 6].
Проблема хірургічного ризику при втручаннях на ПЗ, зокрема при одному з найбільш складних — панкреатодуоденальній резекції (ПДР), детально проаналізована в публікації M. Trede і G. Schwall (1990) на підставі вивчення результатів даної операції, виконаної в 118 хворих із доброякісними й пухлинними ураженнями ПЗ [14]. Автори виділяють три групи факторів операційного ризику: 1) залежні від пацієнта; 2) обумов–лені самим захворюванням; 3) залежні від хірурга. Перша група факторів ризику включала вік понад 65 років; перенесені операції на органах черевної порожнини з приводу ХП, що створювало додаткові технічні труднощі при виконанні радикальної операції; нарешті, серйозні супутні захворювання, головним чином цироз печінки.
Не менш суттєвими, за даними M. Trede і G. Schwall, були ризики, пов’язані з характером основного захворювання ПЗ і його ускладнень; вони визначалися наявністю карциноми залози, її поширенням за межі залози, а також наявністю обтураційної жовтяниці. Останній фактор, за даними авторів, вимагав перед–операційної корекції, що суттєво знижувала число та тяжкість ускладнень хірургічного втручання, особливо у випадках високої доопераційної гіпербілірубінемії [11]. За даними C. Russell (1998), зменшити кількість несприятливих результатів відкритих і малоінвазивних втручань у хворих із ПК ПЗ дозволяє суворе дотримання того принципу, що лікування самої лише кісти ще не може вирішити проблеми лікування панкреатиту. Тому виконанню операції безпосередньо на кістозному утворенні ПЗ повинна передувати поглиблена ревізія ПЗ та її ГПП для того, щоб виявити або виключити наявність обструкції останньої й при необхідності усунути її [13].
Нарешті, роль хірурга в зниженні операційного ризику досить багатогранна й визначається його здатністю виявити до операції та адекватно скоригувати фактори ризику, бездоганно тактично й технічно провести саму операцію, а також своєчасно виявити й скоригувати виникаючі ускладнення [1].
За даними класифікації ХП, розробленої Е.І. Гальпериним (2013), твердість ПЗ та ускладнення ХП — це дві ознаки, що визначають тяжкість ХП, клінічну симптоматику, вибір методу лікування й конкретної операції. Виділені два терміни структурної оцінки паренхіми ПЗ — «тверда» (з вираженими фіброзними змінами) або «м’яка», соковита (ненормальна, змінена залоза з незначно вираженими фіброзними змінами). При діагностичному визначенні м’якої ПЗ протипоказане виконання резекційних втручань унаслідок розвитку тяжких ускладнень — кровотечі, панкреатиту тощо, тоді як твердість ПЗ обумовлює виконання резекційних втручань [2].
Використання хі-квадрату в аналізі даних 5-річного виконання операції Фрея дало можливість виявити, що при виражених фіброзних змінах паренхіми ПЗ (> 75 %) і ГПП діаметром > 4 мм відбувалось значне зменшення больового синдрому. Водночас при мінімально виражених фіброзних змінах ПЗ (< 25 %) та ГПП діаметром ≤ 4 мм зберігався больовий синдром (р < 0,05) [9], що свідчить про неадекватність вибору застосованого обсягу оперативного втручання.
При аналізі невдач хірургічних втручань на ПЗ при ХП провідні фахівці-панкреатологи підкреслюють не лише особливу важливість адекватного вибору того або іншого оперативного методу, але й обов’язковість врахування інколи, здавалося б, малозначимих обставин ураження залози й ретельного дотримання деталей виконуваної операції. Так, C.F. Frey (2005) підкреслює, що результат операції, який розчаровує при хірургічному лікуванні ХП, — це збереження або рецидив болю, і це може бути обумовлене не тільки дефектами самого оперативного втручання, але й помилковим, необґрунтованим вибором типу операції для конкретного пацієнта [10].
На сьогодні ще не розроблені обґрунтовані показання та протипоказання до виконання дренувальних, резекційно-дренувальних та резекційних методик з доопераційним урахуванням факторів ризику їх виконання, немає сучасних діагностично-лікувальних алгоритмів лікування хворих з ускладненнями ХП та ПК ПЗ [2, 6, 9]. Тому ретроспективний аналіз невдач при оперативних втручаннях на ПЗ сприяв би створенню діагностично-лікувального алгоритму з максимальним урахуванням факторів ризику, який дозволив би індивідуалізувати лікувальну програму та забезпечив би хворому тривалий лікувальний ефект із мінімальним ризиком рецидиву захворювання та мінімальною операційною травмою, що є актуальною проблемою сучасної хірургії.
Мета роботи: визначити основні причини, що призвели до невдач при хірургічному лікуванні ускладнень хронічного панкреатиту та кіст підшлункової залози.
Матеріали та методи
Проведено ретроспективний порівняльний аналіз 108 карт спостереження хворих за період 2006–2012 рр., оперованих у відділенні хірургії органів травлення з приводу ускладнень ХП (n = 66) та ПК ПЗ (n = 42) із застосуванням дренуючих, резекційно-дренувальних та резекційних хірургічних втручань, у тому числі з непрямими втручаннями на ПЗ (n = 29). З числа оперованих було 78 (72,2 %) чоловіків віком 30–71 рік (середній вік — 51,4 ± 2,3 року), 30 (27,7 %) жінок віком 27–68 років (середній вік — 47,1 ± 1,6 року).
Діагноз ускладнень ХП та ПК ПЗ встановлювали на підставі анамнезу, даних лабораторних, інструментальних методів дослідження, а також інтраопераційних даних. Морфологічну оцінку ступеня фіброзу ПЗ при ХП проводили за M. Stolte (1991) [12]. Стадія фіброзної трансформації ПЗ характеризувалася як рання (І–ІІ ступінь фіброзу) та пізня (ІІІ–ІV ступінь фіброзу).
При ретроспективному аналізі порівнювали морфологічний стан паренхіми ПЗ та ПК ПЗ на час операції, що супроводжувалась крововтратою (понад 500 мл), частоту й характер інтра- та післяопераційних ускладнень залежно від виду хірургічного втручання, обсягу та адекватності виконання операції, летальність.
Результати та обговорення
Ускладнення ХП встановлено в 66 (61,1 %) хворих. Характер ускладнень ХП: постійний або рецидивуючий больовий синдром, розширення ГПП (вірсунгодилатація), конкремент ГПП (вірсунгокалькульоз, кальциноз паренхіми ПЗ, стеноз інтрапанкреатичної частини холедоху, біліарна гіпертензія, механічна жовтяниця, дуоденальна непрохідність, сегментна допечінкова або підпечінкова портальна гіпертензія, асцит, абсцес ПЗ, зовнішня панкреатична нориця.
ПК ПЗ встановлені в 42 (38,8 %) пацієнтів. Розподіл за локалізацією був таким: ПК у головці виявлена у 18 осіб, у тілі — в 11 та в хвості — у 13 хворих. Розміри ПК ПЗ коливалися від 5 до 15 см. Характер ускладнень ПК ПЗ (26): дуоденальна непрохідність (6), механічна жовтяниця (5), підпечінкова (4) та сегментна допечінкова (4) портальна гіпертензія, асцит (5), абсцес ПЗ (2).
Діагноз ускладнень ХП та ПК ПЗ встановлено на підставі анамнезу, даних лабораторних, інструментальних методів дослідження, а також інтраопераційних даних.
Після обстеження й передопераційної підготовки в 15 хворих планувалося виконання резекційного хірургічного втручання, у 20 хворих — резекційно-дренуючого втручання, у 58 — внутрішнього та в 7 — зовнішнього дренування. У 8 хворих планувалося виконання етапних хірургічних втручань.
Вид оперативних втручань і летальність при хірургічному лікуванні ускладнень ХП та ПК ПЗ наведені в таблиці 1.
Як свідчать дані таблиці 1, летальних випадків при хірургічному лікуванні ускладнень ХП та ПК ПЗ було 4 (3,7 %) — при виконанні дренуючих (продольна панкреатоєюностомія (ППЄС) — 1, цистопанкреатоєюностомія (ЦПЄС) — 1) і резекційних оперативних втручань (ПДР — 2).
Невдачі при хірургічному лікуванні ускладнень ХП та ПК ПЗ відмічені у 57 (57,0%) випадках, у тому числі в 33 (57,9 %) при лікуванні ускладнень ХП та у 24 (42,1%) випадках — при лікуванні ПК ПЗ.
Характер невдач при хірургічному лікуванні ускладнень ХП та ПК ПЗ наведено в таблиці 2.
Як свідчать дані таблиці 2, невдачі хірургічного лікування ускладнень ХП та ПК ПЗ у більшості випадків (64,9 %) становили неможливість виконання адекватного хірургічного втручання (21), післяопераційна кровотеча (5) і значна крововтрата (понад 500 мл) під час операції (5), неспроможність швів анастомозу (6).
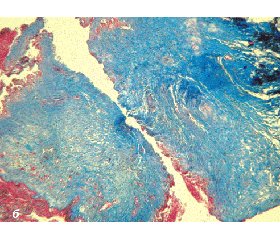
При аналізі даних гістологічного дослідження біоптатів ПЗ та ПК, отриманих під час операції, відзначалися різні морфологічні зміни (рис. 1–4).
Характер морфологічних змін ПЗ за даними гістологічного дослідження біоптатів ПЗ, отриманих у хворих під час операції, подано в таблиці 3.
Як свідчать дані таблиці 3, ознаки активного запалення паренхіми ПЗ за даними морфологічного дослідження простежувались у 42 (45,6 %) випадках, а неактивного запалення — у 50 (54,3 %), прояви ранньої стадії фіброзу — у 45 (48,9 %), а пізньої — у 30 (32,6 %) випадках, ПК ПЗ з сформованою стінкою відмічена у 26 (28,3 %), а з несформованою стінкою — у 5 (5,4 %) випадках.
Основні причини невдач при хірургічному лікуванні ускладнень ХП та ПК ПЗ наведені в таблиці 4.
Як свідчать дані таблиці 4, більшість невдач хірургічного лікування ускладнень ХП та ПК ПЗ була пов’язана з морфологічним станом ПЗ та ПК ПЗ на час операції: активне запалення та його поєднання з різною стадією фіброзу паренхіми ПЗ мало місце в 47 випадках; рання стадія фіброзу паренхіми ПЗ — у 15, ПК ПЗ із несформованою стінкою — у 5, м’яка, соковита ПЗ (ліпоматоз на тлі активного запалення паренхіми ПЗ) — у 8 випадках.
Ретроспективний порівняльний аналіз основних причин невдач при виконанні хірургічних втручань у хворих з ускладненнями ХП та ПК ПЗ показав, що активне запалення та його поєднання з різною стадією фіброзу паренхіми ПЗ у 21 випадку призвело до невдач і змусило відмовитись від запланованого прямого хірургічного втручання на ПЗ і виконати такі непрямі оперативні втручання: холецистостомія, у тому числі лапароскопічна (3), — 7 випадків; холецистоєюностомія + гепатикоєюностомія (ГЄС) — 5; холецистектомія, холедохоєюностомія за Ру, ГЄС із браунівським співустям — 6 (при ускладненнях хронічного панкреатиту — 3, при кістах підшлункової залози — 3); пробна лапаротомія — 3.
У 38 хворих, у яких запланований обсяг хірургічного втручання був виконаний, невдачі хірургічного лікування ускладнень ХП (23) та ПК ПЗ (15) були пов’язані з різноманітними причинами.
При виконанні дистальної резекції ПЗ з ПК ПЗ (1) та ППЄС (2) відзначена інтраопераційна кровотеча, що була обумовлена м’якою, соковитою паренхімою в ПЗ на тлі ліпоматозу при ранній стадії фіброзу її паренхіми.
Після виконання ПДР за Wipple (1) та операції Фрея (1) в ранньому післяопераційному періоді виникла внутрішньочеревна кровотеча, причиною якої послужив недостатній гемостаз при ранній стадії фіброзу на тлі активного запалення паренхіми ПЗ. Зупинка кровотечі з кукси ПЗ після ПДР потребувала релапаротомії й накладання додаткових гемостатичних швів на передню лінію панкреатоєюноанастомозу.
Після виконання операції Фрея (1) з корекцією жовчовідтоку (холецистектомія з холедохоєюностомією) в ранньому післяопераційному періоді виникла кровотеча в просвіт шлунково-кишкового тракту (ШКТ), причиною якої був ненадійний гемостаз на тлі механічної жовтяниці з проявами коагулопатії. При релапаротомії проведено додаткове прошивання часток панкреатоєюноанастомозу, що кровоточили.
Після виконання операції Фрея (1), ППЄС (2) та дистальної резекції ПЗ зі спленектомією (1) в ранньому післяопераційному періоді виник післяопераційний панкреатит, причинами якого була підвищена травматизація «вологої», дуже м’якої, соковитої ПЗ при ранній стадії фіброзу на тлі активного запалення паренхіми головки ПЗ на час операції.
Після виконання операції Фрея (1) проведена релапаротомія із санацією й дренуванням черевної порожнини.
Після виконання дистальної резекції ПЗ (1) сплен–ектомія викликала пригнічення як специфічного, так й неспецифічного імунітету, що на тлі післяопераційного панкреатиту сприяло розвитку й інших ускладнень, а саме виникненню лівобічного ексудативного плевриту та піддіафрагмального абсцесу. Це вимагало проведення декількох пункцій плевральної порожнини, релапаротомії із санацією черевної порожнини й дренуванням абсцесу, проведення тривалої антибактеріальної та імуномодулюючої терапії.
Після виконання ППЄС (2) у ранньому післяопераційному періоді діагностовані піддіафрагмальний та парапанкреатичний абсцеси, що були обумовлені неспроможністю панкреатоєюноанастомозу, сформованого на ранній стадії фіброзу на тлі активного запалення паренхіми ПЗ. В одному випадку при піддіафрагмальному абсцесі виконано міні-інвазивне дренування під ультразвуковим (УЗ) контролем. У другому випадку, при парапанкреатичному абсцесі, виконано релапаротомію із санацією й дренуванням черевної порожнини.
У двох випадках — після виконання дистальної резекції ПЗ із спленектомією (1) та після ППЄС (1) — у ранньому післяопераційному періоді відмічені рідинні скупчення черевної порожнини, причиною яких була негерметичність швів кукси ПЗ (Pancreatic fistula, grade B) при ранній стадії фіброзу на тлі активного запалення паренхіми ПЗ. Це вимагало виконання міні-інвазивних пункційно-аспіраційних втручань під УЗ-контролем.
У випадку після виконання ППЄС (1) з холецистектомією (у зв’язку з ЖКХ) невдача була обумовлена рідкісним ускладненням — жовчевитіканням з додаткової жовчної протоки в ділянці ложа жовчного міхура, що потребувало релапаротомії й перев’язки протоки.
Неспроможність швів гепатикоєюноанастомозу діагностована в ранньому післяопераційному періоді у випадку після виконання ПДР (1) за Wipple на тлі механічної жовтяниці з проявами коагулопатії, що вимагало релапаротомії з додатковим прошиванням лінії анастомозу й дренуванням протоки Т-подібним дренажем.
Неспроможність швів анастомозу, що була діагностована в ранньому післяопераційному періоді після виконання ППЄС (2) та операції Фрея (1), була обумовлена виконанням хірургічного втручання при пізній стадії фіброзу на тлі активного запалення паренхіми ПЗ. Під час релапаротомій виконана санація з додатковою перитонізацією швів по лінії панкреатоєюно–анастомозу.
У двох випадках після виконання вірсунгодуоденостомії в ранньому післяопераційному періоді розвинувся дуоденостаз, що вимагало застосування назоінтестинального зонда, електростимуляції та прокінетичної терапії. Післяопераційне лікування потребувало тривалого часу.
У трьох випадках відзначено невдачі при зовнішньому дренуванні ПК ПЗ під УЗ-контролем. В одному випадку з лікувальною метою (замість виконання внутрішнього дренування) під УЗ-контролем було виконано зовнішнє дренування ПК хвоста ПЗ розміром 10,0 × 3,0 см зі сформованою кістозною стінкою. В отриманому кістозному пунктаті рівень амілази був високий і дорівнював 8842,0 Од/л, а в сироватці крові був нормальним — 13,3 Од/л, що свідчило про наявність зв’язку порожнини ПК ПЗ з ГПП на тлі неактивного запалення паренхіми залози. На 6-ту добу відбулося нагноєння порожнини ПК ПЗ, що вимагало її двотижневої санації розчинами антисептиків.
У другому випадку з лікувальною метою під УЗ-контролем було виконано зовнішнє дренування ПК тіла ПЗ розміром 11,0 × 4,0 см зі сформованою кістозною стінкою. В отриманому кістозному пунктаті рівень амілази був високим і дорівнював 13873,0 Од/л, і в сироватці крові він був також підвищеним — 763,4 Од/л, що свідчило за наявність зв’язку порожнини ПК ПЗ з ГПП на тлі активного запалення паренхіми залози. На 4-ту добу відбулося нагноєння порожнини ПК ПЗ, що вимагало тритижневої санації розчинами антисептиків.
У третьому випадку на тлі механічної жовтяниці внаслідок ПК ПЗ у головці залози розміром 9,0 × 9,0 см із несформованою кістозною стінкою було виконано зовнішнє дренування кісти під УЗ-контролем. В отриманому кістозному пунктаті рівень амілази був високим — 2789,0 Од/л, у сироватці крові він теж був високим — 97,0 Од/л, що свідчить про активний запальний процес у паренхімі ПЗ та зв’язок кісти з панкреатичною протоковою системою. Міні-інвазивне втручання клінічно привело до різкого больового синдрому з розвитком локального перитоніту внаслідок підтікання кістозного вмісту в черевну порожнину. У подальшому це вимагало виконання лапаротомії з санацією черевної порожнини та зовнішнього дренування ПК ПЗ з несформованою стінкою, що можна визначити як застосування неадекватного обсягу хірургічного втручання.
Отже, зовнішнє дренування ПК ПЗ під УЗ-контролем при сполученні порожнини кісти з ГПП приводить до інфікування кістозного вмісту та його нагноєння, а при ПК ПЗ з несформованою стінкою призводить до підтікання кістозного вмісту в черевну порожнину з розвитком перитоніту. Тому при ПК ПЗ зі сформованою стінкою без ознак активного запалення паренхіми залози показане виконання цистодигестивного анастомозу, а при ПК ПЗ із несформованою стінкою з проявами механічної жовтяниці або дуоденальної непрохідності показане виконання пункційної аспірації кістозного вмісту з подальшим забезпеченням адекватного пасажу жовчі та/або панкреатичного секрету — виконання тимчасового стентування холедоху та/або ГПП.
У 4 випадках невдачі відзначено при виконанні цистодигестивних анастомозів. В одному випадку інтраопераційна кровотеча виникла при виконанні цистопанкреатоєюностомії при м’якій, соковитій паренхімі ПЗ на ранній стадії фіброзу. У 3 випадках у ранньому післяопераційному періоді виникли: панкреонекроз після виконання цистопанкреатодигестивного анастомозу, абсцес черевної порожнини та нагноєння післяопераційної рани після виконання цистоєюностомії на тлі активного запалення й ранньої стадії фіброзу паренхіми ПЗ.
У 2 випадках при виконанні етапних хірургічних втручань при ускладненнях ХП мали місце післяопераційні ускладнення. В одному випадку виконання ендоскопічної папілосфінктеротомії (ЕПСТ) ускладнилось кровотечею в просвіт ШКТ унаслідок виконання ЕПСТ на тлі активного гастродуоденіту й папіліту, а в другому випадку — підпечінковим абсцесом унаслідок ятрогенної травми — перфорації стінки дванадцятипалої кишки.
У 4 хворих невдачі хірургічних втручань призвели до летального кінця. В одному випадку при виконанні ППЄС при ранній стадії фіброзу на тлі активного запалення паренхіми ПЗ у ранньому післяопераційному періоді виникла неспроможність швів панкреатоєюноанастомозу, що призвело до розлитого перитоніту, сепсису та летального кінця.
У другому випадку після виконання ЦПЄС з приводу ПК ПЗ із несформованою стінкою при ранній стадії фіброзу на тлі активного запалення паренхіми ПЗ у післяопераційному періоді виник панкреонекроз із летальним кінцем.
У третьому випадку було необґрунтовано застосовано неадекватний обсяг оперативного втручання, а саме виконанно ПДР за Whipple (замість внутрішнього дренування ПК ПЗ) при ПК ПЗ зі сформованою стінкою при пізній стадії фіброзу на тлі активного запалення паренхіми ПЗ — інтраопераційно виникла кровотеча зі значною крововтратою, випадок мав летальний кінець.
У четвертому випадку після виконання ПДР за Whipple на тлі активного запалення при пізній стадії фіброзу паренхіми ПЗ виникла неспроможність швів панкреатоєюноанастомозу з кровотечею в черевну порожнину, що вимагало проведення трьох релапаротомій, як наслідок — розлитий перитоніт із летальним кінцем.
У 43 (43,0 %) оперованих хворих, у тому числі у 27 (62,8 %) при лікуванні ускладнень ХП та у 16 (37,2 %) випадках при лікуванні ПК ПЗ, при оперативному втручанні та в ранньому післяопераційному періоді відмічені позитивні результати.
Результати ретроспективного порівняльного аналізу умов, у яких виконувалися оперативні втручання з позитивними результатами, наведені в таблиці 5.
Як свідчать дані таблиці 5, у хворих з ускладненнями ХП оперативні втручання були виконані на тлі неактивного запалення ПЗ та в більшості випадків (88,8 %) — на пізній стадії фіброзу паренхіми ПЗ.
У хворих із ПК ПЗ більшість операцій була виконана на тлі неактивного запалення ПЗ (75,0 %), частіше на ранній (68,7 %) та рідше на пізній (31,3 %) стадії фіброзу паренхіми ПЗ.
При ПК ПЗ зі сформованою стінкою в 9 випадках були виконані дренуючі операції (цистоєюностомія (ЦЄС), цистогастростомія, цистодуоденостомія, ЦПЄС), в одному випадку — зовнішньодренуюче втручання під УЗ-контролем, в одному випадку — енуклеація кісти та в двох випадках — резекційні операції, без ускладнень. В одному з цих випадків, при ПК ПЗ зі сформованою стінкою на тлі активного запалення паренхіми ПЗ при ранній стадії фіброзу, було виконано ЦЄС, однак без розвитку ускладнень.
При ПК ПЗ із несформованою стінкою (за даними ультразвукового дослідження) у трьох випадках оперативні втручання на тлі активного запалення ПЗ при ранній стадії фіброзу паренхіми ПЗ були обмежені виконанням зовнішньодренуючих операцій під УЗ-контролем.
Отже, як свідчать результати ретроспективного порівняльного аналізу морфологічного стану паренхіми ПЗ та ПК ПЗ на час операції, що супроводжувалася крововтратою, частоти й характеру інтра- та післяопераційних ускладнень, виду хірургічного втручання, об’єму та адекватності його виконання, основними причинами невдач хірургічного лікування ХП та ПК ПЗ є морфологічні зміни ПЗ на час операції, а саме активність запалення, стадія фіброзних змін паренхіми ПЗ, несформованість стінки ПК ПЗ та її ускладнення, неадекватний вибір обсягу хірургічного втручання та неадекватне його виконання.
Висновки
Основні фактори, що обумовлюють невдачі при хірургічному лікуванні ускладнень ХП та ПК ПЗ:
а) активність запалення та стадія фіброзу паренхіми ПЗ на час виконання операції;
б) сформованість стінки ПК ПЗ, її зв’язок з ГПП, локалізація, розмір і характер ускладнень ПК ПЗ;
в) неадекватно вибраний термін і тип хірургічного втручання;
г) неадекватне виконання хірургічного втручання.
Перспективи подальших досліджень. На наступному етапі дослідження буде продовжено поглиблене вивчення патогенезу запалення та фіброзної трансформації паренхіми ПЗ при ХП і ПК ПЗ, будуть розроблені критерії доопераційної неінвазивної оцінки морфологічного стану ПЗ при ХП, знання про який дозволить зменшити кількість невдач хірургічного лікування ускладнень ХП та ПК ПЗ.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.

/83-1.gif)
/84-1.gif)
/84-2.gif)
/85-1.gif)
/86-1.gif)
/87-1.gif)