Международный неврологический журнал Том 16, №5, 2020
Вернуться к номеру
Современное лечение острого ишемического инсульта
Авторы: Natan Bornstein
Tel-Aviv Faculty of Medicine/Neurology, Shaare-Zedek Medical Center, Brain Division, Tel- Aviv, Israel
Рубрики: Неврология
Разделы: Медицинские форумы
Версия для печати
Целью своего доклада доктор N. Bornstein назвал обсуждение научного обоснования и клинических разработок в области применения мультимодального нейропротекторного и нейротрофического препарата Церебролизин в качестве дополнительной терапии инсульта. Он представил обзор данных о развитии стандартов реканализационной терапии и осветил их преимущества и недостатки. Также он остановился на основных вопросах, касающихся применения нейропротекторной терапии, и продемонстрировал, как определенные дополнительные подходы в лечении инсульта, включая применение Церебролизина, могут быть использованы для преодоления важных ограничений реканализации. Из исследований по тромболизису мы узнали постулат «время — это мозг». Чем раньше мы применяем тромболизис, тем выше вероятность клинического успеха реканализации и благоприятного клинического исхода. Метаанализ данных отдельных пациентов из рандомизированных исследований [1] продемонстрировал, что окно успешного применения рекомбинантного тканевого активатора плазминогена (recombinant tissue plasminogen activator, rtPA) может быть расширено до 4,5 часа после инсульта и что такие факторы, как возраст и степень тяжести (до 22 по NIHSS) инсульта, не оказывают отрицательного влияния на клинические преимущества rtPA. В последнем метаанализе [2] (исследования EXTEND, ECASS4-EXTEND и EPITHET) оценивалась возможность дальнейшего расширения терапевтического окна применения тромболизиса с использованием диффузионной нейровизуализации, когда длительность симптомов у пациента с инсультом составляет более 4,5 часа с момента начала инсульта или с момента пробуждения. У таких пациентов тромболизис продемонстрировал свою эффективность при применении в течение 9 часов с момента начала инсульта, если с помощью диффузной нейровизуализации было установлено, что ткань мозга подлежит восстановлению. Результаты были сопоставимы по возрасту, времени и показателям, полученным при оценке слоев крупных сосудов. Принимая во внимание эти положительные достижения, мы должны помнить о некоторых недостатках применения альтеплазы. Одной из основных проблем является увеличение частоты симптоматических внутричерепных кровоизлияний. Другой недостаток заключается в том, что rtPA не всегда эффективен в случаях окклюзии крупных сосудов. Для таких пациентов методом выбора является тромбэктомия. Обычно (у 80 % пациентов) с целью эффективного устранения окклюзии крупного сосуда тромбэктомия комбинируется с применением rtPA [3]. Однако исследования DAWN и DEFUSE 3 показали, что у некоторых пациентов применение вышеуказанных критериев нейровизуализации позволяет использовать тромбэктомию в течение до 24 часов после начала инсульта. Эти успешные попытки расширения терапевтического окна для реканализационной терапии позволяют нам лечить большее количество пациентов и, следовательно, являются основными вехами в оказании помощи при инсульте. Тем не менее есть некоторые существенные ограничения. Хотя окончательная степень реканализации достаточно четко коррелирует с клиническими исходами, не все пациенты, у которых реканализация была успешной, демонстрируют достаточную степень восстановления. Хотя реканализация при инсульте является обязательной (когда это возможно), во многих случаях ее все-таки недостаточно для клинического успеха. В случае применения rtPA неудачи обусловлены несколькими факторами, и все они связаны с его отрицательным воздействием на микроциркуляцию. RtPA индуцирует проницаемость гематоэнцефалического барьера (ГЭБ), что приводит к симптомной и бессимптомной геморрагической трансформации. Также было показано, что альтеплаза индуцирует отложение фибрина в микроциркуляторном русле. Это способствует блокированию нисходящего кровотока в микроциркуляторном русле, а также провоцирует провоспалительные процессы, которые еще больше усугубляют проницаемость ГЭБ. Во многих случаях эти побочные эффекты могут свести на нет преимущества успешной реканализации, которых удалось достичь в результате тромболизиса и тромбэктомии.
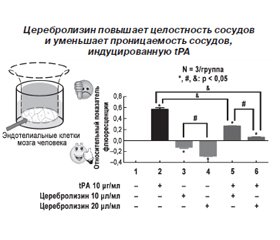
N. Bornstein подчеркнул, что уже доступен для клинического применения дополнительный метод лечения, нейтрализующий эти побочные эффекты на уровне микроциркуляции, — применение Церебролизина. Крупное исследование, которое провел Michael Chopp, продемонстрировало, что Церебролизин уменьшает проницаемость ГЭБ, а также выработку в эндотелиальных клетках головного мозга человека провоспалительных цитокинов, которые обеспечивают проницаемость ГЭБ, индуцированную rtPA и фибрином. Эти данные являются серьезным научным обоснованием для использования Церебролизина в сочетании с rtPA и тромбэктомией. Хотя перфузия мозговой ткани зависит от проходимости сосудов микроциркуляторного русла, а также от целостности и функциональности ГЭБ, защита и восстановление мозговой ткани зависят от сохранения или повторного открытия скрытых коллатеральных контуров и от восстановления кровотока во всей пораженной области. В качестве основного механизма, препятствующего восстановлению кровотока в нисходящем от основной окклюзии направлении, был выделен тромбоз нисходящих сосудов микроциркуляторного русла (ТНС), поскольку он может сохраняться даже после успешной реканализации. Риск и интенсивность ТНС связаны с наличием провоспалительных или прокоагулянтных изменений. Церебролизин проявляет антикоагулянтные, противовоспалительные и профибринолитические свойства и является уникальным средством для улучшения стандарта реканализации (рис. 1).
Общая цель нейропротекции состоит в том, чтобы предотвратить гибель нейронов в зоне ишемической полутени независимо от реканализации. Помимо описанных здесь эффектов на уровне микроциркуляторного русла, Церебролизин обеспечивает нейропротекцию, которая способствует ускоренному восстановлению пораженной ткани мозга. Это уникальная терапевтическая особенность, которая отсутствовала во многих прошлых исследованиях, где изучалось более 1000 потенциальных нейропротекторов. Причины такой неудачи широко обсуждались, но наиболее вероятными из них являются два фактора. Во-первых, недостаточная способность нейропротектора оказывать прицельное воздействие из-за отсутствия коллатералей, доставляющих кровь к области ишемической полутени. Это может объяснить наличие слабого ответа или отсутствие такового у изучаемых нейропротекторов. Другая проблема связана с природой самих исследуемых препаратов. В основном это были молекулы (мономодальные соединения), действие которых нацелено на единый выбранный механизм сложных патофизиологических процессов, происходящих в результате ишемического инсульта. Эффективная нейропротекция, как мы понимаем ее сегодня, требует применения препаратов мультимодального действия с трофическими и регенеративными эффектами, таких как Церебролизин, которые нацелены на целый ряд ключевых механизмов патофизиологического каскада (рис. 2).
В поддержку этого утверждения в настоящее время проводится новое клиническое исследование, в котором изучается неринетид (ESCAPE-NA1) [4] — многообещающий препарат, который ранее уже продемонстрировал нейропротективные эффекты на этапе доклинических исследований и в исследовании II фазы, включающем пациентов с ишемическим инсультом (стратифицированных по тромболитическому лечению), с сохранением коллатералей хорошей или умеренной степени выраженности (оценивались с помощью многофазной КТ-ангиографии). Неринетид достоверно не улучшал функциональную независимость (показатель по модифицированной шкале Рэнкина (mRS) 0–2) в исследуемой популяции (по сравнению с плацебо), и результаты исследования дали основание предположить, что причиной отсутствия терапевтического эффекта был нейтрализующий эффект альтеплазы. Альтеплаза вызывала достоверное снижение уровня неринетида у всех пациентов, которым был проведен тромболизис, что приводило к ингибированию лечебного эффекта. Этот наиболее свежий пример исследования нейропротекции подтверждает важность как современных диагностических методов, так и выбора адекватных терапевтических средств для успешной нейропротекции при инсульте.
Список литературы
1. Lancet. 2014. № 384. Р. 1929-1935.
2. Lancet. 2019 Jul 13. № 394(10193). Р. 139-147.
3. BMJ. 2016. № 353. i1754.
4. Lancet. 2020 March 14. Vol. 395. Issue 10227. Р. 878-887.

/46_21.jpg)
/46_22.jpg)