Резюме
Актуальність. Істотне розширення розуміння ролі вітаміну D в організмі, більш ефективне виявлення целіакії та необхідність моніторингу стану здоров’я дітей на фоні тривалого дотримання безглютенової дієти послужили передумовами до виконання нашого дослідження. Мета дослідження — проаналізувати рівень вітаміну D у дітей, хворих на целіакію. Матеріали та методи. Проаналізовано результати обстеження 29 дітей віком від 6 місяців до 18 років із верифікованим діагнозом «целіакія». Рівні вітаміну D у сироватці крові вимірювали за допомогою електрохемілюмінесцентного методу (Roche Diagnostics GmBH, Мангейм, Німеччина). Результати забезпеченості вітаміном D пацієнтів із целіакією порівнювалися з показниками контрольної групи, яку становили 30 здорових дітей віком від 1 до 18 років. Математична обробка матеріалу включала стандартний алгоритм статистичних досліджень із використанням пакета програм Microsoft Excel 2016, Attestat. Результати. Серед включених у дослідження пацієнтів типова целіакія була встановлена у 24 (82,7 %) випадках, що у 4,8 раза частіше, ніж атипова — у 5 (17,4 %) дітей. У клінічній картині переважали гастроінтестинальні симптоми. Маніфестація захворювання у більшості хворих відзначалася на першому році життя — у 17 (58,6 %) випадках, у 7 (24,1 %) пацієнтів — у віці від 1 до 3 років і лише у 5 (17,4 %) дітей — після 3 років життя. Середній показник вітаміну D у дітей, хворих на целіакію, був вірогідно нижчий щодо показника у здорових дітей і становив 24,4 ± 1,2; 21,2 [16,45–35,21] нг/мл. Число дітей із нормальним умістом вітаміну D найбільше серед пацієнтів раннього віку, тоді як частота дефіциту вітаміну D — найменша. Медіана вітаміну D у сироватці крові пацієнтів, які суворо дотримуються безглютенової дієти, у 1,4 раза вища (p < 0,05), ніж у гострому періоді, але у 1,3 раза нижча (p < 0,05), ніж у контрольній групі. Дотримання безглютенової дієти призводить до підвищення рівня вітаміну D, але не дозволяє досягти рівня здорових дітей. Висновки. У дітей, хворих на целіакію, реєструється недостатність вітаміну D. Усі пацієнти з целіакією, незалежно від стадії захворювання та прихильності до безглютенової дієти, потребують проведення моніторингу забезпеченості вітаміном D.
Background. A significant increase in understanding of the role of vitamin D in the body, more effective detection of celiac disease, and the need to monitor the health of children against the background of long-term adherence to a gluten-free diet were prerequisites for our study. The study was aimed to analyze the level of vitamin D in children with celiac disease. Materials and methods. The results of the examination of 29 children aged from 6 months to 18 years with a verified diagnosis of celiac disease were analyzed. Serum vitamin D levels were measured by the electrochemiluminescent method (Roche Diagnostics GmBH, Mannheim, Germany). The results of vitamin D supplementation in patients with celiac disease were compared with the control group of 30 healthy children aged from 1 to 18. Mathematical processing of the material included a standard algorithm for statistical research using Microsoft Excel 2016, Attestat. Results. Among the patients included in the study, typical celiac disease was found in 24 (82.7 %) cases, which is 4.8 times more common than atypical — in 5 (17.4 %) children. The gastrointestinal symptoms dominated in a clinical picture. Manifestation of the disease in most patients was observed in the first year of life — in 17 (58.6 %) cases, in 7 (24.1 %) patients aged from 1 to 3 years, and only in 5 (17.4 %) children older than 3 years. The average rate of vitamin D in children with celiac disease was probably lower than in healthy children and accounted for 24.4 ± 1.2; 21.2 [16.45–35.21] ng/ml. The number of children with normal vitamin D content is the highest among young patients, while the frequency of vitamin D deficiency is the lowest. The median serum vitamin D in patients on a gluten-free diet was 1.4 times higher (p < 0.05) than in the acute period, but 1.3 times lower (p < 0.05) than in the control group. Adherence to a gluten-free diet leads to increased levels of vitamin D but does not allow reaching the level in healthy children. Conclusions. Vitamin D deficiency is registered in children with celiac disease. All patients with celiac disease, regardless of the stage of the disease and adherence to a gluten-free diet, need to be monitored for vitamin D levels.
Вступ
Серед спадкових форм синдрому мальабсорбції найчастіше трапляється целіакія, яка натепер розглядається як хронічне генетично-детерміноване автоімунне захворювання, що характеризується стійкою непереносимістю специфічних білків деяких злакових культур, які провокують розвиток оборотної атрофічної ентеропатії [1]. За даними [2], поширеність целіакії становить близько 1 %. В Україні коректних популяційних досліджень щодо поширеності целіакії та її клінічних форм не проводилося, отже, можемо орієнтуватися тільки на результати окремих клінічних досліджень.
Беручи до уваги той факт, що при целіакії площа ураження тонкого кишечника досить значна, у хворих часто відбувається порушення всіх видів обміну речовин та відзначається недостатнє надходження в організм нутрієнтів, у тому числі і остеотропних речовин. Атрофія ворсинок слизової оболонки тонкої кишки у хворих на целіакію знижує можливість всмоктування кальцію і вітаміну D, унаслідок чого розвивається гіпокальціємія і підвищується рівень паратиреоїдного гормону, активізуються остеокласти і кальцій вивільняється з кісткової тканини в кровоносне русло. У здорових дітей дефіцит кальцію та вітаміну D організм компенсує шляхом збільшення їх кишкового всмоктування, а при целіакії ця можливість суттєво обмежена [3], оскільки єдиним методом терапії непереносимості глютену з доведеною ефективністю на сьогодні є довічне виключення глютену з раціону харчування [4]. У пацієнтів із целіакією, які перебувають на тривалій безглютеновій дієті (БГД), покращується мінералізація кісткової тканини та знижується процес її резорбції.
Повсюдний науковий та практичний інтерес до вітаміну D супроводжується розширенням показань до обстеження та методик корекції гіповітамінозу D, який часто зустрічається у дітей із хронічними захворюваннями кишечника та синдромом мальабсорбції [5, 6]. Істотне розширення розуміння ролі вітаміну D в організмі, більш ефективне виявлення целіакії та необхідність моніторингу стану здоров’я дітей на фоні тривалого дотримання БГД, і тим більше при її недотриманні, послужили передумовами до виконання нашого дослідження.
Мета дослідження — проаналізувати рівень вітаміну D у дітей, хворих на целіакію.
Матеріали та методи
Проаналізовано результати обстеження 29 дітей і підлітків (14 хлопчиків та 15 дівчаток) віком від 6 місяців до 18 років (середній вік — 5,7 ± 0,29 року) із верифікованим під час стаціонарного обстеження на базі дитячого гастроентерологічного відділення КНП «Чернівецька обласна дитяча клінічна лікарня» відповідно до критеріїв ESPGHAN (1990, 2012 рр.) діагнозом «целіакія».
Методи діагностики целіакії включали три послідовні етапи [7]. На першому етапі проводили серологічні тести [8, 9], що включають визначення в сироватці крові імуноферментним аналізом антигліадинових антитіл (ATA) IgA та IgG (норма 0–12 U/ml), антитіл до тканинної трансглутаматпептидази (анти-ТТГ) IgA та IgG (норма < 10 U/ml) наборами фірми «Вектор-Бест» (Новосибірськ, Росія) та «Euroimmune» (Німеччина), антитіл до ендомізію (АЕМ) IgA та IgG (норма до 1 : 2,5) наборами фірми «IMMCO Diagnostics» (США). Другий етап включав проведення ендоскопічного дослідження дванадцятипалої і тонкої кишки зі взяттям біопсії слизової оболонки дванадцятипалої кишки та/або тонкої кишки з подальшим гістологічним дослідженням за Marsh з модифікаціями Oberhuber [10].
Рівні вітаміну D у сироватці крові вимірювали за допомогою електрохемілюмінесцентного методу (Roche Diagnostics GmBH, Мангейм, Німеччина). Сироватки, отримані центрифугуванням, зберігали при –20 °C і аналізували одночасно. Оцінка результатів проводилася відповідно до рекомендацій Міжнародного товариства ендокринологів (Holick M.F., 2011): дефіцит вітаміну D — менше ніж 20 нг/мл (менше ніж 50 нмоль/л); недостатність вітаміну D — 21–29 нг/мл (51–75 нмоль/л); нормальний вміст вітаміну D — 30–100 нг/мл (76–250 нмоль/л). Результати забезпеченості вітаміном D пацієнтів із целіакією порівнювалися з показниками контрольної групи, яку становили 30 здорових дітей віком від 1 до 18 років (середній вік 6,1 ± 0,4 року), серед яких 15 хлопчиків та 15 дівчаток. На момент обстеження діти контрольної групи не мали затримки фізичного розвитку та будь-яких гострих чи хронічних захворювань. Кожному пацієнту проведено клініко-анамнестичне обстеження, що включало збір та оцінку анкетних та антропометричних даних, а також лабораторно-інструментальне обстеження, що включало загальноклінічні дослідження (загальний аналіз крові, загальний аналіз сечі, копрологічне дослідження), біохімічне дослідження крові (визначення загального білка, кальцію, неорганічного фосфору).
Діти розподілені на три основні групи залежно від стадії захворювання та прихильності до БГД. У гострому періоді целіакії обстежено 7 (24,1 %) дітей, 12 (41,4 %) пацієнтів, які дотримуються суворої БГД (тривалість дієти в середньому 4,8 ± 0,9 року), та 10 (34,5 %) хворих, які не дотримуються дієти (у середньому 3,9 ± 0,8 року).
Математична обробка матеріалу включала стандартний алгоритм статистичних досліджень із використанням пакета програм Microsoft Excel 2016, Attestat. Для непараметричних кількісних даних визначалася медіана, 25-й та 75-й квартилі. Для параметричних кількісних значень обчислювалися середні арифметичні величини (M) та помилка середньої арифметичної величини (m). Визначення вірогідності відмінностей між двома порівнюваними групами у разі аналізу параметричних кількісних значень здійснювалося за допомогою t-критерію Стьюдента, у разі аналізу непараметричних кількісних даних — за допомогою критерію Вілкоксона та U-критерію Манна — Уїтні. Для оцінки зв’язків між кількісними даними був використаний критерій Пірсона із поправками для малих вибірок. З метою визначення кореляційної залежності між показниками були використані коефіцієнти парної кореляції Пірсона (r). Статистично вірогідними відмінності вважалися за р < 0,05.
Результати та обговорення
Серед включених у дослідження пацієнтів типова целіакія була встановлена у 24 (82,7 %) випадках, що у 4,8 раза частіше, ніж атипова — у 5 (17,4 %) дітей. У клінічній картині у більшості пацієнтів переважали гастроінтестинальні симптоми. Маніфестація захворювання у більшості хворих відзначалася на першому році життя — у 17 (58,6 %) випадках, у 7 (24,1 %) пацієнтів — у віці від 1 до 3 років і лише у 5 (17,4 %) дітей — після 3 років життя. Закономірно, що у дітей із типовою формою захворювання латентний період становив 1,1 ± 0,1 року, а з атиповою — 8,4 ± 0,9 року (р < 0,001). Відповідно, і вік верифікації діагнозу у них кардинально різниться. При типовій формі він становить 2,4 ± 0,3 року, а при атиповій — 10,1 ± 1,2 року (р < 0,001).
Структура симптомів наведена на рис. 1.
На першому місці знаходяться гастроінтестинальні симптоми. Клінічні прояви патології кісток та зубів за частотою займають друге місце, виявляючись у 58,6 % дітей у вигляді болі у кістках та множинного карієсу.
У пацієнтів із целіакією медіана вмісту загального кальцію та фосфору в сироватці крові перебувала в межах нормального (табл. 1).
Залежно від віку діти з целіакією поділені на групи раннього (0–3 роки), дошкільного (4–6 років) та шкільного (старше 7 років) віку. Забезпеченість вітаміном D у цих групах наведена на рис. 2.
Число дітей із нормальним умістом вітаміну D найбільше серед пацієнтів раннього віку, тоді як частота дефіциту вітаміну D в них найменша.
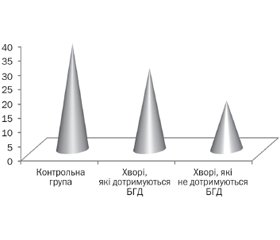
Із 29 дітей із целіакією БГД дотримувалися 5 хлопчиків та 7 дівчаток. Критерієм дотримання дієти, крім даних анамнезу, була відсутність діагностично значимого рівня специфічних антитіл класів IgA і IgG до тканинної трансглутамінази і навіть класів IgA і IgG до гліадину. Число пацієнтів, які не дотримуються дієти, становило 10 осіб, із них 5 хлопчиків та 5 дівчаток. Рівні вітаміну D здорових дітей та пацієнтів із целіакією залежно від періоду захворювання та дотримання БГД показані на рис. 3.
Медіана вітаміну D у сироватці крові пацієнтів, що суворо дотримуються БГД, у 1,4 раза вища (p < 0,05), ніж у гострому періоді, але у 1,3 раза нижча (p < 0,003), ніж у контрольній групі. Дотримання БГД призводить до підвищення рівня вітаміну D, але не дозволяє досягти рівня здорових дітей.
Відомо, що у патогенезі порушень фосфорно-кальцієвого обміну в дітей, хворих на целіакію, що призводять у результаті до розвитку остеопорозу, велику роль відіграє мальабсорбція в кишечнику остеотропних речовин [11]. Атрофія ворсинок слизової оболонки тонкої кишки у хворих на целіакію знижує можливість всмоктування кальцію і вітаміну D, унаслідок чого розвивається гіпокальціємія і підвищується рівень паратиреоїдного гормону [12], активізуються остеобласти і кальцій вивільняється з кісткової тканини в кровоносне русло. Зниження кальцифікації кісткової тканини клінічно може призвести до переломів навіть при невеликій травмі [12]. У хворих на целіакію ймовірність розвитку патологічних переломів вірогідно підвищена.
Кісткова тканина характеризується постійною метаболічною активністю, процес ремоделювання починається ще внутрішньоутробно і продовжується протягом усього життя людини [13]. Особливо вразливою перед несприятливими впливами, такими як зниження рухового режиму або недостатнє надходження остеотропних мікроелементів, кісткова тканина стає у періоди інтенсивного росту — у ранньому віці та пубертатному періоді. У здорових дітей дефіцит кальцію та вітаміну D у ці періоди життя організм компенсує шляхом збільшення їх кишкового всмоктування, а при целіакії ця можливість суттєво обмежена. Крім того, можливість споживання молока як цінного джерела кальцію у пацієнтів з целіакією також значно обмежена внаслідок зниженої активності дисахаридаз і насамперед лактази — ключового ферменту, що відповідає за переносимість вуглеводів молока [14–18].
Таким чином, діти з целіакією є групою ризику розвитку дефіциту остеотропних мікроелементів і вітаміну D.
Висновки
1. У дітей, хворих на целіакію, реєструється недостатність та дефіцит вітаміну D.
2. Усі пацієнти з целіакією, незалежно від стадії захворювання та прихильності до безглютенової дієти, потребують проведення моніторингу забезпеченості вітаміном D.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 01.12.2021
Рецензовано/Revised 15.12.2021
Прийнято до друку/Accepted 23.12.2021
Список литературы
1. Лашкова Ю.С. Профилактика и лечение дефицита витамина D: современный взгляд на проблему. Педиатрическая фармакология. 2015. 12(1). 46-51.
2. Yu X.B., Uhde M., Green P.H., Alaedini A. Autoantibodies in the extraintestinal manifestations of celiac disease. Nutrients. 2018. 10(8). 1123. doi: 10.3390/nu10081123.
3. Tye-Din J.A., Galipeau H.J., Agardh D. Celiac disease: a review of current concepts in pathogenesis, prevention, and novel therapies. Front. Pediatr. 2018. 6. 350. doi: 10.3389/fped.2018.00350.
4. Schumann M., Siegmund B., Schulzke J.D., Fromm M. Celiac disease: role of the epithelial barrier. Cell. Mol. Gastroenterol. Hepatol. 2017. 3(2). 150-162. doi: 10.1016/j.jcmgh.2016.12.006.
5. Miraglia Del Giudice M., Indolfi C., Strisciuglio C. Vitamin D: Immunomodulatory Aspects. J. Clin. Gastroenterol. 2018. 52(1). S86-S88. doi: 10.1097/MCG.0000000000001112.
6. Holick M.F. The death D-fying vitamin. Mayo Clin. Proc. 2018. 93(6). 679-681. doi: 10.1016/j.mayocp.2018.04.014.
7. Husby S., Koletzko S., Korponay-Szabo I., Kurppa K., Mearin M.L., Ribes-Koninckx C. [et al.]. European Society Paediatric Gastroenterology, Hepatology and Nutrition Guidelines for Diagnosing Coeliac Disease 2020. J. Pediatr. Gastroenterol. Nutr. 2019. 10. doi: 10.1097/MPG.0000000000002497.
8. Werkstetter K.J., Korponay-Szabó I.R., Popp A., Villanacci V., Salemme M., Heilig G., Lillevang S.T. [et al.]. Accuracy in Diagnosis of Celiac Disease Without Biopsies in Clinical Practice. Gastroenterology. 2017 Oct. 153(4). 924-935. doi: 10.1053/j.gastro.2017.06.002.
9. Popp A., Kivelä L., Fuchs V., Kurppa K. Diagnosing Celiac Disease: Towards Wide-Scale Screening and Serology-Based Criteria? Gastroenterol. Res. Pract. 2019. 2019. 2916024. doi: 10.1155/2019/2916024.
10. Marsh M.N., Johnson M.W., Rostami K. Rebutting Oberhuber — Again. Gastroenterol. Hepatol. Bed Bench. 2015. 8. 303-305. PMID: 26468353.
11. Бавыкина И.А., Звягин А.А., Гусев К.Ю. [и др.]. Обеспеченность нутриентами детей, длительно соблюдающих безглютеновую диету. Прикладные информационные аспекты медицины. 2017. 20(3). 33-39.
12. Duerksen D., Pinto-Sanchez M.I., Anca A. [et al.]. Management of bone health in patients with celiac disease: Practical guide for clinicians. Can. Fam. Physician. 2018. 64(6). 433-438.
13. Gatti S., Lionetti E., Balanzoni L. [et al.]. Increased Prevalence of Celiac Disease in School-age Children in Italy. Clinical Gastroenterology and Hepatology. 2020. 18(3). 596-603. https://doi.org/10.1016/j.cgh.2019.06.013.
14. Kotze L.M., Skare T., Vinholi A., Jurkonis L., Nisihara R. Impact of a gluten-free diet on bone mineral density in celiac patients. Rev. Esp. Enferm. Dig. 2016 Feb. 108(2). 84-8. doi: 10.17235/reed.2015.3953/2015.
15. Cashman K.D., van den Heuvel E.G., Schoemaker R.J. [et al.]. 25-Hydroxyvitamin D as a Biomarker of Vitamin D Status and Its Modeling to Inform Strategies for Prevention of Vitamin D Deficiency within the Population. Adv. Nutr. 2017. 8(6). 947-957. doi: 10.3945/an.117.015578.
16. Galior K., Grebe S.R., Singh Galior K. Development of vitamin D toxicity from overcorrection of vitamin D deficiency: a review of case reports. Nutrients.2018. 10(8). e953. DOI: 10.3390/nu10080953.
17. Lionetti E., Antonucci N., Marinelli M. [et al.]. Nutritional Status, Dietary Intake, and Adherence to the Mediterranean Diet of Children with Celiac Disease on a Gluten-Free Diet: A Case-Control Prospective Study. Nutrients. 2020. 12(1). 143. doi: 10.3390/nu12010143.
18. Zhu J., Mulder C.J.J., Dieleman L.A. Celiac Disease: Against the Grain in Gastroenterology. J. Can. Assoc. Gastroenterol. 2019. 2(4). 161-169. https://doi.org/10.1093/jcag/gwy042.
/15.jpg)

/14_2.jpg)
/14.jpg)