Вступ
Розлади аутистичного спектра (РАС) — це група гетерогенних нейропсихіатричних порушень, які є варіабельними за фенотипом і клінічно характеризуються дефіцитом соціальних взаємодій, порушенням комунікації та стереотипною поведінкою [18]. Сьогодні відбувається стрімке зростання частоти цієї тяжкої патології в дитячій популяції, причини чого досі недостатньо зрозумілі. Як зазначають H.K. Hughes зі співавт. у систематичному огляді щодо проблеми РАС, в США за період з 1972 по 2014 рік частота зареєстрованих випадків зазначеної нейропсихіатричної патології зросла з 1 випадку на 10 тисяч осіб (0,01 %) до 1 випадку на 57 дітей (2 %), тобто у 200 разів, що не можна пояснити лише підвищенням якості виявлення цієї патології сучасною медициною [25].
На сьогодні накопичені докази участі імунних механізмів в патогенезі РАС у дітей, що може відкрити шлях до апробації імунотерапевтичних втручань при цій тяжкій і поширеній хворобі. Так, продемонстрований зв’язок РАС з певними локусами антигенів гістосумісності HLA, так само як це відзначається і в низки автоімунних та алергічних синдромів людини [49]. У дітей із РАС описані різні форми імунодефіцитів [26, 51, 54], а дослідження, присвячені деяким первинним імунним дисфункціям, вказують на підвищений ризик розвитку аутизму в таких випадках [57, 64, 65]. Існують непоодинокі повідомлення про появу РАС у дорослих і дітей після перенесених епізодів нейроінфекцій, переважно опортуністичної природи [19, 24, 35]. У дітей із РАС виявляють різні автоантитіла до мозкових автоантигенів, що не утворюються у здорових осіб [8, 40, 61]. Більше того, результати низки клінічних досліджень вказують на користь від застосування імунотерапії в окремих пацієнтів із РАС [14, 21, 42]. Усі ці вагомі аргументи змушують звернути увагу на роль імунозалежних механізмів у патогенезі РАС у людей.
Важливим кроком у поглибленні розуміння участі імунозалежних розладів у розвитку нейропсихіатричних порушень є з’ясування асоціації генетичного дефіциту фолатного циклу (ГДФЦ) і РАС у дітей, докази якої наведені в результатах щонайменше 5 метааналізів рандомізованих контрольованих клінічних досліджень [29, 38, 48, 50, 55]. Охарактеризовані специфічні біохімічні порушення, зумовлені ГДФЦ [20, 67], що призводять до патологічних відхилень у функціонуванні імунної системи з формуванням особливого імунодефіциту, ядро якого становить дефіцит природних кілерів (NK) і природних кілерних Т-лімфоцитів (NKТ), а також знижена активність мієлопероксидази нейтрофілів [33]. Видається очевидним, що саме цей імунодефіцит за посередництвом зниження імунорезистентності та індукції стану імунної дисрегуляції відповідальний за розвиток енцефалопатії з клінічними проявами РАС, яка, найбільш імовірно, має імунозалежний запальний механізм розвитку. Сьогодні відомі щонайменше 3 різних імуноопосередкованих механізми ураження центральної нервової системи (ЦНС) при ГДФЦ, зумовлених персистуючою імунною дисфункцією, що роблять суттєвий внесок у формування енцефалопатії з клінічною картиною РАС. Йдеться про розвиток нейротропних опортуністичних та умовно-патогенних інфекцій [35, 41], автоімунних реакцій щодо автоантигенів нейронів і мієліну півкуль великого мозку [8, 61], системного та пов’язаного з цим інтрацеребрального асептичного запалення з нейротоксичною дією [36, 56].
Пригнічення або усунення імунозалежних механізмів пошкодження ЦНС видається перспективною стратегією лікування РАС у дітей з ГДФЦ [9]. Зокрема, вважають, що супресія автоімунітету та нейронів і мієліну ЦНС може суттєво покращити психічні функції хворих дітей. В цьому напрямку вже проведено низку клінічних досліджень. Зокрема, у повідомленнях про клінічні випадки і результатах невеликих випробувань показана користь від застосування глюкокортикостероїдів та деяких інших протизапальних агентів у дітей із РАС, механізм дії яких убачають саме в реалізації протизапальної дії та пригніченні антимозкового автоімунітету. Як зазначають J. Marchezan зі співавт. у систематичному огляді, присвяченому аналізу обмеженої доказової бази клінічних випробувань протизапальних ліків при РАС, всі апробовані дотепер препарати можна поділити на дві основні групи: а) засоби з первинною протизапальною та імуномодулюючою дією, до яких відносяться сульфорафан, целекоксиб, леналідомід, пентоксифілін, спіронолактон, лютеолін флавоноїдів, кортикостероїди, пероральний і внутрішньовенний імуноглобулін, клітинна терапія, діалізований екстракт лімфоцитів крові, міноциклін та піоглітазон; б) інші препарати, що призначаються за неімунологічними показаннями, проте справляють додатковий імуномодулюючий вплив, не пов’язаний з основним механізмом дії, зокрема рисперидон, вітамін D, омега-3 поліненасичені жирні кислоти, гінгко білоба, L-карнозин, N-ацетилцистеїн, та відновлення кишкової мікрофлори [34].
Проведено щонайменше 9 клінічних досліджень щодо випробування імуномодулюючого біологічного агента нормального внутрішньовенного (в/в) імуноглобуліну людини при РАС, що, як вважають, покращує психічні функції пацієнтів завдяки пригніченню інтрацеребрального запалення й автоімунних реакцій проти мозкових автоантигенів [5, 6, 11, 14, 21, 32, 37, 42, 46]. Нещодавно інфліксимаб, препарат моноклональних антитіл проти прозапальної молекули фактора некрозу пухлини альфа, продемонстрував ефективність щодо пригнічення проявів гіперактивності та гіпер-збудливості у дітей із РАС, асоційованими з ГДФЦ, у невеликому контрольованому клінічному дослідженні [30]. Відповідно до цього в іншому контрольованому клінічному випробуванні ритуксимаб, препарат моноклональних антитіл до молекули СD20 В-лімфоцитів, показав здатність призводити до сутєвого покращення психічного статусу дітей із РАС, асоційованими з ГДФЦ, шляхом пригнічення автоімунної реакції проти автоантигенів гіпокампів скроневих часток півкуль великого мозку [31].
Саме нормальний в/в імуноглобулін людини, який вже добре зарекомендував себе у лікуванні різних автоімунних та імунозапальних хвороб людини в неврології та ревматології [7], видається найперспективнішою стратегією лікування імунозалежної запальної енцефалопатії в дітей із ГДФЦ завдяки великій широті терапевтичної дії та гарній переносимості. Раніше вже були опубліковані результати невеликого контрольованого клінічного випробування 6-місячної високодозової в/в імуноглобулінотерапії в дітей із РАС, асоційованими з ГДФЦ, які продемонстрували суттєве покращення за всіма кінцевими точками дослідження наприкінці курсу імунотерапії [32]. Обнадійливі результати цього пілотного дослідження мають спонукати до проведення більшого клінічного випробування з більшою кількістю учасників. Досі достеменно не уточнений механізм впливу імуноглобулінотерапії при РАС, так само як і точно не встановлені підгрупи пацієнтів, які потенційно можуть позитивно відповідати на імунотерапію. Є обґрунтовані підстави припускати, що пацієнти з РАС, асоційованими з ГДФЦ, і є тією специфічною підгрупою, яка належним чином відповідає на в/в імуноглобулінотерапію, що потрібно перевірити у спеціально спланованих контрольованих клінічних дослідженнях.
Мета дослідження: оцінити ефективність і безпечність 6-місячного курсу високодозової імуноглобулінотерапії при імунозалежній енцефалопатії з клінічною картиною РАС у дітей із ГДФЦ.
Матеріали та методи
Для досягнення поставленої мети ретроспективно проаналізовані дані медичних карток 225 дітей віком від 2 до 9 років із ГДФЦ, в яких відзначалися клінічні появи РАС (183 хлопчики і 42 дівчинки). Усі вони були пацієнтами спеціалізованої нейроімунологічної клініки Vivere (реєстраційне досьє від 22.12.2018 № 10/2212-М). Отримання даних для дослідження та обробка матеріалу проводилися згідно з договором № 150221 від 15.02.2021 р. та висновком комісії біоетичної експертизи (протокол № 140 від 21.12.2020 р. НМУ імені О.О. Богомольця). Клінічний діагноз РАС був встановлений дитячими психіатрами за критеріями DSM-IV-TR (Diagnostic and Statistical Manual of mental disorders) та ICD-10 (The International Statistical Classification of Diseases and Related Health Problems).
Патогенні поліморфні варіанти генів фолатного циклу визначали методом полімеразної ланцюгової реакції (ПЛР) з рестрикцією («Сінево», Україна) на підставі виявлення заміни нуклеотидів MTHFR C677T у моноформі (68 пацієнтів), а також у поєднанні з іншими замінами нуклеотидів — MTHFR A1298C, MTRR A66G і/або MTR A2756G (157 осіб). Ці особи становили досліджувану групу (ДГ). Таким дітям, окрім конвенційних освітніх програм, призначали препарати нормального в/в імуноглобуліну людини у дозі 2 г/кг/міс 1 раз на 30 днів протягом 6 місяців поспіль. Уведення в/в імуноглобуліну здійснювали за 3–5 суміжних діб зі швидкістю 20–25 крапель на хвилину, а інтервали між курсами імунотерапії становили від 27 до 25 діб відповідно.
До контрольної групи (КГ) увійшли 50 дітей (36 хлопчиків та 14 дівчаток) аналогічного вікового розподілу, які також страждали на ГДФЦ та РАС відповідної тяжкості. Ці пацієнти не отримували в/в імуноглобулінотерапію, а проходили тільки конвенційні реабілітаційні заходи, що включали роботу з логопедами/дефектологами, спеціально навченими педагогами, психіатрами та фізіотерапевтами.
Динаміку психічних симптомів РАС протягом даного клінічного дослідження у групах спостереження оцінювали за допомогою шкали Aberrant Behavior Checklist (АВС) [1].
Усім пацієнтам проводилось комплексне імунологічне обстеження в Інституті імунології та алергології НМУ імені О.О. Богомольця і/або лабораторії «Сінево», яке, крім загального аналізу крові, включало вивчення субпопуляційного складу лімфоцитів із використанням лазерної проточної цитофлуориметрії (цитофлуориметр Epics Xl, США) і методу непрямої імунофлуоресценції з моноклональними антитілами до CD-маркерів із двома або трьома мітками (CD3+, CD3+CD4+, CD3+CD8+, CD3–CD19+, CD3–CD16+CD56+, CD3+CD16+CD56+) (реактиви Beckman Coulter, США). Фагоцитоз оцінювали за даними латекс-тесту з визначенням показника фагоцитозу, фагоцитарного індексу, кількості активних фагоцитів і фагоцитарної ємності крові, а також за активністю ферментів мієлопероксидази (проточна цитофлуориметрія) і НАДФ-оксидази (НСТ-тест). Сироваткові концентрації імуноглобулінів основних класів (М, G, А) визначали за результатами простої радіальної імунодифузії за Манчіні та твердофазного ІФА. Концентрацію класів IgE, IgD та субкласів IgG (IgG1, IgG2, IgG3, IgG4) у сироватці крові вимірювали за допомогою твердофазного імуноферментного аналізу («ВекторБЕСТ», РФ; MDI Limbach Berlin GmbH, Німеччина).
Крім цього, проводилася діагностика реактивованої вірусної інфекції за результатами кількісної ПЛР лейкоцитів крові з видоспецифічними праймерами герпесвірусів (вірусів простого герпесу 1-го і 2-го типів (HSV-1 і HSV-2), вірусу варицела зостер (VZV), вірусу Епштейна — Барр (EBV), цитомегаловірусу (CMV), вірусів герпесу людини 6, 7 і 8-го типів (HHV-6, HHV-7, HHV-8), вірусів кору і краснухи (реактиви «ДНК-Технологія», РФ).
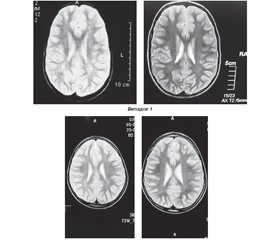
Всі діти проходили контрольну МРТ головного мозку в конвенційних режимах (Т1- і Т2-зважений, FLAIR) на томографах з величиною магнітної індукції не менше 1,5 Тл щонайменше двічі: до початку та після завершення участі в дослідженні. Типовими були ознаки лейкоенцефалопатії різної тяжкості. Також у 46 % випадків спостерігалась додаткова МР-картина скроневого медіанного склерозу (temporal mesial sclerosis). Переважно такі діти страждали на епілептичний синдром і мали когнітивні порушення. У 17 % випадків відзначалися типові ознаки вродженої цитомегаловірусної нейроінфекції у вигляді вентрикуломегалії, перивентрикулярних кальцинованих вогнищ, кіст у полюсах скроневих часток, гіпогенезії мозолистого тіла і зон затримки мієлінізації в тім’яних частках півкуль великого мозку. Ці дані відповідають результатам 18-річного ретроспективного дослідження R. Pinillos-Pisón зі співавт. [44]. Такі діти переважно мали симптоми ураження пірамідних і мозочкових шляхів, у зв’язку з чим їм нерідко встановлювали діагноз дитячого церебрального паралічу, хоча при цьому також спостерігалися прояви РАС.
Критеріями включення пацієнта у дане дослідження були наявність поліморфізмів генів фолатного циклу, дефіциту NK- і/або NKT-клітин, реактивованої інфекції, викликаної лімфотропними герпесвірусами, ознак лейкоенцефалопатії на МРТ головного мозку, клінічних симптомів РАС згідно зі шкалою АВС. Критеріями виключення пацієнта з даного дослідження були відмова батьків дитини від використання медичної документації у дослідженні, наявність додаткової верифікованої генетичної патології, причетної до розвитку картини наявних психічних порушень, відсутність фенотипу дефіциту NK- і/або NKT-клітин та ознак лейкоенцефалопатії, а також розвиток побічних ефектів імунотерапії, які унеможливлювали продовження апробованого лікування згідно з планом. Кінцевими точками дослідження були основні клінічні прояви розладів РАС за шкалою АВС, дані МРТ головного мозку в конвенційних режимах, абсолютна кількість NK- і NKT-клітин у периферичній крові, поточне вірусне навантаження лімфотропними герпесвірусами за даними ПЛР лейкоцитів крові, а також динаміка основних додаткових клінічних проявів, асоційованих з ГДФЦ, включно з PANS/PITANDS/PANDAS (pediatric acute-onset neuropsychiatric syndrome/pediatric infection-triggered autoimmune neuropsychiatric disorder/pediatric autoimmune neuropsychiatric disorders associated with streptococcal infections), кишковим синдромом (персистуючими імунозапальними ентеропатією/колітом), скроневою медіанною епілепсією, асоційованою зі скроневим медіанним склерозом (TME-TMS), і клінічними симптомами ураження пірамідних і мозочкових рухових шляхів ЦНС.
Статистичний аналіз отриманої інформації оброблений з використанням методів структурного і порівняльного аналізів за допомогою електронної програми Microsoft Excel. Для вивчення розподілу варіант у варіаційному ряді використовували тест Shapiro-Wilk. З метою встановлення вірогідності відмінностей результатів застосовували T-критерій Стьюдента з розрахунком коефіцієнта довірчої ймовірності р (параметричний критерій) і кількість знаків Z за Урбахом (непараметричний критерій). Вірогідними вважали відмінності при р < 0,05 і Z < Z0,05.
Дослідження виконувалось як фрагмент науково-дослідної роботи на замовлення МОЗ України (номер держреєстрації 0121U107940).
Результати та обговорення
Нормальний в/в імуноглобулін людини у високій дозі виявився ефективним для зменшення клінічних симптомів РАС за показниками шкали АВС у 199 із 225 дітей ДГ (88 % випадків; відповідачі на імунотерапію), однак вираженість досягнутого позитивного клінічного ефекту, так само як і стійкість отриманого прогресу в психомовленнєвому розвитку дитини, варіювала в різних пацієнтів (табл. 1, рис. 1). Резистентність до проведеної імунотерапії з боку проявів РАС серед дітей ДГ відзначалась відповідно в 12 % випадків (невідповідачі на імунотерапію).
/34.jpg)
/34_2.jpg)
Значне зменшення аутистичних симптомів (щонайменше на 50 % від вихідного рівня) з наявністю вираженого дефіциту знань і вмінь у дитини відзначалось у 61 випадку серед дітей ДГ (27 % випадків; сильні відповідачі). Частковий регрес досягнень у психомовленнєвому розвитку дитини після відміни імунотерапії мав місце лише в п’яти пацієнтів із підгрупи сильних відповідачів на в/в імуноглобулін (8 % випадків). Інші діти розвивалися нормально і досягли рівня однолітків через 3–5 років після курсу імунотерапії під впливом немедикаментозного лікування, включаючи заняття з логопедом, педагогами загального профілю, психіатрами і психотерапевтами. Помірний регрес аутистичних проявів (на 30–50 % від вихідного рівня) спостерігався у 83 випадках серед дітей ДГ (37 % випадків; середні відповідачі), дозволяючи пацієнтам суттєво розширити діапазон поточної соціальної адаптації. 32 дитини із числа середніх відповідачів (39 % випадків цієї підгрупи) продовжили демонструвати позитивну динаміку зменшення психічних розладів після завершення імуноглобулінотерапії під впливом реабілітаційних заходів. Інші діти (61 % випадків цієї підгрупи) зберігали суттєві аутистичні риси через 2–3 роки після імунотерапії. Очевидно, проведений 6-місячний курс імунотерапії виявився для них занадто коротким, а подальшої позитивної динаміки психічних розладів можна було б досягти при кількаразовому повторенні аналогічних курсів високодозової в/в імуноглобулінотерапії за рахунок кумулятивного ефекту. Проте 55 дітей ДГ (24 % випадків; слабкі відповідачі) відповіли лише невираженою позитивною динамікою з боку наявних психічних порушень за типом РАС (покращення не більше як на 20 % від вихідного рівня) після проходження повного курсу імунотерапії. У половини з цих слабких відповідачів відзначалась втрата досягнень у психомовленнєвому розвитку вже через 2–4 місяці після завершення в/в імуноглобулінотерапії, та, очевидно, вони потребували багаторазового повторення курсів імунотерапії в майбутньому для досягнення належного клінічного результату.
Серед дітей КГ слабка або помірна позитивна динаміка з боку основних клінічних симптомів РАС за шкалою АВС у кінці періоду спостереження мала місце в 12 з 51 особи (24 % випадків) і, очевидно, була відображенням природного перебігу захворювання і/або проведених рекомендованих реабілітаційних заходів (p < 0,05; Z < Z0,05). У жодної дитини з КГ у кінці періоду спостереження не зареєстровано скорочення клінічного фенотипу РАС на 50 % і більше від вихідного рівня за шкалою АВС протягом 6-місячного періоду спостереження (p < 0,05; Z < Z0,05).
Отримані дані дозволяють говорити про виражений позитивний модифікуючий вплив високодозової в/в імуноглобулінотерапії на психічний розвиток дітей із РАС, асоційованими з ГДФЦ (рис. 2, табл. 1).
Клінічну ефективність препаратів нормального в/в імуноглобуліну людини при РАС у дітей пов’язують як із прямою нейтралізацією циркулюючих у крові таких пацієнтів антимозкових автоантитіл екзогенними молекулами IgG імунобіологічного агента, так і з непрямим ефектом, обумовленим пригніченням опосередкованої Т-клітинами активації автореактивних В-лімфоцитів, комітованих до синтезу антимозкових автоантитіл [9], хоча в даному клінічному дослідженні ми виявили додаткові механізми позитивного впливу застосовуваної імунотерапії при РАС, про які йтиметься нижче.
Раніше вже повідомлялось про користь від застосування нормального в/в імуноглобуліну людини при РАС у дітей. При цьому застосовували різні дози зазначеного імунобіологічного препарату і режими імунотерапії, які, як сьогодні видається очевидним, суттєво відрізняються за клінічною ефективністю.
Так, A.V. Plioplys уперше провів невелике неконт-рольоване клінічне дослідження за участю 10 дітей (2 дівчинки і 8 хлопчиків) віком від 4 до 17 років, які страждали на РАС. Пацієнти отримували низькодозову імунотерапію нормальним в/в імуноглобуліном людини (у дозі 200–400 мг/кг) кожні 6 тижнів у вигляді чотирьох курсів протягом 5 місяців поспіль. Тільки в однієї дитини із групи спостереження відзначався виражений регрес проявів РАС після курсу імунотерапії. Ще в 4 пацієнтів, які отримали в/в імуноглобулін, мало місце невелике покращення з боку психічних розладів, однак інші 5 дітей виявилися резистентними до лікування [46]. G. DelGiudice-Asch зі співавт. вивчали ефективність низькодозової імунотерапії у відкритому пілотному дослідженні за участю 5 дітей із клінічною картиною РАС. Препарат нормального в/в імуноглобуліну людини призначали в дозі 400 мг/кг на місяць протягом півроку. Із 10 застосованих шкал оцінки тяжкості клінічних симптомів РАС тільки шкала Ritvo-Freeman демонструвала позитивну динаміку клінічних показників психічного статусу протягом курсу імунотерапії [14]. S. Gupta вивчав ефективність низькодозової імуноглобулінотерапії у 10 дітей віком 3–12 років із РАС у відкритому пілотному клінічному дослідженні. Імунобіологічний препарат призначали в дозі 400 мг/кг кожні 4 тижні протягом 6 місяців поспіль. Поліпшення з боку симптомів РАС відзначалося майже в усіх випадках, причому реєструвалось як дослідником, так і фахівцями з поведінкових і мовленнєвих розладів, батьками і медсестрами, які здійснювали інфузії препарату. Діти раннього віку реагували на імунотерапію краще, ніж пацієнти старших вікових груп [21]. Н. Niederhofer зі співавт. провели невелике подвійне сліпе плацебо-контрольоване перехресне клінічне дослідження за участю 12 хлопчиків віком від 4,2 до 14,9 року з РАС. Пацієнти отримували низькодозову терапію нормальним в/в імуноглобуліном людини одноразово (400 мг/кг).
Продемонстроване покращення за основними критеріями шкали ABC: гіперзбудливість, гіперактивність, неадекватний зоровий контакт, невідповідне мовлення [42]. M. Boris зі співавт. провели ретроспективне дослідження ефективності імунотерапії у 27 дітей із РАС (21 хлопчик і 6 дівчаток). Пацієнти отримували нормальний в/в імуноглобулін людини у дозі 400 мг/кг кожні 4 тижні протягом 6 місяців поспіль. Для контролю динаміки показників психічного статусу використовували шкалу АВС. Майже в усіх учасників даного дослідження відзначалось істотне покращення за досліджуваними показниками, що характеризують РАС: гіперактивністю, невідповідним мовленням, гіперзбудливістю, млявістю і стереотипіями. Проте у 22 із 26 дітей, які відповіли на імунотерапію, спостерігалось повернення багатьох усунених симптомів РАС через 2–4 місяці після завершення курсу в/в імуноглобуліну [5].
Таким чином, накопичені дотепер докази свідчать, що низькодозова імуноглобулінотерапія (400 мг/кг/міс) дає непостійний, помірний і, очевидно, недовготривалий позитивний клінічний ефект при РАС у дітей.
Перше неконтрольоване клінічне дослідження, в якому вивчалась ефективність високодозової імуноглобулінотерапії, показало більш обнадійливі результати. 13 дітей із РАС віком від 2,7 до 10,9 року (10 хлопчиків і 3 дівчаток) отримували нормальний в/в імуноглобулін людини у дозі 1,5–2,0 г/кг/міс. Відзначалось виражене покращення поведінки, мовлення, функції соціальної інтерференції в усіх учасників, причому у двох дітей мало місце повне усунення фенотипу аутизму. На відміну від низькодозового режиму, не відзначалось втрати досягнень у психомовленнєвому розвитку після завершення курсу імунотерапії [6].
В подальшому I.R. Melamed зі співавт. провели неконтрольоване пілотне клінічне дослідження високодозової в/в імуноглобулінотерапії (1 г/кг/міс) 14 пацієнтам із РАС у вигляді 10 курсів з інтервалом 1 раз на 3 тижні, отримавши позитивну динаміку щодо неадекватної поведінки, соціальної інтерференції та комунікації згідно з даними шкал оцінки тяжкості клінічних проявів РАС Children’s Communication Checklist (CCC-2), Social Responsiveness Scale (SRS), ABC, Clinical Global Impressions-Severity (CGI-S) і Clinical Global Impressions-Improvement (CGI-I), Autism Diagnostic Observation Schedule (ADOS) та Peabody Picture Vocabulary Test (PPVT). Паралельно відзначалося зниження рівня лабораторних біомаркерів церебрального запалення, таких як CD154, Toll-like receptor-4, B-клітини пам’яті, FOXP3 і результати тесту стимуляції лімфоцитів [37].
Згідно з цим K. Connery зі співавт. здійснили контрольоване клінічне дослідження за участю 82 пацієнтів із РАС з ознаками автоімунної енцефалопатії за результатами панелі Каннінгема (наявність автоантитіл до дофамінових рецепторів 2-го типу та тубуліну нейронів). 49 із них додатково отримали нормальний в/в імуноглобулін людини у високій дозі, а 32 пацієнти — лише рекомендовані освітні програми. Покращення з боку хоча б одного показника шкал оцінки тяжкості РАС SRS та ABC відзначалось у 90 % випадків, тоді як поліпшення з боку 2 і більше показників — у 71 % випадків серед пацієнтів ДГ, що вірогідно відрізнялося від результатів КГ. Як і в попередньому дослідженні, не відзначався регрес отриманих навиків після відміни імунотерапії. Імуно-біологічний препарат не тільки зменшував прояви РАС, але й призводив до позитивної динаміки з боку інших імунозалежних симптомів хвороби [11].
Сьогодні найбільше за кількістю учасників проспективне контрольоване клінічне дослідження з апробації високодозової в/в імуноглобулінотерапії (2 г/кг/міс протягом 6 місяців поспіль) за участю 78 пацієнтів із РАС, асоційованими з ГДФЦ, та 32 аналогічних осіб, які не приймали нормальний в/в імуноглобулін людини, продемонструвало майже повне усунення клінічних проявів РАС у найближчій перспективі принаймні у третині випадків, а також виражене і стійке покращення симптомів РАС за даними шкали АВС ще в 40 % пацієнтів. Як демонструють результати даного дослідження, правильний відбір пацієнтів за наявністю ГДФЦ і асоційованих з ним клінічних і параклінічних проявів, включаючи лейкоенцефалопатію, дозволяє суттєво підвищити ефективність проведеної імунотерапії [32].
Результати проведених клінічних досліджень в галузі імуноглобулінотерапії РАС сьогодні узагальнені в даних систематичного огляду та метааналізу клінічних досліджень, підготовлених D.A. Rossignol, R.E. Frye зі співавт. в 2021 році. Проаналізовано 27 відповідних випробувань, із них 4 проспективних контрольованих (одне — подвійне сліпе плацебо-контрольоване), 6 проспективних неконтрольованих, 2 ретроспективних контрольованих і 15 ретроспективних неконтрольованих. Загальний клінічний результат апробації препаратів нормального в/в імуноглобуліну людини, за даними цього метааналізу, полягає в покращенні з боку спілкування, гіперзбудливості, гіперактивності, пізнання, уваги, соціальної взаємодії, зорового контакту, ехолалії, мовлення, реакції на команди, сонливості, зниженої активності, а в деяких випадках — і в повному усуненні симптомів РАС [52].
Дані цієї наукової роботи не увійшли до зазначеного метааналізу, однак повністю узгоджуються з його результатами. Результати презентованого дослідження відповідають даним попередніх чотирьох клінічних випробувань, що продемонстрували вищу ефективність високодозової в/в імуноглобулінотерапії у дітей із РАС [6, 11, 32, 37] порівняно з режимами низькодозового застосування в/в імуноглобуліну [5, 14, 21, 42, 46] зі збереженням отриманих досягнень у психічному розвитку дитини після завершення курсу імунотерапії.
Щодо інших клінічних проявів ГДФЦ, то усунення або виражене пригнічення симптомів PANS/PITANDS/PANDAS мало місце у 27 із 32 % випадків в ДГ, тоді як в КГ не спостерігалося позитивної динаміки екстрапірамідних розладів і обсесивно-компульсивного синдрому в усіх дітей з проявами автоімунного субкортикального енцефаліту (p < 0,05; Z < Z0,05). Раніше у подвійному сліпому плацебо-контрольованому клінічному дослідженні була продемонстрована клінічна ефективність високодозової імуноглобулінотерапії при PANDAS у дітей, причому досягнутий результат відповідав такому у плазмаферезу [43].
Покращення з боку епілептичного синдрому, що полягало у зменшенні частоти/тяжкості епінападів і позитивній динаміці даних ЕЕГ, було досягнуто у 33 із 43 % випадків у пацієнтів ДГ, які мали вказані розлади, і лише у 12 із 40 % дітей КГ (p < 0,05; Z < Z0,05). L. Monge-Galindo зі співавт. у клінічному лонгітюдному дослідженні показали тісний зв’язок між РАС і скроневим медіанним склерозом у дітей [39]. Водночас нейротропний опортуністичний агент HHV-6, що часто зазнає реактивації в дітей із РАС, виявили у біоптатах із зони гіпокампального склерозу при TME-TMS [15], прояви якої нерідко реєструються в дітей з аутизмом. Раніше A. Plebani зі співавт. продемонстрували ефективність в/в імуноглобулінотерапії при рефрактерній дитячій епілепсії в пацієнтів із селективним дефіцитом субкласів IgG. Клінічний ефект імунотерапії пояснили поєднаною імунозамісною й імуномодулюючою дією імунобіологічного препарату [45]. Пізніше A.D. Billiau зі співавт. продемонстрували клінічну ефективність нормального в/в імуноглобуліну людини при рефрактерній епілепсії в дітей без урахування особливостей імунного статусу пацієнта [3].
Позитивна динаміка з боку клінічних проявів кишкового синдрому зареєстрована у 69 із 82 % випадків у ДГ, що підсилювало ефект призначеної раніше елімінаційної безглютенової/безказеїнової дієти. Водночас подальше покращення роботи кишечника спостерігалося тільки в 25 із 84 % випадків у КГ (p < 0,05; Z < Z0,05). Раніше A.J. Russo зі співавт. описали ілеоцекальну лімфоїдну нодулярну гіперплазію в дітей із РАС, яка нагадувала добре відому лімфоцитарну нодулярну гіперплазію кишечника у пацієнтів з первинними імунодефіцитами [54]. Разом із тим F. Torrente зі співавт. охарактеризували імунозапальну тонкокишкову ентеропатію з епітеліальними депозитами білків комплементу та молекул IgG у дітей з регресивним аутизмом [63]. Ефективність нормального в/в імуноглобуліну людини щодо кишкового синдрому в дітей із РАС, асоційованими з ГДФЦ, можна пояснити відомим імуномодулюючим, протимікробним і протизапальним впливом імунобіологічного препарату, враховуючи встановлений імунозалежний механізм ураження кишечника в таких випадках. Раніше препарат перорального нормального імуноглобуліну показав клінічну ефективність при кишковому синдромі в дітей із РАС у проспективному пілотному дослідженні [58], хоча подальше плацебо-контрольоване клінічне випробування не підтвердило отриманого позитивного ефекту [22]. В даній науковій роботі продемонстрована клінічна ефективність системної високодозової імуноглобулінотерапії при персистуючій ентеропатії/коліті в дітей із РАС, асоційованими з ГДФЦ.
Рухові прояви зменшились тільки у 7 з 21 % випадків серед дітей ДГ і в 5 з 19 % у пацієнтів КГ (p > 0,05, Z > Z0,05) (табл. 2), що вказує на відсутність вірогідного позитивного впливу нормального в/в імуноглобуліну людини у високій дозі на симптоми ураження пірамідних і мозочкових провідникових шляхів нервової системи в дітей із РАС, асоційованими з ГДФЦ. Частково це можна пояснити тим, що нерідко наявні рухові симптоми були резидуальними явищами перенесеного раніше патологічного процесу, наприклад природженої цитомегаловірусної інфекції [16], тобто не були наслідком імуноопосередкованих реакцій у реальному часі. Проте в деяких пацієнтів з ДГ відзначався драматичний позитивний ефект з боку рухових розладів після призначення нормального в/в імуноглобуліну людини, і ці пацієнти змогли самостійно ходити після тривалого періоду часткового знерухомлення.
Таким чином, нормальний в/в імуноглобулін людини в високій дозі (2 г/кг/міс) чинить комплексний полімодальний позитивний вплив у дітей із РАС, асоційованим з ГДФЦ, що полягає не тільки в усуненні або зменшенні розладів психіки за типом РАС, але й у поліпшенні з боку екстрапірамідних порушень, обсесивно-компульсивного синдрому, кишкових розладів та епілептиформної активності головного мозку. Такий широкий клінічний ефект застосованого імунобіологічного агента можна пояснити подібними імунозалежними механізмами розвитку на перший погляд різних за своєю природою клінічних проявів хвороби. Раніше про широкий клінічний фенотип, що включає епілепсію, кишкові порушення, автоімунні розлади, гіперчутливість сповільненого типу та дефіцит специфічних антиполісахаридних антитіл, при РАС у дітей повідомляли H. Jyonouchi зі співавт. в результатах спеціально спланованого дослідження [26].
Наявність множинних реактивованих вірусних інфекцій у дітей ДГ можна повністю пояснити наявним дефіцитом NK- і/або NKT-клітин. Раніше T. Binstock виділив особливу підгрупу дітей із РАС, в яких спостерігалася патологічно знижена резистентність до інтрамоноцитарних патогенів [4], а G.L. Nicolson зі співавт. виявили в таких дітей аномально підвищену частоту виявлення в крові ДНК Mycoplasma sрp., Chlamydia pneumoniae та HHV-6 [41]. Видається очевидним, що йшлося саме про випадки розладів РАС, асоційованих з ГДФЦ, при яких відзначається первинний дефіцит NK- і/або NKT-клітин. Вірусні агенти можуть індукувати затримку мієлінізації/демієлінізацію в головному мозку, як продемонстрували A. Kamei зі співавт. у разі первинної HHV-6-інфекції [27], а R. Pinillos-Pisón зі співват. — при реактивації CMV зі стану латентності [44]. Відповідно до цього існує низка описів розвитку фенотипу аутизму після перенесених вірусних енцефалітів у раніше психічно здорових людей [19, 24, 35].
Крім того, шляхом механізму молекулярної мімікрії віруси можуть бути причетними до феномена продукції антимозкових автоантитіл у дітей із РАС. Так, V.K. Singh зі співавт. продемонстрували стійку асоціацію наявності вірусу кору або HHV-6 у реактивованому стані та продукції автоантитіл до мозкових антигенів у дітей із РАС, в тому числі й до мієліну білої речовини півкуль великого мозку [60]. В іншому дослідженні показана перехресна реактивність між антикоровими антитілами та автоантитілами до основного білка мієліну в дітей із РАС [59].
З огляду на ці дані ми вважаємо вкрай корисним, що нормальний в/в імуноглобулін людини в високій дозі призводив до поступового, але неухильного зниження сумарного вірусного навантаження, обумовленого лімфотропними герпесвірусами, в лейкоцитах крові серед пацієнтів ДГ (рис. 3), чого не відбувалося в КГ (p < 0,05; Z < Z0,05).
На сьогодні нормальний в/в імуноглобулін людини рутинно застосовується для профілактики реактивованих опортуністичних вірусних інфекцій в імуноскомпрометованих осіб із рівнем доказовості А-С залежно від нозології. Так, J. Cowan зі співавт. нещодавно провели систематичний огляд контрольованих клінічних досліджень, присвячених вивченню ефективності імунотерапії для профілактики вірусних інфекцій у реципієнтів алогенних гемопоетичних клітин крові, продемонструвавши очевидну користь від застосування імунотерапії [12].
Також під час даного дослідження виявили поступове зростання раніше патологічно зниженої абсолютної кількості NK-клітин у периферичній крові пацієнтів ДГ, яке було відтермінованим і найсильніше проявлялось лише на 5–6-й місяць курсу імунотерапії (рис. 4). Раніше R.W. Finberg зі співавт. продемонстрували, що високодозова імуноглобулінотерапія сприяє зростанню функціональної активності NK-клітин у людей, найбільш імовірно, шляхом імуномодуляції за рахунок впливу на Fc-рецептори цих лімфоцитів [17]. Водночас використання середньо- і низькодозового режиму імунотерапії (400–800 мг/кг/міс) призводить, навпаки, до зниження кількості й активності природних кілерів, як це продемонстрували J.E. Ruiz зі співавт. у клінічному дослідженні за участю жінок із множинними епізодами спонтанних абортів, пов’язаними з імунною дисрегуляцією [53].
/38.jpg)
Окрім цього, застосовуваний нормальний в/в імуноглобулін людини сприяв компенсації гіпо- або дисімуноглобулінемії, що спостерігалася в багатьох дітей ДГ, тобто реалізовував імунозамісний ефект щодо гуморального компонента імунодефіциту, зумовленого ГДФЦ. Як відомо, препарати нормального в/в імуноглобуліну людини сьогодні рутинно застосовуються з замісною метою при лікуванні первинних гіпоімуноглобулінемій у людей з рівнем доказовості В [2]. Раніше L. Heuer зі співавт. встановили, що знижені рівні імуноглобулінів у крові при РАС тісно корелюють із тяжкістю клінічних проявів розладів психіки в дітей [23]. Таким чином, застосована високодозова імуноглобулінотерапія сприяла компенсації або принаймні субкомпенсації обумовленого ГДФЦ специфічного імунодефіциту в дітей ДГ шляхом імуномодуляції й імунного заміщення.
І, нарешті, під час даного клінічного дослідження була отримана виражена позитивна динаміка з боку тяжкості МР-ознак лейкоенцефалопатії, що відзначалась у більшості дітей із РАС. Раніше T. Strunk зі співавт. описали феномен аномально полегшеної демієлінізації провідників білої речовини півкуль великого мозку при ГДФЦ [62]. Повне або часткове усунення МР-ознак передіснуючої лейкоенцефалопатії спостерігалось в 69 із 88 % випадків у ДГ (рис. 5). Відсутність позитивних змін з боку МР-ознак лейкоенцефалопатії в кінці курсу імунотерапії, що були зареєстровані в 19 % випадків серед пацієнтів ДГ, виявилась асоційованою з незначним клінічним покращенням з боку проявів психічних розладів і високим ризиком повернення усунених симптомів РАС після припинення курсу імунотерапії. У КГ помірна позитивна динаміка з боку МР-ознак лейкоенцефалопатії відзначалась тільки в 15 із 83 % випадків (p < 0,05; Z < Z0,05) (табл. 2), що, очевидно, відображало природній перебіг хвороби. Отриманий позитивний нейрорадіолоігчний ефект імунотерапії можна пояснити антимікробними й імуномодулюючими властивостями нормального в/в імуноглобуліну людини, зокрема, продемонстрованою вище здатністю знижувати аномально високе мікробне навантаження, сформоване лімфотропними герпесвірусами, та здатністю пригнічувати автоімунні реакції проти автоантигенів мієліну ЦНС.
/39.jpg)
Відомо, що нормальний в/в імуноглобулін людини в високій дозі здатний стимулювати ремієлінізацію периферичних нервових волокон при синдромі Гієна — Барре і хронічній запальній демієлінізуючій полінейропатії (рівень доказовості А), що пов’язують із пригніченням під впливом імунобіологічного препарату автоімунної реакції, яка є основною патогенетичною ланкою при розвитку цих хвороб [7]. Однак
B. Cіrіc зі співавт. описали прямий стимулюючий вплив нормального в/в імуноглобуліну людини на процес ремієлінізації периферичних нервових волокон, не залежний від імуномодуляції, що, як вважають, пов’язаний із безпосереднім впливом молекул IgG препарату на Fc-рецептори шванівських клітин, які є продуцентами мієліну [10].
У даному клінічному дослідженні констатований виражений потенціюючий вплив високодозової в/в імуноглобулінотерапії на процес мієлінізації/ремієлінізації нервових провідників у білій речовині півкуль великого мозку в дітей із РАС, асоційованими з ГДФЦ, за даними МРТ головного мозку в конвенційних режимах. На нашу думку, саме цим індукованим імунотерапією нейрореабілітаційним феноменом значною мірою можна пояснити позитивний модифікуючий терапевтичний вплив проведеної імунотерапії на основні клінічні прояви РАС у дітей ДГ згідно зі шкалою АВС.
Досягнуті зміни з боку всіх кінцевих точок даного клінічного дослідження у групах спостереження підсумовані у табл. 2.
Нормальний в/в імуноглобулін людини зарекомендував себе під час даного клінічного дослідження як безпечний препарат із задовільною толерантністю. Транзиторний грипоподібний синдром під час інфузій цього імунобіологічного агента відзначався тільки в 74 із 225 пацієнтів ДГ (33 % випадків). У 29 дітей ДГ (13 % випадків) мали місце однократні епізоди блювання невдовзі після введення в/в імуноглобуліну. Ці помірні побічні ефекти не були перешкодою для продовження курсу імунотерапії. Інших небажаних явищ на фоні застосування нормального в/в імуноглобуліну людини серед дітей ДГ не було зареєстровано.
/40.jpg)
Раніше C.S. Price зі співавт. у спеціально спланованому клінічному дослідженні продемонстрували, що препарати нормального в/в імуноглобуліну людини безпечні та не сприяють розвитку аутизму в дітей [47]. Відповідно до цього L.A. Croen зі співавт. показали, що застосування антирезусного імуноглобуліну для профілактики гемолітичної хвороби плода також не підвищує ризик розвитку аутистичних розладів у дітей [13]. Як вказують J.L. Wynn зі співавт., застосування високодозової в/в імуноглобулінотерапії не тільки не пригнічує розвиток імунної системи дитини, але й сприяє пришвидшеному дозріванню незрілої імунної системи в недоношених дітей [66].
Висновки
Таким чином, констатовано факт високої клінічної ефективності й належної безпечності в/в імуноглобулінотерапії в дозі 2 г/кг/міс у дітей із РАС, асоційованими з ГДФЦ. Таке лікування призводить не тільки до усунення або принаймні послаблення наявних психічних порушень, але й до покращення з боку додаткових екстрапірамідних, епілептичних і кишкових розладів. Полімодальний позитивний клінічний ефект нормального в/в імуноглобуліну людини, очевидно, пов’язаний з добре відомою імунозамісною, імуномодулюючою, протимікробною і протизапальною дією препарату та асоційований із різким зниженням вірусного навантаження у крові, підвищенням раніше критично зниженої абсолютної кількості природніх кілерів і усуненням радіологічних проявів лейкоенцефалопатії в таких дітей. Раніше відзначили, що в пацієнтів із ГДФЦ, які страждають від РАС, має місце особливий первинний імунодефіцит, який, очевидно, і є безпосередньою причиною широкого клінічного фенотипу імунозалежних проявів, що охоплює психічні, екстрапірамідні, епілептичні, рухові, когнітивні, кишкові, інфекційні, автоімунні та алергічні синдроми, а також лейкоенцефалопатію. Нормальний в/в імуноглобулін людинии в високій дозі чинить комплексний (полімодальний) позитивний вплив на більшість компонентів широкого клінічного фенотипу в дітей із ГДФЦ. Цей лікувальний підхід сприяє компенсації або принаймні субкомпенсації різноманітних імунозалежних мозкових і позамозкових клінічних проявів первинного імунодефіциту, асоційованого з ГДФЦ, а не тільки зменшує симптоми РАС.
Чинні сьогодні клінічні рекомендації не підтримують застосування імуноглобулінотерапії при РАС у дітей [28], хоча ми твердо переконані, що така терапевтична стратегія може бути випробувана у багатьох пацієнтів з резистентністю до інших лікувальних підходів, особливо в дітей із ГДФЦ у разі позитивних клінічних, лабораторних та інструментальних біомаркерів імунозалежної запальної енцефалопатії. З огляду на обнадійливі результати даного ретроспективного аналізу клінічних випадків, доцільно продовжити дослідження в зазначеному напрямку з більшою кількістю учасників і досконалішим дизайном.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів і власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 26.11.2021
Рецензовано/Revised 08.12.2021
Прийнято до друку/Accepted 14.12.2021
Список литературы
1. Amman M.G., Singh N.N., Stewart A.W., Field C.J. Psychometric characteristics of the aberrant behavior checklist. Am. J. Ment. Def. 1985. Vol. 99. P. 492-502.
2. Baris S., Ercan H., Cagan H.H. Efficacy of intravenous immunoglobulin treatment in children. with common variable immunodeficiency. Immunol. 2011. Vol. 21(7). P. 514-521.
3. Billiau A.D., Witters P., Ceulemans B. et al. Intravevous immunoglobulins in refractory childhood-onset epilepsy: effects on seizure frequency, EEG activity and cerebrospinal fluid cytokine profile. Epilepsia. 2007. Vol. 48. P. 1739-1749.
4. Binstock T. Intra-monocyte pathogens delineate autism subgroups. Med. Hypotheses. 2001. – Vol. 56(4). P. 523-531.
5. Boris M., Goldblatt A., Edelson S.M., Edelson P.A.-C. Improvement in children with autism treated with intravenous gamma globulin. J. Nutr. Environ. Medicine. 2006. Vol. 15(4). P. 1-8.
6. Bradstreet J., Singh V.K., El-Dahr J. High dose intravenous immunoglobulin improves symptoms in children with autism. The international symposium on autism. 1999 Dec. 28. Atnhem, Netherlands.
7. Buchwald B., Ahangari R., Weishaupt A., Toyka K.V. Intravenous immunoglobulins neutralize blocking antibodies in Guillain-Barré syndrome. Annals of Neurology. 2002. Vol. 51. P. 673-680.
8. Cabanlit M., Wills S., Goines P. et al. Brain-specific autoantibodies in the plasma of subjects with autistic spectrum disorder. Ann. N. Y. Acad. Sci. 2007. Vol. 107. P. 92-103.
9. Chez G.M., Guido-Estrada N. Immune therapy in autism: historical experience and future directions with immunomodulatory therapy. Neurotherapeutists. 2010. Vol. 7. P. 293-301.
10. Ciric B., Van Keulen V., Paz Soldan M. et al. Antibody-mediated remyelination operates through mechanism independent of immunomodulation. J. Neuroimmunology. 2004. Vol. 146. P. 153-161.
11. Connery K., Tippett M., Delhey L.M., Rose S. Intravenous immunoglobulin for the treatment of autoimmune encephalopathy in children with autism. Transl. Psychiatry. 2018. Vol. 8(1). P. 148.
12. Cowan J., Camero n D.W., Knoll G., Tay J. Protocol for updating a systematic review of randomised controlled trials on the prophylactic use of intravenous immunoglobulin for patients undergoing haematopoietic stem cell transplantation. BMJ Open. 2015. Vol. 5(8). e008316.
13. Croen L.A., Matevia M., Yoshida C.K., Grether J.K. Maternal Rh D status, anti-D immune globulin exposure during pregnancy, and risk of autism. Spectrumdisorders. Am. J. Obstet. Gynecol. 2008. Vol. 99(3). P. 234.
14. DelGiudice-Asch G., Simon L., Schmeidler J. Brief report: a pilot open clinical trial of intravenous immunoglobulin in childhood autism. J. Autism Dev. Disord. 1999. Vol. 29(2). P. 157-160.
15. Donati D., Akhyani N., Fogdell-Hahn A. et al. Detection of human herpesvirus-6 in mesial temporal lobe epilepsy surgical brain resections. Neurology. 2003. Vol. 61(10). P. 1405-1411.
16. Engman M.L., Sundin M., Miniscalco C. Prenatal acquired cytomegalovirus infection should be considered in children with autism. Acta Paediatr. 2015. Vol. 104(8). P. 792-795.
17. Finberg R.W., Newburger J.W., Mikati M.A. et al. Effect of high doses of intravenously administered immune globulin on natural killer cell activity in peripheral blood. J. Pediatr. 1992. Vol. 120(3). P. 376-380.
18. Frye R.E. Metabolic and mitochondrial disorders associated with epilepsy in children with autism spectrum disorder. Epilepsy Behav. 2015. Vol. 47. P. 147-157.
19. Ghaziuddin M., Al-Khouri I., Ghоaziuddin N. Autistic symptoms following herpes encephalitis. Eur. Child. Adolesc. Psychiatry. 2002. Vol. 11(3). P. 142-146.
20. Guo B.Q., Li H.B., Ding S.B. et al. Blood homocysteine levels in children with autism spectrum disorder: An updated systematic review and meta-analysis. Psychiatry Res. 2020. Vol. 291. P. 113283.
21. Gupta S. Treatment of children with autism with intravenous immunoglobulin. J. Child. Neurol. 1999. Vol. 14(3). P. 203-205.
22. Handen B.L., Melmed R.D., Hansen R.L. et al. A double-blind, placebo-controlled trial of oral human immunoglobulin for gastrointestinal dysfunction in children with autistic disorder. J. Autism. Dev. Disord. 2009. Vol. 39(5). P. 796-805.
23. Heuer L., Ashwood P., Schauer J. et al. Reduced Levels of Immunoglobulin in Children With Autism Correlates With Behavioral Symptoms. Autism. Res. 2008. Vol. 1(5). P. 275-283.
24. Hiroshi H., Seiji K., Toshihiro K., Nobuo K. An adult case suspected of recurrent measles encephalitis with psychiatric symptoms. Seishin Shinkeigaku Zasshi. 2003. Vol. 105(10). P. 1239-1246.
25. Hughes H.K., Ko E.M., Rose D., Ashwood P. Immune Dysfunction and Autoimmunity as Pathological Mechanisms in Autism Spectrum Disorders. Front. Cell. Neurosci. 2018. Vol. 12. P. 405. doi: 10.3389/fncel.2018.00405.
26. Jyonouchi H., Geng L., Streck D.L., Toruner G.A. Immunological characterization and transcription profiling of peripheral blood (PB) monocytes in children with autism spectrum disorders (ASD) and specific polysaccharide antibody deficiency (SPAD): case study. J. Neuroinflammation. 2012. Vol. 9. P. 4.
27. Kamei A., Ichinohe S., Onuma R. et al. Acute disseminated demyelination due to primary human herpesvirus-6 infection. Eur. J. Pediatr. 1997. Vol. 156(9). P. 709-712.
28. Kooij S.J., Bejerot S., Blackwell A. et al. European consensus statement on diagnosis and treatment of adult ADHD: The European Network Adult ADHD. BMC Psychiatry. 2010. Vol. 10. P. 67.
29. Li Y., Qiu S., Shi J. et al. Association between MTHFR C677T/A1298C and susceptibility to autism spectrum disorders: a meta-analysis. BMC Pediatr. 2020. Vol. 20(1). P. 449.
30. Maltsev D., Natrus L. The effectiveness of infliximab in autism spectrum disorders associated with folate cycle genetic deficiency. Psychiatry, Psychotherapy and Clinical Psychologythis. 2020. Vol. 11(3). P. 583-594.
31. Maltsev D.V. Efficacy of Rituximab in Autism Spectrum Di-sorders Associated with Genetic Folate Cycle Deficiency with Signs of Antineuronal Autoimmunity. Psychiatry, Psychotherapy and Clinical Psychologythis. 2021. Vol. 12(3). P. 471-486.
32. Maltsev D.V. Efficiency of a high dose of intravenous immunoglobulin in children with autistic spectrum disorders associated with genetic deficiency of folate cycle enzymes. Journal of global pharma technology. 2019. Vol. 11(05). P. 597-609.
33. Maltsev D.V. Features of folate cycle disorders in children with ASD. Bangladesh Journal of Medical Sciencethis. 2020. Vol. 19(4). P. 737-742.
34. Marchezan J., Winkler Dos Santos E.A., Deckmann I., Dos Santos Riesgo R. Immunological Dysfunction in Autism Spectrum Disorder: A Potential Target for Therapy. Neuroimmunomodulation. 2018. Vol. 25(5–6). P. 300-319. doi: 10.1159/000492225.
35. Marques F., Brito M.J., Conde M. Autism spectrum disorder secondary to enterovirus encephalitis. J. Child Neurol. 2014. Vol. 29(5). P. 708-714.
36. Masi A., Quintana D.S., Glozier N. et al. Cytokine aberrations in autism spectrum disorder: a systematic review and meta-analysis. Mol. Psychiatry. 2015. Vol. 20(4). P. 440-446.
37. Melamed I.R., Heffron M., Testori A., Lipe K. A pilot study of high-dose intravenous immunoglobulin 5 % for autism: Impact on autism spectrum and markers of neuroinflammation. Autism Res. 2018. Vol. 11(3). P. 421-433.
38. Mohammad N.S., Shruti P.S., Bharathi V. et al. Clinical uti-lity of folate pathway genetic polymorphisms in the diagnosis of autism spectrum disorders. Psychiatr. Genet. 2016. Vol. 26(6). P. 281-286.
39. Monge-Galindo L., Pérez-Delgado R., López-Pisón J. Mesial temporal sclerosis in paediatrics: its clinical spectrum. Our experience gained over a 19-year period. Rev. Neurol. 2010. Vol. 50(6). P. 341-348.
40. Mostafa G.A., Al-Ayadhi L.Y. Increased serum levels of anti-ganglioside M1 auto-antibodies in autistic children: relation to the di-sease severity. J. Neuroinflammation. 2011. Vol. 25. P. 8-39.
41. Nicolson G.L., Gan R., Nicolson N.L., Haier J. Evidence for Mycoplasma ssp., Chlamydia pneunomiae, and human herpes virus-6 coinfections in the blood of patients with autistic spectrum disorders. J. Neurosci Res. 2007. Vol. 85(5). P. 1143-1148.
42. Niederhofer H., Staffen W., Mair A. Immunoglobulins as an alternative strategy of psychopharmacological treatment of children with autistic disorder. Neuropsychopharmacology. 2003. Vol. 28(5). P. 1014-1015.
43. Perlmutter S.J., Leitman S.F., Garvey M.A. et al. Therapeutic plasma exchange and intravenous immunoglobulin for obsessive-compulsive disorder and tic disorders in childhood. Lancet. 1999. Vol. 354(9185). P. 1153-1158.
44. Pinillos-Pisón R., Llorente-Cereza M.T., López-Pisón J. Congenital infection by cytomegalovirus. A review of our 18 years’ experience of diagnoses. Rev. Neurol. 2009. Vol. 48(7). P. 349-353.
45. Plebani A., Duse M., Tiberti S. Intravenous gamma-globulin therapy and serum IgG subclass levels in intractable childhood epilepsy. Monogr. Allergy. 1988. Vol. 23. P. 204-215.
46. Plioplys A.V. Intravenous immunoglobulin treatment of children with autism. J. Child. Neurol. 1998. Vol. 13(2). P. 79-82.
47. Price C.S., Thompson W.W., Goodson B. Prenatal and infant exposure to thimerosal from vaccines and immunoglobulins and risk of autism. Pediatrics. 2010. Vol. 126(4). P. 656-664
48. Pu D., Shen Y., Wu J. Association between MTHFR gene polymorphisms and the risk of autism spectrum disorders: a meta-analysis. Autism Res. 2013. Vol. 6(5). P. 384-392.
49. Puangpetch A., Suwannarat P., Chamnanphol M. et al. Significant Association of HLA-B Alleles and Genotypes in Thai Children with Autism Spectrum Disorders: A Case-Control Study. Dis. Markers. 2015. Vol. 2015. P. 724935.
50. Rai V. Association of methylenetetrahydrofolate reductase (MTHFR) gene C677T polymorphism with autism: evidence of genetic susceptibility. Metab. Brain Dis. 2016. Vol. 31(4). P. 727-735.
51. Reinert P., Moulias R., Goust J.M. Demonstration of cellular immunity deficiency limited to measles virus in 20 cases of subacute sclerosing leukoencephalitis. Arch. Fr. Pediatr. 1972. Vol. 29(6). P. 655-665.
52. Rossignol D.A., Frye RE. A Systematic Review and Meta-Analysis of Immunoglobulin G Abnormalities and the Therapeutic Use of Intravenous Immunoglobulins (IVIG) in Autism Spectrum Disorder. J. Pers. Med. 2021. Vol. 11(6). P. 488.
53. Ruiz J.E., Kwak J.Y., Baum L. et al. Intravenous immunoglobulin inhibits natural killer cell activity in vivo in women with recurrent spontaneous abortion. Am. J. Reprod. Immunol. 1996. Vol. 35(4). P. 370-37.
54. Russo A.J., Krigsman A., Jepson B., Wakefield A. Low serum myeloperoxidase in autistic children with gastrointestinal disease. Clinical and Experimental Gastroenterology. 2009. Vol. 2. P. 85-94.
55. Sadeghiyeh T., Dastgheib S.A., Mirzaee-Khoramabadi K. et al. Association of MTHFR 677C>T and 1298A>C polymorphisms with susceptibility to autism: A systematic review and meta-analysis. Asian J. Psychiatr. 2019. Vol. 46. P. 54-61.
56. Saghazadeh A., Ataeinia B., Keynejad K. et al. A meta-ana-lysis of pro-inflammatory cytokines in autism spectrum disorders: Effects of age, gender, and latitude. J. Psychiatr. Res. 2019. Vol. 115. P. 90-102.
57. Santaella M.L., Varela Y., Linares N., Disdier O.M. Prevalence of autism spectrum disorders in relatives of patients with selective immunoglobulin A deficiency. P.R. Health. Sci J. 2008. Vol. 27(3). P. 204-208.
58. Schneider C.K., Melmed R.D., Barstow L.E. et al. Oral human immunoglobulin for children with autism and gastrointestinal dysfunction: a prospective, open-label study. J. Autism. Dev. Disord. 2006. Vol. 36(8). P. 1053-1064.
59. Singh V.K., Lin S.X., Newell E., Nelson C. Abnormal measles-mumps-rubella antibodies and CNS autoimmunity in children with autism. J. Biomed. Sci. 2002. Vol. 9(4). P. 359-364.
60. Singh V.K., Lin S.X., Yang V.C. Serological association of measles virus and human herpesvirus-6 with brain autoantibodies in autism. Clin. Immunol. Immunopathol. 1998. Vol. 89(1). P. 105-108.
61. Singh V.K., Warren R.P., Odell J.D. et al. Antibodies to myelin basic protein in children with autistic behavior. Brain. Behav. Immun. 1993. Vol. 7(1). P. 97-103.
62. Strunk T., Gottschalk S., Goepel W. Subacute leukencephalopathy after low-dose intrathecal methotrexate in an adolescent hete-rozygous for the MTHFR C677T polymorphism. Med. Pediatr. Oncol. 2003. Vol. 40(1). P. 48-50.
63. Torrente F., Ashwood P., Day R. et al. Small intestinal enteropathy with epithelial IgG and complement deposition in children with regressive autism. Mol. Psychiatry. 2002. Vol. 7(4). P. 375-382.
64. Warren R.P., Odell J.D., Warren W.L. et al. Brief report: immunoglobulin A deficiency in a subset of autistic subjects. J. Autism. Dev. Disord. 1997. Vol. 27(2). P. 187-192.
65. Wasilewska J., Kaczmarski M., Stasiak-Barmuta A. et al. Low serum IgA and increased expression of CD23 on B lymphocytes in peripheral blood in children with regressive autism aged 3–6 years old. Arch. Med. Sci. 2012. Vol. 8(2). P. 324-331.
66. Wynn J.L., Seed P.C., Cotten C.M. Does IVIg administration yield improved immune function in very premature neonates? J. Perinatol. 2010. Vol. 30(10). P. 635-642.
67. Yektaş Ç., Alpay M., Tufan A.E. et al. Comparison of serum B12, folate and homocysteine concentrations in children with autism spectrum disorder or attention deficit hyperactivity disorder and healthy controls. Neuropsychiatr. Dis. Treat. 2019. Vol. 15. P. 2213-2219.
/34.jpg)
/35.jpg)

/34_2.jpg)
/38.jpg)
/39.jpg)
/40.jpg)