Пандемія коронавірусної інфекції (COVID-19) суттєво змінила психологічний фон, що впливає на здоров’я населення багатьох країн. Передусім йдеться про дію несподіваних, тривалих і комплексних психотравматичних чинників із високим ступенем невизначеності в оцінюванні розвитку ситуації, що впливають на адаптацію населення. Потреба швидкої психологічної перебудови в цих умовах з руйнуванням запланованого, появою нових вимог і завдань призвела до напруженості та тривоги у суспільстві.
Відомо, що в нормі тривога і страх мають захисний характер, мобілізуючи організм через активацію центральної нервової, ендокринної та імунної систем. В умовах загальної стресової ситуації переважають саме адаптаційні варіанти. Проте при особливій вираженості, тривалості та індивідуальній значущості психічні травми спричиняють розвиток тривожних, стресових і депресивних розладів [1].
Досі не зрозуміло, чи є основною причиною потенційних психічних розладів самі віруси або імунна відповідь на них. Інтерес становить той факт, що інтерлейкін-1 (ІЛ-1), ІЛ-6 і фактор некрозу пухлини альфа (ФНП-α) (цитокіни, які беруть участь в імунній відповіді проти грипу) підсилюють активацію системи «гіпоталамус — гіпофіз — надниркові залози» [2–5]. Інтерферон альфа також бере участь в імунній відповіді. Добре відомим побічним ефектом цього цитокіну є індукція депресивного розладу [6].
Цитокіни спричиняють виснаження триптофану, який є попередником серотоніну. Вони стимулюють індоламін-2,3-диоксигеназу, яка перетворює триптофан у кінуренін, що робить його недоступним для синтезу серотоніну [7, 8]. Є докази того, що зниження рівня триптофану і, відповідно, серотоніну відіграє роль у патогенезі депресивних розладів [9]. Під час вивчення можливості безпосереднього впливу вірусів на мозок з розвитком емоційних розладів необхідно брати до уваги той факт, що як віруси грипу, так і коронавіруси є потенційно нейротропними і були виділені з центральної нервової системи [10–14].
Масштаби психологічного дистресу у суспільстві, пов’язаного з пандемією коронавірусної інфекції, першими визначили китайські дослідники [15]. На початку пандемії майже у половини опитаних відзначалися помірні і виражені ознаки депресивних (16,5 %) або тривожних (28,8 %) розладів. Під час повторного опитування (через 4 тижні) не виявлено вірогідного зниження показників, що свідчить про стабільність цих реакцій. Найчастіше тривожно-депресивні стани спостерігалися у респондентів, які раніше мали ті чи інші психічні розлади [1].
Результати іншого інтернет-опитування населення Китаю (n = 7236) показали домінування симптомів генералізованого тривожного розладу (35,1 %) у популяції. Часто також спостерігалися симптоми депресії (20,1 %) і порушення сну (18,2 %). Психічні порушення частіше спостерігалися у молодому віці (до 35 років) [16].
Дослідження предикторів тривожних станів, які розвинулися у початковий період пандемії коронавірусної інфекції у Нідерландах у березні 2020 року, показало значення психологічних чинників фіксації на власному здоров’ї та ймовірності інфікування близьких, насамперед похилого віку. Окрім того, значним негативним предиктором розвитку тривоги був постійний пошук інформації у медіа-ресурсах, зокрема на радіо, телебаченні та в інтернеті. Автори роблять висновок, що чим більше є загрозливої, невизначеної і водночас сенсаційної інформації у медіа-ресурсах, тим більший ризик тривожних станів серед населення [17].
Виражений дистрес, що проявляється тривожною і депресивною симптоматикою, виявлено також у квітні 2020 року серед 6500 жителів Німеччини. Серед населення вираженість дистресу, визначеного за допомогою шкали PHQ-4, виявилася у 2,4 раза вище від нормальних показників [1]. Близько половини опитаних були фіксовані на повторних думках про можливі негативні наслідки пандемії. Водночас власний досвід контактів з інфекцією мав меншу значущість, ніж психологічні та соціальні чинники, які провокують симптоми тривоги і депресії.
Впевненість у своїх можливостях контролювати ситуацію, пов’язану з пандемією, соціальна підтримка і достатня інформованість щодо варіантів отримання допомоги у зв’язку з інфекцією були значущими захисними чинниками, що попереджають тривогу [18].
Дослідження поширеності симптомів психічних розладів серед дорослого населення США (n = 5470) у квітні — травні 2020 року показало, що є як мінімум одна ознака у 40,9 % респондентів. Серед них домінували симптоми тривожних розладів (25,5 %), які спостерігалися у 3 рази частіше, ніж за аналогічний період минулого року; ознаки депресії (24,3 %; у 4 рази частіше, ніж торік), розладів, пов’язаних з психічною травмою або стресором (26,3 %), а також початок або загострення залежностей від психоактивних речовин, зокрема й алкоголю (13,3 %). Окрім того, відзначено високу поширеність суїцидальних думок (10,7 %), які спостерігалися у 2 рази частіше, ніж за попередній рік, і були найбільш значущими для населення молодого віку (18–24 роки; 25,5 %). Загалом ознаки психічних розладів частіше спостерігалися серед населення молодого віку, яке не мало постійної зайнятості і доходів, а також мало в минулому психічні розлади [1, 19].
Метааналіз 17 досліджень симптомів тривожних і депресивних розладів серед населення різних країн вперше проведений іранськими вченими [20]. В аналізованих роботах використовували переважно шкалу стресу, тривоги і депресії (DASS-21). Частота тривоги відзначена у 31,9 % (95% довірчий інтервал (ДІ) 27,5–36,7), дещо частіше депресії — у 33,7 % (95% ДІ 27,5–40,6) і стресового стану — у 29,6 % (95% ДІ 24,3–35,4). Найбільша частота тривоги і депресії відзначена в азіатських країнах — 32,9 % (95% ДІ 28,2–37,9) і 35,3 % (95% ДІ 27,3–44,1), в Європі — стресового стану — 31,9 % (95% ДІ 23,1–42,2).
Порівняння психічного здоров’я до і після початку пандемії проведено у Великій Британії із застосуванням інтернет-опитування з використанням скринінгової шкали, яка визначає вираженість дистресу (GHQ-12), серед 42 330 респондентів. Під час порівняння з результатами опитувань 2018–2019 років відзначено збільшення середніх популяційних показників шкали з 11,5 (95% ДІ 11,3–11,6) до 12,6 (95% ДІ 12,5–12,8) у період ізоляції у квітні 2020 року. Найвираженіший дистрес відзначений у безробітних, незайнятих, а також у респондентів з низьким доходом. Під час аналізу статево-вікових відмінностей найбільша вираженість дистресу виявлена у жінок молодого (16–24 роки) віку (44 %; 95% ДІ 39,2–48,9) [21].
Попередні результати показують, що наявний тривожний або депресивний розлад практично не впливає на ризик зараження коронавірусною інфекцією. Результати національного дослідження у Південній Кореї показали подібні результати показників інфікування коронавірусною інфекцією серед хворих на психічні розлади і серед психічно здорових. Пацієнти з психічними розладами мали дещо гірший прогноз щодо результатів інфекції (відношення шансів 1,27; 95% ДІ 1,01–1,66). Серед пацієнтів з вираженими психічними розладами, переважно з психозами, ризик негативних наслідків виявився набагато (у 2,3 раза) вищим, ніж у психічно здорових [1, 22].
Дослідження, проведене у Китаї у березні 2020 року (n = 2168), показало, що найчастіше проблеми психічного здоров’я виявлялися серед працівників охорони здоров’я, ніж серед тих, хто працює в інших галузях [23]. Зокрема, частіше спостерігалися безсоння (38,4 % проти 30,5 %, p < 0,01), тривога (13,0 % проти 8,5 %, p < 0,01), депресія (12,2 % проти 9,5 %, p = 0,04), соматизація (1,6 % проти 0,4 %, p < 0,01), нав’язливість (5,3 % проти 2,2 %, p < 0,01). На розвиток симптомів психічного розладу впливали такі чинники: контакти з хворими на коронавірусну інфекцію, наявне хронічне соматичне захворювання і жіноча стать.
Онлайн-скринінг за валідними шкалами й опитувальниками серед більш ніж 18 тис. осіб в Італії, які перебували на карантині протягом 3–4 тижнів, у період епідемічного піку COVID-19 (26 березня — 5 квітня 2020 р.), свідчить, що клінічно значущі симптоми розладу адаптації спостерігалися у 21,8 % опитаних, тривоги — у 20,8 %, депресії — у 17,3 % і безсоння — у 7,3 % [24].
У період коронавірусної інфекції чинники індивідуального психологічного захисту і чинники ризику отримали особливу значущість для профілактики розладів тривожно-депресивного спектра. До захисних механізмів сьогодні належить так звана пружність, що містить комплекс соціальних, психологічних і біологічних чинників, які дають змогу запобігти розвитку психічної патології у разі впливу психічних травм. Цей комплекс охоплює індивідуальні психологічні чинники (соціальну залученість та експресивність, позитивну самооцінку, нормальний інтелект), стійкі сімейні зв’язки і зовнішню систему підтримки (робота, навчання, церква) [25]. У період ізоляції найбільш значущими чинниками пружності у 5000 жителів Європи були: позитивний стиль оцінки ситуації, швидке подолання стресової ситуації і сприйнята соціальна підтримка [26]. У німецькому дослідженні до захисних чинників, які запобігають тривозі, віднесені впевненість у своїх можливостях контролювати ситуацію, пов’язану з пандемією; наявна соціальна підтримка і достатня інформація щодо можливості отримати допомогу у зв’язку із захворюванням [18]. Серед негативних чинників, які спонукають до тривожних станів, виокремлені високий рівень нейротизму і пригнічення негативних емоцій [26].
Можливо припустити, що суттєву частку виявлених серед населення ознак тривожних і депресивних розладів слід зарахувати до нормальних стресових реакцій, які здійснюють адаптивну функцію. Проте результати досліджень динаміки призначення психофармакологічних препаратів у США у лютому — березні 2020 р. [27] свідчать про серйозніший вплив комплексної і тривалої психічної травми. Протягом місяця відзначено суттєве (на 21 %) збільшення призначення психофармакологічних препаратів, переважно протитривожних (на 34 %) і антидепресивних (на 18 %), що побічно свідчить про збільшення частоти тривожних і депресивних розладів у популяції.
Великою практичною значущістю вирізняється ретроспективне мультицентрове дослідження прогнозу перебігу коронавірусної інфекції залежно від застосування антидепресантів, проведене у Франції. Результати дослідження (n = 9509) показують вірогідно менший ризик несприятливої динаміки інфекції із потребою інтубації і смертельним наслідком під час лікування психічних розладів антидепресантами з груп селективних інгібіторів зворотного захоплення серотоніну (СІЗЗС) (флуоксетин, есциталопрам) і селективних інгібіторів зворотного захоплення серотоніну і норадреналіну (венлафаксин). Позитивний вплив антидепресантів автори пояснюють встановленим останніми роками протизапальним, а також можливим противірусним ефектом сучасних антидепресантів [1, 28].
Виходить, очевидно, що в умовах пандемії COVID-19 і швидкого погіршання епідеміологічної обстановки, введення карантинних заходів створюються умови для різкого погіршання психічного здоров’я широкого кола осіб з групи ризику. Маніфестація або загострення психічних захворювань так само сприяють поширенню вірусної інфекції та пов’язані з частішим розвитком соматичних ускладнень і несприятливим прогнозом.
Практичною проблемою, яка потребує найшвидшого розв’язання, стає підбір ефективних психофармакологічних засобів для лікування психічних розладів, зважаючи на потребу їх поєднання із противірусними препаратами у соматично ослаблених COVID-19 пацієнтів. Якщо є потреба проведення терапії вірусного захворювання, слід оцінювати психічний стан хворого та ризик ймовірного загострення симптоматики у разі відміни терапії або зниження дози. При низькій імовірності швидкого загострення, з огляду на високе додаткове медикаментозне навантаження, — зменшити дози препаратів. У разі високого ризику загострення слід брати до уваги вираженість соматичних симптомів COVID-19 і можливі лікарські взаємодії [29].
Вибір психофармакологічного препарату повинен визначатися спектром його соматотропної активності і побічними ефектами та враховувати соматичний стан пацієнта. Усі психотропні засоби слід призначати у суворій відповідності з наявними показаннями і протипоказаннями, з дотриманням встановленого режиму доз, а також з урахуванням вікових особливостей. Коли бракує репрезентативних даних в даний час, автори тематичних публікацій звертають увагу на вже відомі особливості дії і лікарські взаємодій психотропних засобів [29–34].
Під час проведення психофармакотерапії пацієнтам з COVID-19 лікарі повинні уважно оцінювати потенційні користь і ризики її застосування в аспекті використання препаратів з мінімально вираженою побічною дією, особливо на дихальну функцію, і можливі несприятливі лікарські взаємодії, при ретельному конт-ролі соматичного стану хворих.
Вважається, що для лікування депресій придатні будь-які антидепресанти [35–38]. Одним із сучасних препаратів, який можна рекомендувати для застосування у загальномедичній практиці, є сертралін, який належить до класу СІЗЗС.
Сертралін — антидепресант, потужний специфічний інгібітор зворотного захоплення серотоніну у нейронах. Він має дуже малий вплив на зворотне захоплення норадреналіну і дофаміну. У терапевтичних дозах сертралін блокує захоплення серотоніну у тромбоцитах людини. Він не має стимулювальної, седативної або антихолінергічної дії. Завдяки селективному пригніченню захоплення серотоніну сертралін не посилює адренергічну активність. Сертралін не має спорідненості до мускаринових (холінергічних), серотонінергічних, дофамінергічних, адренергічних, гістамінергічних рецепторів, ГАМК-рецепторів або бензодіазепінових рецепторів [39]. Ще однією важливою перевагою сертраліну є його слабка блокувальна дія на ізоферменти печінки (цитохроми P450IID6, P450IA2 і P450IIIA4), які беруть участь у біотрансформації соматотропних препаратів, що знижує ризик небажаної лікарської взаємодії. Загальна ефективність у разі застосування сертраліну коливається від 51,7 до 75 % [40].
Останнім часом опубліковані дані про те, що деякі антидепресанти можуть модулювати прозапальні цитокіни [41]. R.J. Tynan et al. виявили, що у мікроглії, що її стимулює ліпополісахарид, сертралін інгібував продукцію прозапальних ФНП-α [42]. У дослідженні M. Sitges et al. продемонстрована здатність сертраліну знижувати базальну експресію прозапальних цитокінів ІЛ-1b та ФНП-α у гіпокампі [43]. Це свідчить про протизапальну дію сертраліну на мозок.
З моменту появи сертраліну в 1990 році проведено велику кількість порівняльних досліджень цього препарату з іншими антидепресантами. Сертралін має високу ефективність, яку можна порівняти з такою у трициклічних антидепресантів, але водночас відрізняється значно кращою переносимістю і вищим профілем безпеки [44, 45]. З порівняння препаратів з групи СІЗЗС між собою була виявлена їх ефективність, водночас cертралін характеризувався кращою переносимістю порівняно з рештою препаратів групи СІЗЗС [46]. Профіль побічних дій також суттєво відрізняється у різних препаратів групи СІЗЗС. Застосування СІЗЗС супроводжується істотно меншою кількістю антимускаринових ефектів, водночас частіше спостерігаються шлунково-кишкові та психостимулювальні ефекти [47].
Сертралін досить широко використовують під час лікування депресій у пацієнтів загальносоматичної системи останні кілька років. Коло показань до застосування препарату істотно розширилося. Окрім ендогенних депресій, сертралін ефективний і при депресіях іншого генезу, зокрема, при різноманітних психогенно зумовлених депресивних станах, депресіях в межах органічних захворювань, а також при депресивних розладах в межах хронічних соматичних захворювань, що до сьогодні практично не вивчали. Вивчення ефективності, безпеки та переносимості сертраліну у лікуванні афективних розладів і насамперед депресивних розладів у пацієнтів з коронавірусною інфекцією є неодмінною ланкою у з’ясуванні повноти клінічного ефекту препарату.
Мета дослідження — порівняльне вивчення динаміки показників тривожно-депресивної симптоматики, когнітивної дисфункції та якості життя (ЯЖ), а також наявних побічних ефектів у хворих з коронавірусною інфекцією під впливом лікування антидепресантами (флуоксетин і сертралін).
Обстежено 107 пацієнтів, із них 77 (72 %) чоловіків і 30 (28 %) жінок, віком від 25 до 80 років (середній вік — 55,8 ± 6,4 року), з коронавірусною інфекцією, госпіталізованих у інфекційну клініку Військово-медичного клінічного центру Західного регіону (м. Львів) протягом 2020–2021 років.
У дослідження залучали пацієнтів з тривожно-депресивними розладами, які дали письмову інформовану згоду на участь у ньому. Критеріями виключення були: коморбідність депресивного епізоду з гострим психотичним станом; тяжкий ступінь артеріальної гіпертензії (артеріальний тиск 180/115 мм рт.ст. і вище до початку терапії); будь-які клінічно значущі декомпенсовані захворювання нирок, печінки, серцево-судинної, дихальної систем; органічні захворювання центральної нервової системи; гіперчутливість до досліджуваних препаратів. Для пацієнтів, які приймали будь-які психотропні препарати до початку дослідження, проводили 7-денний період «вимивання» («wash out»).
Пацієнти були розподілені на три групи: 1-ша група (n = 38) — пацієнти отримували традиційну стандартну терапію з флуоксетином в дозі 20–40 мг/добу; 2-га група (n = 42) — пацієнти отримували традиційну стандартну терапію з сертраліном в дозі 50–100 мг/добу; 3-тя група (контрольна, n = 27) — пацієнти отримували традиційну стандартну терапію без додаткового призначення антидепресантів. Флуоксетин був обраний препаратом для порівняння як антидепресант з групи СІЗЗС, що найбільш часто виписують хворим. На початку дослідження не виявили вірогідних відмінностей між групами за віком, статтю, наявністю асоційованих соматичних захворювань, чинників ризику серцево-судинних ускладнень і психосоціальних чинників. Фармакотерапію коронавірусної хвороби здійснювали відповідно до клінічних рекомендацій.
Тривалість дослідження становила 6 місяців. Анкетування пацієнтів проводили на початку терапії, через 21 день, 3 і 6 місяців від початку лікування. На кожному етапі оцінювали клініко-функціональний стан і психоемоційний статус пацієнтів. У ці ж дні протягом усього дослідження реєстрували всі небажані явища (НЯ) із зазначенням їх тяжкості, часу виникнення і тривалості.
Критеріями ефективності терапії як флуоксетином, так і сертраліном були відсутність протягом періоду спостереження екзацербацій і виражених побічних ефектів, що потребують відміни препарату.
Завершили дослідження 102 пацієнти. Троє пацієнтів вибули у зв’язку із відмовою від подальшої участі у дослідженні, двоє пацієнтів — у зв’язку із розвитком НЯ на 3-й день терапії.
Під час діагностики психопатологічних розладів використовували психометричні шкали: госпітальну шкалу депресії і тривоги (Hospital Anxiety and Depression Seale — HADS), опитувальник депресії Бека (Beck Depression Inventory — BDI), шкалу особистісної (ОТ) і реактивної тривожності (РТ) Спілбергера — Ханіна. З метою оцінки когнітивних функцій використовували Коротку шкалу оцінки психічного статусу (Mini-Mental State Examination — MMSE) (Folstein M. et al., 1975); таблиці Шульте (Блейхер В.М., 2002) — для визначення сенсомоторних реакцій, ефективності роботи; тест Лурія (показники 5 безпосередніх відтворень і одного відстроченого) (Лурія А.Р., 1969) — для оцінки оперативної і короткочасної слухомовленнєвої пам’яті, якості відтворення.
Оцінку якості життя проводили з використанням опитувальника «Medical Outcomes Study Short Form» (MOS) SF-36, розробленого Бостонським інститутом здоров’я. Опитувальник містить шкали, що відображають різні аспекти ЯЖ, і два комплексних показники «Фізичний компонент здоров’я» і «Психологічний компонент здоров’я».
У дослідженні використовували пакети прикладних програм Statistica for Windows v. 8.0 (StatSoft Inc, США, 2012) відповідно до рекомендацій з обробки результатів медико-біологічних досліджень.
За психометричними шкалами на початку лікування легкий ступінь депресії діагностований у 30 (28,0 %) пацієнтів, помірний — у 55 (51,4 %), тяжкий — у 22 (20,6 %); легкий ступінь тривоги діагностований у 23 (21,5 %) пацієнтів, помірний — у 50 (46,7 %), тяжкий — у 34 (31,8 %) пацієнтів. Встановили, що середній бал депресії за HADS дорівнював 11,8 ± 0,9, за BDI — 17,1 ± 1,4 бала, що відповідало депресії помірного ступеня тяжкості. Рівень тривоги за HADS дорівнював 12,8 ± 0,9 бала. Рівні РТ і ОТ становили 42,3 ± 2,1 бала і 47,8 ± 2,5 бала відповідно. Обстежені пацієнти характеризувалися середнім рівнем РТ і високою ОТ.
Під час об’єктивного оцінювання когнітивної сфери за допомогою нейропсихологічних тестів когнітивні розлади (КР) виявлені у 81 (75,7 %) пацієнта. У більшості пацієнтів виявили легкі — 36 (44,4%) когнітивних розладів і помірні — 41 (50,7 %). У структурі когнітивних розладів відзначили порушення уваги, запам’ятовування, короткочасної та оперативної пам’яті, сповільненість мислення і труднощі у підборі слів. За MMSE показник когнітивної дисфункції становив 25,0 ± 0,6 бала. Водночас найбільш виражені були порушення оперативної пам’яті, розлади концентрації уваги, рахування. Це ж підтверджувалось під час проведення тесту «10 слів» і проби Шульте.
Коронавірусна інфекція погіршує ЯЖ хворих, впливаючи на всі рівні життєдіяльності: фізичний, емоційний, рольовий, психологічний, соціального функціонування. Встановили, що показник за шкалою фізичного функціонування (ФФ) становив 63,5 ± 4,8 бала, що вказувало на те, що фізична активність у пацієнтів істотно обмежена станом їх здоров’я. Аналіз рольового фізичного функціонування (РФФ) показав, що цей показник здоров’я становив 19,6 ± 3,8 бала. Сприйняття загального стану здоров’я (ЗЗ) становило 44,3 ± 4,1 бала. Комплексна оцінка фізичного компонента здоров’я, який знаходить відображення у ФФ, РФФ і ЗЗ, показала, що він становив 42,5 ± 3,2 бала. Життєздатність як суб’єктивна оцінка власного життєвого тонусу (енергія, бажання енергійних дій), відчуття себе повним сил і енергії або, навпаки, знесиленим, у пацієнтів була знижена до 43,9 ± 3,6 бала. Показник соціального функціонування, який визначає, якою мірою фізичний або емоційний стан обмежує спілкування з друзями, колегами по роботі, рідними, становив 49,1 ± 5,3 бала, що свідчить про істотне обмеження соціальних контактів, зниження рівня спілкування у зв’язку з погіршанням фізичного та емоційного стану. Роль емоційного функціонування — це суб’єктивна оцінка хворим ступеня обмеження своєї буденної діяльності, зумовленої емоційними проблемами. Цей показник був істотно зниженим і становив 31,3 ± 2,9 бала. Показник психічного здоров’я становив 48,2 ± 4,8 бала, що свідчить про наявність депресивних і тривожних ознак, психічного неблагополуччя у хворих з COVID-19. Комплексна оцінка психологічного компонента здоров’я, який складають життєздатність, соціальне функціонування, емоційні проблеми в обмеженні життєдіяльності, психічне здоров’я, показала, що він знижений — 43,1 ± 3,5 бала.
Вже на 21-й день лікування пацієнти 1-ї і 2-ї груп відзначали поліпшення самопочуття, зменшення головного болю, пітливості, поліпшення якісних характеристик сну. До 3-го місяця зменшилися тривога, страх за майбутнє, емоційна лабільність. У хворих, які отримували антидепресанти, поліпшилися настрій і загальне самопочуття, підвищилася повсякденна активність, з’явилися мотивації до якнайшвидшого одужання і відновлення втрачених функцій. Водночас динаміка соціальної адаптації у 3-й групі залишилася практично без зміни.
Початково не було виявлено вірогідних відмінностей між групами за показниками депресії і тривоги. У 1-й і 2-й групах на фоні лікування спостерігали вірогідне зниження рівня депресії починаючи з 3-го місяця лікування. Зокрема, середній бал депресії за HADS порівняно з початковим рівнем зменшився через 3 місяці терапії: у 1-й групі — на 18,5 % (р = 0,045), у 2-й групі — на 20,8 % (р = 0,049). Далі антидепресивна активність препаратів підвищувалась, і через 6 місяців лікування сумарний бал депресії за HADS у 1-й групі зменшився на 37,8 % (р < 0,001), у 2-й групі — на 42,5 % (р < 0,001). У 3-й групі через 3 і 6 місяців лікування відзначили зниження депресії за HADS на 6,0 і 12,9 % відповідно, без вірогідних відмінностей (p > 0,05) (рис. 1).
/82.jpg)
Середній бал депресії за BDI через 3 місяці лікування проти початкового показника у 1-й і 2-й групах зменшився на 19,3 % (р = 0,044) і 22,4 % (р = 0,032) відповідно, що можна розцінити як помірний антидепресивний ефект. Через 6 місяців терапії середній бал депресії у 1-й і 2-й групах вірогідно відрізнявся від початкового показника — на 38,6 % (р < 0,001) і 43,1 % (р < 0,001) відповідно. У 3-й групі через 3 і 6 місяців лікування відзначили зниження депресії за BDI на 6,5 і 13,6 % відповідно без вірогідних відмінностей (p > 0,05) (рис. 2).
З порівняння ефективності фармакотерапії антидепресантами за динамікою показників через 3 і 6 місяців виявлена більша ефективність сертраліну порівняно з флуоксетином. На фоні лікування сертраліном через 6 місяців досягнута виражена редукція депресивних скарг. Повна нормалізація настрою досягнута у 59,5 % хворих. Зникли болісне збудження, страх за життя у 88,1 % випадків, істотно поліпшився сон у 78,6 % хворих, вирівнялися добові коливання настрою у 78,6 % випадків, відновився інтерес до професійної діяльності у 71,4 % пацієнтів.
Відмінною рисою сертраліну є не тільки його виражений антидепресивний, але й антитривожний ефект, що було відзначено за даними психологічного дослідження.
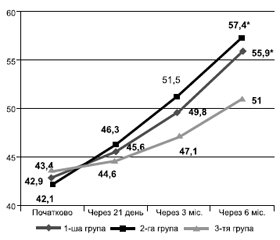
У всіх групах виявлено зниження рівня тривоги порівняно з початковим. Статистично вірогідне зниження середнього сумарного бала тривоги за HADS відзначили лише у 2-й групі починаючи з 3-го місяця лікування — на 16,1 % (р = 0,045); через 6 місяців — на 32,3 % (р < 0,001) (рис. 3). У 2-й групі виявили вірогідне більш значуще зниження рівня РТ і ОТ через 3 місяці лікування порівняно з початковим рівнем — на 12,8 % (р = 0,048) і 12,9 % (р = 0,049) відповідно; через 6 місяців — на 26 % (р < 0,001) і 16,3 % (р = 0,01) відповідно (рис. 4, 5). Вірогідного зниження показників тривожності у 1-й і 3-й групах не спостерігали.
Результати проведеного дослідження дають змогу зробити висновок про вищу антидепресивну й антитривожну активність сертраліну порівняно з флуоксетином.
Усі хворі до лікування під час нейропсихологічного тестування зазначали чергування періодів вираженої загальмованості, небажання виконувати тестові завдання. Після регресу депресивних порушень як наслідку застосування антидепресантів «песимістична» оцінка власного стану і небажання виконувати тестові завдання змінилися на адекватнішу поведінку. Водночас звертає на себе увагу той факт, що до кінця перебування у стаціонарі у пацієнтів 1-ї і 2-ї груп рівень порушення вищих психічних функцій зменшився на 21 і 26,2 % відповідно порівняно з початковими показниками, а у 3-й групі — на 7,4 %.
Через 21 день після початку лікування відзначили невірогідне збільшення балів за шкалою MMSE порівняно з початковими даними в усіх групах, переважно показників уваги та пам’яті. У пацієнтів 1-ї групи загальний бал за MMSE збільшився на 4,6 % через 3 місяці (р = 0,23) і на 8,4 % через 6 місяців (p = 0,024); у пацієнтів 2-ї групи збільшення загального бала становило 5,7 % (р = 0,15) і 10,1 % (р = 0,008) відповідно. У пацієнтів 3-ї групи вірогідних змін показників не виявили. Збільшення балів у 1-й і 2-й групах було зумовлено насамперед поліпшенням показника пам’яті і збереженням на попередньому рівні показника уваги (рис. 6).
Під час аналізу функціональної рухливості нервової системи у пацієнтів досліджуваних груп виявили зменшення часу, що витрачається на перегляд таблиць Шульте (рис. 7). Після лікування відзначали позитивну динаміку сенсомоторних функцій із статистично вірогідними відмінностями в обох групах, але більш виражену у 2-й групі (р = 0,005), де ефективність роботи підвищувалась на 10,8 с (у 1-й групі — на 9,1 с (р = 0,013), у 3-й групі — на 3,9 с (р = 0,313)).
/84.jpg)
Дослідження мнестичних процесів (табл. 1) на початку лікування виявило порушення пам’яті у пацієнтів досліджуваних груп. Кількість відтворених елементів серії з 10 слів у всіх випадках була неповною, реєструвалися порушення довготривалої пам’яті. Виявляли виснаженість мнестичних процесів — зигзагоподібний характер кривої запам’ятовування з коливаннями у кількості відтворених слів. Через 6 місяців після лікування поліпшення з вірогідною різницею (р < 0,05) показників короткочасної і довготривалої пам’яті зазначили у пацієнтів 1-ї і 2-ї груп. Збільшилася кількість запам’ятованих слів за тестом Лурія при безпосередньому (з першого по п’яте) (5,5 ± 0,3 — 6,9 ± 0,3) і відстроченому (7,2 ± 0,4) відтвореннях. У пацієнтів 3-ї групи відзначали збільшення кількості слів при безпосередньому і відстроченому відтвореннях (р > 0,05).
/84_2.jpg)
Аналізуючи динаміку інтелектуально-мнестичних розладів, можна констатувати, що лікування із застосуванням сертраліну більш ефективно. Зміни когнітивних показників на фоні приймання сертраліну полягали у зниженні часу рухових реакцій, підвищенні рівня активації і психомоторного темпу, що свідчило про позитивний вплив досліджуваного препарату на функціональний стан пацієнтів з СОVID-19 і що у сертраліну немає поведінкової токсичності, що охоплює погіршення показників пам’яті, уваги, працездатності, темпу сенсомоторних реакцій.
Отже, найбільш ефективним щодо корекції когнітивних розладів виявилося використання у схемі лікування антидепресантів (1-ша і 2-га групи). Виявлена у процесі лікування позитивна динаміка показників короткочасної і довготривалої пам’яті дає підставу припустити, що терапія антидепресантами має позитивний вплив на перебіг когнітивних функцій у хворих з коронавірусною інфекцією. Вплив антидепресантів на когнітивні функції зумовлений вегетостабілізуючою дією, пов’язаною з наданням регулювального впливу на надсегментарні відділи вегетативної нервової системи і нормалізацією обміну нейромедіаторів. Сертралін впливає як інгібітор на зворотне захоплення дофаміну й активізує мозкові структури.
Зниження ЯЖ за початковими показниками виявили в усіх хворих з коронавірусною інфекцією, що визначалося наявними депресивними розладами. У пацієнтів, які приймали антидепресанти, в динаміці через 6 місяців (рис. 8) відзначили вірогідне підвищення ЯЖ з фізичного компонента (53,9 ± 4,8 бала проти 42,5 ± 3,2 бала до лікування, р = 0,05) завдяки вірогідному поліпшенню за показниками ФФ (р = 0,044), РФФ (р = 0,026), ЗЗ (р = 0,038). Показник психічного здоров’я також вірогідно підвищився: 59,3 ± 4,2 бала проти 48,2 ± 3,6 бала до лікування (р = 0,05). Поліпшення ЯЖ за психологічним компонентом відбувалося завдяки вірогідному поліпшенню показників життєздатності (p = 0,035), соціального функціонування (p = 0,01), психічного здоров’я (p = 0,013). За шкалою РФФ відзначали тенденцію до поліпшення ЯЖ хворих, але вірогідних відмінностей показників не виявили. Аналіз показників у 1-й і 2-й групах показав, що ЯЖ після лікування не мала вірогідних відмінностей за антидепресивним препаратом.
/85.jpg)
У пацієнтів 3-ї групи поліпшення ЯЖ через 6 місяців спостереження суттєво не відбувалось внаслідок збереження ознак депресії. Відзначена тенденція позитивної динаміки низки показників ЯЖ у 3-й групі, ймовірно, пов’язана із загальним поліпшенням стану на фоні етіотропної і патогенетичної терапії, що проводилась хворим з COVID-19.
Отже, використання сучасних антидепресантів (флуоксетину і сертраліну) сприяє відновленню і підвищенню показників ЯЖ.
Аналіз безпеки і переносимості сертраліну показав, що терапія цим препаратом дуже рідко спричиняє НЯ. Зокрема, НЯ на фоні приймання сертраліну відзначали у 10,0 % пацієнтів. У табл. 2 наведені побічні ефекти сертраліну, частота яких перевищила 1,0 %. Найчастіше відзначали сухість у роті, запаморочення, нудоту. НЯ мали виражений характер і були причиною зміни дози лише у 2 пацієнтів, відміни — в 1 пацієнта. Привертає до себе увагу той факт, що у 1-й групі лікарі скасовували призначене лікування внаслідок розвитку НЯ частіше (5,3 % випадків), ніж у пацієнтів, які приймали сертралін.
З НЯ у 2 (4,8 %) пацієнтів зареєстровано деяке підвищення тривожності у перші дні лікування, яке згодом редукувалося самостійно і не потребувало відміни або корекції дози препарату. Не відзначили негативного впливу сертраліну на частоту серцевих скорочень та артеріальний тиск, а також несприятливої взаємодії з іншими препаратами, які призначали пацієнтам.
Хоча оцінки переносимості терапії, зроблені пацієнтами і лікарями, відрізнялися кількісно, їх модальність була односпрямованою (табл. 3). Зокрема, на думку лікарів, помірну і погану переносимість лікування, рекомендованого з приводу тривожно-депресивних розладів на фоні коронавірусної інфекції, відзначили у 15,8 % пацієнтів 1-ї групи і 9,8 % пацієнтів 2-ї групи, а на думку хворих — у 2 рази частіше.
Отже, додавання сертраліну до стандартної терапії коронавірусної інфекції сприяло кращій оцінці переносимості проведеного лікування як лікарями, так і пацієнтами.
Додатковим підтвердженням задовільного клінічного ефекту і переносимості сертраліну можуть бути дані про прихильність хворих до подальшого лікування. Якщо до початку лікування хворі неохоче приймали препарат, то після — з’явилася стійка мотивація до приймання препарату. Ймовірно, це зумовлено нейрорецептивною активністю сертраліну, безпосередньо пов’язаною з поліпшенням показників психологічної сфери, а також ефективним поєднанням з іншими препаратами і відсутністю побічних ефектів та ускладнень. Із загальної кількості пацієнтів, які приймали сертралін до кінця курсу лікування, висловили бажання і далі його приймати 92,8 %. І ще більшою мірою (95,2 %) схильні були до подальшого лікування ті хворі, у яких відбулася повна редукція депресивних симптомів.
Результати виконаного дослідження дали змогу розширити уявлення про пацієнтів з коронавірусною інфекцією. Висока частота депресивних розладів у хворих на COVID-19 потребує проведення додаткового психіатричного консультування пацієнтів із підвищеним рівнем депресії за даними психометричних опитувальників. Проведення скринінгу для виявлення тривожно-депресивних розладів, із застосуванням оціночних психодіагностичних опитувальників, є доцільним і обґрунтованим методом дослідження. Це дає змогу інфекціоністу або терапевту об’єктивно оцінити психічний стан пацієнтів з коронавірусною інфекцією та визначити подальшу тактику ведення хворих при взаємодії з фахівцями психіатричного профілю.
Загальні принципи медикаментозної терапії коронавірусної інфекції, асоційовані з тривожно-депресивними розладами, полягають у приєднанні психофармакотерапії до класичної схеми лікування хворих на COVID-19. Основна мета психофармакотерапії — редукція психопатологічних розладів тривожно-депресивного спектра, зниження ризику погіршання соматичного стану хворого, відновлення соціального функціонування пацієнтів.
Проведене дослідження показало, що при клінічно однорідних початкових даних застосування у хворих як флуоксетину, так і сертраліну призвело до позитивних змін тривожно-депресивної симптоматики. Причому поліпшення було вищим серед хворих, які отримували сертралін. Зниження рівня депресивної симптоматики позитивно корелювало з поліпшенням рівня соціальної компетенції пацієнтів і з показниками ЯЖ у субсферах як ядерного, так і специфічного модуля.
Призначення сертраліну у пацієнтів з коронавірусною інфекцією актуально і патогенетично обґрунтовано. Істотний регрес депресивної симптоматики, зумовлений збалансованою дією сертраліну, що охоплює помірний анксіолітичний і виражений активуючий ефекти, став важливим прогностичним чинником для відновлення втрачених функцій і соціальної адаптації.
Результати проведеного дослідження дали змогу дійти таких висновків. Комбінована терапія у пацієнтів із коронавірусною інфекцією і коморбідними тривожно-депресивними розладами із застосуванням антидепресантів є ефективною в плані редукції депресії, тривоги, когнітивних розладів і поліпшення якості життя пацієнтів. Сертралін має вищу клінічну ефективність у лікуванні пацієнтів з тривожно-депресивними розладами на фоні коронавірусної інфекції, а також задовільну безпеку і переносимість порівняно з флуоксетином.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 02.11.2021
Рецензовано/Revised 15.11.2021
Прийнято до друку/Accepted 18.11.2021
Список литературы
1. Вельтищев Д.Ю., Лисицына Т.А., Борисова А.Б. Психическое здоровье населения различных стран в период пандемии коронавирусной инфекции (COVID-19). Социальная и клиническая психиатрия. 2020. Т. 30. № 4. С. 83-86. URL: https://psychiatr.ru/files/magazines/2020_12_scp_1894.pdf.
2. Besedovsky Н., Rey A.D., Sorkin E., Dinarello C.A. Immunoregulatory feedback between interleukin-1 and glucocorticoid hormones. Science. 1986. Vol. 233(4764). P. 652-654. DOI: 10.1126/science.3014662.
3. Besedovsky H.O., Rey A.D., Klusman I. et al. Cytokines as modulators of the hypothalamus-pituitary-adrenal axis. The Journal of Steroid Biochemistry and Molecular Biology. 1991. Vol. 40(4–6). Р. 613-618. DOI: 10.1016/0960-0760(91)90284-c.
4. Licinio J., Wong M.L The role of inflammatory mediators in the biology of major depression: central nervous system cytokines modulate the biological substrate of depressive symptoms, regulate stress-responsive systems, and contribute to neurotoxicity and neuroprotection. Molecular Psychiatry. 1999. Vol. 4(4). Р. 317-327. DOI: 10.1038/sj.mp.4000586.
5. Wang J., Dunn A.J. Mouse interleukin-6 stimulates the HPA axis and increases brain tryptophan and serotonin metabolism. Neurochemistry International. 1998. Vol. 33(2). Р. 143-154. DOI: 10.1016/s0197-0186(98)00016-3.
6. Capuron L., Fornwalt F.B., Knight B.T. et al. Does cytokine-induced depression differ from idiopathic major depression in medically healthy individuals? Journal of Affective Disorders. 2009. Vol. 119(1–5). Р. 181-185. DOI: 10.1016/j.jad.2009.02.017.
7. Vollmer-Conna U. Acute sickness behaviour: an immune system-to-brain communication? Psychological Medicine. 2001. Vol. 31(5). Р. 761-767. DOI: 10.1017/s0033291701003841.
8. Wichers M., Maes М. Psychoneuroimmuno-pathophysiology of cytokine-induced depression in humans. International Journal of Neuropsychopharmacology. 2002. Vol. 5(4). Р. 375-388. DOI: https://doi.org/10.1017/S1461145702003103.
9. Dursun S.M., Blackburn J.R., Kutcher S.P. An exploratory approach to the serotonergic hypothesis of depression: bridging the synaptic gap. Medical Hypotheses. 2001. Vol. 56(2). Р. 235-43. DOI: 10.1054/mehy.2000.1187.
10. Arbour N., Day R., Newcombe J., Talbot P.J. Neuroinvasion by human respiratory coronaviruses. Journal of Virology. 2000. Vol. 74(19). Р. 8913-8921. DOI: https://doi.org/10.1128/JVI.74.19.8913-8921.2000.
11. Dessau R.B., Lisby G., Frederiksen J.L. Coronaviruses in brain tissue from patients with multiple sclerosis. Acta Neuropatho-logy. 2001. Vol. 101(6). Р. 601-604. DOI: 10.1007/s004010000331.
12. Fujimoto S., Kobayashi M., Uemura O. et al. PCR on cerebrospinal fluid to show influenza-associated acute encephalopathy or encephalitis. The Lancet. 1998. Vol. 352(9131). Р. 873-875. DOI: 10.1016/S0140-6736(98)12449-2.
13. Xu J., Zhong S., Liu J. et al. Detection of severe acute respiratory syndrome corona virus in the brain: potential role of the chemokine migration in pathogenesis. Clinical Infectious Disease. 2005. Vol. 41(8). Р. 1089-1096. DOI: 10.1086/444461.
14. Yeh А., Arlene С., Cohen М.Е. et al. Detection of corona virus in the central nervous system of a child with acute disseminated encephalomyelitis. Pediatrics. 2004. Vol. 113. Р. 73-76. DOI: 10.1542/peds.113.1.e73.
15. Wang С., Pan R., Wan X. et al. Immediate psychological responses and associated factors during the initial stage of the 2019 coronavirus disease (COVID-19) epidemic among the general population in China. Int. J. Envir. Res. Publ. Hlth. 2020. Vol. 17. № 5. Р. 17-29. DOI: https://doi.org/10.3390/ijerph17051729.
16. Huang Y., Zhao N. Generalized anxiety disorder, depressive symptoms and sleep quality during COVID-19 outbreak in China: a web-based cross-sectional survey. Psychiatr. Res. 2020. Vol. 288. DOI: 10.1016/j.psychres.2020.112954.
17. Mertens G., Gerritsen L., Duijndam S. et al. Fear of the coronavirus (COVID-19): Predictors in an online study conducted in March 2020. J. Anxiety Dis. 2020. Vol. 74. DOI: 10.1016/j.janxdis.2020.102258.
18. Petzold M.B., Bendau А., Plag J. et al. Risk, resilience, psychological distress, and anxiety at the beginning of the COVID-19 pandemic in Germany. Brain Behav. 2020. Vol. 10. № 9. P. 17-45. DOI: https://doi.org/10.1002/brb3.1745.
19. Czeisler M.É., Lane R.I., Petrosky E. et al. Mental Health, Substance Use, and Suicidal Ideation During the COVID-19 Pandemic — United States, June 24–30, 2020. Morbidity and Mortality Weekly Report. 2020. August 14, 2020. Vol. 69. № 32. P. 1049-1057. DOI: 10.15585/mmwr.mm6932a1.
20. Salari N., Hosseinian-Far A., Jalali R. et al. Prevalence of stress, anxiety, depression among the general population during the COVID-19 pandemic: A systematic review and meta-analysis. Global and Health. 2020. Vol. 16. № 1. 57 р. DOI: https://doi.org/10.1186/s12992-020-00589-w.
21. Pierce M., Hope H., Ford T. et al. Mental health before and during the COVID-19 pandemic: a longitudinal probability sample survey of the UK population. Lancet Psychiatry. 2020. Vol. 7. № 10. P. 883-892. DOI: https://doi.org/10.1016/S2215-0366(20)30308-4.
22. Lee S.W., Yang J.M., Moon S.Y. et al. Association between mental illness and COVID-19 susceptibility and clinical outcomes in South Korea: a nationwide cohort study. Lancet Psychiatry. 2020. Vol. 17. P. 12-15. DOI: https://doi.org/10.1016/S2215-0366(20)30421-1.
23. Zhang W.R., Wang K., Yin L. et al. Mental Health and Psychosocial Problems of Medical Health Workers during the COVID-19 Epidemic in China. Psychother. Psychosom. 2020. Vol. 8. № 4. P. 242-250. DOI: https://doi.org/10.1159/000507639.
24. Fagiolini А., Cuomo А., Frank Е. Fagiolini A. COVID-19 diary from a psychiatry department in Italy. J. Clin. Psychiatry. 2020. Vol. 81(3). Р. 133-57. DOI: 10.4088/JCP.20com13357.
25. Hoge E.A., Austin E.D., Pollack M.H. Resilience: Research evidence and conceptual considerations for posttraumatic stress disorder. Depression and Anxiety. 2007. Vol. 24. № 2. P. 139-152. DOI: 10.1002/da.20175.
26. Veer I.M., Riepenhausen A., Zerban M. et al. Mental resi-lience in the Corona lockdown: First empirical insights from Europe. PsyArXiv Preprints. 2020. URL: https://www.researchgate.net/publication/340865488.
27. Canady V.A. New report examines medication trends for depression, anxiety and insomnia. Mental Health Weekly. 2020. Р. 342-344. DOI: 10.1002/mhw.32344.
28. Hoertel N., Rico M., Vernet R. et al. Association between SSRI Antidepressant Use and Reduced Risk of Intubation or Death in Hospitalized Patients with Coronavirus Disease 2019: a Multicenter Retrospective Observational Study. MedRxiv. preprint. 2020. DOI: https://doi.org/10.1101/2020.07.09.20143339.
29. Медведев В.Э., Доготарь О.А. COVID-19 и психическое здоровье: вызовы и первые выводы. Неврология, нейро-психиатрия, психосоматика. 2020. № 12(6). С. 4-10. DOI: doi.org/10.14412/2074-2711-2020-6-4-10.
30. Медведев В.Э. Депресcивные расстройства. В кн.: Путеводитель врачебных назначений. Современное руководство для практикующих врачей. Т. 6. Под ред. А.И. Мартынова. М.: Бионика Медиа, 2018. С. 57-69. URL: https://lib.medvestnik.ru/articles/DEPRESSIVNYE-RASSTROISTVA.html.
31. Медведев В.Э., Кардашян Р.А., Фролова В.И. Исследование эффективности различных схем замены антидепрессанта при развитии синдрома СИОЗС-индуцированной апатии. Неврология, нейропсихиатрия и психосоматика. 2020. № 12(2). С. 48-56. DOI: https://doi.org/10.14412/2074-2711-2020-2-48-56.
32. Медведев В.Э., Тер-Исраелян А.Ю., Фролова В.И. и др. Оптимизация терапии психических расстройств с мультисиндромальной клинической картиной. Психиатрия и психофармакотерапия им. П.Б. Ганнушкина. 2020. № 1. С. 23-27. URL: https://psychiatr.ru/download/4522?view=1&name=Psy+1_2020.pdf.
33. Медведев В.Э. Эффективность и переносимость современных антидепрессантов: результаты сетевых мета-анализов и российский опыт. Журнал неврологии и психиатрии им. С.С. Корсакова. 2018. № 118(11). С. 109-17. DOI: 10.17116/jnevro2018118111109.
34. Мосолов С.Н. Проблемы психического здоровья в условиях пандемии COVID-19. Журнал неврологии и психиатрии им. С.С. Корсакова. 2020. № 120(5). С. 7-15. DOI: 10.17116/jnevro20201200517.
35. Бауэр М., Пфенниг А., Северус Э. и др. Клинические рекомендации Всемирной федерации обществ биологической психиатрии по биологической терапии униполярных депрессивных расстройств. Часть 1: Острое и продолженное лечение униполярных депрессивных расстройств по состоянию на 2013 год. Современная терапия психических расстройств. 2015. № 4. С. 33-39. URL: https://www.psypharma.ru/sites/default/files/klinicheskie_rekomendacii_vsemirnoy.pdf.
36. Всемирная организация здравоохранения. Антидепрессанты (трициклические антидепрессанты и селективные ингибиторы обратного захвата серотонина) в лечении взрослых людей с депрессией. URL: https://www.who.int/mental_health/mhgap/evidence/depression/q1/ru.
37. The treatment and management of depression in adults (updated edition): National Clinical Practice Guideline 90 / National Collaborating Centre for Mental Health commissioned by the National Institute for Health & Clinical Excellence. Available from: https://www.nice.org.uk/guidance/cg90/evidence/full-guideline-pdf-4840934509.
38. Won Е., Park S.C., Han K.M. et al. Evidence-based, pharmacological treatment guideline for depression in Korea, revised edition. Journal of Korean Medical Science. 2014. Vol. 29(4). Р. 468-484. DOI: https://doi.org/10.3346/jkms.2014.29.4.468.
39. Пизова Н.В., Пизов А.В. Депрессия и посттравматическое стрессовое расстройство при новой коронавирусной инфекции. Лечебное дело. 2020. № 1. С. 82-88. DOI: 10.24411/2071-5315-2020-12197.
40. Путилина М.В., Федин А.И. Постинсультная депрессия, возможности терапии у больных в остром периоде инсульта. Атмосфера: Нервные болезни. 2005. С. 6-9. URL: https://cyberleninka.ru/article/n/postinsultnaya-depressiya-vozmozhnosti-terapii-u-bolnyh-v-ostrom-periode-insulta.
41. Janssen D.G., Caniato R.N., Verster J.C., Baune B.T. A psychoneuroimmunological review on cytokines involved in antidepressant treatment response. Human Psychopharmacology. 2010. Vol. 25(3). Р. 201-215. DOI: 10.1002/hup.1103.
42. Tynan R.J., Weidenhofer J., Hinwood M. et al. A comparative examination of the anti-inflammatory effects of SSRI and SNRI antidepressants on LPS stimulated microglia. Brain, Behavior and Immunity. 2012. Vol. 26(3). P. 469-479. DOI: https://doi.org/10.1016/j.bbi.2011.12.011.
43. Sitges M., Gómez C.D., Aldana B.I. Sertraline reduces IL-1β and TNF-α mRNA expression and overcomes their rise induced by seizures in the rat hippocampus. PLoS One. 2014. Vol. 9(11). Р. 11-16. DOI: https://doi.org/10.1371/journal.pone.0111665.
44. Casey D.E. Striking a balance between safety and efficacy: experience with the SSRI sertraline. International Clinical Psychopharmacology. 1994. Vol. 9(Suppl. 3). Р. 5-12. DOI: 10.1142/9789814440912_0201.
45. Khouzam H.R., Emes R., Gill Т., Raroque R. The antidepressant sertraline: a review of its uses in a range of psychiatric and medical conditions. Comprehensive Therapy. 2003. Vol. 29(1). Р. 47-53. DOI: 10.1007/s12019-003-0007-6.
46. Edwards J.G., Anderson I. Systematic review and guide to selection of selective serotonin re-uptake inhibitors. Drugs. 1999. Vol. 57(4). Р. 507-533. DOI: 10.2165/00003495-199957040-00005.
47. Anderson I.M. Meta-analytical studies on new antidepressants. British Medical Bulletin. 2001. Vol. 57(1). Р. 161-178. DOI: https://doi.org/10.1093/bmb/57.1.161.
/82.jpg)
/85.jpg)

/83.jpg)
/83_2.jpg)
/84.jpg)
/84_2.jpg)
/85_2.jpg)
/86.jpg)