Oral and General Health Том 2, №4, 2021
Вернуться к номеру
Методичні рекомендації для лікарів-стоматологів щодо проведення професійних онкологічних оглядів губ і ротової порожнини. Частина 1. Злоякісні новоутворення губ та ротової порожнини: епідеміологія та фактори ризику
Рубрики: Стоматология
Разделы: Справочник специалиста
Версия для печати
Рекомендовано координаційною радою ГО «Асоціація стоматологів України»
(протокол засідання № 1 від 01.07.2021) та схвалено резолюцією
6-го Національного українського стоматологічного конгресу
«Інноваційні технології в стоматології»
Вступ
Розвиток цивілізації супроводжується невпинним зростанням частоти виникнення певних захворювань людини, що можна розцінювати як плату за прогрес, зміну/погіршення стану навколишнього середовища і природного образу життя. До цих захворювань відносять серцево-судинні, генетичні, онкологічні та деякі інші. Онкологічні захворювання відносяться до основних неінфекційних хвороб, їх поширеність збільшується з віком, вони мають високу вартість лікування та високу смертність, а також вкрай негативно впливають на психологічний стан хворого.
Порожнина рота включає такі відділи: присінок порожнини рота та власне порожнину рота. Присінок — це анатомічне утворення, яке спереду обмежене губами і щоками, а позаду — зубами і яснами. У свою чергу, власне порожнина рота спереду і з боків обмежена зубами і яснами, а позаду переходить у глотку. Межа між цими ділянками пролягає між твердим та м’яким піднебінням, між передніми 2/3 та задньою 1/3 язика та по передніх дужках мигдаликів [1].
Злоякісні новоутворення (ЗН) губ і слизової оболонки ротової порожнини (РП) є вагомою проблемою охорони здоров’я у зв’язку з частим запізненням встановлення правильного діагнозу внаслідок малосимптомності або асимптомності цих пухлин на початкових стадіях, недостатньої інформованості лікарів щодо проблеми [2, 3]. Серед онкологічних захворювань, що діагностували у 2019 році, питома вага хворих із запущеними випадками (ІІІ і IV стадія) серед хворих з уперше встановленим діагнозом ЗН найбільша для ротової порожнини (53,3 %), суттєво менша для гортані (14,9 %) та губ (8,6 %). Про роль профілактичних оглядів у ранній діагностиці онкологічних захворювань свідчить той факт, що лише в 19,4 % хворих онкологічне захворювання було діагностовано під час профілактичних медичних оглядів у лікаря-стоматолога. Усе це свідчить про актуальність своєчасної діагностики ЗН губ та ротової порожнини та підкреслює необхідність впровадження обов’язкових медичних оглядів та нагадування пацієнтам про їх користь та допомогу у своєчасній діагностиці онкологічних захворювань.
Крім того, первинне джерело пухлини може бути розташованим у глибоких відділах обличчя, під основою черепу, в недоступних для прямого візуального контролю відділах щелепно-лицевої ділянки, голови та шиї. Іншою проблемою раннього виявлення ЗН губ та РП є відсутність у багатьох країнах чітких та доступних алгоритмів обстеження та подальшого скерування пацієнтів з підозрою на рак даної анатомічної локалізації. Безумовно, рання діагностика, подальше якісне обстеження, лікування, реабілітація та диспансеризація таких хворих здатні покращити прогноз і підвищити виживаність [4].
Визначна роль у діагностиці раку порожнини рота належить лікарям-стоматологам, проте не варто недооцінювати і роль лікарів загальної медичної практики (сімейних лікарів), оскільки відсутність мотивації та висока вартість стоматологічної медичної допомоги нерідко перешкоджають пацієнтам регулярно відвіду-вати стоматолога [5–7].
Етіологія
Основними ініціюючими факторами ризику раку порожнини рота є куріння та вживання алкоголю, спадкова схильність, надмірна інсоляція, слабкий імунітет, вірус папіломи людини, травмування слизової оболонки зубними протезами, хронічні захворювання слизової оболонки порожнини рота, а основним методом лікування — хірургічне втручання, у деяких випадках — з до- та післяопераційною ад’ювантною променевою терапією, хіміотерапією, імунотерапією [1].
Епідеміологія
Рак порожнини рота входить до 15 найбільш поширених видів раку у всьому світі [8, 9]. У 2018 р. у світі було діагностовано 354,8 тис. випадків раку губ та порожнини рота, що становить 2 % усіх нових випадків раку [8]. Медіана віку на момент встановлення діагнозу сквамозноклітинної карциноми порожнини рота або ротоглотки становить 63 роки, а 97 % випадків цих пухлин припадають на вік старше 35 років [10].
На частку раку порожнини рота припадає 1,9 % усієї смертності від раку, хоча показники різних країн значно відрізняються [11, 12]. Протягом останнього десятиліття спостерігається зростання частоти раку ротової порожнини у США [13], Австралії [14], Великобританії [15, 16] та Європі [17]. Незважаючи на появу та розвиток сучасних методів лікування протягом останніх кількох десятиліть, загальна смертність від сквамозноклітинної карциноми рота порівняно з 1980-ми роками істотно не знизилася. Це можна пояснити недосконалими системами скринінгу та раннього виявлення пухлин, що призводить до великої частки виявлення новоутворень на пізніх стадіях [18].
Виживаність при сквамозноклітинній карциномі значною мірою залежить від стадії процесу: при локалізованому раку даний показник через 5 років становить 83,7 %, за наявності регіонарних метастазів — 64,2 %, а за наявності віддалених метастазів — 38,5 %. Близько 70 % випадків діагностують на пізніх стадіях, що підкреслює важливість своєчасного виявлення та профілактики раку ротової порожнини [19].
Хоча губи та слизова оболонка порожнини рота добре піддаються візуальному огляду, у 2019 р. було планово оглянуто лише 18,8 % населення України, і кожний другий українець, оглянутий у порядку планової санації, потребував стоматологічної допомоги.
За даними Національного канцер-реєстру, у 2019 р. в Україні було виявлено 512 осіб (69 % чоловіків та 31 % жінок) з пухлинами губ. Показник захворюваності на злоякісні новоутворення губ становив 1,4 на 100 тис. населення (стандартизований показник захворюваності, світовий стандарт — 0,7).
За останнє десятиліття відмічена тенденція до зниження захворюваності на злоякісні новоутворення губ серед жителів України (у 2010 році стандартизований показник був вищим і становив 1,2). Тим не менше, необхідно звернути увагу на проблему своєчасної діагностики онкологічного захворювання. Хоча переважна більшість хворих з новоутвореннями червоної облямівки губ звертається за стоматологічною допомогою на ранніх стадіях захворювання (за даними 2019 р., у 83,9 % хворих було діагностовано І–ІІ стадію раку губ), питома вага хворих, яким було встановлено III і IV стадію раку, становила 14,6 % (1,6 % — не визначено). Тобто кожному десятому жителю України, що звернувся із новоутворенням губ, було діагностовано III або IV стадію раку. Цей показник коливається в різних регіонах України, що наведено на рис. 1.
У 2019 р. мали місце 104 випадки смерті від злоякісних новоутворень губ. Смертність від злоякісних новоутворень губ у 2019 році становила 0,3 на 100 тис. населення (серед чоловіків — 0,5, серед жінок — 0,1), а стандартизований показник захворюваності, світовий стандарт становив 0,1.
Злоякісні новоутворення ротової порожнини (ЗН РП) у 2019 р. були виявлені у 2266 осіб (77 % чоловіків та 23 % жінок). Показник захворюваності на злоякісні новоутворення ротової порожнини становив 6,4 на 100 тис. населення (серед чоловіків — 10,5, серед жінок — 2,7). Стандартизований показник захворюваності на ЗН РП, світовий стандарт — 3,9.
Загалом за останнє десятиліття спостерігається щорічне збільшення показника захворюваності на ЗН РП: у 2008 році цей показник становив 4,9 на 100 тис. населення, а у 2019 році показник онкологічної захворюваності ротової порожнини сягає 6,4 на 100 тис. населення.
Викликає значне занепокоєння пізня і неякісна, недостатня діагностика злоякісних новоутворень порожнини рота. Питома вага хворих із занедбаними випадками (ІІІ та ІV стадія раку порожнини рота) серед хворих з уперше встановленим діагнозом злоякісних новоутворень становила 53,3 %. Тобто кожному другому українцю, який звернувся з приводу новоутворень у порожнині рота, діагностували ІІІ та ІV стадію раку. Результати порівняльного аналізу стандартизованого показника захворюваності на ЗН РП в різних областях України показали, що найвищі показники спостерігаються у Тернопільській (5,0) та Житомирській областях (4,9) (рис. 2).
/31.jpg)
Смертність від злоякісних новоутворень порожнини рота у 2019 р. становила 4,1 випадку на 100 тис. населення (серед чоловіків — 7,3, серед жінок — 1,3). Стандартизований показник, світовий стандарт становить 2,5 на 100 тис. населення.
Фактори ризику
Факторами ризику ЗН губ та РП є куріння та інші види вживання тютюну, вживання алкоголю, опромінення, вірусні інфекції, імунодефіцити, хронічне запалення та хронічні травми (постійне накусування, тиск знімних ортопедичних конструкцій), ультрафіолетове опромінення (переважно для раку губ), інфікування папіломавірусом людини, незадовільна гігієна порожнини рота та генетична схильність (рис. 3) [11, 19–25]. Рак рота частіше розвивається у чоловіків, осіб старшого віку та представників нижчих соціально-економічних верств населення [11, 26].
Беручи до уваги те, що впливу більшості цих факторів можна уникнути, відповідно, розвитку раку слизової оболонки порожнини рота можливо запобігти. Тим не менше, цей вид раку може розвиватися й у пацієнтів, які не мають перелічених факторів ризику [23].
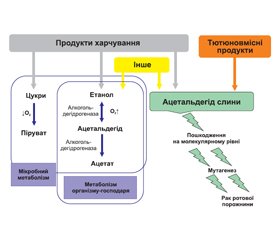
Куріння є найвагомішим фактором ризику раку рота внаслідок впливу на слизову оболонку канцерогенних хімікатів, у тому числі нітрозамінів, бензпіренів та ароматичних амінів [25]. У курців ризик розвитку раку ротової порожнини утричі більший, ніж в осіб без шкідливої звички [27]. Ризик також несе і пасивне куріння [28], а одночасне споживання алкоголю ще більше підвищує ймовірність розвитку пухлини [1]. Можливо, причиною цього є те, що алкоголь збільшує проникність слизових оболонок порожнини рота, полегшуючи надходження канцерогенів [29].
Наведені дані узгоджуються із останніми науковими дослідженнями вітчизняних вчених у даному напрямку, пов’язаними із вивченням клітинного складу слизової оболонки порожнини рота в осіб, що мали шкідливу звичку — куріння тривалістю 1–5 років. Отримані результати демонструють, що куріння є одним із чинників, які ініціюють пухлинну трансформацію [1–3].
Куріння, залежно від тривалості та інтенсивності, запускає процеси перебудови клітинного складу слизової оболонки порожнини рота у двох напрямках: запалення та дискератоз.
У першому випадку зміни клітинного складу характеризують цитоморфологічну картину хронічного катарального запалення — типового патологічного процесу, який виникає у разі ушкодження букального епітелію травматичними чинниками (у випадку куріння — поєднаним термічним та хімічним впливом). У курців було діагностовано і якісні, і кількісні зміни клітинного складу букальних епітеліоцитів. Кількісні зміни проявляються реорганізацією відсоткового співвідношення епітеліальних клітин, а саме зменшенням кількості рогових лусочок порівняно із нормою та появою парабазальних епітеліоцитів. Якісні зміни характеризуються зменшенням кількості еозинофільних гранул та структур у клітинах проміжного та поверхневого шарів, появою серед епітеліоцитів клітин із вакуолізованою цитоплазмою та узурованими контурами плазмолеми.
Аналіз клітинного складу надав можливість розробити ймовірну схему механізму порушення диференціації епітелію слизової оболонки порожнини рота у курців (рис. 4).
Зміни клітинного складу цитограм букального епітелію за умов впливу нікотину в обстеженого контингенту осіб є проявом захисно-пристосувальної реакції слизової оболонки порожнини рота на вплив патогенних факторів, спрямованої на відмежування, знищення та видалення флогогенного агента.
У свою чергу, другий напрямок морфологічної перебудови епітелію слизової оболонки порожнини рота відображає стійку тенденцію до розвитку дискератозу — порушення зроговіння епітелію. У даному випадку якісні зміни клітин проявляються цитоспецифічною організацією, характерною для різновиду білкової дистрофії, а саме рогової, яка характеризується надлишковим утворенням рогової речовини у незроговілому епітелії, тобто гіперкератозом слизової оболонки порожнини рота. Наведені зміни клітинного складу створюють передумови для розвитку лейкоплакії, яка належить до передракових станів.
Відповідно до літературних джерел останніх років, куріння, яке поєднує в собі несприятливий вплив фізичних та хімічних чинників, ініціює та підтримує хронічне запалення і, як наслідок, провокує порушення трофіки та рогову дистрофію, які супроводжуються підвищеним ризиком виникнення злоякісних проліферативних процесів. Тривале існування вогнища патологічного зроговіння слизової оболонки порожнини рота може стати джерелом розвитку ракової пухлини (рис. 5) [2]. Запальний та дискератозний процеси можна розглядати як два автономних, які виникли на слизовій оболонці порожнини рота у курців. Також їх можна розглядати і як ланки одного і того ж патогенетичного механізму на етапі пухлинної трансформації.
Останніми роками відзначається зростання захворюваності на рак порожнини рота, пов’язаний з інфікуванням вірусом папіломи людини [33]. Хоча найчастіше цей вірус асоціюють із раком шийки матки та орофарингеальними пухлинами (зокрема, новоутвореннями мигдаликів та кореня язика), існують докази зв’язку інфікування і з раком порожнини рота. Так, ця інфекція учетверо частіше має місце в осіб із сквамозноклітинною карциномою, ніж в осіб із здоровими слизовими оболонками [34].
Далі буде
Список литературы
1. Гасюк Н.В. Статистичне обґрунтування компенсаторних механізмів епітелію ясен в умовах нікотинової інтоксикації. Медична інформатика та інженерія. 2015. Т. 1. № 29. С. 42-46.
2. Гасюк Н.В., Єрошенко Г.А. Патогенетичні механізми передпухлинної цитотрансформації слизової оболонки порожнини рота в умовах нікотинової інтоксикації. Шпитальна хірургія. 2015. Т. 1. № 69. С. 64-68.
3. Гасюк Н.В., Мошель Т.Н., Попович И.Ю. Особенности качественной и количественной перестройки клеточного состава буккального эпителия в условиях никотиновой интоксикации. Український стоматологічний альманах. 2016. № 1. С. 16-20.
4. Данилевський М.Ф., Борисенко А.В., Антоненко М.Ю., Сідєльнікова Л.Ф., Несін О.Ф., Рахній Ж.І. Терапевтична стоматологія. Захворювання слизової оболонки порожнини рота. К.: Медицина, 2010. 640 с.
5. Ніколішин А.К. Терапевтична стоматологія. Вінниця: Нова книга, 2012. 680 с.
6. Abati S., Bramati C., Bondi S., Lissoni A., Trimarchi M. Oral Cancer and Precancer: A Narrative Review on the Relevance of Early Diagnosis. International journal of environmental research and public health. 2020. Vol. 17. № 24. Р. 9160. https://doi.org/10.3390/ijerph17249160
7. Applebaum E., Ruhlen T.N., Kronenberg F.R., Hayes C., Peters E.S. Oral cancer knowledge, attitudes and practices: a survey of dentists and primary care physicians in Massachusetts. Journal of the American Dental Association (1939). 2009. Vol. 140. № 4. Р. 461-467.
8. Australian Institute of Health and Welfare 2014. Head and neck cancers in Australia. Cancer series no. 83. Cat. no. CAN 80. Canberra: AIHW. https://www.aihw.gov.au/getmedia/bdccebf2-dbe6-44e2-9104-8461d7e7c165/16933.pdf.aspx?inline=true
9. Awan K.H., Patil S. Efficacy of Autofluorescence Imaging as an Adjunctive Technique for Examination and Detection of Oral Potentially Malignant Disorders: A Systematic Review. The journal of contemporary dental practice. 2015. Vol. 16. № 9. Р. 744-749.
10. Barnett T., Hoang H., Stuart J., Crocombe L. “Sorry, I’m not a dentist”: perspectives of rural GPs on oral health in the bush. Med. J. Aust. 2016. Vol. 204. № 1. doi: 10.5694/mja15.00740.
11. Bray F., Ferlay J., Soerjomataram I., Siege R.L., Torre L.A., Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: a cancer journal for clinicians. 2018. Vol. 68. № 6. Р. 394-424.
12. Cancer Research UK. Mouth and oropharyngeal cancer. 2018. https://www.cancerresearchuk.org/about-cancer/mouth-cancer/about
13. Candotto V., Lauritano D., Nardone M. et al. HPV infection in the oral cavity: epidemiology, clinical manifestations and relationship with oral cancer. Oral Implantol (Rome). 2017. Vol. 10. № 3. Р. 209-220.
14. Chainani-Wu N., Madden E., Cox D., Sroussi H., Epstein J., Silverman S. Jr. Toluidine blue aids in detection of dysplasia and carcinoma in suspicious oral lesions. Oral diseases. 2015. Vol. 21. № 7. Р. 879-885.
15. Chaturvedi P., Singh A., Chien C.Y., Warnakulasuriya S. Tobacco related oral cancer. BMJ (Clinical research ed.). 2019. Vol. 365. l2142. https://doi.org/10.1136/bmj.l2142
16. Chaturvedi P., Singhvi H.R., Malik A. The role of chronic mucosal trauma in oral cancer: A review of literature. Indian journal of medical and paediatric oncology: official journal of Indian Society of Medical & Paediatric Oncology. 2017. Vol. 38. Р. 44-50.
17. Chow L. Head and Neck Cancer. The New England journal of medicine. 2020. Vol. 382. № 1. Р. 60-72.
18. Crossman T., Warburton F., Richards M.A., Smith H., Ramirez A., Forbes L.J. Role of general practice in the diagnosis of oral cancer. The British journal of oral & maxillofacial surgery. 2016. Vol. 54. № 2. Р. 208-212.
19. de Veld D.C., Skurichina M., Witjes M.J., Duin R.P., Sterenborg H.J., Roodenburg J.L. Autofluorescence and diffuse reflectance spectroscopy for oral oncology. Lasers in surgery and medicine. 2005. Vol. 36. № 5. Р. 356-364.
20. Ferlay J., Colombet M., Soerjomataram I., Dyba T., Randi G., Bettio M., Gavin A., Visser O., Bray F. Cancer incidence and mortality patterns in Europe: Estimates for 40 countries and 25 major cancers in 2018. European journal of cancer (Oxford, England: 1990). 2018. Vol. 103. Р. 356-387.
21. Gandini S., Botteri E., Iodice S., Boniol M., Lowenfels A.B., Maisonneuve P., Boyle P. Tobacco smoking and cancer: a meta-analysis. International journal of cancer. 2008. Vol. 122. № 1. Р. 155-164.
22. Ganly I., Goldstein D., Carlson D.L., Patel S.G., O’Sullivan B., Lee N., Gullane P., Shah J.P. Long-term regional control and survival in patients with “low-risk”, early stage oral tongue cancer managed by partial glossectomy and neck dissection without postoperative radiation: the importance of tumor thickness. Cancer. 2013. Vol. 119. № 6. Р. 1168-1176.
23. Gelažius R., Gervickas A., Kubilius R. Epidemiology of primary oral cancer diagnostics in Kaunas. Stomatologija. 2018. Vol. 20. Р. 49-53.
24. Gelband H., Jha P., Sankaranarayanan R., Horton S. (eds.). Cancer: Disease Control Priorities, Third Edition. Vol. 3. The International Bank for Reconstruction and Development/The World Bank. doi: 10.1596/978-1-4648-0349-9.
25. Howlander N., Noone A.M., Krapcho M. SEER Cancer Statistics Review, 1975–2010. https://seer.cancer.gov/archive/csr/1975_2010/
26. International Agency for Research on Cancer. Incidence, Mortality and Prevalence by Cancer Site. World Source: Globocan. 2020. http://gco.iarc.fr/today/data/factsheets/populations/900-world-fact-sheets.pdf
27. Irfan M., Delgado R., Frias-Lopez J. The Oral Microbiome and Cancer. Frontiers in immunology. 2020. Vol. 11. Р. 591088. https://doi.org/10.3389/fimmu.2020.591088
28. Jafarey N.A., Mahmood Z., Zaidi S.H. Habits and dietary pattern of cases of carcinoma of the oral cavity and oropharynx. JPMA. The Journal of the Pakistan Medical Association. 1977. Vol. 27. № 6. Р. 340-343.
29. Johnson N.W., Warnakulasuriya S., Gupta P.C. et al. Global oral health inequalities in incidence and outcomes for oral cancer: causes and solutions. Advances in dental research. 2011. Vol. 23. № 2. Р. 237-246.
30. Joseph B.K. Oral cancer: prevention and detection. Medical principles and practice : international journal of the Kuwait University, Health Science Centre. 2002. Vol. 11. № 1. Р. 32-35.
31. Kato M.G., Baek C.H., Chaturvedi P. et al. Update on oral and oropharyngeal cancer staging — International perspectives. World journal of otorhinolaryngology — head and neck surgery. 2020. Vol. 6. № 1. Р. 66-75.
32. Kerawala C., Roques T., Jeannon J.P., Bisase B. Oral cavity and lip cancer: United Kingdom National Multidisciplinary Guidelines. The Journal of laryngology and otology. 2016. Vol. 130. № S2. Р. 83-89.
33. Kumar M., Nanavati R., Modi T.G., Dobariya C. Oral cancer: Etiology and risk factors: A review. Journal of cancer research and therapeutics. 2016. Vol. 12. Р. 458-463.
34. Lee Y.C., Marron M., Benhamou S. et al. Active and involuntary tobacco smoking and upper aerodigestive tract cancer risks in a multicenter case-control study. Cancer Epidemiol. Biomarkers Prev. 2009. Vol. 18. № 12. Р. 3353-3361.
35. Li Y.-N., Lu R., Zhang J., Zhou G. Inter-and intra-observer agreement on the judgment of toluidine blue staining for screening of oral potentially malignant disorders and oral cancer. Clinical Oral Investigations. 2019. Vol. 23. № 11. Р. 1709-1714.
36. Lingen M.W. et al. Evidence-based clinical practice guideline for the evaluation of potentially malignant disorders in the oral cavity. A report of the American Dental Association. Journal of the American Dental Association (1939). 2017. Vol. 148. № 10. Р. 712-727.
37. Macey R., Walsh T., Brocklehurst P. et al. Diagnostic tests for oral cancer and potentially malignant disorders in patients presenting with clinically evident lesions. The Cochrane database of systematic reviews. 2015. Vol. 2015. № 5. CD010276. https://doi.org/10.1002/14651858.CD010276.pub2
38. Macpherson L.M.D. Raising awareness of oral cancer from a public and health professional perspective. Br. Dent. J. 2018. № 225. Р. 809-814.
39. Maymone M., Greer R.O., Kesecker J. et al. Premalignant and malignant oral mucosal lesions: Clinical and pathological findings. Journal of the American Academy of Dermatology. 2019. Vol. 81. № 1. Р. 59-71.
40. Montero P.H., Patel S.G. Cancer of the oral cavity. Surgical oncology clinics of North America. 2015. Vol. 24. № 3. Р. 491-508.
41. Naruse T., Yanamoto S., Matsushita Y. et al. Cetuximab for the treatment of locally advanced and recurrent/metastatic oral cancer: An investigation of distant metastasis. Molecular and clinical oncology. 2016. Vol. 5. № 2. Р. 246-252.
42. Network NCCN. NCCN Clinical Practice Guidelines in Oncology. Head and Neck Cancers. 2013. https://oncolife.com.ua/doc/nccn/Head_and_Neck_Cancers.pdf
43. Omar E. Current concepts and future of noninvasive procedures for diagnosing oral squamous cell carcinoma — a systematic review. Head & face medicine. 2015. Vol. 11. № 6. doi: 10.1186/s13005-015-0063-z.
44. Oral Cancer — Prevention and Patient Management. URL: https://www.fdiworlddental.org/sites/default/files/2020-11/fdi-oral_cancer-prevention_and_patient_management.pdf
45. Oral Health Foundation. The State of Mouth Cancer UK Report 2018/2019. 2019. https://www.dentalhealth.org/stateofmouthcancer
46. Paré A., Joly A. Cancers de la cavité buccale: facteurs de risque et prise en charge [Oral cancer: Risk factors and management]. Presse medicale (Paris, France: 1983). 2017. Vol. 46. № 3. Р. 320-330.
47. Patton L.L., Ashe T.E., Elter J.R., Southerland J.H., Strauss R.P. Adequacy of training in oral cancer prevention and screening as self-assessed by physicians, nurse practitioners, and dental health professionals. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Endod. 2006. Vol. 102. № 6. Р. 758-764.
48. Peres M.A., Macpherson L., Weyant R.J. et al. Oral diseases: a global public health challenge. Lancet (London, England). 2019. Vol. 394. № 10194. Р. 249-260.
49. Sankaranarayanan R., Ramadas K., Thara S., Muwonge R., Thomas G., Anju G., Mathew B. Long term effect of visual screening on oral cancer incidence and mortality in a randomized trial in Kerala, India. Oral oncology. 2013. Vol. 49. № 4. Р. 314-321.
50. Sankaranarayanan R., Ramadas K., Thomas G., Muwonge R., Thara S., Mathew B., Rajan B.; Trivandrum Oral Cancer Screening Study Group. Effect of screening on oral cancer mortality in Kerala, India: a cluster-randomised controlled trial. Lancet (London, England). 2005. Vol. 365. № 9475. Р. 1927-1933.
51. Sciubba J.J. Improving detection of precancerous and cancerous oral lesions. Computer-assisted analysis of the oral brush biopsy. U.S. Collaborative OralCDx Study Group. Journal of the American Dental Association. 1999. Vol. 130. № 10. Р. 1445-1457.
52. Shanti R.M., O’Malley B.W. Jr. Surgical Management of Oral Cancer. Dental clinics of North America. 2018. Vol. 62. № 1. Р. 77-86.
53. Siegel R.L., Miller K.D., Jemal A. Cancer Statistics. CA Cancer J. Clin. 2017. Vol. 67. № 1. Р. 7-30.
54. Szturz P., Vermorken J.B. Management of recurrent and metastatic oral cavity cancer: Raising the bar a step higher. Oral oncology. 2020. Vol. 101. Р. 104492. https://doi.org/10.1016/j.oraloncology.2019.104492
55. Tiwari L., Kujan O., Farah C.S. Optical fluorescence imaging in oral cancer and potentially malignant disorders: A systematic review. Oral diseases. 2020. Vol. 26. № 3. Р. 491-510.
56. Torre L.A., Bray F., Siegel R.L., Ferlay J., Lortet-Tieulent J., Jemal A. Global cancer statistics, 2012. CA: a cancer journal for clinicians. 2015. № 65(2). Р. 87-108.
57. Wang B., Zhang S., Yue K., Wang X.D. The recurrence and survival of oral squamous cell carcinoma: a report of 275 cases. Chinese journal of cancer. 2013. Vol. 32. № 11. Р. 614-618.
58. Watters C., Brar S., Pepper T. Oral mucosa cancer. StatPearls Publishing, 2021.
59. Wong T., Wiesenfeld D. Oral Cancer. Australian dental journal. 2018. Vol. 63. № 1. Р. 91-99.
60. World Health Organisation. Oral health. 2018. https://www.who.int/news-room/fact-sheets/detail/oral-health
61. Zhang H., Dziegielewski P.T., Biron V.L. et al. Survival outcomes of patients with advanced oral cavity squamous cell carcinoma treated with multimodal therapy: a multi-institutional analysis. Journal of otolaryngology — head & neck surgery = Le Journal d’oto-rhino-laryngologie et de chirurgie cervico-faciale. 2013. Vol. 42. № 1. Р. 30. https://doi.org/10.1186/1916-0216-42-30
62. Zhang L., Williams M., Poh C.F. et al. Toluidine blue staining identifies high-risk primary oral premalignant lesions with poor outcome. Cancer Research. 2005. Vol. 65. № 17. Р. 8017-8021.

/32.jpg)
/33.jpg)
/34.jpg)