Международный эндокринологический журнал Том 18, №1, 2022
Вернуться к номеру
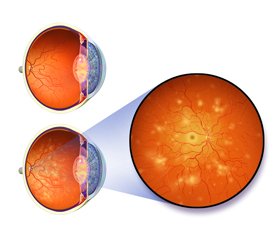
Діабетична ретинопатія: перспективи лікування
Авторы: Рудковська О.Д.
Оптика «Ясний зір», м. Сторожинець, Чернівецька обл., Україна
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
Діабетична ретинопатія (ДР) на тлі цукрового діабету (ЦД) 2-го типу — одна з основних причин сліпоти у похилому віці [1]. Деструкція макули (набряк, неоваскуляризація, рубцювання) — найчастіша причина порушення зору у пацієнтів із ЦД. Ця патологія радикально не лікується. За допомогою певних процедур (анти-VEGF терапія (терапія за допомогою антитіл до фактора росту ендотелію судин), лазерна коагуляція, хірургія) можна лише сповільнити втрату зору [2].
Золотим стандартом лікування на сьогодні вважається анти-VEGF терапія, яка зменшує набряк і неоваскуляризацію в макулі. Проте значна частина пацієнтів залишається нечутливою до анти-VEGF терапії, що підкреслює участь інших патофізіологічних механізмів у розвитку деструкції макули.
Цю тезу підтверджує наступне: вичікувальна тактика у лікуванні ДР з макулярним набряком (багатоцентрові рандомізовані дослідження [3]) дає кращі візуальні та анатомічні результати у віддаленому періоді, ніж агресивна інвазивна терапія (анти-VEGF препарати, лазерна коагуляція).
Привертає увагу і той факт, що при ДР макулярний набряк виникає на будь-якій її стадії, як на початковій, так і на кінцевій. Можна зробити висновок: процес контролюється не сітківкою, а, скоріше за все, мозком.
Нині причини виникнення очних хвороб, у тому числі ДР, до кінця не з’ясовані [3].
Ми вважаємо, що тригером офтальмопатології є слабкість акомодації [4]. Якщо у певному періоді життя зіниця надмірно звужується (хронічний стрес, переохолодження, перегрівання, гіподинамія, шкідливі звички), відстань між екватором кришталика і циліарним тілом стає меншою за вікову норму, циннові зв’язки дещо провисають, їх вплив на кришталик ослаблюється, об’єм акомодації зменшується. Оскільки акомодація (здатність сканувати небезпеку на різних відстанях) відігравала вирішальну роль у виживанні людини як виду в процесі еволюції, мозок розробив компенсаторні реакції, здатні полегшити роботу ослабленої акомодації.
Усі очні хвороби у початковій стадії спрямовані на забезпечення збільшення об’єму акомодації. Якщо це відбувається, патологічний процес стабілізується, якщо ні — відбувається хронічне прогресування захворювання (кератоконус, міопія, катаракта, глаукома, увеїт тощо).
Розглянемо викладене вище на прикладі ДР.
У початковій стадії процесу — непроліферативної ДР — спостерігається помірне зниження гостроти зору. Якщо цього достатньо для відновлення акомодаційної здатності ока (на тлі компенсованого ЦД), процес у сітківці стабілізується. Якщо організм ослаблений (ЦД некомпенсований, з ускладненнями) і акомодаційний м’яз теж слабкий, розвивається макулярний набряк, ДР переходить у проліферативну стадію.
Для «відключення» макули є ще одне обґрунтування.
Зоровий аналізатор дуже енергозатратний: його роботу обслуговують 6 пар черепно-мозкових нервів (половина із 12 наявних). Оскільки акомодаційний м’яз — один із найактивніших в організмі, при його дисфункції мозку треба виконувати значно більший об’єм роботи.
Коли загальний стан організму тяжкий, мозок намагається полегшити собі життя — блокувати зоровий аналізатор (щоб приділити більше уваги іншим життєво важливим органам і системам [3]). Мозок вибирає різні шляхи блокування зорового аналізатора (моторної і сенсорної його частин): паралітична косоокість, паралітичний мідріаз, оклюзія судин сітківки і зорового нерва, оптичний неврит, дірчастий розрив макули, відшарування сітківки, гемофтальм, метастази у центральну частину очного дна (при онкології) тощо.
У кожному випадку мозок прораховує найбільш ергономічний шлях «відключення» зорової системи, щоб не було виснаження мозкових процесів, що реалізується у нейропсихічних (включаючи деменцію) і/або соматичних хворобах.
Певно, вказані механізми контролюються на генетичному рівні.
Один із видів блоку зорової системи — набряк макули (різке зниження центрального зору). Оскільки це полегшує роботу мозку, сучасне лікування макулярного набряку не дає бажаних функціональних результатів.
Який вихід із ситуації? Підказку нам дає природа. Захворювання сітківки і зорового нерва часто супроводжуються аферентним зіничним дефектом — зіниця розширена, слабко реагує на світло. Мозок показує, що йому потрібен спокій акомодації (іннервація м’язів райдужки і акомодаційного м’яза синергічна).
Якщо проводити лікування патології заднього відділу ока на тлі циклоплегії, то ми будемо діяти в інтересах мозку (полегшимо йому роботу: економія ресурсів, які зазвичай витрачаються на акомодацію). Тому функціональні результати лікування повинні бути більш високими, ніж при стандартній терапії.
У нас є позитивний досвід: ми лікували патологію зорового нерва (передню ішемічну нейрооптикопатію, оптичний неврит), оклюзію вен сітківки на тлі циклоплегії (сумісно з носінням сонцезахисних окулярів) [4, 5]. Візуальні результати були вищими і досягались за більш короткі строки, ніж у контрольній групі, де використовувалась традиційна терапія без циклоплегії.
Ми вважаємо, що у віддаленому періоді доцільно проводити лазерний мідріаз, щоб не було умов для виникнення слабкості акомодації у майбутньому (при надмірному звуженні зіниці). Розширенню зіниці сприяє також здоровий спосіб життя [5].
При цьому слід звернути увагу на той факт, що сітківка є особливою структурою як частина мозку, винесена на периферію. Тому розлади у сітківці можуть свідчити, наприклад, про зниження когнітивних здібностей.
Одними із системних ускладнень успішної анти-VEGF терапії набряку макули є тромбоемболії: інсульт, інфаркт. Як це можна трактувати у світлі вищевикладеного? На наш погляд, при низьких ресурсах мозку підвищення гостроти зору (тобто розблокування зорового аналізатора) провокує «відключення» життєво важливих органів — мозку, серця. Іншими словами, організм хотів сплатити частковою сліпотою за своє відносне благополуччя (з двох лих вибрати менше), а ми, підвищивши гостроту зору в результаті анти-VEGF терапії, не дали йому це зробити. І тоді почались серйозні проблеми в роботі організму.
Тому циклоплегія при лікуванні патології макули повинна бути тривалою, з поступовою відміною, щоб мозок мав час адаптуватись до розблокування зорової системи.
Якщо ресурси мозку виснажені, то, очевидно, що для мозку (і організму в цілому) краще «погасити» око, щоб підтримати діяльність інших життєво важливих органів і систем на належному рівні.
В ідеалі повинні бути розроблені високочутливі інтегральні показники роботи мозку і виявлена їх динаміка залежно від стану сітківки (без ураження макули — з ураженням макули) у людей різного віку і стану здоров’я.
Тоді буде зрозуміло, у яких випадках патології сітківки офтальмологи можуть тривало боротись за підвищення зорових функцій, а в яких (резистентний набряк макули тощо) це безперспективно, оскільки при значному підвищенні зору в ослабленому організмі можуть наступити необоротні зміни, які погіршать його виживання, і мозок, не зацікавлений у такій ситуації, все одно «погасить» хворе око.
Отже, нами теоретично обґрунтовано, що терапія патології сітківки (у тому числі діабетичної ретинопатії) на тлі «виключеної» акомодації (а в подальшому — лазерного мідріазу) може забезпечити певний приріст зорових функцій не тільки у короткотривалій, але й у довготривалій перспективі. Цій стратегії повинні передувати глибокі нейрофізіологічні дослідження.
Отримано 11.01.2022
Список литературы
- Wang W., Lo A.C.Y. Diabetic Retinopathy: Pathophysiology and Treatments. Int J. Mol. Sci. 2018 Jun 20. 19(6). 1816. doi: 10.3390/ijms19061816.
- Duh E.J., Sun J.K., Stitt A.W. Diabetic retinopathy: current understanding, mechanisms, and treatment strategies. JCI Insight. 2017 Jul 20. 2(14). e93751. doi: 10.1172/jci.insight.93751.
- Prescrire Redaction. Diabetic macular oedema without visual impairment. Prescrire International. 2020. 29(217). 190.
- Rudkovska O. Refraction and Accommodation in the Etiopathogenesis of the Eye Diseases. Collection of scientific articles. Saarbrucken, Germany: LAP LAMBERT Academic Publishing, 2013. 75 p.
- Rudkovska O. Weakness of Accommodation is a Trigger for Eye Diseases. Saarbrucken, Germany: LAP LAMBERT Academic Publishing, 2017. 85 p.