Резюме
Проблема зловживання алкоголем, яка спостерігається у майже п’ятої частини населення нашої планети, є однією з найбільш соціально значущих у всьому світі. Відомо, що від 25 до 85 % пацієнтів перебувають у стані алкогольної інтоксикації під час госпіталізації до відділення політравми. Метою роботи було визначити вміст основних метаболітів вуглеводного метаболізму, зокрема глюкози, піровиноградної кислоти та молочної кислоти, у крові пацієнтів із поєднаною травмою та алкогольним делірієм залежно від способу седації. Матеріали та методи. У дослідження включено 80 пацієнтів з політравмою середньої тяжкості та у стані відміни алкоголю, ускладненому алкогольним делірієм. Медіана віку становила 45 років [39–54]. Пацієнтам групи 1 (n = 40) як метод седації вводили дексмедетомідин, у групі 2 (n = 40) використовували седацію діазепамом за симптом-тригерним протоколом. Для діагностики делірію використовували метод CAM-ICU. У крові пацієнтів визначали концентрацію глюкози, молочної кислоти та піровиноградної кислоти (пірувату). Результати. Уміст глюкози в крові хворих 1-ї групи при надходженні до ВІТ становив 7,45 [6,52; 8,97] ммоль/л, що у 1,7 раза вище цього показника у контрольній групі, на 3-тю добу зменшувався на 9,4 % порівняно з рівнем, що визначався на 1-шу добу надходження до ВІТ, та становив 6,75 [6,13; 8,0] ммоль/л, але не досягав рівня глюкози у контрольній групі та залишався вищим на 55,1 % порівняно з контролем. На 7-му добу вміст глюкози в крові зменшувався до нормальних значень та становив 5,55 [4,9; 5,9] ммоль/л. У хворих 2-ї групи рівень глюкози становив 8,3 [7,2; 9,87] ммоль/л, що в 1,9 раза вище, ніж у контрольній групі. На 3-тю добу рівень глюкози в крові зменшувався на 6 % до 7,8 [6,95; 9,2] ммоль/л, а через тиждень після надходження становив 6,6 [4,9; 5,9] ммоль/л. У хворих 1-ї групи рівень пірувату у день надходження до ВІТ становив 0,127 [0,115; 0,130] ммоль/л, лактату — 2,345 [2,11; 2,66] ммоль/л, співвідношення лактат/піруват — 18,46. Ці ж показники у пацієнтів 2-ї групи були дещо вищими: піруват — 0,129 [0,104; 0,147] ммоль/л, лактат — 2,535 [2,33; 2,81] ммоль/л, лактат/піруват — 19,65. На 7-му добу серед пацієнтів 1-ї групи рівень пірувату сягав 0,103 [0,098; 0,111] ммоль/л, лактату — 2,040 [1,86; 2,19] ммоль/л, лактат/піруват — 19,81. У пацієнтів 2-ї групи на 7-й день рівень пірувату сягав 0,108 [0,093; 0,129] ммоль/л, лактату — 2,455 [2,26; 2,748] ммоль/л, лактат/піруват — 22,73. Таким чином, гіперглікемія спостерігалася в крові хворих з політравмою та синдромом відміни алкоголю, ускладненим алкогольним делірієм, під час надходження до стаціонару, на 3-тю добу перебування в стаціонарі (1-ша та 2-га групи) та на 7-му добу у пацієнтів 2-ї групи, що свідчить про порушення біохімічних механізмів, що сприяють гомеостазу глюкози в крові. Висновки. Використання дексмедетомідину для седації пацієнтів у стані відміни алкоголю та з алкогольним делірієм і політравмою зменшує прояви порушень вуглеводного обміну.
Alcohol abuse, which affects almost one-fifth of the world’s population, is one of the most socially significant in the world. It is known that from 25 to 85 % of patients are in a state of alcohol intoxication during hospitalization to the Polytrauma Department. The study was aimed to determine the content of major metabolites of carbohydrate metabolism, in particular glucose, pyruvic acid, and lactic acid in the blood of patients with combined trauma and alcoholic delirium, depending on the method of sedation. Materials and methods. The study included 80 patients with moderate polytrauma and alcohol withdrawal complicated by alcohol delirium. The median age was 45 years [39–54]. Patients in group 1 (n = 40) were given dexmedetomidine as a sedation method, and in group 2 (n = 40), diazepam sedation was used according to the symptom-trigger protocol. The CAM-ICU method was used to diagnose delirium. The concentration of glucose, lactic acid, and pyruvic acid (pyruvate) was determined in the patients’ blood. Results. The blood content of glucose of patients of group 1 on admission to ICU was 7.45 [6.52; 8.97] mmol/L, which is 1.7 times higher than this indicator in the control group; on the 3rd day, it decreased by 9.4 % compared to the first day of admission to ICU and was 6.75 [6.13; 8.0] mmol/L but did not reach the level of glucose in the control group and remained higher by 55.1 % compared to the control. On the 7th day, the blood glucose content decreased to normal values and amounted to 5.55 [4.9; 5.9] mmol/L. In patients of group 2, the glucose level was 8.3 [7.2; 9.87] mmol/L, which is 1.9 times higher than in the control group. On the 3rd day, the blood glucose level decreased by 6 % to 7.8 [6.95; 9.2] mmol/L, and a week after admission, it was 6.6 [4.9; 5.9] mmol/L. In patients of group 1, the level of pyruvate at the admission to the ICU was 0.127 [0.115; 0.130] mmol/L, lactate — 2.345 [2.11; 2.66] mmol/L, lactate/pyruvate ratio — 18.46. The same rates in patients of group 2 were slightly higher: pyruvate — 0.129 [0.104; 0.147] mmol/L, lactate — 2.535 [2.33; 2.81] mmol/L, lactate/pyruvate ratio — 19.65. On the 7th day, among the patients of group 1, the level of pyruvate reached 0.103 [0.098; 0.111] mmol/L, lactate — 2.040 [1.86; 2.19] mmol/L, lactate/pyruvate ratio — 19.81. In patients of group 2, on the 7th day the level of pyruvate reached 0.108 [0.093; 0.129] mmol/L, lactate — 2.455 [2.26; 2.748] mmol/L, lactate/pyruvate ratio — 22.73. Thus, hyperglycemia was observed in the blood of patients with polytrauma and alcohol withdrawal syndrome complicated by alcoholic delirium on admission, on the 3rd day of hospital stay (groups 1 and 2) and the 7th day in patients of group 2, indicating violation of biochemical mechanisms that promote blood glucose homeostasis. Conclusions. The use of dexmedetomidine for sedation of patients with alcohol withdrawal and alcoholic delirium and polytrauma reduces the manifestations of carbohydrate metabolism disorders.
Вступ
Проблеми, пов’язані зі зловживанням алкоголем, є глобальним тягарем хвороб. Алкоголь має здатність погіршувати перебіг ендогенних захворювань, включаючи серцево-судинні захворювання, нервово-психічні розлади, злоякісні новоутворення та захворювання шлунково-кишкового тракту [1]. Вживання алкоголю збільшує ризик травмування, потенціює агресивну поведінку та подовжує час реакції [2]. Серед важливих ланок обміну речовин в організмі є метаболізм вуглеводів. В умовах розвитку патологічних станів, зокрема інтоксикації, системної запальної реакції, гіпоксії при синдромі відміни алкоголю (СВА), ускладненому алкогольним делірієм у поєднанні з політравмою, можуть виникати зміни перебігу реакцій обміну вуглеводів, біосинтезу глікопротеїнів та інших важливих біологічно активних речовин, у яких складовою є саме вуглеводи. Відомо, що вуглеводи можуть виконувати роль медіаторів запалення, речовин з протизапальними властивостями, структурну функцію як компоненти клітинних мембран (гліколіпіди) та екстрацелюлярного матриксу тощо. За даними авторів, через гіпоксичний стан в організмі пацієнтів відбуваються адаптивні зміни метаболізму вуглеводів з інтенсифікацією анаеробного гліколізу [3, 4]. Відповідно до результатів клінічних та експериментальних досліджень, компенсаторні зміни на тлі гіпоксії включають модуляцію вуглеводного обміну, зокрема інтенсифікацію анаеробного гліколізу. Закономірним наслідком цих змін є зсув співвідношення лактат/піруват (із переважанням лактату), що з точки зору енергозабезпечення клітин є невигідним.
Тому метою роботи було визначити вміст основних метаболітів вуглеводного метаболізму, зокрема глюкози, піровиноградної кислоти та молочної кислоти, у крові пацієнтів із поєднаною травмою та СВА з алкогольним делірієм залежно від способу седації.
Матеріали та методи
У дослідження включено 80 пацієнтів з політравмою середньої тяжкості у стані відміни алкоголю, ускладненому алкогольним делірієм (АД), які перебували на лікуванні у 2016–2018 роках на базі відділення політравми та анестезіології на 12 ліжок для інтенсивної терапії хворих зі сполученою травмою КЗОЗ «Харківська міська клінічна лікарня швидкої та невідкладної медичної допомоги ім. проф. О.І. Мещанінова». Контрольну групу становили 20 здорових добровольців віком від 20 до 48 років. Критерії включення пацієнтів: вік від 19 до 60 років, наявність пошкоджень у двох і більше анатомо-функціональних ділянках, ступінь тяжкості травматичного пошкодження за шкалою ISS 9–15 балів (середня тяжкість), тяжкість стану постраждалих за шкалою APACHE II 7–14 балів, стан хронічної алкогольної інтоксикації (ХАІ), виявлений при кількості балів ≥ 7 у модифікованому тесті «Сітка LeGo», 3 і більше позитивні відповіді в опитувальнику «CAGE», встановлений АД (збудження за шкалою RASS ≥ +2; галюцинації; судоми та наявність АД за шкалою CAM-ICU). У дослідження не входили пацієнти, яким було необхідне проведення загальної анестезії, які мали тяжку супутню патологію (черепно-мозкова травма; декомпенсація будь-якої супутньої патології на момент отримання травми, хвороби крові, онкологічні захворювання, гостре порушення мозкового кровообігу; психічні захворювання, вживання будь-яких наркотичних речовин, окрім алкоголю), шок. Усім 80 хворим у стаціонарі проводились обстеження згідно з медико-економічними стандартами надання медичної допомоги. Дослідження проводилося згідно з принципами Гельсінської декларації Світової медичної асоціації «Етичні засади медичних досліджень, що стосуються людських суб’єктів» (змінена в жовтні 2013 року). Письмова інформована згода була отримана від усіх хворих, які брали участь у дослідженні.
Для забезпечення виконання завдань дослідження пацієнти були розділені на 2 групи, виходячи з методів седації. Для розподілу пацієнтів використовувалася фіксована проста рандомізація із застосуванням методу випадкових чисел.
Група 1 (n = 40) включала пацієнтів з політравмою та тяжким станом відміни алкоголю, ускладненим алкогольним делірієм, яким проводилась седація дексмедетомідином. Початкову швидкість інфузії встановлювали на рівні 0,7 мкг/кг/год та коригували в межах 0,2–1,4 мкг/кг/год залежно від досягнення цілей седації (–2 до 0 за шкалою RASS і оцінка CIWA-Ar < 15).
Група 2 (n = 40) включала пацієнтів з політравмою та тяжким станом відміни алкоголю, ускладненим алкогольним делірієм, яким проводилась седація діазепамом за симптом-тригерним протоколом. Діазепам вводили кожні 30 хвилин за необхідності, щоб контролювати активні симптоми відміни.
Концентрацію глюкози в крові визначали глюкозооксидазним методом з використанням наборів реактивів фірми «Філісіт-Діагностика» (Україна). Концентрацію молочної кислоти в сироватці крові визначали ферментативним колориметричним методом. У роботі використовували реактиви фірми Dialab (Австрія). Уміст піровиноградної кислоти (пірувату) в крові визначали за Фрідеманом і Хаугеном ферментативним методом.
Статистичний аналіз проводили з використанням пакета прикладних програм для статистичної обробки даних Statistica 7.0 for Windows (StatSoft Inc., США) та Microsoft Excel 2010, призначених для вирішення медико-біологічних завдань. Математичну обробку отриманих результатів проводили відповідно до загальноприйнятої методики статистичного аналізу. З урахуванням характеру розподілу аналізованих величин застосовувалися параметричні (середнє значення, стандартне відхилення) і непараметричні методи. Кількісні ознаки з нормальним розподілом наведені у вигляді М ± σ, де М — середнє значення, σ — стандартне відхилення. Ознаки, розподіл яких відрізнявся від нормального, наведені у вигляді Ме (медіана), довірчий інтервал у межах першого та третього квартиля [QI–QIII].
Результати
Характеризуючи такий біохімічний показник вуглеводного обміну, як уміст глюкози у сироватці крові, треба зазначити, що в усіх пацієнтів з політравмою та СВА, ускладненим алкогольним делірієм, яким для седації застосовувався дексмедетомідин (група 1), та у пацієнтів, яким застосовували як седативні препарати діазепам, галоперидол (група 2), спостерігалися зміни цього інтегрального показника обміну вуглеводів у крові порівняно зі здоровими людьми. Що стосується вмісту глюкози в крові хворих 1-ї групи, які потрапили до відділення інтенсивної терапії (ВІТ), то у них на 1-шу добу спостерігалася стійка гіперглікемія: рівень глюкози становив 7,45 [6,52; 8,97] ммоль/л, що у 1,7 раза вище цього показника у контрольній групі. Під час надання періопераційної інтенсивної терапії пацієнтам визначали вміст глюкози в крові на 3-тю та 7-му добу після госпіталізації. Після застосування інтенсивної терапії з додаванням препарату дексмедетомідину (1-ша група пацієнтів) уміст глюкози на 3-тю добу зменшувався на 9,4 % порівняно з показником, що визначався на 1-шу добу надходження до ВІТ, та становив 6,75 [6,13; 8,0] ммоль/л, але не досягав рівня глюкози у контрольній групі та залишався вищим на 55,1 % порівняно з контролем. На 7-му добу вміст глюкози в крові зменшувався до нормальних значень та становив 5,55 [4,9; 5,9] ммоль/л, що на 26,5 % нижче порівняно зі вмістом глюкози в крові на 1-шу добу (Р < 0,0001) після надходження до стаціонару (рис. 1).
У другій групі пацієнтів з алкогольним анамнезом при політравмі (призначення діазепаму за симптом-тригерним протоколом та галоперидолу в якості седативних препаратів) під час надходження до відділення інтенсивної терапії також спостерігалася гіперглікемія — вміст глюкози в крові становив 8,3 [7,2; 9,87] ммоль/л, що в 1,9 раза вище, ніж у контрольній групі. На третю добу рівень глюкози в крові зменшувався на 6 %, до 7,8 [6,95; 9,2] ммоль/л, а через тиждень після надходження до стаціонару знижувався на 20,5 % порівняно з першим вимірюванням глюкози, але не досягав нормальних значень цього показника у контрольній групі та становив 6,6 [4,9; 5,9] ммоль/л, що було на 51,7 % вище, ніж у контрольній групі (рис. 2).
/65.jpg)
Таким чином, гіперглікемія спостерігалася в крові хворих з політравмою та СВА, ускладненим алкогольним делірієм, під час надходження до стаціонару, на 3-тю добу перебування в стаціонарі (1-ша та 2-га групи) та на 7-му добу у пацієнтів 2-ї групи, що свідчить про порушення біохімічних механізмів, що сприяють гомеостазу глюкози в крові. Це може бути пов’язано зі змінами гормонального патерну, панкреатопатією, патологією печінки (токсичний гепатит, цироз), підвищенням умісту гормонів стресу тощо.
Так, проведені дослідження дали змогу інтегрально оцінити можливі порушення обміну вуглеводів та охарактеризувати особливості енергетичного забезпечення організму при поєднанні політравми та СВА, ускладненого алкогольним делірієм. Уміст метаболітів обміну вуглеводів у сироватці крові при надходженні у стаціонар та через тиждень перебування у відділенні інтенсивної терапії за умов прийому різних седативних препаратів у групах пацієнтів наведено в табл. 1 та на рис. 3.
В основному всі чинники, що викликають підвищення вмісту лактату, як правило, призводять і до збільшення концентрації пірувату в крові, тому лактат і піруват рекомендовано визначати одночасно.
Відомо, що піровиноградна кислота є одним із основних метаболітів вуглеводного обміну. Ця речовина утворюється в тканинах у процесах глікогенолізу, дихотомічного розщеплення глюкози (гліколізу), при перетворенні лактату за умов дії лактатдегідрогенази, а також унаслідок перетворень низки амінокислот. З даних літератури відомо, що найбільш різке підвищення концентрації пірувату спостерігається при інтенсивній м’язовій роботі, гіповітамінозі В1 тощо, що визначається при хронічному алкоголізмі.
За результатами проведених досліджень, у хворих з політравмою на тлі хронічного алкоголізму спостерігається підвищення вмісту пірувату порівняно зі здоровими людьми (табл. 1, 2, рис. 3, 4). Так, у пацієнтів 1-ї групи при надходженні до стаціонару вміст пірувату в крові був на 53,0 % вищий порівняно з контрольною групою, через тиждень лікування із застосуванням дексмедетомідину вірогідно знижувався на 18,9 %, але не досягав значень контрольної групи (залишався на 24,1 % вищим порівняно з контролем) (рис. 3).
У 2-й групі пацієнтів також спостерігалася гіперпіруватемія: при надходженні до стаціонару вміст був на 55,4 % вищим порівняно зі здоровими людьми, залишався також підвищеним через тиждень лікування на 30,1 % (рис. 4, табл. 2) та не повертався до нормальних значень.
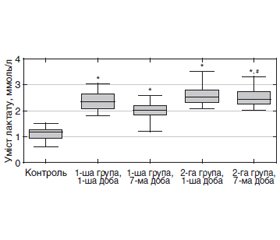
При аналізі вмісту лактату в крові хворих з політравмою та СВА, ускладненим алкогольним делірієм, при надходженні до ВІТ спостерігалось суттєве підвищення цього показника на 97,1 та 113,0 % відповідно у пацієнтів 1-ї та 2-ї групи (табл. 1, рис. 4). Через тиждень після проведення інтенсивної терапії у пацієнтів 1-ї групи спостерігалося вірогідне зниження вмісту лактату в крові на 13 % (Р < 0,0001) порівняно з умістом цього показника під час надходження до стаціонару (табл. 2, рис. 5).
Щодо вмісту лактату в крові пацієнтів, яким було призначено бензодіазепіни та галоперидол за потребою (2-га група), через тиждень цей показник залишався незмінним (Р > 0,31) та на 106,3 % перевищував рівень лактату в контрольній групі (рис. 5).
Причиною гіперпіруватемії та гіперлактатемії у пацієнтів може також бути порушення ферментативного перетворення цих сполук на продукти розпаду.
Одним із важливих чутливих показників стану метаболізму вуглеводів, а саме балансу анаеробних та аеробних процесів в організмі, є співвідношення лактат/піруват, яке у контрольній групі становило 14,33. У хворих 1-ї групи спостерігалося значне підвищення цього співвідношення: 18,6 та 19,81 при надходженні до ВІТ та через тиждень після лікування відповідно. Практично таке ж значення цього співвідношення спостерігалося у хворих 2-ї групи — 19,65 та 22,73 відповідно до часу перебування у ВІТ. Останні цифри свідчать про перебудову енергетичного забезпечення тканин організму під час перебування пацієнтів у ВІТ.
Обговорення
У пацієнтів з політравмою відмічається накопичення лактату як результат прогресуючої гіпоксії тканин. Зважаючи на те, що за хронічного алкоголізму також має місце порушення трофіки тканин та розвиток гіпоксії, у пацієнтів із поєднанням політравми та алкоголізму ці зміни будуть ще більш вираженими. Крім того, за умов зловживання алкоголем дуже типовим є пригнічення функціонування піруват- та альфакетоглутаратдегідрогеназних комплексів через нестачу деяких коферментів, зокрема тіамінпірофосфату (абсорбція тіаміну із ШКТ виражено знижується при прийомі алкоголю) [5, 6]. Тому для даної категорії пацієнтів характерним є накопичення пірувату у тканинах, що, з одного боку, свідчить про порушення функціонування циклу трикарбонових кислот, а з іншого — спричиняє клінічні прояви у вигляді периферичної нейропатії та симптомокомплексу синдрому Верніке — Корсакова [7, 8]. Застосування дексмедетомідину асоціюється з менш вираженим впливом на метаболізм вуглеводів у пацієнтів з травмою [6, 8].
Висновки
Таким чином, у пацієнтів з політравмою та СВА, ускладненим алкогольним делірієм, відбувається інтенсифікація процесів анаеробного гліколізу, про що свідчить підвищення вмісту пірувату, лактату, співвідношення лактат/піруват та розвиток гіпоксичного стану.
За умов застосування дексмедетомідину як седативного засобу в терапії алкогольного делірію у пацієнтів з політравмою та синдромом відміни алкоголю відбувається зменшення проявів порушення обміну вуглеводів.
Беручи до уваги провідну роль процесів анаеробного гліколізу при стані відміни алкоголю, ускладненому алкогольним делірієм, у пацієнтів з політравмою показники метаболізму вуглеводів можуть використовуватись для прогнозування перебігу даної патології, а також ефективності обраної тактики лікування.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів і власної фінансової зацікавленості при підготовці даної статті.
Інформація про фінансування. Дослідження є фрагментом науково-дослідницької роботи кафедри медицини невідкладних станів, анестезіології та інтенсивної терапії Харківського національного медичного університету МОЗ України «Вибір методів знеболення та інтенсивної терапії у пацієнтів з синдромом системної запальної відповіді» (номер державної реєстрації 0199U001773).
Інформація про внесок кожного автора: А.В. Омельченко-Селюкова — збір та обробка матеріалів, аналіз отриманих даних, написання тексту; С.С. Дубівська — концепція та дизайн дослідження, написання тексту.
Отримано/Received 12.11.2021
Рецензовано/Revised 26.11.2021
Прийнято до друку/Accepted 30.11.2021
/66_3.jpg)

/65.jpg)
/65_2.jpg)
/66.jpg)
/66_2.jpg)