Журнал «Медицина неотложных состояний» Том 18, №2, 2022
Вернуться к номеру
COVID-19 і сепсис: клінічні паралелі особливостей перебігу та напрямки лікування
Авторы: Кучинська І.А. (1, 2), Богомаз В.М. (2, 3), Галушко О.А. (1), Сидорова А.О. (2, 3), Андрюхов А.Г. (2), Романюк В.П. (2, 3), Антонюк Л.І. (2)
(1) — Національний університет охорони здоров’я України імені П.Л. Шупика, м. Київ, Україна
(2) — МЦ «Універсальна клініка «Оберіг», м. Київ, Україна
(3) — Національний медичний університет імені О.О. Богомольця, м. Київ, Україна
Рубрики: Медицина неотложных состояний
Разделы: Справочник специалиста
Версия для печати
Стаття присвячена аналізу синдромокомплексів при сепсисі та тяжкому перебігу COVID-19, визначені основні патофізіологічні пріоритети в діагностиці та відмінності в лікуванні.
The article analyzes syndrome complex in sepsis and severe COVID-19, identifies the main pathophysiological priorities in the diagnosis and differences in treatment. Adaptation of existing treatment regimens for diseases with similar pathogenesis may help to improve treatment outcomes and reduce SARS-CoV-2-related mortality. However, when discussing the parallels between COVID-19 and sepsis, focusing on their similarities in immunopathogenesis and pathophysiology, the proposed treatment options should be reviewed based on the patient’s clinical assessment and laboratory parameters individually.
сепсис; синдром системної запальної відповіді; COVID-19; імуносупресія; діагностичні критерії; лікування; огляд
sepsis; systemic inflammatory response syndrome; COVID-19; immunosuppression; diagnostic criteria; treatment; review
Вступ
Імунопатогенез та патофізіологічні аспекти сепсису та COVID-19
COVID-19 — дизрегуляція імунної системи?
Власні спостереження
Обговорення
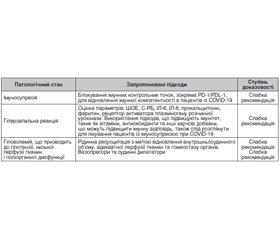
Підходи до лікування тяжкої форми COVID-19: уроки сепсису
Відмінності у лікуванні тяжкої форми COVID-19: уроки сепсису
Висновки
- Schlapbach L.J., Trick J., Roger T. Editorial: The immunology of sepsis-understanding host susceptibility, pathogenesis of disease, and avenues for future treatment. Front. Immunol. 2020. 11. 1-4. doi: 10.3389/fimmu.2020.01263.
- Rudd K.E., Johnson S.C., Agesa K.M. et al. Global, regional, and national sepsis incidence and mortality, 1990–2017: analysis for the Global Burden of Disease Study. Lancet. 2020. 395. 200-11. doi: 10.1016/S0140-6736(19)32989-7.
- Chang J.C. Sepsis and septic shock: endothelial molecular pathogenesis associated with vascular microthrombotic disease. Thromb. J. 2019. 17. 1-9. doi: 10.1186/s12959-019-0198-4.
- Angus D.C., Van Der Poll T. Severe sepsis and septic shock. New Engl. J. Med. 2013. 369. 840-51. doi: 10.1056/NEJMra1208623.
- Pop-Began V., Păunescu V., Grigorean V., Pop-Began D., Popescu C. Molecular mechanisms in the pathogenesis of sepsis. J. Med. Life. 2014. 7. 38-41. doi: 10.4172/2155-9899.S1.019.
- Chousterman B.G., Swirski F.K., Weber G.F. Cytokine storm and sepsis disease pathogenesis. Semin. Immunopathol. 2017. 39. 517-28. doi: 10.1007/s00281-017-0639-8.
- Huang M., Cai S., Su J. The pathogenesis of sepsis and potential therapeutic targets. Int. J. Mol. Sci. 2019. 20. 1-31. doi: 10.3390/ijms20215376.
- Poll T., van de Veerdonk F.L., Scicluna B.P., Netea M.G. The immunopathology of sepsis and potential therapeutic targets. Nat. Rev. Immunol. 2017. 17. 407-20. doi: 10.1038/nri.2017.36.
- Huang C., Wang Y., Li X., Ren L., Zhao J., Hu Y. et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020. 395. 497-506. doi: 10.1016/S0140-6736(20)30183-5.
- Qin C., Zhou L., Hu Z. et al. Dysregulation of immune response in patients with Coronavirus 2019 (COVID-19) in Wuhan, China. Clin. Infect. Dis. 2020. 71. 762-8. doi: 10.1093/cid/ciaa248.
- Huang C., Wang Y., Li X. et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020. Feb. 15. 395(10223). 497-506.
- Qin C., Zhou L., Hu Z. et al. Dysregulation of Immune Response in Patients with Coronavirus 2019 (COVID-19) in Wuhan, China. Clin. Infect. Dis. 2020 Jul. 28. 71(15). 762-768.
- Wang C., Xie J., Zhao L. et al. Alveolar macrophage dysfunction and cytokine storm in the pathogenesis of two severe COVID-19 patients. E. Bio. Med. 2020. 57. 1-9. doi. 10.1016/j.ebiom.2020.102833.
- Leisman D.E., Ronner L., Pinotti R., Taylor M.D., Sinha P., Calfee C.S. et al. Cytokine elevation in severe and critical COVID-19: a rapid systematic review, meta-analysis, and comparison with other inflammatory syndromes. Lancet Respiratory Med. 2020. 8. 1233-44. doi: 10.1016/S2213-2600(20)30404-5.
- Remy K.E., Mazer M., Striker D.A., Ellebedy A.H., Walton A.H., Unsinger J. et al. Severe immunosuppression and not a cytokine storm characterizes COVID-19 infections. JCI Insight. 2020. 5. 1-15. doi. 10.1172/jci.insight.140329.
- Wang F., Nie J., Wang H., Zhao Q., Xiong Y., Deng L. et al. Characteristics of peripheral lymphocyte subset alteration in COVID-19 pneumonia. J. Infect. Dis. 2020. 221. 1762-9. doi: 10.1093/infdis/jiaa150.
- Zheng M., Gao Y., Wang G., Song G., Liu S., Sun D. et al. Functional exhaustion of antiviral lymphocytes in COVID-19 patients. Cell. Mol. Immunol. 2020. 17. 533-5. doi: 10.1038/s41423-020-0402-2.
- Костюк Т.Р., Левчук А.О., Сидорова А.О. Вивчення ролі лімфопенії у перебігу коронавірусної хвороби COVID-19 у госпіталізованих пацієнтів. Український науково-медичний молодіжний журнал. 2021. № 3. С. 42.
- Roham M., Abbaszadeh A., Zendehdel A., Momeni M., Mirzae N., Gholami M. Prognostic factors of sepsis rapid progression in patients admitted to Intensive Care Unit. Ann. Trop. Med. Public. Health. 2017. 10. 1770-3. doi: 10.4103/ATMPH.ATMPH_646_17.
- Perez-Guzman P.N., Daunt A., Mukherjee S., Crook P., Forlano R., Kont M.D. et al. Clinical characteristics and predictors of outcomes of hospitalized patients with Coronavirus Disease 2019 in a Multiethnic London National Health Service Trust: A retrospective cohort study. Clin. Infect. Dis. 2020. 1-11. doi: 10.1093/cid/ciaa1091.
- Zhou F., Yu T., Du R., Fan G., Liu Y., Liu Z. et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020. 395. 1054-62. doi: 10.1016/S0140-6736(20)30566-3.
- Zhou F., Yu T., Du R. et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020 Mar. 28. 395(10229). 1054-1062.
- Alhazzani W., Miller M.H., Arabi Y.M., Loeb M., Gong M.N., Fan E. et al. Surviving sepsis campaign: guidelines on the management of critically ill adults with Coronavirus Disease 2019 (COVID-19). Intens. Care Med. 2020. 46. 854-7. doi: 10.1007/s00134-020-06022-5.
- Grein J., Ohmagari N., Shin D. et al. Compassionate Use of Remdesivir for Patients with Severe COVID-19. Engl. J. Med. 2020 Jun. 11. 382(24). 2327-2336.
- Shakoory B., Carcillo J.A., Chatham W.W. et al. Interleukin-1 Receptor Blockade Is Associated With Reduced Mortality in Sepsis Patients With Features of Macrophage Activation Syndrome: Reanalysis of a Prior Phase III Trial. Crit. Care Med. 2016 Feb. 44(2). 275-81.
- Horby P., Lim W.S., Emberson J.R. et al. Dexamethasone in Hospitalized Patients with COVID-19. RECOVERY Collaborative Group. Engl. J. Med. 2021 Feb. 25. 384(8). 693-704. [PubMed] [Ref list] (RECOVERY).
- Кучинська І.А., Савченко Б.О., Андрюхов А.Г., Іванченко А.М., Асташкіна Н.В., Гулеватий Є.О. Синдром поліорганної недостатності в пацієнтів із тяжким перебігом коронавірусної хвороби (COVID-19). Медицина невідкладних станів. 2021. 17 (2). C. 30-38. DOI: https. //doi.org/10.22141/2224-0586.17.2.2021.230632.
- Langford B.J., So M., Raybardhan S., Leung V., Westwood D., MacFadden D.R., Soucy J.R., Daneman N. Bacterial co-infection and secondary infection in patients with COVID-19: a living rapid review and meta-analysis. Clin. Microbiol. Infect. 2020 Dec. 26(12). 1622-1629.
- Ketcham S.W., Bolig T.C., Molling D.J., Sjoding M.W., Flanders S.A., Prescott H.C. Causes and Circumstances of Death among Patients Hospitalized with COVID-19: A Retrospective Cohort Study. Ann. Am. Thorac. Soc. 2021 Jun. 18(6). 1076-1079.
- Halushko O., Loskutov O., Kuchynska I., Boliuk M., Synytsyn M. The Main causes of the complicated course of COVID-19 in patients with diabetes mellitus and treatment (review). Georgian Medical News. 2020 Oct. 307. 114-120. PMID: 33270588.

/23.jpg)