Вступ
Більшість пацієнтів травматологічного профілю — це люди літнього віку, які мають багаж супутніх хронічних захворювань, що нерідко змушують відмовлятися від давно відомих схем післяопераційного знеболювання з метою запобігання небажаним наслідкам. Ця категорія пацієнтів є складною для менеджменту як травматологів, так і анестезіологів. Оперативні втручання проводяться в умовах застосування як тотальної інтравенозної анестезії (ТІВА) із традиційним використанням наркотичних анальгетиків, інгаляційних анестетиків, так і нейроаксіальних методів знеболювання: спінальної анестезії, епідуральної анальгезії, їх комбінації між собою та з провідниковими методиками, наприклад PENG блоком. Особливістю лікування є металоостеосинтез (МОС). МОС — це сучасний метод лікування складних ушкоджень кісток і суглобів за допомогою спеціальних імплантів: пластин, стрижнів та спиць для зовнішньої фіксації, які закріплюються на кісткових уламках і відновлюють єдність кісток. МОС у даний час є одним із найбільш ефективних втручань у травматології та ортопедії. За допомогою МОС вдається повністю або частково відновлювати функціональність після складних осколкових пошкоджень, переломів, уроджених чи набутих дефектів кісткової тканини. Зазвичай у низці випадків такі оперативні втручання довготривалі і болючі, тому вимагають адекватного післяопераційного знеболювання.
Ефективне післяопераційне знеболювання пацієнтів травматологічного профілю, як і всіх післяопераційних хворих, одне з найважливіших і водночас непростих завдань сучасної медицини. Сучасні схеми мультимодальної анальгезії обов’язково включають парацетамол та нестероїдні протизапальні препарати (НПЗП) із метою впливу на різні ланцюги сприйняття болю та зменшення використання опіоїдів та уникнення всім відомих побічних ефектів від їх використання.
За останні роки на фармацевтичному ринку не з’являються нові неопіоїдні анальгетики, якими б можливо було доповнити або змінити сучасні схеми мультимодального знеболювання. Тому єдиної ефективної на 100 % схеми мультимодального післяопераційного знеболювання пацієнтів травматологічного профілю на сьогодні не існує.
Ми пропонуємо огляд мультимодальної схеми знеболювання післяопераційного періоду в травматології та перспективи використання неопіоїдного анальгетика центрального механізму дії — нефопаму гідрохлориду.
Матеріали та методи
Проведений аналіз існуючих алгоритмів та рекомендацій щодо періоперативного знеболювання, пошук у медичних базах даних MEDSCAPE, PubMed, наведений власний досвід застосування нефопаму для знеболювання в періоперативному періоді пацієнтки із МОС стегнової кістки.
Результати
Сучасний алгоритм менеджменту болю у ВРІТ «Clinical Practice Guidelines for the Prevention and Management of Pain, Agitation/Sedation, Delirium, Immobility, and Sleep Disruption in Adult Patients in the ICU (PADIS)» рекомендує застосовувати як базовий анальгетик опіоїди, такі як морфін та фентаніл. Морфін шляхом постійної інфузії 2–5 мг/год або фентаніл шляхом постійної інфузії 20–50 мкг/год. Сильна рекомендація щодо застосування парацетамолу, що доведено знижує необхідність в опіоїдних анальгетиках через 24 години після операції. Щодо використання нефопаму гідрохлориду, то експерти PADIS пропонують використовувати нефопам (якщо немає протипоказань) як допоміжний засіб або навіть заміну опіоїдам для лікування пацієнтів із вираженим болем, але зазначають, що ця рекомендація умовна (дуже низька якість доказів), що визначає необхідність у його подальшому вивченні. Нефопам 20 мг має анальгетичну дію, порівнянну з дією 6 мг морфіну. Він має потенційні переваги щодо безпеки порівняно з наркотичними анальгетиками та неопіоїдними анальгетиками (наприклад, селективними нестероїдними протизапальними препаратами циклооксигенази), зокрема, не має шкідливого впливу на систему гемостазу, слизової оболонки шлунка, функцію нирок, моторику та роботу кишечника.
Клінічний випадок
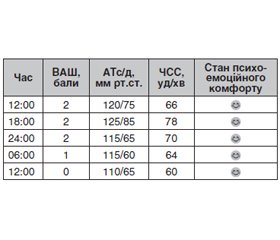
До відділення травматології та ортопедії Київської міської клінічної лікарні № 6 (КМКЛ № 6) надійшла пацієнтка К., 72 років, із діагнозом «перелом лівої стегнової кістки». Враховуючи категоричну відмову пацієнтки від регіонарних методик знеболювання, оперативне втручання проводилось в умовах класичної схеми: ТІВА + ШВЛ. Перед оперативним втручанням пацієнтка отримала як премедикацію: нефопам гідрохлорид 20 мг в/м, парацетамол 1000 мг в/в, кеторолак 30 мг в/в, ондасетрону 8 мг в/в. Індукція ввідної анестезії проводилась уведенням пропофолу 1% 2,5 мг/кг, фентанілу 0,5 мкг/кг, есмерону 0,5 мг/кг. Підтримання анестезії проводилось розчином пропофолу 1% за допомогою постійної інфузії через перфузор із розрахунку 6–8 мг/кг/год, глибина анестезії постійно контролювалася біспектральним ЕЕГ-моніторингом. Анальгетичний компонент інтраопераційно підтримувався розчином фентанілу 0,005% 0,3 мкг/кг/хв. Після закінчення оперативного втручання з приводу МОС стегнової кістки лівої нижньої кінцівки пацієнтка лікувалась у відділенні анестезіології та інтенсивної терапії, знеболювання проводили за мультимодальною схемою із додаванням нефопаму гідрохлориду 20 мг в/м кожні 6 годин до парацетамолу 1000 мг через 6 год, кожні 8 годин кеторолак 30 мг в/в. Весь час лікування хвора не потребувала введення наркотичних анальгетиків. Біль оцінювали кожні 4 години протягом 2 днів за допомогою візуальної аналогової шкали болю (ВАШ), здійснювали контроль гемодинаміки (АТс, АТд, ЧСС), ЕКГ-моніторинг, стан психоемоційного комфорту.
Наша пацієнтка відмічала адекватне знеболювання, відсутність дискомфорту в місці оперативного втручання, стан психоемоційного комфорту залишався задовільним. Схематично в табл. 1 ми подали досліджувані параметри та отримані результати із досліджуваним часовим інтервалом.
Обговорення
Незважаючи на ефективність сучасних схем мультимодальної анальгезії, основним рекомендованим препаратом для знеболювання у ВРІТ, а часто і поза ВРІТ досі лишається морфін.
Морфіну гідрохлорид має гарний анальгетичний ефект, однак у низці ситуацій використовувати його потрібно з обережністю, а в деяких випадках і взагалі слід відмовитися й перейти на інші, більш безпечні анальгетики, у тому числі і ненаркотичні анальгетики центральної дії.
Знеболювання морфіну гідрохлоридом пацієнтів літнього віку в післяопераційному періоді нерідко спричиняє виражену ейфорію з подальшим розвитком делірію. Слід пам’ятати про депресію дихання та гіпотензію з розвитком циркуляторної недостатності й коматозного стану. Пов’язані з опіоїдами побічні ефекти в післяопераційному періоді призводять до подовження перебування пацієнта в стаціонарі та збільшення витрат на лікування.
Нестероїдні протизапальні препарати можуть збільшувати ризики геморагічних ускладнень, кровотеч, ерозивно-виразкових уражень шлунково-кишкового тракту. Парацетамол може давати такі небажані побічні реакції, як тромбоцитопенія, підвищення рівня печінкових трансаміназ, із боку серцево-судинної системи — артеріальну гіпотензію, тахікардію. Однак при внутрішньовенному введенні парацетамол у періопераційному періоді зменшує ризик нудоти та блювання, що пов’язане із покращенням анальгезії, а не зі зменшенням кількості опіоїдів.
Враховуючи вік пацієнтів і наявність супутньої артеріальної гіпертензії, не слід використовувати в післяопераційному періоді з метою знеболювання розчин кетаміну. Також грізним ускладненням у пацієнтів літнього віку при використанні кетаміну є делірій. У свою чергу, використання ненаркотичного анальгетика нефопаму гідрохлориду дає надійний анальгетичний ефект у комбінації із НПЗП та парацетамолом. Також нефопаму гідрохлорид виявляє позитивну властивість запобігати післяопераційному тремтінню. Але слід бути обережним, призначаючи препарат пацієнтам із печінковою та нирковою недостатністю в зв’язку з ризиком накопичення, що підвищує ймовірність виникнення побічних реакцій.
Нашу увагу привернула робота авторів із служби ортопедичної та травматологічної хірургії, Університет Франсуа Рабле, CHRU de Tours, Франція, які проводили своє дослідження щодо післяопераційного знеболювання пацієнтів після операції МОС нижньої кінцівки, поєднуючи в післяопераційному періоді парацетамол, кетопрофен, кетамін і нефопам. Останній, за інформацією авторів, пацієнти отримували у вигляді постійної інфузії (120 мг/добу) протягом 48 годин. За висновками авторів, дана методика не дала можливості повністю відмовитись від наркотичних анальгетиків у післяопераційному періоді, із використанням саме такої схеми мультимодальної анальгезії. Автори відзначають: хоча нефопам і не зміг зменшити потребу в морфіні в їхньому дослідженні, але він зменшив декілька побічних ефектів морфіну, включаючи порушення зору, ейфоричний стан, свербіж та нудоту/блювання. На відміну від французьких колег, наш досвід використання непофаму гідрохлориду відрізняється, ми включили його в премедикацію, а в післяопераційному періоді — і в схему мультимодальної анальгезії до комбінації парацетамол + кеторолак, дана схема демонструє суттєвий результат щодо зменшення інтенсивності болю, а також це дало нам можливість утриматись від використання наркотичних анальгетиків після операцій на нижній кінцівці. Також, на відміну від французьких колег, наші пацієнти не були прикуті до перфузора з постійною інфузією нефопаму гідрохлориду, тим самим не затримувалася рання активізація пацієнтів.
Висновки
Сучасні подходи до лікування гострого післяопераційного болю дозволили значно зменшити використання опіоїдів, але так і не вирішили основне завдання — тривале та ефективне знеболювання. Незважаючи на постійну увагу медичної спільноти до лікування саме гострого післяопераційного болю (2017 рік був роком боротьби з болем), ця проблема є досі актуальною та невирішеною. На думку авторів, додавання препарату нефопаму гідрохлориду в схему мультимодальної анальгезії може бути перспективним у менеджменті болю. Треба взяти до уваги таку особливость препарату, як профілактика післяопераційного тремтіння, що є корисним у наших умовах. Безумовно, для кінцевого висновку необхідні додаткові дослідження.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 03.12.2021
Рецензовано/Revised 13.12.2021
Прийнято до друку/Accepted 15.12.2021
/89.jpg)