Вступ
Серцево-судинні захворювання є однією з головних причин смертності в усьому світі, й Україна не є винятком. Результати проведеного у 2019 році дослідження STEPS свідчать, що показник смертності при серцево-судинних захворюваннях серед усіх неінфекційних захворювань у нашій країні становить 63 % [1]. Україна посідає одне з перших місць в Європі за показниками смертності від хвороб системи кровообігу (459,48 на 100 000 населення), які істотно перевищують показники у Франції (30,08 на 100 000 населення), Німеччині (75,09 на 100 000 населення), Польщі (88,37 на 100 000 населення), Великобританії (76,11 на 100 000 населення) [2]. Причиною серцево-судинних захворювань є атеросклероз судин. Ураження артерії атеросклерозом має улюблені локалізації: серце (інфаркт), судини головного мозку (інсульт), судини нижніх кінцівок (гангрена). Хронічна серцева недостатність (ХСН) є серйозним тягарем для здоров’я, що вражає 40 мільйонів людей у всьому світі, а дилатаційна кардіоміопатія є однією з її основних причин [3]. Кількість пацієнтів із ХСН, яким планується оперативне втручання, продовжує зростати, і анестезіологи відповідальні за надання безпечної періопераційної допомоги пацієнтам з низькою фракцією викиду (ФВ). Таким чином, наявна велика кількість пацієнтів, які мають кардіологічну патологію та потребують досконалої передопераційної підготовки, безпечного інтраопераційного анестезіологічного менеджменту та якісного післяопераційного знеболювання з метою зниження періопераційних ускладнень. Основними цілями передопераційної оцінки кардіологічних пацієнтів для некардіологічного оперативного втручання є стратифікація ризику та потенційне зниження цього ризику безпечними методами. Ці втручання можуть включати модифікацію медикаментозної терапії або хірургічного підходу, більш інтенсивний інтраопераційний моніторинг, техніку анестезії. У випадку з практики, який буде наведено, описується поєднання найбільш безпечних методик анестезіологічного та хірургічного забезпечення з метою мінімізації інтраопераційного та післяопераційного ризику.
Мета: на основі аналізу клінічного випадку анестезіологічного забезпечення пацієнта з низькою фракцією викиду лівого шлуночка при реконструктивній операції з приводу облітеруючого атеросклерозу нижніх кінцівок провести порівняння тактики анестезії зі світовою практикою.
Клінічний випадок
За період з 2019 по 2021 рік проведено в особистій практиці анестезіологічне забезпечення п’яти пацієнтам з низькою фракцією викиду лівого шлуночка при реконструктивних операціях з приводу облітеруючого атеросклерозу нижніх кінцівок. Фракція викиду лівого шлуночка (ФВЛШ) становила від 28 до 37 %, що вказує на тяжке порушення систолічної функції серця. Пацієнтам проводились такі оперативні втручання: тромбектомія стегнової артерії пацієнту з ФВЛШ 28 % під епідуральною анестезією, стегново-підколінне шунтування пацієнту з ФВЛШ 32 % під блокадою n. femoralis, n. ischiadicus, n. obturatorius, ампутація нижньої кінцівки пацієнту з ФВЛШ 37 % під спінальною анестезією та стегново-підколінне шунтування під комбінацією епідуральної анестезії та блокад n. femoralis, n. ischiadicus, n. obturatorius пацієнту з ФВЛШ 33 %.
Один із цих клінічних випадків у пацієнта старечого віку з синдромом Леріша, тяжкою хронічною обструктивною хворобою легень та ФВЛШ 30 % пропонуємо детально розглянути в цій статті.
Пацієнт N., 90 років (вага 72 кг, зріст 175 см), був госпіталізований до нашої лікарні з приводу критичної ішемії правої нижньої кінцівки. З анамнезу відомо, що страждає на хронічну серцеву недостатність IV ФК за NYHA на фоні дисметаболічної кардіоміопатії. Пред’являв скарги на наявність виразок та постійного інтенсивного болю в спокої, що відповідає 4-й стадії облітеруючого атеросклерозу нижніх кінцівок за класифікацією Фонтейна — Покровського. За візуальною аналоговою шкалою хворий відчував інтенсивний біль, що відповідає 8–9 балам. На рентгенограмі грудної клітки виявлена кардіомегалія. ЕКГ-дані: фібриляції передсердь, постійна форма, ЧСС 61–103/хв. На ехокардіографії виявлено розширене ліве передсердя, кальцифікований аортальний клапан, легенева гіпертензія, діастолічна дисфункція лівого шлуночка ІІ ступеня та фракція викиду лівого шлуночка 30 %. Результат тесту легеневої функції: тяжка обструкція, ОФВ1 25–75 %, PRE = 40 %. Концентрація гемоглобіну становила 140 г/л, а гематокрит — 35 %. Інші біохімічні порушення включали легку гіперглікемію та лейкоцитоз. Препарати, які пацієнт приймав до госпіталізації, включали аспірин, аторвастатин, фуросемід і метопролол. Ризик за класифікацією Американської асоціації анестезіологів — IV. Ми також розрахували ризик серцево-судинних ускладнень за критеріями Lee > 11 %, ризик за шкалою Голдмана (мультифакторний індекс ризику кардіальних ускладнень при некардіологічних оперативних втручаннях) відповідав 50 балам, тобто IV класу — кількість ускладнень 78 % [4].
Беручи до уваги тяжкість коморбідного стану пацієнта, йому показано таке екстраанатомічне хірургічне лікування синдрому Леріша, як пахвово-стегнове алошунтування [5].
Після отримання інформованої згоди та пояснення ризиків пацієнта доставили в операційну, де встановили стандартний моніторинг, а через носову канюлю подачу зволоженого кисню 3 л/хв. Для контролю виділення сечі встановили сечовий катетер. Потім пацієнта перемістили в положення сидячи для проведення епідуральної анестезії. Проведено катетеризацію епідурального простору на рівні L2–L3 із заведенням катетера на 6 см, введено тест-дозу 12,5 мг бупівакаїну 0,25% та в подальшому з метою інтраопераційного знеболювання — 25 мг бупівакаїну 0,25%.
Під час операції контролювали ЕКГ, неінвазивний артеріальний тиск (АТ), частоту пульсу (ЧСС) та насичення киснем SPO2. Передопераційні показники: ЧСС 99/хв, АТ 130/100 мм рт.ст. та SPO 95–99 % при диханні повітрям. Для тунелювання трансплантата підшкірно використовували ін’єкції розведеного розчину місцевого анестетика. Життєві показники підтримувалися в межах 20 % від вихідного рівня. За час оперативного втручання внутрішньовенно введено 800 мл ізотонічного розчину натрію хлориду. Вазопресори не призначались. Візуальна аналогова шкала 1–2 бали через 3,8 та 12 годин після операції. Післяопераційне знеболювання проводилось через епідуральний катетер 0,125% розчином бупівакаїну гідрохлориду. Пацієнт був переведений у ВРІТ для подальшого спостереження, а потім через 2 години доставлений у відділення. Він не відчував жодних побічних ефектів післяопераційної терапії, включаючи нудоту, блювання, свербіж, гіпотензію, під час післяопераційного періоду.
Обговорення
Облітеруючий атеросклероз нижніх кінцівок — це захворювання магістральних артерій, яке проявляється частковим (стеноз) або повним (оклюзія) перекриттям просвіту артерії атеросклеротичними бляшками, що утворюються внаслідок відкладення в стінці артерії холестерину. Наростаюче звуження просвіту артерій неминуче призводить до порушення живлення м’язів та інших тканин нижніх кінцівок. У результаті цього відбувається порушення функції нижніх кінцівок, розвиток трофічних виразок і гангрени, що згодом призводить до ампутації нижньої кінцівки.
При прогресуванні симптомів облітеруючого атеросклерозу збільшується частота виникнення ішемічної хвороби серця на 54–57 %, гіпертонічної хвороби — на 70–75 %, порушень мозкового кровообігу — на 20–22 % [6].
Класифікація Фонтейна — Покровського (табл. 1) є класичною та найчастіше вживаною. Пацієнти з І стадією зазвичай навіть не звертаються до лікаря. ІІ стадія переміжної кульгавості є найбільш поширеною, однак клінічну зацікавленість лікаря-анестезіолога викликають ІІІ та ІV стадії, що й відносять до критичної ішемії. Наявність виразок та постійного болю в спокої є одним із основних симптомів цього стану. Больовий синдром підсилюється в горизонтальному положенні, при русі та в нічний час. Звичайні схеми призначення анальгетиків зазвичай є неефективними, що призводить до збільшення їх дозувань та призначення наркотичних препаратів [7, 8].
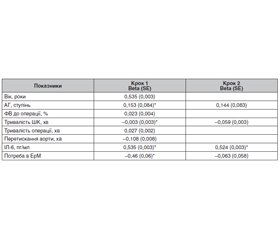
Причиною, чому пацієнту виконано пахвово-феморальне шунтування, а не аортобіфеморальне відкрите алошунтування, є саме те, що пацієнт має вкрай високий анестезіологічний та кардіальний ризик. Пахвово-стегнове шунтування (аксилярно-стегнове шунтування) зазвичай використовується як один із хірургічних методів лікування синдрому Леріша. Це важливий екстраанатомічний хірургічний підхід, що включає різноманітні хірургічні тактики, такі як пахвово-одностороннє шунтування стегнової артерії, аксилярно-двостороннє стегнове шунтування та двостороннє аксилярно-стегнове шунтування [9]. Його функціональність, як правило, не перевершує інтраанатомічний абдомінальний аортобіфеморальний шунт, але цей доступ відіграє важливу роль при таких станах, як інфекційні захворювання черевної аорти та тяжкість загального стану пацієнта [9], тобто у пацієнтів з високим ризиком періопераційних ускладнень. Довгострокові ускладнення після пахвово-стегнового шунтування включають тромбоз, артеріальну емболію нижніх кінцівок та інфекцію. В табл. 2 описано вплив хірургічної процедури на кардіальні ускладнення в періопераційному періоді.
Серцева недостатність є патологією високого ризику зі значною періопераційною захворюваністю та смертністю, що демонструє необхідність ретельної оцінки, оптимізації та планування анестезії для пацієнтів, які перенесли кардіологічні або некардіологічні операції. Якщо є ознаки загострення ХСН у пацієнтів, які госпіталізовані для невідкладного хірургічного втручання, процедуру слід відкласти, якщо це можливо, до тих пір, поки не буде компенсована серцева функція і не буде досягнута стабільність гемодинаміки [10]. У США близько 2 мільйонів пацієнтів із хронічною серцевою недостатністю. Низька фракція викиду лівого шлуночка, низький серцевий викид, високий кінцевий діастолічний тиск у лівому шлуночку та ехокардіографічно виміряні норми руху стінки є важливими індикаторами дисфункції лівого шлуночка.
/93.jpg)
Фракція викиду — це відсоток об’єму крові, що викачується з лівого шлуночка при кожному ударі серця, зазвичай він становить 55–70 %. Легко/помірно знижена ФВ — на 40–54 % вказує на неоптимальну систолічну функцію, тоді як ФВ менше від 35 % часто вказує на серйозне порушення систолічної функції серця.
Існує обмаль даних щодо використання певної анестезіологічної методики для пацієнтів зі зниженою ФВЛШ [11]. При будь-якій хірургічній процедурі за низької ФВЛШ підтримка гемодинамічної стабільності та навіть інтраопераційне виживання стає складним питанням. Необхідно докласти зусиль для запобігання інтраопераційній артеріальній гіпотензії та досягнення належного глибокого рівня анестезії [4].
Наприклад, у статті H. Mulugeta та співавторів вказано, що результати застосування нейроаксіальної анестезії у пацієнтів із серцевими захворюваннями чітко не відомі, але багато клініцистів можуть рекомендувати епідуральну анестезію для досягнення більш поступової та гемодинамічно стабільної анестезії. Під час свого дослідження вони з командою вибрали методом анестезіологічного забезпечення низькодозову унілатеральну спінальну анестезію з додаванням ад’юванту дексметомідину та фентанілу, у висновках вказавши, що одноразово використовували болюсне введення фенілефрину для уникнення гіпотонії [12]. Це дуже показово перекликається з особистим випадком із практики проведення спінальної анестезії пацієнту з ФВЛШ 37 % під час ампутації нижньої кінцівки. Під час оперативного втручання також виникали гемодинамічні зміни, а саме гіпотонія. Автори також зазначають, що встановлено, що дексмедетомідин, високоселективний агоніст α2-рецепторів, має антиноцицептивну дію при інтратекальному введенні. Це було пов’язано з тривалим руховим і сенсорним блоком хребта і знижувало потребу в післяопераційних анальгетиках [13].
У 2014 році A. Shaheen та співавторами було проведено ретроспективне дослідження, у якому описано досвід проведення анестезіологічного забезпечення у 236 пацієнтів з дуже низькою ФВЛШ (20–35 %) з 1 липня 2014 року по 30 червня 2017 року [14]. У цьому ретроспективному дослідженні порівнювались різні методи анестезії. Регіонарна анестезія, що використовується окремо або в комбінації із загальною анестезією, має перевагу щодо зменшення післянавантаження, що може покращити серцевий викид.
Однак, щоб уникнути гіпотонії, необхідно запобігти гіпоперфузії міокарда. Саме регіонарні блокади досягають достатньої анестезії і таким чином дають можливість уникнути загальної, нейроаксіальної анестезії, супутньої гіпотензії та аритмії, які можуть бути шкідливими для пацієнтів з низькою фракцією викиду [14]. Також у статті наголошується, що порівняно із загальною анестезією нейроаксіальна анестезія може знизити 30-денну смертність у пацієнтів із середнім та високим серцевим ризиком, які перенесли некардіологічну операцію [15].
У статті іншого автора також наводиться випадок проведення анестезіологічного забезпечення літньому пацієнту зі зниженою ФВЛШ. Vishwanath R. Hiremath описує застосування регіонарних блокад нервових сплетень під час пластики пахової грижі. І також робить висновки, що регіонарна анестезія, яка використовується окремо або в поєднанні із загальною анестезією, має перевагу щодо зменшення післянавантаження, що може покращити серцевий викид [16].
А в статті Amit Kumar Mittal та співавторів описується випадок проведення анестезії пацієнту із серцевою недостатністю та зниженою фракцією викиду при радикальній холецистектомії з операцією з резекції печінки. Пацієнту проводилось оперативне втручання під комбінованою анестезією (епідуральна анестезія та загальна анестезія). Під час індукції у пацієнта виникла гіпотензія, яка інтраопераційно корегувалась міметиками. Середній артеріальний тиск тримався в межах 44–62 мм рт.ст. [17].
Також дуже цікавий опис проблематики можна знайти в тексті роботи Valérie Smit-Fun та Wolfgang F. Buhre, які зазначають, що за останні 18 місяців було опубліковано нові відомості про короткострокові та довгострокові наслідки ХСН у періопераційному періоді. Роль фракції викиду лівого шлуночка була вивчена у пацієнтів, які не перенесли хірургічну операцію, і було продемонстровано, що фракція викиду менше ніж 30 % пов’язана зі значним збільшенням смертності та інфаркту міокарда [17]. У висновках автори відзначають: «ХСН є джерелом значної періопераційної захворюваності та смертності, і на відміну від ішемічної хвороби серця знання щодо неї дуже обмежені, отже, терміново необхідні додаткові дослідження» [18].
Висновки
1. Пацієнти, які мають кардіологічну патологію, потребують досконалої передопераційної підготовки, безпечного інтраопераційного анестезіологічного менеджменту та якісного післяопераційного знеболювання з метою зниження періопераційних ускладнень. ХСН є джерелом значної періопераційної захворюваності та смертності, і на відміну від ішемічної хвороби серця знання щодо неї дуже обмежені, отже, терміново необхідні додаткові дослідження.
2. Застосування епідуральної анальгезії, регіонарних методик та низьких доз місцевих анестетиків є безпечним методом анестезії у пацієнтів високого анестезіологічного ризику зі зниженою фракцією викиду.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 17.12.2021
Рецензовано/Revised 22.12.2021
Прийнято до друку/Accepted 24.12.2021

/93.jpg)