Вступ
Цереброваскулярна патологія (ЦВП) залишається однією з провідних причин летальності, головною причиною інвалідизації, зниження якості життя [1]. В Україні відзначається тенденція до збільшення поширеності ЦВП та захворюваності на неї, особливо хронічних прогресуючих форм [2, 3]. При цьому слід зазначити, що практично всі прояви ЦВП супроводжуються різними вегетативними розладами. Не завжди констатується те, що така дизрегуляція вегетативної нервової системи (ВНС), може існувати задовго до перших проявів ЦВП та давати поштовх до клінічної реалізації останньої [4, 5].
Серед найпоширеніших вегетативних синдромів особливе місце займає так званий синдром вегетативної дистонії (СВД) — узагальнюючий термін і клінічне поняття, що трактується по-різному, в структурі якого виділяють ще три досить великі синдроми [6, 7].
Основним патогенетичним механізмом СВД є дисбаланс вегетативної регуляції, дисфункція симпатико-парасимпатичних взаємин з перманентним або пароксизмальним перебігом, що має генералізований, переважно системний характер. Найчастішим проявом СВД є церебральна ангіодистонія (ЦАД), яка може існувати самостійно або супроводжувати інші порушення вегетативної регуляції. ЦАД — переважно вогнищеве або системне порушення кровотоку в головному мозку, що виникло в результаті зниження або підвищення тонусу його судин через погану адаптацію до умов, що змінюються [6, 7].
Відомо, що церебральна гемодинаміка знаходиться під ретельним збалансованим вегетативним контролем судинного гомеостатичного діапазону і бере активну участь у вазомоторній адаптації, причому її компенсаторні можливості швидко виснажуються. Це положення лежить в основі розвитку безлічі захворювань (хвороб адаптації), включаючи цефалгії, які є ключовим проявом при ЦАД різного генезу. Насамперед це стосується провідних факторів розвитку ЦВП — церебрального атеросклерозу та гіпертонічної хвороби. При цьому виникають вогнищеві чи системні порушення мозкового кровотоку внаслідок зміни тонусу судин як прояву дезадаптації за умов ішемії мозку. Таким чином, ЦАД є облігатною патологією при вегетативних дисфункціях, а також при хронічній ішемії мозку (ХІМ) [6–8].
Складність будови та функціонування неспецифічних систем та нейрогуморального регулювання судинної системи зумовлюють різноманітність клінічних проявів при змінах церебральної вазомоторики, що потребує подальшого уточнення та певного розмежування на рівні дезінтеграції для адекватної діагностики та ефективної терапії [9, 10].
На наш погляд, важливо оцінити гемодинамічну значущість патогенетичних факторів порушення кровообігу, ступінь неповноцінності системи його регуляції, потенціал функціональних можливостей судинного русла. Для цього інтегральним показником адаптаційної здатності може стати цереброваскулярна реактивність (ЦВР) у відповідь на зміни функціонування системи мозкового кровообігу з метою забезпечення адекватної гемоциркуляції [11, 12].
Метою дослідження було оцінити стан ВНС при церебральній ангіодистонії на тлі вегетативних дисфункцій або хронічних ішемічних ушкоджень мозку.
Матеріали та методи
Обстежений 121 пацієнт з ЦАД на тлі ХІМ у стадії компенсації (І група — 38 осіб) та субкомпенсації (ІІ група — 43 особи), а також на тлі СВД (ІІІ група — 40 осіб) віком від 40 до 65 років. Для виявлення вегетативних дисфункцій використаний анкетний метод — опитувальник для виявлення ознак вегетативних змін [11]. Дослідження вегетативного тонусу (ВТ) проводилося за допомогою таблиці «24 стигми» для експрес-діагностики ВТ [10].
Інтенсивність цефалгій вивчали за допомогою візуальної аналогової шкали (ВАШ), а їхні характеристики — за допомогою опитувальника — бланка з оцінки головного болю (ГБ) [13]. Викликані шкірні симпатичні потенціали (ВШСП) реєструвалися з вивченням показників амплітуди другої фази (А2), а також тривалості латентного періоду (ЛП), що змінюються залежно від вихідного стану ВТ, ступеня ішемічного ушкодження ЦНС [14].
Дослідження церебральних артерій проводилось у триплексному режимі на ультразвуковому сканері Ultima-PA («Радмир», Україна). Досліджувалися показники усередненої за часом максимальної швидкості кровотоку (TAMX) у передніх (ПМА), середніх (СМА), задніх (ЗМА) мозкових, хребетних (ХА) та основній (ОА) артеріях. Також проводилось визначення показників цереброваскулярної реактивності мозкових судин на тлі таких функціональних навантажень:
1) гіперкапнічне навантаження, коефіцієнт реактивності КрСО2;
2) гіпервентиляційне навантаження, коефіцієнт реактивності КрО2;
3) індекс вазомоторної реактивності — ІВМР;
4) функціональний нітрогліцериновий тест, коефіцієнт реактивності — КрФНТ.
Для статистичної обробки використано програму Statisticа 8.0 з оцінкою критерію Вілкоксона, а також критерію U Манна — Уїтні. Статистично значущими вважали розбіжності при Р < 0,05.
Результати
Клінічна картина ЦАД у першу чергу характеризується наявністю ГБ як провідного синдрому, який відзначався у 102 (84,3 %) пацієнтів. У групі III при СВД цефалгії зареєстровані у всіх пацієнтів (Р < 0,05).
При ішемічному ушкодженні мозку цефалгії реєструвалися у 76,5 % (Р < 0,05). Значно частіше цефалгії зустрічалися при компенсованій (I група) стадії ХІМ — 92,1 проти 62,8 % при субкомпенсованій стадії (II група), Р < 0,05.
Незважаючи на те, що цефалгії були провідними симптомами у всіх групах, вони значно відрізнялися за своїми якісними характеристиками. Ішемічно-гіпоксичні превалювали у пацієнтів з ХІМ та були важливим компонентом у тріаді так званого псевдоневрастенічного синдрому, особливо у стадії компенсації. Виявлено закономірність зниження частоти та інтенсивності ГБ у міру прогресування ішемічного ушкодження мозку (в 1,5 раза). При цьому, у разі атеросклеротичного генезу ХІМ, біль був постійним, дифузним, а при артеріальній гіпертензії частіше реєструвалися пульсуючі цефалгії переважно в першій половині дня, коливання АТ посилювалися при зміні положення тіла, у той же час інтенсивність та частота ГБ у стадії субкомпенсації зменшуються.
При СВД цефалгії зустрічалися частіше, ніж при ХІМ, та мали ширший діапазон етіопатогенетичних та клінічних відмінностей. Ці факти можна пояснити залученням до патологічного процесу низки рівнів та відділів ВНС з проявом рефлекторних, ангіодистонічних, іритативних, тензійних та психовегетативних механізмів ГБ. Останні легко провокувалися метеофакторами, перевтомою, стресом тощо.
За наявності дегенеративно-дистрофічних змін у шийному відділі хребта з м’язово-тонічними реакціями у потиличній ділянці ГБ підтримувався або посилювався в усіх групах пацієнтів.
Згідно з середніми показниками ВАШ, інтенсивність цефалгій була вища у I групі (на 11,5 %) порівняно з II групою. У той же час у III групі з вираженими ЦАД на тлі вегетативних дисфункцій інтенсивність цефалгій була максимальною та її середні значення досягали 4,1 ± 0,5 бала, що вірогідно перевищувало значення II групи (Р < 0,05).
ВТ, за даними таблиці «24 стигми» для експрес-діагностики, був змінений у 82 (67,8 %) обстежених пацієнтів, у І групі — у 26 (68,4 %), у ІІ групі — у 32 (74,4 %), у ІІІ групі — у 24 (60,0 %).
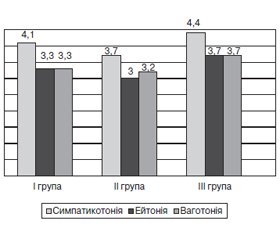
Симпато-парасимпатичний дисбаланс переважав у бік симпатикотонії: у III групі СВД — 21 пацієнт (52,5 %) з мінімумом при ваготонії — 3 пацієнти (7,5 %), у групах ХІМ аналогічний розподіл зберігався у компенсованій стадії — 19 (50,0 %) проти 7 (18,4 %), однак при субкомпенсації зареєстровано вірогідну (Р < 0,05) інверсію цих показників: 15 (34,9 %) проти 17 (39,5 %), що вказує на послаблення ерготропних впливів у процесі прогресування органічної патології мозку (рис. 1).
При симпатикотонії частота цефалгій була максимальною в усіх обстежених групах — 94,7; 86,7 і 90,5 % відповідно. При ваготонії — 100; 64,7; 100 %. У випадках ейтонії ці показники були нижчими: 83,3; 27,3; 82,2 %. Слід зазначити, що у ІІ групі скарги на цефалгії пацієнти пред’являли значно рідше, проте загальні закономірності розвитку ГБ зберігалися у всіх досліджених групах з максимумом при крайніх значеннях ВТ та мінімальною кількістю нападів ГБ при симпато-парасимпатичному балансі. Таким чином, розподіл цефалгічного синдрому був безпосередньо пов’язаний зі станом ВТ, а саме з патологічними його значеннями.
За даними ВАШ, максимальна інтенсивність цефалгій була також на тлі симпатикотонії в обох групах ХІМ: 4,10 ± 0,08 бала (І група) та 3,70 ± 0,06 бала (ІІ група) (Р < 0,05), з максимумом у групі ЦАД — 4,40 ± 0,14 бала (Р < 0,05).
При реєстрації ВШСП у групі з вегетативними дисфункціями середні значення тривалості ЛП скорочувалися до 1,32 ± 0,07 с. У групах з ХІМ ЛП подовжувався при збільшенні ішемічного ушкодження мозку: від 1,43 ± 0,09 (група I) до 1,77 ± 0,20 с (група II), Р < 0,05.
Зіставлення тривалості ЛП залежно від інтенсивності ГБ, характерного для ЦАД, виявило закономірність, пов’язану з укороченням латенції ВШСП при виражених цефалгіях, що можна трактувати як підвищення ерготропних впливів, що дозволяють легше реалізовувати розвиток ГБ. У той же час при слабоінтенсивних цефалгіях ЛП подовжувався, що пов’язано з можливим трофотропним гальмуванням розвитку цефалгій (табл. 1).
При цьому залучаються надсегментарні автономні структури, тобто центральна ланка шкірно-гальванічного рефлексу з відповідною центральною затримкою у вигляді феномена «розтягування пружини» як прояву дизрегуляції лімбіко-ретикулярного комплексу, нестійкості надсегментарних структур автономної системи, що клінічно проявляється ЦАД.
Отримані дані ЛП ВШСП при різних типах ВТ вказують на виснаження ерготропних процесів з прогресуванням ХІМ та відомим наростанням парасимпатикотонії (табл. 2).
Вірогідно зменшується А2 ВШСП також залежно від виснаження ерготропної системи (табл. 2). Середні значення А2 у I та II групах були нижчими за нормальні значення (2,66 ± 0,10 та 2,55 ± 0,20 мВ, Р < 0,05), однак у III групі вони наближалися до нормативних і становили 2,71 ± 0,20 мВ.
Вірогідна різниця між показниками А2 у 2 і більше рази в обстежених групах (Р < 0,05) вказує на те, що незалежно від етіологічної причини, функціональних або органічних судинних уражень різного ступеня тяжкості ВНС значно впливає та/або супроводжує патологічний процес із урахуванням стану адаптивних можливостей організму, вираженості вегетативних дисфункцій, що може впливати на прогноз, перспективи терапії тощо.
Швидкісні показники в III групі у всіх церебральних артеріях, крім ОА, перевищували нормативні. Найбільшою мірою це було виражено у СМА. Дані особливості пов’язані з наявністю у переважної більшості пацієнтів із СВД гіперконстрикторних реакцій. Параметри гемодинаміки у пацієнтів II групи істотно не відрізнялися від даних КГ, лише значення кровотоку у СМА були злегка знижені, що ще раз підтверджує роль гемодинаміки СМА як індикатора церебральних судинних порушень. У пацієнтів I групи спостерігалося незначне зниження показників кровотоку у СМА, ХА та ОА. Аналогічні показники у ПМА та ЗМА суттєво не відрізнялися від нормативних (табл. 3). Ці зміни можна пояснити появою у пацієнтів із субкомпенсованою ХІМ локальних стенозуючих процесів у магістральних артеріях, що впливають на мозкову гемодинаміку.
Показники КрСО2 та ІВМР у III групі трохи перевищували нормативні, що може бути пов’язане з пошуком оптимального гомеостатичного діапазону у пацієнтів із СВД. Реактивність на О2 та ФНТ у цій групі не змінювалася.
У пацієнтів I та ІІ груп спостерігалося вірогідне зниження показників КрСО2 (I група — 1,14 ± 0,03, КГ — 1,28 ± 0,06, p < 0,05; II група — 1,17 ± 0,04, КГ — 1,28 ± 0,06, p < 0,05). Значення КрО2 у II групі суттєво не змінювалися, у I групі були значно знижені (I група — 0,26 ± 0,03, КГ — 0,36 ± 0,03, p < 0,05; II група — 0,34 ± 0,04, КГ — 1,28 ± 0,06). Відсутність значних змін реактивності на О2 у II групі порівняно з I групою можна пояснити тим, що вазоконстрикторний механізм регуляції у пацієнтів із судинною патологією виснажується пізніше відповідного вазодилататорного. Значення ІВМР як інтегрального показника стійкості церебральної авторегуляції були різко знижені в I та II групах порівняно як з КГ, так і з III групою (І група — 54,2 ± 8,8, КГ — 81,5 ± 6,9, p < 0,05; ІІ група — 62,9 ± 7,5, КГ — 81,5 ± 6,9, p < 0,05). Ці зміни найбільшою мірою були властиві пацієнтам I групи. Також у I групі відзначалася значно виражена гіпореактивність на ФНТ (0,05 ± 0,03, КГ — 0,16 ± 0,04, p < 0,05), який є найбільш чутливим індикатором порушень функції вазодилатації на різних стадіях ЦВЗ (табл. 4).
Можна припускати, що вичерпання резервів вазоконстрикторного компонента при органічному судинному ураженні мозку настає пізніше за аналогічні зміни вазодилататорного компонента.
Збільшення реактивності з ІВМР як ознака пошуку оптимального саногенетичного варіанта церебральної гемодинаміки відбувається переважно за рахунок вазодилататорного компонента, причому він коливався у значних межах: від значного зниження (I група) до деякого збільшення (III група).
Наведені дані свідчать про значимість ІВМР як інтегрального фактора, що відображає динамічні властивості гомеостатичного діапазону судинної авторегуляції, у тому числі при органічному ураженні її більш високих рівнів.
Таким чином, зміни реактивності за міогенним контуром у міру прогресування ХІМ подібні до показніків метаболічного контура авторегуляції, а інверсія відповіді на нітрогліцеринове навантаження є маркером зриву авторегуляції і корелює зі ступенем ішемічних пошкоджень мозку.
Висновки
1. Встановлено, що цефалгії є ключовим проявом ЦАД, яка є облігатною до ХІМ.
2. У всіх групах пацієнтів переважав патологічний вегетативний тонус, а інтенсивність цефалгій наростала на тлі симпатикотонії, що можна трактувати як підвищення ерготропності з полегшенням розвитку больового синдрому.
3. Зміни фаз викликаних шкірних симпатичних потенціалів були характерними для дисфункції надсегментарних відділів ВНС, виснаження ерготропного функціонування з погіршенням проявів ЦАД.
4. ВД беруть участь у реалізації, втручаються у розвиток, супроводжують клінічний перебіг ЦАД в умовах функціонального або структурного ураження мозку в процесі розвитку ЦВП.
5. ВД активно впливають на стан усіх відомих регуляторних контурів мозкового кровотоку, а також на вазомоторні центри, що призводить до порушення тонусу та реактивності церебральних судин.
6. Результати досліджень мають сприяти оптимізації лікувальної тактики при ХІМ з урахуванням індивідуальних особливостей стану ВНС, реактивності мозкового кровотоку.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 20.03.2022
Рецензовано/Revised 02.04.2022
Прийнято до друку/Accepted 13.04.2022

/20.jpg)
/21.jpg)
/22.jpg)