Резюме
Актуальність. Дослідження поглинальної та цитокініндукуючої функції фагоцитозу є обов’язковим початком в оцінюванні стану протиінфекційного захисту дітей, які хворіють на часті респіраторні інфекції. Важливо розуміти та порівняти особливості функціонування фагоцитозу у цих дітей залежно від віку пацієнта. Мета дослідження: удосконалення діагностики імунних порушень у дітей віком 2–5 років та 6–10 років, які часто хворіють на гострі респіраторні захворювання, шляхом порівняльного аналізу даних, отриманих на підставі дослідження параметрів фагоцитозу та сироваткових рівнів деяких цитокінів. Матеріали та методи. Під спостереженням знаходилося 60 дітей віком від 2 до 10 років, які часто хворіють на гострі інфекційні захворювання респіраторного тракту, з яких було сформовано 2 групи: 1) діти віком 2–5 років (n = 30); 2) діти віком 6–10 років (n = 30). Результати. Серед дітей 1-ї групи порівняно з дітьми 2-ї групи реєструється збільшення частоти низьких показників фагоцитарного числа (на 36,7 %, р < 0,05), фагоцитарного індексу (на 46,7 %, р < 0,05), індексу завершеності фагоцитозу (на 66,6 %, р < 0,05) і стимульованого стафілококом НСТ-тесту (на 46,4 %, р < 0,05), збільшення частоти реєстрації високих показників вмісту у сироватці крові інтерлейкіну-1β (на 33,3 %, р < 0,05), інтерлейкіну-10 (на 27,7 %, р < 0,05), зменшення частоти реєстрації високих показників інтерлейкіну-6 (на 16,7 %, р < 0,05). У дітей 2-ї групи порівняно з 1-ю частіше реєструвалися високі показники індексу завершеності фагоцитозу (на 70,0 %, р < 0,05), збільшення співвідношення інтерлейкін-6/інтерлейкін-10 в 2 та більше рази. Висновки. У дітей віком 6–10 років в основі реалізації більш частої захворюваності лежить цитокіновий дисбаланс, що відобразилося у збільшенні співвідношення інтерлейкін-6/інтерлейкін-10 в 2 та більше рази, що є негативним фактором, який вказує на посилення прозапальних процесів у цих дітей та більш тривале пошкодження клітин імунного мікрооточення.
Background. The study of the absorbing and cytokine-inducing function of phagocytosis is a mandatory starting point in assessing the state of anti-infective protection in children who suffer from frequent respiratory infections. It is important to understand and compare the features of phagocytosis in these children depending on their age. The purpose: to improve the diagnosis of immune disorders in children aged 2–5 and 6–10 years, who often suffer from acute respiratory diseases, by means of a comparative analysis of phagocytosis parameters and serum levels of some cytokines. Materials and methods. Under observation, there were 60 children aged 2 to 10 years who often suffer from acute infectious diseases of the respiratory tract. Two groups were formed: 1) children aged 2–5 years (n = 30); 2) children aged 6–10 years (n = 30). Results. Among patients of the first group compared to those of group 2, an increase in the frequency of low indicators of the phagocytic number (by 36.7 %, p < 0.05), phagocytic index (by 46.7 %, p < 0.05), the index of completion of phagocytosis (by 66.6 %, p < 0.05) and the staphylococcus-stimulated nitroblue tetrazolium test (by 46.4 %, p < 0.05), an increase in the frequency of high serum levels of interleukin-1β (by 33.3 %, p < 0.05), interleukin-10 (by 27.7 %, p < 0.05), a decrease in the frequency of high levels of interleukin-6 (by 16.7 %, p < 0.05). In the children of group 2 compared to those in the first one, high index of completion of phagocytosis was more often registered (by 70.0 %, p < 0.05), as well as more than a twofold increase in the ratio of interleukin-6/interleukin-10. Conclusions. In children aged 6–10 years, more frequent morbidity is due to a cytokine imbalance that was reflected in a more than a twofold increase in interleukin-6/interleukin-10 ratio, which is a negative factor indicating an enhancement of pro-inflammatory processes and a longer damage to the cells of the immune microenvironment.
Вступ
Захист людини від респіраторних захворювань на ранніх етапах контакту з інфекцією відбувається завдяки комплексу цілеспрямованих дій вродженого та набутого імунітету. Початковою індуктивною ланкою цього процесу є фагоцитоз, який включає не тільки швидке знешкодження та елімінацію патогена, а й створення відповідних умов для здійснення подальших, більш специфічних імунних реакцій. Це відбувається шляхом синтезу та ліберації цілого набору цитокінів, які регулюють подальший перебіг захисного процесу [1].
Зокрема, це інтерлейкіни (ІЛ) — ІЛ-1β, ІЛ-6, ІЛ-10 та фактор некрозу пухлини α (ФНП-α). Інтерлейкін-1β синтезують та секретують різноманітні макрофаги. Основними мішенями є Т-клітини, В-клітини, ендотелій і тканинні клітини. ІЛ-1 викликає активацію лімфоцитів, підвищення адгезії лейкоцитів до ендотелію [2].
Інтерлейкін-6 продукується макрофагами. Основні ефекти IL-6 спрямовані на диференціювання В-клітин і стимуляцію білків гострої фази [3]. Інтерлейкін-10 є важливим протизапальним цитокіном. Його основними мішенями є Th1-клітини. Він викликає інгібування ІЛ-2 та інтерферону гамма. Також він зменшує презентацію антигена та експресію МНС класу II дендритних клітин, костимулюючих молекул на макрофагах [4]. Два пов’язаних явища пояснюють важливість продукування ІЛ-10 у цьому контексті: по-перше, широкий спектр клітин, здатних виробляти цей цитокін, а по-друге, широкий вплив, який він справляє на клітини-мішені. Під час інфекцій вироблення ІЛ-10 зменшує пошкодження тканин хазяїна та полегшує його виживання [5].
Фактор некрозу пухлини α призводить до перехресної активації нейроендокринної і усіх ланок імунної системи [6]. Тобто ця складна послідовність процесів запускає відповідну повноцінну систему протиінфекційного захисту.
Саме тому коли в різноманітних клінічних випадках лікар стикається зі збільшенням кількості інфекційних захворювань у пацієнта, насамперед виникає необхідність дослідження ефективності функціонування фагоцитарної ланки імунітету. Це є особливо важливим у дітей, у яких імунні процеси ще знаходяться у стані дозрівання [7].
Так, коли часто хворіє на гострі респіраторні захворювання (ГРЗ) дитина віком до 5 років, то звичайно враховується певна транзиторна недостатність мікро- і макрофагальних клітин в умовах збільшення потреби у лімфоцитарних клітинах. І лише коли ситуація виходить за межі фізіологічних коливань, розглядаються питання діагностики імунних порушень. Але коли підвищення кількості захворювань має місце у дитини старше 6 років, після так званого лейкоцитарного перехресту, то виникає необхідність ретельного встановлення наявності можливих імунних відхилень. Адже в цьому віці у дитини, крім функціонування достатнього вродженого імунітету, вже є сформованими набуті механізми. У такому випадку дослідження поглинальної та цитокініндукуючої функції фагоцитозу є обов’язковим початком в оцінюванні стану протиінфекційного захисту дитини, яка хворіє на часті респіраторні інфекції [8].
Тому важливо розуміти особливості функціонування фагоцитозу у дітей, які хворіють на рекурентні ГРЗ, залежно від віку пацієнта. Для пошуку таких відмінностей потрібен був порівняльний аналіз даних імунологічного обстеження таких дітей.
Мета дослідження: удосконалення діагностики імунних порушень у дітей віком 2–5 років та 6–10 років, які часто хворіють на ГРЗ, шляхом порівняльного аналізу даних, отриманих на підставі дослідження параметрів фагоцитозу та сироваткових рівнів деяких цитокінів.
Матеріали та методи
Під спостереженням знаходилося 60 дітей віком від 2 до 10 років, які часто хворіють на гострі інфекційні захворювання респіраторного тракту, з яких було сформовано 2 групи: 1) діти віком 2–5 років (n = 30); 2) діти віком 6–10 років (n = 30).
Визначення «часті повторні респіраторні інфекції» у дітей базувалося на наступних міжнародних критеріях: 1) більше ніж 6 епізодів інфекцій дихальних шляхів протягом 1 року; 2) більше ніж 1 епізод інфекції верхніх дихальних шляхів на місяць у період з вересня по квітень; 3) понад 3 епізоди інфекцій нижніх дихальних шляхів протягом одного року [9].
Діти в групах спостереження були порівнянні за віком, статтю, тривалістю та тяжкістю хвороби, супутньою патологією. Клінічний метод складався з оцінки анамнезу, фенотипової характеристики дитини, загальноклінічних методів обстеження.
Кров для дослідження стану імунної системи брали з кубітальної вени вранці натще. Обстеження проводилось в міській лабораторії клінічної імунології КНП «Міська дитяча лікарня № 1» Запорізької міської ради (свідоцтво про атестацію № 004313 від 21.08.2020 р.).
Вивчення показників фагоцитозу здійснювалося методом відновлення нітросинього тетразолію (НСТ-тест), спонтанного та стимульованого (антигеном Staphylococcus), розрахунком фагоцитарного числа, індексу завершеності фагоцитозу. Референтні показники визначалися за сертифікованими нормативами лабораторії, де проводилися дослідження, та викладені у локальних протоколах з імунодіагностики у дітей КНП «Міська дитяча лікарня № 1» Запорізької міської ради. Кількісне визначення концентрації ІЛ-1β, ІЛ-6, ІЛ-10, ФНП-α у сироватці крові проводилося методом імуноферментного аналізу (ІФА) на фотометрі-аналізаторі «Humareader SINGLE» (Німеччина).
Референтні показники визначалися за сертифікованими нормативами лабораторії, де проводилися дослідження, та викладені у локальних протоколах з імунодіагностики у дітей КНП «Міська дитяча лікарня № 1» Запорізької міської ради.
Для статистичної обробки отриманих результатів використовувався кутовий критерій Фішера ϕ (для порівняння двох вибірок за частотою виявлення відхилень показників сироваткового вмісту цитокінів).
Для оцінки ймовірності того, що за наявності виявленого відхилення дитина матиме часту захворюваність на ГРЗ, використовувався метод розрахунку відношення шансів (ВШ). Значення ВШ від 0 до 1 відповідали зниженню ймовірності, більше за 1 — її збільшенню, ВШ, що дорівнювало 1, означало відсутність відмінностей.
Дослідження було проведено відповідно до етичних принципів медичного дослідження, проведеного на людях, які були прийняті Гельсінською декларацією, і якісної клінічної практики (GCP).
Результати
Для порівняльної оцінки частоти виникнення відхилень у параметрах фагоцитозу в сироватці крові у дітей, які часто хворіють, залежно від віку було встановлено кількість пацієнтів, у яких вони реєструвалися. Дані наведені в табл. 1.
Наведені в табл. 1 дані щодо частоти виникнення відхилень у параметрах фагоцитозу демонструють, що серед дітей віком 2–5 років, які часто хворіють на ГРЗ, порівняно з дітьми 6–10 років статистично значимо реєструється збільшення частоти низьких показників фагоцитарного числа (на 36,7 %, р < 0,05), фагоцитарного індексу (на 46,7 %, р < 0,05), індексу завершеності фагоцитозу (на 66,6 %, р < 0,05) і стимульованого стафілококом НСТ-тесту (на 46,4 %, р < 0,05).
У дітей 2-ї групи порівняно з 1-ю частіше реєструвалися високі показники індексу завершеності фагоцитозу (на 70,0 %, р < 0,05).
Отримані результати продемонстрували існування більш високої ймовірності (відношення шансів) наявності вікових особливостей порушень фагоцитозу у дітей віком 2–5 років зі збільшеною частотою захворюваності на ГРЗ.
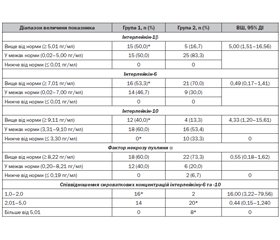
Результати порівняльної оцінки даних дослідження рівня цитокінів, що синтезуються макро- та мікрофагоцитарними клітинами, у дітей 1-ї та 2-ї груп спостереження наведені у табл. 2.
Наведені в табл. 2 дані щодо частоти виникнення відхилень сироваткового вмісту деяких цитокінів демонструють, що серед дітей віком 2–5 років, які часто хворіють на ГРЗ, порівняно з дітьми 6–10 років має місце статистично значиме збільшення частоти реєстрації високих показників вмісту у сироватці крові інтерлейкіну-1β (на 33,3 %, р < 0,05), інтерлейкіну-10 (на 27,7 %, р < 0,05), зменшення частоти реєстрації високих показників інтерлейкіну-6 (на 16,7 %, р < 0,05). У дітей 2-ї групи частіше реєструвалося збільшення співвідношення інтерлейкін-6/інтерлейкін-10 в 2 та більше рази. Отримані результати продемонстрували існування високої ймовірності (відношення шансів) наявності вікових особливостей відхилень сироваткового вмісту деяких цитокінів у дітей зі збільшеною частотою захворюваності на ГРЗ.
Обговорення
Часта захворюваність на респіраторні інфекції у дітей не є прямим показником існування недостатності функціонування імунної системи, адже, частіше за все, є проявом неспроможності слизових оболонок верхніх дихальних шляхів локалізувати та знешкодити патоген, що може відбуватися за багатьох причин, у тому числі фізіологічних, зокрема вікових особливостей [10]. Та якщо для дітей віком до 5 років часта захворюваність на ГРЗ є, скоріше за все, транзиторним станом, то у пацієнтів раннього шкільного віку така ситуація викликає більше занепокоєння з боку як лікарів, так і батьків і вчителів. Тобто рекурентні ГРЗ у дітей віком 6–10 років є такою клінічною ситуацією, коли вже може виникати підозра щодо наявності будь-яких порушень протимікробного захисту — початкових неспецифічних стадій (зокрема, фагоцитозу) або специфічних реакцій, обумовлених імунологічною пам’яттю [11].
Тому в даному дослідженні було вирішено проаналізувати відмінності у параметрах ранніх ланок захисного процесу у дітей різного віку зі схожими клінічними проявами — повторні ГРЗ без тяжких бактеріальних ускладнень. Тобто у них мали місце проблеми не з набутими антибактеріальними механізмами, а з бар’єрною спроможністю вродженого захисту — процесами імунного кліренсу та виключення, а отже, компонентами фагоцитарної ланки. Однією з важливих функцій фагоцитарних клітин, окрім безпосереднього захоплення та лізису патогенів, є утворення хімічного забезпечення відповідного лейкоцитарного мікрооточення шляхом продукції деяких цитокінів, зокрема інтерлейкіну-1β, -6, -10 та ФПН-α [12], сироваткову концентрацію яких також було досліджено.
Отримані в дослідженні дані продемонстрували, що у дітей віком 2–5 років, які часто хворіють на ГРЗ, порівняно з дітьми 6–10 років мала місце набагато частіша реєстрація більш низьких поглинальних параметрів фагоцитозу і стимульованого стафілококом НСТ-тесту. Це загалом пояснювало причини рекурентної захворюваності на ГРЗ у молодших пацієнтів 1-ї групи. Але ж з клінічної точки зору діти в обох групах не відрізнялися, тобто часті респіраторні інфекції у дітей віком 6–10 років не були асоційовані з такими же зсувами функціонування макро- і мікрофагальних клітин, як у дітей 2–5 років.
У цих умовах важливими були порівняльні дані сироваткового вмісту деяких цитокінів, які демонстрували, що серед дітей віком 6–10 років, які часто хворіють на ГРЗ, порівняно з дітьми 2–5 років мало місце статистично значуще збільшення частоти реєстрації високих рівнів інтерлейкіну-6 та низьких рівнів інтерлейкіну-10. Це відобразилося у збільшенні величини співвідношення інтерлейкін-6/інтерлейкін-10 в 2 та більше рази у пацієнтів 2-ї групи, що є негативним моментом, адже вказує на посилення прозапальних процесів у цих дітей та більш тривале пошкодження клітин імунного мікрооточення [13].
Тобто в даному випадку у дітей віком 6–10 років в основі реалізації частої захворюваності лежить цитокіновий дисбаланс, адже у дітей 2–5 років підвищення вмісту прозапальних цитокінів відбувалося на фоні компенсаторної реакції з боку протизапального інтерлейкіну-10 [14]. У пацієнтів 6–10 років такого ефекту не було, прозапальний процес мав більш тривалий та виснажливий для захисних механізмів характер. Ймовірно, саме такі діти раннього шкільного віку, які мали дану налаштованість імунних реакцій у віці до 5 років, й формують у подальшому групу пацієнтів з частими ГРЗ, а згодом, маючи такий цитокіновий дисбаланс, з іншими хворобами, в основі яких лежить тривалий імуноопосередкований патогенез [15], що обумовлює необхідність пошуку нових лікувально-профілактичних підходів.
Висновки
Таким чином, дослідженням встановлено, що у дітей віком 6–10 років в основі реалізації більш частої захворюваності лежить цитокіновий дисбаланс, що відображається у збільшенні співвідношення інтерлейкін-6/інтерлейкін-10 в 2 та більше рази, що є негативним фактом і вказує на посилення прозапальних процесів у цих дітей та більш тривале пошкодження клітин імунного мікрооточення.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Інформація про фінансування. Дослідження не має окремого додаткового фінансування та проведено в рамках науково-дослідної роботи кафедри педіатрії та неонатології Державного закладу «Запорізька медична академія післядипломної освіти МОЗ України» «Клінічні та імуноендокринні особливості формування та перебігу запальних захворювань органів дихання у дітей з дисбалансом центральних та автономних механізмів нейрогенної регуляції» (номер державної реєстрації 0117U004385).
Отримано/Received 02.08.2022
Рецензовано/Revised 10.08.2022
Прийнято до друку/Accepted 20.08.2022

/14.jpg)
/15.jpg)