Гіпоглікемія — клінічний синдром, який характеризується низкою суб’єктивних та об’єктивних симптомів, зумовлених зниженням рівня глюкози в крові. У здорових людей вміст глюкози крові протягом доби коливається в досить широких межах — від 3,3 до 7,8 ммоль/л. Ці коливання зумовлені прийомами їжі, фізичними навантаженнями, періодами голодування, у тому числі нічного, психоемоційними та іншими чинниками [1].
Гіпоглікемічний синдром є станом, якому, на жаль, приділяється невиправдано мало уваги під час підготовки як лікарів загального профілю, так і спеціалістів з інтенсивної терапії. Причиною цього є оманливе уявлення про те, що «гіпоглікемія діагностується просто, а лікується ще простіше». Але, за влучним висловлюванням S. Kalra et al. (2013), «обличчя гіпоглікемії є набагато похмурішим, ніж сприймається в нашій повсякденній практиці» [2]. Гіпоглікемію не слід розглядати лише як гостре короткочасне поєднання незручних, але безпечних для хворого симптомів. Велика кількість ускладнень, що супроводжують гіпоглікемічні стани, доводить, що такий підхід не може розглядатися як раціональний, а гіпоглікемічний синдром потребує своєчасної та адекватної терапії.
Згідно з дефініцією Американської діабетичної асоціації (ADA), гіпоглікемія може бути визначена як «будь-яка аномально низька концентрація глюкози в плазмі, яка може завдати суб’єкту потенційної шкоди». Зазвичай межею такої глікемії є рівень 70 мг% (3,89 ммоль/л) [3]. Однак європейська школа клінічної практики рекомендує для визначення межі гіпоглікемії використовувати більш низькі цифри (нижче ніж 60 мг%, або нижче ніж 3,3 ммоль/л) [4].
У здорових людей пригнічення ендогенної секреції інсуліну після всмоктування глюкози в кров починається при її концентрації 4,2–4 ммоль/л, а подальше зниження рівня глюкози супроводжується викидом контрінсулярних гормонів. Через 3–5 годин після прийому їжі прогресивно зменшується надходження з кишечника глюкози і організм перемикається на ендогенне вироблення глюкози (глікогеноліз, глюконеогенез). Під час цього переходу можливий розвиток функціональної гіпоглікемії: ранньої — у перші 1,5–3 години і пізньої — через 3–5 годин. «Голодна» гіпоглікемія не пов’язана з прийомом їжі та розвивається натще або через 5 годин після її прийому.
Гіпоглікемічна кома — крайній ступінь гіпоглікемії, небезпечний для життя хворого, розвивається у разі швидкого зниження вмісту глюкози в крові.
Слід відзначити і деякі епідеміологічні особливості розвитку гіпоглікемії у хворих на цукровий діабет (ЦД), а саме:
— гіпоглікемія — це найчастіший невідкладний стан при цукровому діабеті;
— 10–25 % хворих на ЦД хоч раз на рік переносять епізоди гіпоглікемії;
— практично у всіх хворих, які отримують інсулін, розвиваються з тою чи іншою частотою легкі гіпоглікемії, а у 30 % — тяжкі;
— у 0,25–5 % хворих тяжкі гіпоглікемії стають причиною смерті [5].
Причини гіпоглікемії
Найчастіше гіпоглікемія пов’язана з уведенням зависокої дози інсуліну або пероральних цукрознижувальних препаратів, насамперед похідних сульфонілсечовини і меглітинідів. Тому часто вважається, що гіпоглікемія — здебільшого ятрогенний стан.
Іншими причинами гіпоглікемії можуть бути: дефіцит контрінсулярних гормонів (хвороба Аддісона, гіпопітуїтаризм, гіпотиреоз), підвищення чутливості до інсуліну (втрата маси тіла, менструальний цикл), зміни якісного складу, кількості та проміжків прийому їжі, надмірне фізичне навантаження, прийом деяких медикаментів та алкоголю.
Ми наводимо основні причини гіпоглікемій нижче.
Основні причини розвитку гіпоглікемії
Помилки в інсулінотерапії:
— перевищення дози;
— невідповідність дози потребам.
Дефіцит контрінсулярних гормонів:
— хвороба Аддісона;
— гіпопітуїтаризм;
— гіпотиреоз.
Інсулінсекретуючі пухлини, наприклад інсулінома.
Підвищення чутливості до інсуліну:
— втрата маси тіла;
— зміна чутливості у зв’язку з менструальним циклом.
Зміни якісного складу, кількості та проміжків прийому їжі.
Порушення засвоєння їжі через блювання, діарею чи внаслідок інших захворювань та/або хірургічних втручань.
Надмірне фізичне навантаження.
Прийом деяких речовин та медикаментів:
— алкоголю, що пригнічує продукцію глюкози печінкою (неоглюкогенез);
— саліцилатів і сульфаніламідів, що посилюють дію інсуліну;
— неселективних адреноблокаторів, що блокують адренергічні реакції та підвищують ризик малосимптомних гіпоглікемій;
— довгодіючих похідних сульфонілсечовини і меглітинідів.
Уведення деяких антимікробних засобів:
— фторхінолонів (гатифлоксацин, левофлоксацин);
— пентамідину, триметоприм-сульфаметоксазолу.
У хворих без цукрового діабету — печінкова і ниркова недостатність.
Слід також зауважити, що печінка і нирки є головними органами, які беруть участь у метаболізмі інсуліну і препаратів сульфонілсечовини, тому розвиток ниркової або печінкової недостатності може загальмувати кліренс цих препаратів і призвести до гіпоглікемії.
Патогенез
В основі гіпоглікемічного стану лежить зниження утилізації глюкози клітинами головного мозку, тому що він найбільш чутливий до зниження вмісту глюкози. Це обумовлено тим, що глюкоза є основним джерелом енергії для головного мозку, а вміст глікогену в ньому обмежений. Слідом за нестачею глюкози в клітинах головного мозку наступає порушення їх функції, а у разі глибокої та тривалої гіпоглікемії — дегенерація та загибель. Існує припущення, що ураження відділів головного мозку відбувається в певній послідовності, що й визначає клінічну симптоматику різних періодів гіпоглікемічної коми.
Раніше за всіх випадає функція кори головного мозку, у той час як дихальний центр продовжує ще довго функціонувати після згасання активності півкуль головного мозку.
Певною мірою гіпоглікемія може розглядатися як своєрідна пристосувальна реакція на надмірну кількість інсуліну. При збереженні гіпофізарно-наднирникової функції терміново включаються захисні, компенсаторні механізми, зокрема підвищується тонус симпатоадреналової системи, відбувається викид в кров контрінсулярних гормонів: адреналіну, глюкагону, кортизолу, соматотропного гормона. Ці механізми супроводжуються підвищенням глікогенолізу в печінці, стимуляцією неоглюкогенезу. У легких випадках мобілізація цих факторів здатна компенсувати гіпоглікемію без відповідних терапевтичних втручань [5].
Класифікація
Залежно від наявності або відсутності симптомів і результатів моніторингу глюкози гіпоглікемію розділяють на біохімічну, симптоматичну та змішану [3]. Ця класифікація створена на основі консенсусу робочої групи ADA, згідно з яким гіпоглікемічні епізоди можуть бути класифіковані таким чином:
— тяжка гіпоглікемія — гіпоглікемічний епізод, при якому для активного введення вуглеводів, глюкагону або застосування інших заходів потрібна допомога іншої особи;
— документально симптомна гіпоглікемія — поєднання виміряної в плазмі концентрації глюкози нижче ніж 70 мг/дл (3,89 ммоль/л) з типовими симптомами гіпоглікемії;
— безсимптомна гіпоглікемія — стан, при якому концентрація глюкози в плазмі є нижчою, ніж 70 мг/дл (3,89 ммоль/л), але це не супроводжується відомими симптомами звичайної гіпоглікемії;
— можлива симптомна гіпоглікемія — подія, під час якої виявлення симптомів гіпоглікемії не супроводжувалося визначенням глюкози в плазмі (але ці симптоми, імовірно, виникли внаслідок зниження концентрації глюкози в плазмі менше ніж 70 мг/дл (3,89 ммоль/л));
— відносна гіпоглікемія — наявність будь-яких з типових симптомів гіпоглікемії у пацієнта з діабетом, які інтерпретуються самим пацієнтом як ознака гіпоглікемії, але при цьому концентрація глюкози в плазмі є вищою за 70 мг/дл (3,89 ммоль/л).
У рекомендаціях ADA 2022 року з’явилася нова класифікація, згідно з якою виділяють три рівні гіпоглікемії (табл. 1).
Гіпоглікемія 1-го рівня визначається як рівень глюкози в крові < 70 мг/дл (3,9 ммоль/л), але ≥ 54 мг/дл (3,0 ммоль/л). Концентрація глюкози в крові 70 мг/дл (3,9 ммоль/л) була визнана пороговою для нейроендокринної реакції на зниження рівня глюкози у людей без діабету. Оскільки багато людей з цукровим діабетом демонструють порушення контррегуляторних реакцій на гіпоглікемію та/або не відчувають ознак гіпоглікемії, виміряний рівень глюкози < 70 мг/дл (3,9 ммоль/л) вважається клінічно важливим (незалежно від тяжкості гострих гіпоглікемічних симптомів). Гіпоглікемія 2-го рівня (визначена як концентрація глюкози в крові < 54 мг/дл (3,0 ммоль/л)) є порогом, при якому починають виникати нейроглікопенічні симптоми, і вимагає негайних заходів для усунення гіпоглікемічної події. Якщо у пацієнта спостерігається гіпоглікемія 2-го рівня без адренергічних або нейроглікопенічних симптомів, імовірно, що він не усвідомлює гіпоглікемію. Цей клінічний сценарій вимагає дослідження та перегляду лікувального режиму. Нарешті, гіпоглікемія 3-го рівня визначається як тяжка подія, що характеризується зміною психічного та/або фізичного функціонування, що потребує допомоги іншої людини для відновлення [6].
Клінічна картина
Слід зазначити, що немає жорсткої кореляції між рівнем глюкози в крові та клінічними симптомами гіпоглікемії. Симптоми гіпоглікемії відрізняються поліморфізмом і неспецифічністю. Для гіпоглікемічної хвороби патогномонічною є тріада Уїппла:
— симптоми гіпоглікемії;
— концентрація глюкози в плазмі < 55 мг/дл (3,0 ммоль/л);
— купірування гіпоглікемічного нападу внутрішньовенним введенням глюкози або пероральним прийомом глюкози [7].
Гіпоглікемічна кома розвивається швидко. Зазвичай їй передує короткочасний період передвісників — своєрідна «аура». Як прояв адекватної реакції антистресових механізмів на початку гіпоглікемії відбувається активація симпатичної нервової системи з викидом адреналіну. Це супроводжується відчуттями тривоги, голоду, тремтінням, руховим збудженням, надмірною пітливістю, тахікардією. З поглибленням гіпоглікемії психомоторне збудження змінюється оглушенням, втратою свідомості, появою вогнищевих неврологічних знаків, судом та поглибленням коми.
У деяких хворих, особливо з тривалим перебігом ЦД, зменшується викид адреналіну та знижується секреція глюкагону у відповідь на гіпоглікемію. Це призводить до збіднення клінічної картини нейроглікопенії. Поріг розвитку симптомів «вегетативної бурі» підвищується, тоді як поріг порушення свідомості, моторних та психомоторних проявів залишається на попередньому рівні. Унаслідок цього ознаки нейроглікопенії — розгорнута клініка гіпоглікемії — виникають раптово, без «аури». У таких хворих гіпоглікемічний синдром супроводжується суттєвішими розладами кровообігу, дихання та метаболізму й має затяжний перебіг.
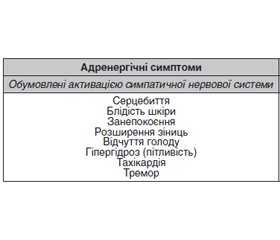
Симптоматика гіпоглікемії поліморфна й зумовлена двома головними механізмами: зменшенням вмісту глюкози в головному мозку (нейроглікопенією) та реакціями, що пов’язані з надмірним збудженням симпатоадреналової системи. Характерні прояви цих розладів наведені в табл. 2.
Виокремлюють кілька стадій розвитку гіпоглікемічного синдрому.
1-ша стадія — характеризується дратівливістю, відчуттям голоду, головним болем. На цій стадії в процес залучена кора головного мозку. Ранні симптоми можуть бути відсутніми у хворих, які отримують інсулін.
У 2-й стадії відбувається залучення діенцефальних утворень мозку та маніфестація вегетативних реакцій: слинотеча, тремор, пітливість, неадекватні зміни поведінки (агресивність чи веселощі). Свідомість у цей період ще не порушена. У міру поглиблення гіпоглікемії психомоторне збудження змінюється оглушенням, втратою свідомості.
Цікавий опис хворої у цій стадії наводить Пітер Дж. Уоткінс: «Здавалось, що вона нетвереза. Її поведінка змінювалась несподівано та дуже помітно: мовлення ставало незрозумілим; зовнішній вигляд — як сонна, вона постійно позіхала. Якщо вона ще могла ходити, то постійно наштовхувалася на різні предмети на своєму шляху і взагалі була дуже незграбною. Вона ледь розуміла, де вона і що тут робить...» [8].
3-тя стадія обумовлена залученням середнього мозку та супроводжується підвищенням тонусу м’язів, розвитком тоніко-клонічних судом, гіпертензією (іноді — з почервонінням обличчя, що загалом не характерно для гіпоглікемії і може викликати певні діагностичні труднощі). Можуть з’являтися галюцинації та марення.
4-та стадія (гіпоглікемічна кома) характеризується ураженням верхніх відділів довгастого мозку з маренням, судомами та втратою свідомості. Хворий у гіпоглікемічній комі блідий, шкіра волога, дихання рівне, язик вологий, відсутній запах ацетону.
5-та стадія пов’язана з ураженням нижніх відділів довгастого мозку і супроводжується глибокою комою, тахікардією, гіпотонією, порушенням дихання центрального генезу. У разі гіпоглікемічної коми, що затягнулася, артеріальний тиск знижується; виникають брадикардія, гіпотермія, атонія м’язів, гіпо- та арефлексія; пригнічення фотореакцій [5].
Іноді у хворих з тривалим перебігом цукрового діабету нерозпізнана гіпоглікемія може виникати уві сні (феномен Сомоджі). На цей стан організм реагує надлишковою секрецією контрінсулярних гормонів. У ранкові години показники глюкози в крові значно зростають, і їх неправильно оцінюють як наслідок недостатньої дози інсуліну. У зв’язку з цим збільшують дозу препарату, що, звичайно, погіршує перебіг цукрового діабету. У цьому випадку спостерігаються різкі коливання глікемії протягом доби [9].
У разі своєчасного та правильного лікування гіпоглікемічний синдром не становить загрози для життя хворого. Летальні випадки у разі розвитку коми рідкісні. Але гіпоглікемії небезпечні у хворих з діабетичними ангіопатіями, ішемічною хворобою серця (ІХС), хронічною коронарною недостатністю. Гіпоглікемічна кома може ускладнитись гострим порушенням мозкового кровообігу або інфарктом міокарда, тому після купірування гіпоглікемічного стану обов’язково потрібно записати контрольну ЕКГ.
Крім того, слід пам’ятати, що тяжкі та довготривалі гіпоглікемії та коматозні стани призводять до необоротних дегенеративних змін у ЦНС, сприяють розвитку та прогресуванню енцефалопатії. З часом розвиваються зміни психіки (до деменції), паркінсонізм, епілептиформні напади. Особливо небезпечною є гіпоглікемія для хворих, у яких в анамнезі вже були порушення церебрального кровообігу, а також для пацієнтів похилого віку з ІХС.
Гіпоглікемічні стани у хворих без цукрового діабету
Гіпоглікемія — це синдром, який може розвиватися як у здорових людей, так і за різних захворювань. Відомо, що будь-який критичний стан супроводжується тяжкими порушеннями метаболізму. Одним з таких порушень є гостра гіпоглікемія, що не пов’язана з цукровим діабетом або введенням хворим препаратів інсуліну. Вважається, що подібна гіпоглікемія виникає внаслідок швидкого використання запасів глікогену в умовах гіперметаболізму.
Гіпоглікемічний синдром значною мірою погіршує перебіг основного захворювання, а несвоєчасна корекція гіпоглікемії заважає виходу пацієнта з коми і є причиною тяжких психоневрологічних порушень, які складно піддаються лікуванню. Факторами, що сприяють виникненню гіпоглікемії у хворих без ЦД, є: голодування або недостатнє харчування протягом декількох діб, недостатня нутритивна підтримка в післяопераційному періоді та (у деяких з пацієнтів) загальне переохолодження [5].
Виникнення цього синдрому часто створює додаткові складнощі у лікуванні хворих, адже його доводиться диференціювати з гострими порушеннями мозкового кровообігу, прогресуванням дихальної недостатності та погіршенням загального стану хворих у зв’язку з прогресуванням основного захворювання. У таких випадках без екстреної лабораторної діагностики гіпоглікемії важко обрати раціональну тактику інтенсивної терапії. Іноді таким пацієнтам призначають складні і непотрібні методи лікування. Так, часто хворим призначають седативні препарати при психомоторному збудженні, антиконвульсанти при судомних проявах гіпоглікемії, у деяких випадках необґрунтовано проводиться штучна вентиляція легень.
Гіпоглікемії у разі недостатньої продукції глюкози
Дефіцит гормонів. Гіпоглікемія завжди зустрічається при пангіпопітуїтаризмі — захворюванні, що характеризується зниженням або випаданням функції передньої долі гіпофіза (секреції адренокортикотропіну, пролактину, соматотропіну, фолікулотропіну, лютропіну, тиреотропіну). У результаті різко знижується функція периферичних ендокринних залоз. Однак гіпоглікемія зустрічається і в разі первинного ураження ендокринних органів (вроджена дисфункція кори наднирникових залоз, хвороба Аддісона, гіпотиреоз, гіпофункція мозкового шару наднирникових залоз, дефіцит глюкагону). За дефіциту контрінсулярних гормонів знижується швидкість глюконеогенезу в печінці (вплив на синтез ключових ферментів), підвищується утилізація глюкози на периферії, знижується утворення амінокислот у м’язах — субстрату для глюконеогенезу.
Дефіцит глюкокортикоїдів. Первинна наднирникова недостатність є наслідком зменшення секреції гормонів кори наднирникових залоз. Під цим терміном мають на увазі різні за етіологією та патогенезом варіанти гіпокортицизму. Симптоми наднирникової недостатності розвиваються тільки після руйнування 90 % обсягу тканини наднирникових залоз.
Причини гіпоглікемії за наднирникової недостатності схожі з причинами гіпоглікемії при гіпопітуїтаризмі. Відмінністю є рівень виникнення блоку — у разі гіпопітуїтаризму знижується секреція кортизолу через дефіцит АКТГ, а у разі наднирникової недостатності — через руйнування тканини самих наднирникових залоз.
Гіпоглікемічні стани у хворих із хронічною наднирниковою недостатністю можуть виникати як натщесерце, так і через 2–3 години після прийому їжі, багатої вуглеводами. Напади супроводжуються слабкістю, почуттям голоду, пітливістю. Гіпоглікемія розвивається в результаті зниження секреції кортизолу, зменшення глюконеогенезу, запасів глікогену в печінці.
Дефіцит катехоламінів. Цей стан може виникати у разі наднирникової недостатності з ураженням мозкового шару наднирникових залоз. Катехоламіни, потрапляючи у кров, регулюють вивільнення і метаболізм інсуліну, знижуючи його, а також збільшують вивільнення глюкагону. При зниженні секреції катехоламінів спостерігаються гіпоглікемічні стани, що обумовлено надмірною продукцією інсуліну і зниженою активністю глікогенолізу.
Дефіцит глюкагону. Глюкагон — гормон, який є фізіологічним антагоністом інсуліну. Він бере участь у регуляції вуглеводного обміну, впливає на жировий обмін, активуючи ферменти, що розщеплюють жири. Основна кількість глюкагону синтезується альфа-клітинами острівців підшлункової залози. Проте встановлено, що спеціальні клітини слизової оболонки дванадцятипалої кишки і слизової оболонки шлунка також синтезують глюкагон. У разі надходження у кровоток глюкагон викликає підвищення в крові концентрації глюкози, аж до розвитку гіперглікемії. У нормі глюкагон запобігає надмірному зниженню концентрації глюкози. Завдяки існуванню глюкагону, що перешкоджає гіпоглікемічній дії інсуліну, досягається тонка регуляція обміну глюкози в організмі.
Деякі гіпоталамо-гіпофізарні синдроми можуть супроводжуватися гіпоглікемією: синдром Лоренса — Муна — Бідля — Борді, синдром Дебре — Марі, синдром Пехкранца — Бабинського (адипозогенітальна дистрофія).
Синдром Лоренса — Муна — Бідля — Борді характеризується ожирінням, гіпогонадизмом, розумовою відсталістю, дегенерацією сітківки, полідактилією, глибокими дегенеративними змінами гіпоталамо-гіпофізарної системи.
Синдром Дебре — Марі обумовлений гіперфункцією задньої долі гіпофіза і гіпофункцією аденогіпофіза. Виявляється в ранньому дитячому віці. Хворі інфантильні, низькорослі, з надмірною масою. У клінічній картині характерне порушення водного обміну з олігурією й олігодипсією, щільність сечі висока. Психічний розвиток не порушений.
Синдром Пехкранца — Бабинського — причиною захворювання вважають органічні і запальні зміни гіпоталамуса, які ведуть до ожиріння, аномалій розвитку скелета і гіпоплазії статевих органів.
Гіпоглікемії, що розвиваються внаслідок дефіциту ферментів
Дефіцит глюкозо-6-фосфатази (Г-6-Фази) становить основу хвороби Гірке, або глікогенозу типу 1. Недостатність цього ферменту призводить до неможливості перетворення глюкозо-6-фосфату (Г-6-Ф) в глюкозу, що супроводжується накопиченням глікогену в печінці та нирках. Хвороба успадковується за автосомно-рецесивним типом.
Надходження глюкози в організм з їжею в принципі дає можливість підтримувати в крові нормальний рівень глікемії, однак для цього надходження їжі, що містить глюкозу, має бути практично безперервним. У реальних умовах існування, тобто за відсутності безперервного надходження глюкози, у здоровому організмі остання депонується у вигляді глікогену, який у разі необхідності використовується для деполімеризації.
Первинне порушення при хворобі Гірке відбувається на генетичному рівні. Воно полягає в повній (або майже повній) нездатності клітин продукувати Г-6-Фазу, що забезпечує відщеплення вільної глюкози від Г-6-Ф. Унаслідок цього глікогеноліз переривається на рівні Г-6-Ф і далі не відбувається. Дефосфорилювання за участю Г-6-Фази є ключовою реакцією не тільки глікогенолізу, а й глюконеогенезу, який, таким чином, при хворобі Гірке також переривається на рівні Г-6-Ф. Виникнення стійкої гіпоглікемії, яка в реальних умовах неминуча через ненадходження в кров глюкози як кінцевого продукту глікогенолізу і глюконеогенезу, у свою чергу, призводить до постійно підвищеної секреції глюкагону як стимулятора глікогенолізу. Однак глюкагон в умовах переривання цього процесу здатний лише без користі для організму безперервно стимулювати його початкові стадії.
Якщо нестача ферменту помірна, хворі досягають юнацького, а нерідко й більш старшого віку. Однак психічний і соматичний розвиток, а також метаболічний статус у цих хворих різко порушені. Зокрема, часто спостерігаються підвищення рівня тригліцеридів, холестерину, гіперурикемія, гіпофосфатемія. Характерними рисами є олігофренія, затримка росту, ожиріння, остеопороз, великий живіт (унаслідок збільшення печінки і нирок), ксантоматоз, ліпемія сітківки, геморагічний діатез. Уміст глюкози в плазмі натще постійно знижено, у зв’язку з чим навіть у разі короткочасного голодування розвиваються гіпоглікемічні судоми, кетонурія та метаболічний ацидоз. Останній обумовлений не тільки гіперкетонемією, але й підвищеним накопиченням і утворенням в крові пірувату і лактату, що є результатом порушеного глюконеогенезу. Порушення обміну ліпідів супроводжується розвитком панкреатиту.
Діагноз ґрунтується на даних клінічної картини, зниженому вмісті глюкози і підвищеній концентрації ліпідів і лактату в крові. Рівень глюкози в плазмі практично не змінюється після введення глюкагону. Однак вміст лактату в крові після його введення зростає.
Дефіцит аміло-1,6-глюкозидази — глікогеноз типу 3, або хвороба Корі, належить до найбільш частих глікогенозів і має відносно легкий клінічний перебіг. Функція цього ферменту полягає в деградації білкових гілок глікогену і відщеплення від них вільної глюкози. Однак зниження вмісту глюкози в крові при цьому захворюванні не настільки істотне, як у разі глікогенозу типу 1, тому що певна кількість глюкози утворюється через активування фосфорилази в печінці. Для клінічної картини захворювання характерні гепатомегалія, м’язова слабкість, затримка росту і періодичні «голодні» гіпоглікемії. При лабораторному дослідженні виявляється підвищення рівня печінкових трансаміназ. Уміст лактату і сечової кислоти в плазмі крові зазвичай у нормі. У відповідь на введення глюкагону відсутнє підвищення рівня глюкози в плазмі крові, якщо проба з глюкагоном проводиться натщесерце, тоді як при введенні глюкагону через 2 години після прийому їжі відповідь вже нормальна. Для підтвердження діагнозу необхідна біопсія печінки і м’язів, у яких виявляють змінений глікоген і недостатність відповідного ферменту.
Дефект печінкової фосфорилази (хвороба Герса) — глікогеноз, викликаний недостатністю фосфорилази печінки (глікогенова хвороба типу 6). Фосфорилаза печінки каталізує фосфорилювання (розщеплення) глікогену з утворенням глюкозо-1-фосфату. Порушення цього механізму призводить до надлишкового відкладення глікогену в печінці. Успадковується, ймовірно, за автосомно-рецесивним типом.
Проявляється зазвичай на першому році життя. Характерними є затримка росту, «лялькове» обличчя, значне збільшення печінки в результаті глікогенної інфільтрації гепатоцитів, гіпоглікемія, гіперліпемія, підвищений уміст глікогену в еритроцитах. Діагноз ґрунтується на зниженні активності фосфорилази в лейкоцитах.
Недостатність глікогенсинтетази. Дуже рідкісне спадкове захворювання. У хворих, які мають дефект синтезу цього ферменту, глікоген взагалі не синтезується. Голодування викликає тяжку гіпоглікемію.
Недостатність фосфоенолпіруваткарбоксикінази — ключового ферменту глюконеогенезу. Дефект синтезу цього ферменту є дуже рідкісною причиною гіпоглікемії. Фосфоенолпіруваткарбоксикіназа бере участь у синтезі глюкози з лактату, метаболітів циклу Кребса, амінокислот і жирних кислот. Тому у разі недостатності цього ферменту інфузія лактату або аланіну не дає можливості домогтися нормоглікемії. Навпаки, введення гліцерину нормалізує концентрацію глюкози, оскільки для синтезу глюкози з гліцерину фосфоенолпіруваткарбоксикінази не потрібно. У разі тяжкої гіпоглікемії проводять інфузію глюкози.
Голодні гіпоглікемії
Голодування — найпоширеніша причина гіпоглікемії у здорових людей. У разі голодування глюкоза не надходить в організм, але продовжує споживатися насамперед так званими глюкозозалежними органами і тканинами. Під час короткочасного голодування дефіцит глюкози покривається шляхом глікогенолізу та глюконеогенезу в печінці. У разі тривалого голодування запаси глікогену в печінці виснажуються і виникає гіпоглікемія.
Гіпоглікемія може виникнути у людей, які дотримуються суворих правил у харчуванні під час посту (наприклад, у православних під час Великого посту і у мусульман під час Рамадану). Зрозуміло, що в таких випадках гіпоглікемія обумовлена повним (або практично повним) тривалим голодуванням.
Ця ж форма гіпоглікемії розвивається на тлі виснажливого фізичного навантаження, наприклад під час бігу, плавання та велоперегонів на довгі дистанції, у багатоборців, альпіністів, лижників, культуристів. У таких ситуаціях основна причина гіпоглікемії — посилене споживання глюкози м’язами.
Гіпоглікемія під час вагітності. Усі види обміну речовин під час вагітності зазнають значних змін, перебудовуються ферментативні реакції. Глюкоза є основним субстратом для забезпечення енергетичних потреб плода і матері. З прогресуванням вагітності витрата глюкози безперервно збільшується, що вимагає постійної перебудови регулюючих механізмів. Збільшується секреція як «гіперглікемічних» гормонів (глюкагон, естрогени, кортизол, гіпофізарний пролактин, плацентарний лактоген, соматотропін), так і «гіпоглікемічного» гормону інсуліну. Таким чином встановлюється динамічна рівновага механізмів, що регулюють вуглеводний обмін. Рівень глюкози в крові у вагітних жінок залишається в межах норми, повністю забезпечується при цьому потреба в глюкозі організмів матері та плода.
На пізніх термінах вагітності, на тлі виснаження компенсаторних механізмів, може виникати гіпоглікемічний стан. Клінічна картина гіпоглікемії вагітних включає почуття голоду, головний біль, пітливість, слабкість, тремор, нудоту, парестезії, нечіткість і звуження полів зору, сплутаність свідомості, сопор, втрату свідомості, кому і судоми.
Захворювання печінки. Дифузне і тяжке ураження печінки, при якому виходить з ладу 80–85 % її маси, може призвести до гіпоглікемії внаслідок порушення продукції глюкози. Це пов’язують з такими ураженнями, як гострий некроз печінки, гострий вірусний гепатит, синдром Рейє і тяжка застійна серцева недостатність. Метастатична або первинна пухлина печінки (якщо уражена більша частина печінкової тканини) може викликати гіпоглікемію, але метастази в печінку зазвичай не супроводжуються гіпоглікемією. Гіпоглікемія була описана як частина синдрому жирового переродження печінки під час вагітності. Повідомлялося також про поєднання гіпоглікемії з HELLP-синдромом (гемоліз, підвищений рівень печінкових ферментів і зниження числа тромбоцитів у периферичній крові). Під час вагітності можуть виникати ураження печінки, як у разі прееклампсії, HELLP-синдрому та гострого жирового її переродження. Тому у всіх хворих жінок у III триместрі вагітності слід визначати рівень глюкози. Хронічне захворювання печінки дуже рідко супроводжується гіпоглікемією. Хворі з тяжкою печінковою недостатністю, здатною викликати гіпоглікемію, часто знаходяться в коматозному стані. Гіпоглікемія як причина коматозного стану може бути пропущена, якщо кома розцінюється як наслідок печінкової енцефалопатії.
Гіпоглікемією може супроводжуватися хронічна ниркова недостатність. Це пов’язано з тим, що здорова нирка здатна до глюконеогенезу. У деяких випадках цей процес обумовлює до 50 % утвореної ендогенної глюкози. За уремії глюконеогенез може бути пригнічений. До того ж нирка виробляє інсулінази, що руйнують інсулін, який у хворих з хронічною нирковою недостатністю кумулюється. З цієї ж причини небезпека гіпоглікемії збільшується і у хворих з цукровим діабетом, ускладненим хронічною нирковою недостатністю.
Алкоголь і медикаменти. Вживання спиртних напоїв — поширена причина гіпоглікемії як у дорослих людей, так і у дітей. Розщеплення етанолу з утворенням ацетальдегіду в печінці каталізується ферментом алкогольдегідрогеназою. Цей фермент працює тільки в присутності особливого кофактора — нікотинаміддинуклеотиду (НАД). Але ця ж речовина необхідна і для печінкового глюконеогенезу. Прийом алкоголю призводить до швидкої витрати НАД і різкого гальмування глюконеогенезу. Тому алкогольна гіпоглікемія виникає у разі виснаження запасів глікогену, коли для підтримання нормального рівня глюкози в крові особливо необхідний глюконеогенез. У випадку прийому великої кількості алкоголю ввечері симптоми гіпоглікемії зазвичай виникають наступного ранку. Найчастіше алкогольна гіпоглікемія спостерігається у хворих, виснажених алкоголізмом, але буває і у здорових людей після прийому великої кількості алкоголю або у разі вживання алкоголю натще. Діагноз алкогольної гіпоглікемії ґрунтується на даних анамнезу і виявленні гіпоглікемії у поєднанні з підвищеним рівнем алкоголю та молочної кислоти в крові.
Описані випадки гіпоглікемії у разі прийому неселективних бета-блокаторів. Вони застосовуються для лікування ішемічної хвороби серця, порушень серцевого ритму, а також деяких форм гіпертонічної хвороби. Такий ефект обумовлений підвищеною утилізацією глюкози м’язами, зниженням утворення глюкози з глікогену, інгібуванням ліполізу і зниженням умісту неестерифікованих жирних кислот у крові. Бета-блокатори не рекомендується застосовувати у разі інсулінозалежного цукрового діабету, тому що вони «маскують» більшість симптомів гіпоглікемії і можуть бути токсичними для клітин острівців підшлункової залози. Також варто пам’ятати, що за одночасного застосування пропранололу і гіпоглікемічних препаратів існує ризик розвитку гіпоглікемії через посилення їх дії.
Гіпоглікемію можуть викликати протизапальні і знеболюючі препарати з класу саліцилатів (аспірин). Саліцилати впливають на обмін речовин: при введенні у великих дозах спостерігається зменшення синтезу і збільшення розпаду амінокислот, білків і жирних кислот. У хворих на цукровий діабет саліцилати сприяють зниженню вмісту глюкози в крові. Також саліцилати, як і бета-адреноблокатори, посилюють дію препаратів, що застосовуються для зниження рівня цукру в крові.
Гіпоглікемії, пов’язані з підвищеною утилізацією глюкози
Інсулінома — пухлина, частіше доброякісна, яка походить із бета-клітин острівців Лангерганса і характеризується безконтрольною гіперсекрецією інсуліну, що викликає гіпоглікемічні стани. У 80–85 % випадків пухлина солітарна і доброякісна, тільки в 10–15 % випадків пухлини злоякісні і множинні [1]. Нерідко інсулінома виявляється компонентом множинної ендокринної неоплазії типу І. Украй рідко пухлини розташовуються поза підшлунковою залозою (ворота селезінки, печінка, стінка дванадцятипалої кишки). Найчастіше пухлина діагностується у віці від 25 до 55 років.
Для інсуліноми характерні напади гіпоглікемії, пов’язані з постійним, незалежним від рівня глюкози в крові, викидом інсуліну. Часті напади гіпоглікемії викликають ураження центральної нервової системи. У деяких хворих вони нагадують епілептичний напад, з яким госпіталізують у неврологічне відділення. Напади гіпоглікемії перериваються прийомом їжі, у зв’язку з чим хворі постійно вживають велику кількість продуктів, головним чином вуглеводів, що сприяє розвитку ожиріння.
Діагностика інсуліноми базується на виявленні класичної та патогномонічної для неї тріади Уїппла, а також типової для гіпоглікемії клінічної картини. Золотим стандартом на першому етапі діагностики гіпоглікемічного синдрому та підтвердження ендогенного гіперінсулінізму є проба з голодуванням.
Голодування — фізіологічний спосіб пригнічення секреції інсуліну. У здорових людей під час голодування знижуються рівні як глюкози, так і інсуліну. Деякі люди здатні переносити голодування протягом 24–72 год без будь-яких ознак гіпоглікемії. Ці симптоми виникають тільки тоді, коли концентрація глюкози падає до дуже низького рівня (1,7–1,9 ммоль/л). Чим довше голодування, тим сильніше пригнічується секреція інсуліну. Тому зменшується відношення «концентрація інсуліну в сироватці (пмоль/л)/концентрація глюкози у плазмі (ммоль/л)». У здорових суб’єктів натщесерце це відношення завжди менше ніж 37. У хворих на інсуліному секреція інсуліну у разі голодування не зменшується або навіть підсилюється, і в результаті відношення інсулін/глюкоза збільшується і перевищує 37. Найбільш надійний спосіб діагностики інсуліноми — подовження нічного голодування до появи симптомів голодування.
Проба зазвичай проводиться протягом 72 годин і вважається позитивною при розвитку тріади Уїппла. Початок голодування відзначають як час останнього прийому їжі. Рівень глюкози в крові оцінюють спочатку через 3 години після останнього прийому їжі, потім через кожні 6 годин, а при зниженні рівня глюкози в крові менше ніж 3,4 ммоль/л інтервал між його дослідженнями скорочують до 30–60 хв. Коли рівень глюкози у крові, взятої з пальця, виявився меншим ніж 2,8 ммоль/л або коли з’явились ознаки гіпоглікемії, ще раз беруть кров з вени для визначення концентрації глюкози та інсуліну в плазмі. Діагноз інсуліноми вважається підтвердженим, якщо відношення інсулін/глюкоза у будь-якій пробі перевищує 37. Приблизно у 70 % пацієнтів з інсуліномою симптоми гіпоглікемії з’являються вже на 1-шу добу голодування, у 25 % хворих — на 2-гу добу і у 5 % хворих — на 3-тю добу.
Другим етапом у діагностиці інсуліноми є топічна діагностика пухлини. Використовують УЗД, комп’ютерну томографію, магнітно-резонансну томографію, ендоскопічне УЗД, сцинтиграфію, ангіографію, інтраопераційне УЗД. Найбільш інформативні в діагностиці інсуліном ендоскопічне ультразвукове дослідження і забір крові з печінкових вен після внутрішньоартеріальної стимуляції підшлункової залози кальцієм. У багатьох пацієнтів за допомогою сучасних методів дослідження вдається на доопераційному етапі встановити локалізацію пухлини, її розмір, стадію і темпи прогресування пухлинного процесу, виявити метастази.
Лікування інсуліноми в більшості випадків хірургічне: енуклеація пухлини, дистальна резекція підшлункової залози. Консервативна терапія проводиться у разі нерезектабельних пухлин та їхніх метастазів: при незидіобластозі, множинних пухлинах, а також у разі відмови пацієнта від оперативного лікування. Ця терапія спрямована на пригнічення секреції інсуліну [1]. Призначають діазоксид у дозі 100 мг перорально 3–4 рази на добу, який виявляється дійовим приблизно у 50 % хворих. В окремих випадках хороший ефект забезпечують: фенітоїн, хлорпромазин, пропранолол і верапаміл. У разі злоякісної інсуліноми з метастазами препаратом вибору є стрептозоцин, а при резистентності до цього препарату інколи ефективні аспарагіназа, доксорубіцин або плікаміцин.
Періопераційне ведення. Основні принципи періопераційного ведення пацієнтів і контролю їх стану включають: інвазивний моніторинг гемодинаміки; безперервне або болюсне введення розчинів глюкози, інсуліну і калію під відповідним лабораторним контролем; при маніпуляціях безпосередньо на пухлині виникає необхідність введення 50% розчину глюкози; діагностику точної локалізації пухлини, яка часто необхідна інтраопераційно; моніторинг рівня глюкози та інсуліну в крові після операції.
Серед радикально прооперованих пацієнтів виживають протягом 5 років 90 %, при виявленні метастазів — 20 %.
Гіперплазія бета-клітин у новонароджених і грудних дітей. У нормі об’єм ендокринної частини острівців підшлункової залози становить 1–2 % у дорослих і 10 % у новонароджених. У дітей раннього віку гіпер–плазія острівців зустрічається при незидіобластозі, фетальному еритробластозі, синдромі Беквіта — Відемана, а також у дітей, народжених від матерів з цукровим діабетом.
Незидіобластоз — вроджена дисплазія ендокринних клітин (мікроаденоматоз). З незидіобластів, які внутрішньоутробно формуються з епітелію панкреатичних протоків, утворюються острівці Лангерганса. Цей процес починається з 10–19-го тижнів внутрішньоутробного розвитку і закінчується на 1–2-му році життя дитини. У деяких випадках формування ендокринних клітин може прискорюватися або утворюються додаткові клітини в ацинарній тканині підшлункової залози. Подібні порушення, які мають транзиторний характер, часто зустрічаються в нормальній тканині підшлункової залози. Вважається, що до 2 років незидіобластоз є варіантом норми, у дітей старше 2 років є патологією. Незидіобластоз супроводжується нерегульованою секрецією інсуліну з розвитком вираженої гіпоглікемії.
Гіперінсулінемічна гіпоглікемія зустрічається у дітей, народжених від матерів, які хворіють на цукровий діабет. Гіпоглікемія у таких новонароджених викликана тим, що внутрішньоутробно надмірна кількість глюкози дифундує від вагітної до плода і викликає у нього гіпертрофію острівцевого апарату. Після народження дитини бета-клітини продовжують надлишково виробляти інсулін, викликаючи у частини дітей симптоми гіпоглікемії. Слід мати на увазі, що за тривалого введення концентрованих розчинів глюкози вагітним можливий розвиток транзиторної гіпоглікемії у новонароджених.
Гіперплазія інсулярного апарату у новонароджених може розвиватися у разі гемолітичної хвороби. Руйнування еритроцитів внутрішньоутробно супроводжується деградацією інсуліну, що викликає гіпертрофію бета-клітин. Лікування таких хворих замінним переливанням крові припиняє гемоліз, а отже, руйнування інсуліну. Але транзиторна гіпоглікемія зберігається деякий час.
У період новонародженості гіпоглікемія може бути проявом синдрому Відемана — Беквіта. Причиною тяжкої неонатальної гіпоглікемії є гіпертрофія і гіперплазія острівців підшлункової залози. Діти народжуються з надмірною масою тіла. Характерним є збільшення органів: печінки, нирок, підшлункової залози. Часто виявляють кісти пупкового канатика, макроглосію, різні органні аномалії. Якщо хворі не гинуть у неонатальному періоді, то відставання в психічному розвитку пов’язують з гіпоглікемічними станами.
Штучно викликана гіпоглікемія
Ейфорія, викликана введенням інсуліну, зустрічається у здорових дівчат (синдром Мюнхгаузена). Деякі хворі з цукровим діабетом також активно викликають у себе симптоми гіпоглікемії. Мотив такої поведінки пов’язаний з особливостями характеру і соціальним середовищем. Такі хворі дуже винахідливі і активно приховують препарати. Передбачувана штучна гіпоглікемія діагностується за наявності її симптомів, високих показників інсуліну і низького рівня С-пептиду в крові [10].
Системний дефіцит карнітину
Тяжка гіпоглікемія може виникнути у хворих із системною карнітиновою недостатністю. Карнітин — біологічно активна вітаміноподібна речовина. Основними його функціями є участь в енергетичному обміні, зв’язування і виведення з організму токсичних похідних органічних кислот. У разі системного дефіциту карнітину периферичні тканини позбавляються здатності утилізувати жирні кислоти для утворення енергії, а печінка не може виробляти альтернативний субстрат — кетонові тіла. Це призводить до того, що всі тканини стають залежними від глюкози, а печінка не в змозі задовольнити їхні потреби. Системна карнітинова недостатність проявляється нудотою, блюванням, гіперамоніємією і печінковою енцефалопатією. Ця патологія є однією з форм синдрому Рейє.
Рідше гіпоглікемія зустрічається у разі недостатності карнітинпальмітоїлтрансферази — ферменту, що переносить жирні кислоти з ацил-КоА на карнітин для окиснення. У більшості хворих має місце частковий дефект, тож тенденція до гіпоглікемії зводиться до мінімуму. Некетозна (або гіпокетозна) гіпоглікемія може зустрічатися також у разі зниження активності інших ферментів окиснення жирних кислот, наприклад, у випадку недостатності дегідрогенази ацил-КоА.
Діти раннього віку особливо чутливі до недостатності карнітину. Ендогенні запаси у них швидко виснажуються у разі інфекційних захворювань, шлунково-кишкових розладів, порушень вигодовування.
Лікування
Перше, що за можливості повинно бути зроблено під час епізоду гіпоглікемії будь-якого ступеня тяжкості, — це визначення рівня глюкози в крові. Це забезпечить лікарю діагностику гіпоглікемії як документально симптомної.
Невідкладне лікування хворого проводиться згідно з новим клінічним протоколом «Екстрена медична допомога: догоспітальний етап» (Наказ МОЗ України № 1269 від 05.06.2019 р.) [11].
При легкій гіпоглікемії — пацієнт у свідомості і відмічає ознаки гіпоглікемії — необхідно швидко прийняти легкозасвоювані вуглеводи (дорослі: приблизно 15–20 г глюкози, діти: доза глюкози — 0,5–1 г/кг). Для цього потрібно випити солодкий напій (чай з цукром, солодкий сік), почати розсмоктувати льодяник або шматочок цукру-рафінаду.
Якщо хворий втратив свідомість (у разі підтвердження діагнозу гіпоглікемічної коми), вводять 40–80 мл 40% розчину глюкози. У деяких хворих відновлення свідомості відбувається швидко, «на кінці голки», у інших потребує певного проміжку часу.
Якщо симптоми гіпоглікемії не усуваються протягом 15–20 хвилин, необхідно знову перевірити рівень глікемії і при низьких показниках (глюкоза крові ≤ 3,3 ммоль/л (60 мг/дл)) повторно дати 10–20 г глюкози.
Одним із способів виведення хворих з гіпоглікемічного стану є ін’єкція глюкагону, який стимулює швидкий розпад глікогену і викид глюкози в кров. Доза глюкагону для дорослих становить 1 мг в/м або назально, для дітей — 1 мг в/м або назально, якщо маса тіла ≥ 20 кг або вік дитини ≥ 5 років, та 0,5 мг в/м або назально, якщо маса дитини менше ніж 20 кг або вік молодше від 5 років [11]. Слід пам’ятати, що гіперглікемічний ефект глюкагону зумовлений його глікогенолітичною дією, тому він неефективний у разі виснаження запасів глікогену в печінці, наприклад, у випадках голодування, гіпокортицизму, печінкової недостатності [5].
Для пацієнтів з інсуліновою помпою, у яких наявна гіпоглікемія з пов’язаним з нею зміненим станом свідомості (ШКГ < 15 балів), слід зупинити помпу або від’єднати її, якщо пацієнт не може самостійно ковтати пероральну глюкозу або якщо спеціалізована допомога недоступна.
Якщо максимальна доза глюкози не призвела до еуглікемії та нормалізації свідомості, транспортуйте хворого до найближчого приймального відділення для подальшого лікування стійкої гіпоглікемії. Хворі без свідомості підлягають терміновій госпіталізації. Їм необхідний моніторинг глікемії. Обов’язково госпіталізують також пацієнтів з гіпоглікемію, які мали судоми. Їх доставляють до приймального відділення незалежно від стану свідомості та відповіді на терапію.
У стаціонарі продовжується внутрішньовенне введення глюкози протягом усього часу очікуваної дії інсуліну чи перорального цукрознижувального препарату, які викликали цю кому. Наприклад, якщо кома викликана прийомом хлорпропаміду, введення глюкози, можливо, необхідно буде проводити протягом декількох днів.
Якщо в подальшому рівень глікемії утримується нижче за 5,5 ммоль/л (99 мг/дл), слід розпочати краплинне введення 10% глюкози зі швидкістю, що забезпечує рівень глікемії вище ніж 5,5 моль/л [12].
В окремих випадках корисно додавати до програми лікування:
— бікарбонат натрію для помірного залуження сечі, що скорочує період напіввиведення більшості цукрознижувальних засобів, особливо хлорпропаміду;
— октреотид по 50–100 мкг двічі на добу, який знижує секрецію інсуліну.
Якщо свідомість не відновилась, потрібно повторно визначити рівень глікемії та провести обстеження, спрямоване на виключення інших причин коми. Подальша інтенсивна терапія містить: штучну вентиляцію легень, інфузійну терапію, зазвичай у нульовому балансі, та глюкокортикоїди.
Для інфузійної терапії застосовують розчини глюкози (розчин ГІК) та розчини гідроксиетильованих крохмалів (ГЕК, наприклад гекотон). Крім впливу на об’єм циркулюючої крові, препарати ГЕК під час свого метаболізму частково перетворюються на глюкозу і підвищують рівень глікемії, що є, безумовно, бажаним ефектом у хворих з гіпоглікемією.
Для лікування гіпоглікемічних станів у хворих без цукрового діабету (так само, як і при лікуванні хворих на цукровий діабет) важливим є фактор часу надання допомоги. У разі усунення гіпоглікемії не пізніше ніж за 2–3 год з моменту її виникнення вона не призводить до тяжких ускладнень. Більш пізня корекція гіпоглікемії призводить до сповільнення виходу хворого з коми з тривалим періодом психомоторного збудження та погіршенням результатів відновлення психічних функцій.
Слід також зазначити, що у частини пацієнтів з гіпоглікемією можливий розвиток кетоацидозу — так званого кетоацидозу голодування. Таким пацієнтам у програмі інфузійної терапії потрібно передбачити введення препаратів антикетогенної дії, наприклад ксилату (5–6 мл/кг на добу протягом 1–2 днів). Патогенетично обґрунтованим і перспективним є використання у цих пацієнтів препарату глюксил, основними діючими складовими якого є глюкоза, ксилітол та натрію ацетат.
Профілактика гіпоглікемії
Найпростіший профілактичний захід, який потрібно рекомендувати кожному хворому, — постійно мати при собі шматочки цукру та у разі появи перших ознак гіпоглікемії приймати їх по 10–20 г. Важливе значення має також регулярний контроль рівня глікемії крові, особливо в періоди змін режиму харчування та при значних фізичних навантаженнях. У цілому будь-який епізод гіпоглікемії можна певною мірою розглядати як результат помилки лікаря чи пацієнта або як наслідок неадекватності схеми інсулінотерапії. Необхідно обов’язково знайти причину розвитку гіпоглікемії та оцінити ймовірність її рецидивування. За можливості слід направити пацієнта в школу діабету та порадити носити із собою картку з вказаним діагнозом та описом заходів, які слід провести у разі розвитку гіпоглікемії. Пацієнт повинен постійно пам’ятати про ризик розвитку гіпоглікемії; лікар повинен нагадувати йому про це на кожній консультації.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 14.09.2022
Рецензовано/Revised 25.09.2022
Прийнято до друку/Accepted 06.10.2022

/7/10.jpg)