Журнал «Здоровье ребенка» Том 17, №7, 2022
Вернуться к номеру
Клінічний досвід застосування дитячого опитувальника дерматологічного індексу якості життя (CDLQI) у дітей з атопічним дерматитом
Авторы: Мозирська О.В.
Національний медичний університет імені О.О. Богомольця, м. Київ, Україна
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
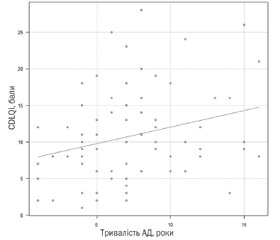
Актуальність. Атопічний дерматит є поширеним свербіжним захворюванням шкіри, що несе значний тягар для пацієнтів, їхніх сімей і суспільства. Метою даного дослідження було оцінити якість життя дітей, хворих на атопічний дерматит, та вивчити кореляційний зв’язок тяжкості атопічного дерматиту та показника якості життя за опитувальником CDLQI (Children’s Dermatology Life Quality Index). Матеріали та методи. У дослідження були включені пацієнти з атопічним дерматитом (n = 71) віком 4–17 років з алергологічного відділення Київської міської дитячої клінічної лікарні № 2. Проводилась оцінка тяжкості атопічного дерматиту за шкалою SCORAD та якості життя за опитувальником CDLQI. Для проведення кореляційного аналізу показників за СDLQI та SCORAD використовували показник рангової кореляції Спірмена. Кореляційний зв’язок вважали вірогідним при р < 0,05. Результати. Кількість хворих, у яких відповідно до результату прояви атопічного дерматиту справляли малий ефект на якість життя, становила 25,4 %, помірний ефект — 40,8 %, дуже великий ефект — 19,7 %, у 12,7 % хворих атопічний дерматит спричиняв надзвичайно великий ефект на якість життя. Коефіцієнт кореляції Спірмена показників тяжкості за шкалою SCORAD та балів за CDLQI становив Ro = 0,932; виявлено кореляційний зв’язок на рівні значимості p < 0,01. При оцінці кореляційних показників у підгрупах дітей за ступенем тяжкості було виявлено різницю: у підгрупі легкого атопічного дерматиту не було кореляції (Ro = 0, p > 0,05) на відміну від підгруп з середньотяжким (Ro = 0,625, p < 0,01) та тяжким атопічним дерматитом (Ro = 0,688, p = 0,01). Показник якості життя мав позитивну кореляцію з віком хворих та тривалістю захворювання, що може бути пов’язано з більш тяжким перебігом хвороби та більшим соціально-психологічним тягарем для дітей старшого віку. Висновки. Опитувальник CDLQI в україномовній версії є надійним інструментом для оцінки якості життя педіатричних хворих з атопічним дерматитом.
Background. Atopic dermatitis is a common pruritic skin disease that causes a significant burden on patients, their families, and society. The purpose of this work was to evaluate the quality of life of children with atopic dermatitis and to study the correlation between the severity of atopic dermatitis and the quality of life according to the Children’s Dermatology Life Quality Index (CDLQI). Materials and methods. Patients with atopic dermatitis (n = 71) aged 4–17 years from the allergy department of the Kyiv City Children’s Clinical Hospital No. 2 were included in the study. The severity of atopic dermatitis was assessed by the SCORing Atopic Dermatitis (SCORAD) tool, and the quality of life — by the CDLQI. Spearman’s rank correlation coefficient was used for correlation analysis of the CDLQI and the SCORAD indicators. Correlation was considered probable at p < 0.05. Results. Atopic dermatitis had a small effect on the quality of life in 25.4 % patients, a moderate effect — in 40.8 %, a very large effect — in 19.7 %, and in 12.7 % of patients, atopic dermatitis caused an extremely large effect on the quality of life. Spearman’s correlation coefficient of severity indicators on the SCORAD and the CDLQI was Ro = 0.932; a correlation was found at the significance level of p < 0.01. When evaluating correlation indicators in subgroups of children by degree of severity, a difference was found: in patients with mild atopic dermatitis, there was no correlation (Ro = 0, p > 0.05), in contrast to the group with moderate to severe (Ro = 0.625, p < 0.01) and severe atopic dermatitis (Ro = 0.688, p = 0.01). The quality of life indicator had a positive correlation with the age of patients and duration of the disease, which may be related to a more severe course and a greater social and psychological burden for older children. Conclusions. The Ukrainian version of CDLQI is a reliable tool for assessing the quality of life of paediatric patients with atopic dermatitis.
дерматит; якість життя; опитувальник; діти
atopic dermatitis; quality of life; questionnaire; children