Вступ
Математичне моделювання біомеханічних систем стає одним з основних методів дослідження. Для визначення внутрішнього напружено-деформованого стану (НДС) біомеханічних моделей найбільш популярним став метод скінченних елементів (МСЕ). За допомогою методу скінченних елементів можна досліджувати складні тривимірні моделі, а також швидко виконувати розрахунки при зміні параметрів моделі, що дає можливість враховувати вплив зміни одного параметра на результат розрахунку всієї моделі. Крім того, МСЕ надає інформацію, яку неможливо отримати звичайними методами вимірювань, і дає можливість моделювати ситуації, які неможливо виміряти експериментальними методами. Одним з важливих прикладів такого дослідження є оцінка розподілу напружено-деформованого стану в хребті [1, 2].
Розвиток обчислювальної потужності комп’ютерів, побудова стійких алгоритмів вирішення завдань за допомогою МСЕ уможливили аналіз різних моделей травм і захворювань хребетного стовпа. У літературі досить багато робіт присвячено вивченню хребта за допомогою МСЕ. Були проаналізовані поперековий відділ хребта [3–5], грудопоперековий відділ хребта [6, 7] і меншою мірою — весь хребет у цілому [8, 9], що пов’язано зі складністю побудови геометричної моделі й моделювання її правильної функціональної поведінки.
Щодо завдання найближчими до нашого дослідження є роботи [10–13], у яких проводиться аналіз у структурах на предмет міжтілового спондилодезу. Існує широкий спектр конструкцій і видів матеріалів кейджів для спинномозкових імплантатів, які можуть використовуватися при спондилодезі хребта, але такі імплантати часто викликають ушкодження замикальної пластини, що може призвести до травми й біомеханічної нестабільності. Існує чотири різних типи матеріалів, які використовують для виготовлення кейджів: металевий, керамічний, полімерний і композитний.
У роботі [10] автори проаналізували поведінку імплантату, виготовленого з двох різних матеріалів: PEEK і PLA. Дослідження проводилося за допомогою МСЕ. Була побудована модель для хребців L4 і L5. На підставі результатів моделювання автори дійшли висновку, що в цілому при використанні матеріалу PEEK спостерігається більш високе напруження в замикальній пластині.
У роботі [11] автори провели порівняльний аналіз імплантата PEEK і титанового імплантата на предмет заднього поперекового міжкорпусного спондилодезу. Це дослідження оцінило біомеханічний ефект, який ці типи імплантатів з різним рівнем твердості справляють на остеопорозний хребець пацієнтів з остеопорозом. Це дослідження показало, що імплантати PEEK у хребцях з остеопорозом порівняно з титановими імплантатами менш схильні до просідання, викликаного мікротріщинами кісткової тканини.
У роботі [12] автори також оцінили вплив імплантатних матеріалів на НДС моделі. Була розглянута модель хребців L3 і L4. У результаті досліджень як краща альтернатива і більш дешевий матеріал був обраний титановий сплав для металевих імплантатів і PLA для композитних імплантатів.
Негативні аспекти імплантатів PEEK (такі як незрощення кістки), незважаючи на кращу біомеханічну стійкість, змушують дослідників вести подальший пошук різних типів імплантатних конструкцій і матеріалів. Так, автори [13] у своїй роботі досліджують новий композитний хребетний кейдж, який має пористу структуру з титанового сплаву. Недавній експеримент на тваринах підтвердив припущення про кращий ступінь зрощення, ніж для кейджа PEEK, і меншу просадку, ніж для титанового кейджа.
Мета: проаналізувати НДС нового міжтілового опорного пристрою і порівняти його з міжтіловою опорою з матеріалу PEEK хребетного блока L5-S1 і заднього спондилодезу.
Матеріали та методи
При побудові розрахункової моделі як основа була використана інтактна модель таза лабораторії біомеханіки ІПХС ім. М.І. Ситенка з крижем і блоком хребців L3-L5 [14] (рис. 1).
У неушкоджену модель були внесені такі зміни:
1) міжхребцевий диск L5-S1 був замінений стандартною міжтіловою опорою з матеріалу PEEK. Задній спондилодез L4-S1 (рис. 2);
2) міжхребцевий диск L5-S1 був замінений новою міжтіловою опорою. Задній спондилодез L4-S1 (рис. 3).
У цьому дослідженні матеріал вважався однорідним та ізотропним. При виборі властивостей кісткових структур і біологічних тканин ми спиралися на дані, які найбільш часто зустрічаються в літературі [15–17]. Використовувані характеристики (Е — модуль пружності (модуль Юнга), υ — коефіцієнт Пуассона) зведені в табл. 1.
Був розглянутий варіант вертикального двоопорного стояння. Згідно з дослідженнями [18], навантаження на хребет у неушкодженій моделі розподіляється між тілом хребця й суглобовими відростками. У нашій моделі, згідно з дослідженням [19], 75 % навантаження припадає на тіло хребця L3 і 25 % — на його суглобові відростки. Основним навантаженням є маса тіла. У цьому дослідженні маса тіла дорівнює 700 Н. Без урахування ваги нижніх кінцівок [20] на верхню поверхню тіла хребця L3 і його суглобові відростки прикладають силу в 422 Н. Місце застосування і напрямок зусиль подані на рис. 4. Модель закріплена у вертлюжних западинах.
Дослідження моделей виконували за допомогою методу скінченних елементів. Як критерій оцінки напружено-деформованого стану моделей використовували напруження за Мізесом [16].
Моделювання виконували за допомогою системи автоматизованого проєктування SolidWorks. Розрахунки напружено-деформованого стану моделей виконували за допомогою програмного комплексу CosmosM [21].
Результати
На першому етапі роботи досліджували напружено-деформований стан моделі поперекового відділу хребта в нормі. Картину розподілу напружень у моделі наведено на рис. 5.
Аналіз результатів розрахунку моделі в нормі показав, що рівень напруження в блоці хребців L3-S1 варіює в межах 15 МПа. Найбільш напруженим є хребець L5. У передній частині рівень напруженого стану досягає значення 9,4 МПа. На нижній поверхні тіла хребця L5 значення напруження за Мізесом становить 14,8 МПа.
З розрахунку можна зробити висновки про те, що в хребетному блоці L3-S1 розподіл НДС відбувається по-різному, більш напруженою є передня частина тіл хребців, а також верхня і нижня поверхні тіл хребців.
На наступному етапі роботи вивчали напружено-деформований стан моделі поперекового відділу хребта із заднім міжтіловим спондилодезом L4-S1 імплантатом з PEEK. Розподіл напружень у моделі наведено на рис. 6.
Аналіз результатів розрахунку моделі порівняно з інтактною моделлю показав, що змінився характер розподілу НДС у хребетному блоці L3-S1. Рівень напруженого стану зріс. Рівень напруження в хребці L5 на передній поверхні тіла хребця досягає значення 14,7 МПа (9,4 МПа в інтактній моделі), а на нижній площині тіла хребця — 40,2 МПа (14,8 МПа в інтактній моделі). У хребці S1 максимальний рівень напруження досягає значення 13,5 МПа (8,1 МПа в інтактній моделі).
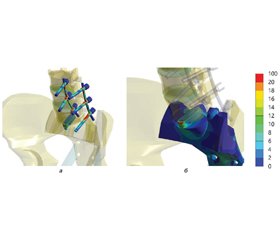
Напружений стан у ділянці міжтілової опори й у фіксуючій конструкції подано на рис. 7.
У міжтіловій опорі передня частина більш напружена, рівень напруженого стану досягає значення 35,7 МПа. Максимальні значення напруження за Мізесом у точках входу гвинтів у кістку спостерігаються в хребці S1 — 27,3 МРа. У фіксуючій конструкції в місцях кріплення гвинтів зі стрижнями рівень напруження досягає значення 80,8 МПа.
З розрахунку можна зробити висновки про те, що характер розподілу НДС у блоці хребців L3-S1 змінився порівняно з інтактною моделлю. Тіла хребців L5 і S1 стали більш напруженими. У зоні контакту фіксуючої структури з кістковою тканиною ділянки концентрації напружень розташовуються в місцях входу гвинтів у кістку.
Останній етап роботи — моделювання варіанта заднього міжтілового спондилодезу L5-S1 імплантатом нової конструкції. Розподіл напружень у моделі можна спостерігати на рис. 8.
Аналіз результатів розрахунку даної моделі порівняно з попередньою показав, що характер розподілу НДС у блоці хребців L3-S1 не змінився. Рівень напруження в хребці L5 на передній поверхні тіла хребця досягає значення 14,7 МПа (14,1 МПа в моделі з імплантатом PEEK), а на нижній площині тіла хребця — 40,7 МПа (40,2 МПа в моделі з імплантатом PEEK). У хребці S1 максимальний рівень напруження досягає значення 14,5 МПа (13,5 МПа в моделі з імплантатом PEEK).
Напружений стан у ділянці міжтілової опори й у фіксуючій конструкції подано на рис. 9.
Для міжтілової опори більш напруженою є передня частина, де рівень напруженого стану досягає значення 113,3 МПа (27,3 МПа в моделі з імплантатом PEEK). Максимальні значення напруження за Мізесом у точках входу гвинтів у кістку спостерігаються в хребці S1 — 17,8 МПа (35,7 МПа в моделі з імплантатом PEEK). У фіксуючій структурі, вузлах кріплення гвинтів зі стрижнями, рівень напруження досягає значення 72,2 МПа (80,8 МПа в моделі з імплантатом PEEK).
Дані про величини напружень у хребцях L3-S1 моделей поперекового відділу хребта в нормі та при різних варіантах заднього міжтілового спондилодезу наведені в табл. 2.
На рис. 10 подано порівняння значень максимальних напружень за Мізесом у тілах хребців інтактної і розрахункової моделей.
Як можем бачити на діаграмі, напруження в хребцях L3 і L4 практично не відрізняються від показників моделі в нормі незалежно від типу міжтілової опори. У хребцях L5 і S1 рівень напружень значно перевищує показники моделі в нормі. Що стосується відмінностей залежно від типу міжтілової опори, слід відзначити, що імплантат нової конструкції забезпечує значно нижчий рівень напружень на передній поверхні хребця S1 і навколо фіксуючих гвинтів у ньому.
У табл. 3 наведені дані про величини напружень в елементах металевої конструкції і міжтілових імплантатах.
Наочно порівняти рівень напружень в елементах транспедикулярної конструкції і міжтілових опорах можна за допомогою діаграми, яка наведена на рис. 11.
Наведена діаграма наочно демонструє, що нова міжтілова опора приймає на себе основне навантаження, про що свідчить величина напружень у ній, яка втричі перевищує максимальний рівень напружень в імплантаті з матеріалу PEEK. Це дозволяє розвантажити елементи транспедикулярної конструкції, що підтверджується низьким рівнем напружень на всіх фіксуючих гвинтах і по всій довжині опорного стрижня.
Висновки
1. Характер розподілу напружень у блоці хребців L3-S1 не змінився порівняно з моделлю PEEK.
2. У тілах хребців L4 і S1 рівень напруження незначно підвищився порівняно з моделлю PEEK, а в хребці L5 — знизився.
3. Використання більш жорсткої міжтілової опори дозволило знизити напружений стан на вході фіксуючих гвинтів до кістки хребця S1.
4. Більш високий рівень напруження в самій міжтіловій опорі порівняно з моделлю PEEK не є критичним з точки зору міцності для металу.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів і власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 05.11.2022
Рецензовано/Revised 13.11.2022
Прийнято до друку/Accepted 22.11.2022
Список литературы
1. Попсуйшапка К.О., Тесленко С.О., Попов А.І., Карпінський М.Ю., Яресько О.В. Дослідження напружено-деформованого стану моделей хребта залежно від обсягу руйнування хребця Th6 і варіанту остеосинтезу. Травма. 2022. Т. 23. № 5. С. 53-64. DOI: https://doi.org/10.22141/1608-1706.5.23.2022.916.
2. Нехлопочин А.С., Нехлопочин С.Н., Карпинский М.Ю., Швец А.И., Карпинская Е.Д., Яресько А.В. Математический анализ и оптимизация конструктивных характеристик стабилизирующих телозамещающих систем для субаксиального цервикоспондилодеза с применением метода конечных элементов. Хирургия позвоночника. 2017. Т. 14. № 1. С. 37-45.
3. Ben-Hatira F., Saidane K., Mrabet A. A finite element modeling of the human lumbar unit including the spinal cord. J. Biomedical Science and Engineering. 2012. 5. 146-152. http://dx.doi.org/10.4236/jbise.2012.53019.
4. Srinivas G.R., Kumar M.N., Deb A. Adjacent Disc Stress Following Floating Lumbar Spine Fusion: A Finite Element Study. Asian Spine J. 2017. 11(4). 538-547. DOI: https://doi.org/10.4184/asj.2017.11.4.538.
5. Zhang Z., Fogel G.R., Liao Z., Sun Y., Sun X., Liu W. Biomechanical evaluation of four surgical scenarios of lumbar fusion with hyperlordotic interbody cage: A finite element study/ Bio-Medical and Materials Engineering. 2018. 29. 485-497. DOI: 10.3233/BME-181004.
6. Tyndyk M.A., Barron V., Mchugh P.E., O’Mahoney D. Generation of a finite element model of the thoracolumbar spine. Acta of bioengineering and biomechanics. Wroclaw University of Technology. 2007. 9(1). 35-46.
7. Aroeira R.M.C., de Melo Pertence A.E., Kemmoku D.T., Greco М. Three-dimensional geometric model of the middle segment of the thoracic spine based on graphical images for finite element analysis. Res. Biomed. Eng. 2017 June. 33(2). 97-104. DOI: http://dx.doi.org/10.1590/2446-4740.08916.
8. Nakashima D., Kanchiku T., Nishida N., Ito S., Ohgi J., Suzuki H. et al. Finite element analysis of compression fractures at the thoracolumbar junction using models constructed from medical images. Experimental and Therapeutic Medicine. 2018. 15. 3225-3230. DOI: 10.3892/etm.2018.5848.
9. Nishida N., Ohgi J., Jiang F., Ito S., Imajo Y., Suzuki H. et al. Finite Element Method Analysis of Compression Fractures on Whole-Spine Models Including the Rib Cage. Hindawi Computational and Mathematical Methods in Medicine. 2019. Vol. 2019. Article ID 8348631. 10 p. https://doi.org/10.1155/2019/8348631.
10. Jalil M.H., Mazlan M.H., Todo М. Biomechanical Comparison of Polymeric Spinal Cages Using Ct Based Finite Element Method. International Journal of Bioscience, Biochemistry and Bioinformatics. 2017. Vol. 7. № 2. doi: 10.17706/ijbbb.2017.7.2.110-117.
11. Sato T., Yonezawa І., Todo М., Takano H., Kaneko K. Biomechanical effects of implant materials on posterior lumbar interbody fusion: comparison of polyetheretherketone and titanium spacers using finite element analysis and considering bone density. J. Biomedical Science and Engineering. 2018. Vol. 11. № 4. Р. 45-59. DOI: 10.4236/jbise.2018.114005.
12. Yahya R., Mazlan M.H., Shuib S., Abdullah A.H. Biomechanical Analysis of Spinal Fusion Cage for Lumbar Vertebrae. International Journal of Recent Technology and Engineering. 2019. Vol. 8. Issue 4. ISSN: 2277-3878. DOI: 10.35940/ijrte.D5206.118419.
13. Lim K.-M., Park T.-H., Lee S.-J., Park S.-J. Design and Biomechanical Verification of Additive Manufactured Composite Spinal Cage Composed of Porous Titanium Cover and PEEK Body. Appl. Sci. 2019. 9. 4258. doi: 10.3390/app9204258.
14. Куценко В.О., Карпінський М.Ю., Суббота І.А., Яресько О.В. Моделювання впливу механічних властивостей міжхребцевих дисків та заднього опорного комплексу на стан поперекових опорно-рухових сегментів. Медицина и... 2007. № 1(16). С. 15-20.
15. Kurowski P.M. Engineering Analysis with SolidWorks Simulation 2012. Published April 11, 2012. 475 р. ISBN: 978-1-58503-710-0.
16. Zienkiewicz O.C., Taylor R.L. The Finite Element Me-thod for Solid and Structural Mechanics. Sixth edition. Butterworth-Heinemann, 2005. 736 p.
17. Kong W.Z., Goel V.K. Ability of the Finite Element Mo-dels to Predict Response of the Human Spine to Sinusoidal Vertical Vibration. Spine. 2003. Vol. 28. № 17. Р. 1961-1967. DOI: 10.1097/01.BRS.0000083236.33361.C5.
18. Vidal-Lesso A., Ledesma-Orozco E., Daza-Benítez L., Lesso-Arroyo R. Mechanical Characterization of Femoral Cartilage Under Unicompartimental Osteoarthritis. Ingenierí Amecánica Tecnología y Desarrollo. 2014. Vol. 4. № 6. 239-246.
19. Boccaccio A., Pappalettere C. Mechanobiology of Fracture Healing: Basic Principles and Applications in Orthodontics and Orthopaedics. Theoretical Biomechanics / Dr Vaclav Klika (Ed.). 2011. Р. 21-48.
20. Mobbs R.J., Loganathan А., Yeung V., Rao P.J. Indications for Anterior Lumbar Interbody Fusion. Orthopaedic Surgery. 2013. 5(3). 153-63. DOI: 10.1111/os.12048.
21. Алямовский А.А. SolidWorks/COSMOSWorks. Инженерный анализ методом конечных элементов. Москва: ДМК Пресс, 2004. 432.

/48.jpg)
/49.jpg)
/50.jpg)
/51.jpg)
/53.jpg)
/52.jpg)