Вступ
Дві третини пацієнтів потребують комбінованої антигіпертензивної терапії. Найбільш ефективні фіксовані комбінації антигіпертензивних препаратів включають блокатори ренін-ангіотензин-альдостеронової системи в комбінації з антагоністами кальцію і/або діуретиками [24].
Артеріальна жорсткість починається зі структурних змін у судинній стінці перед появою в ній бляшки або тромбу. Є показник для оцінки жорсткості артерій — швидкість поширення пульсової хвилі (ШППХ) артеріями еластичного та м’язового типу як сурогатний маркер атеросклерозу. Проте він залежить від рівня системного артеріального тиску й майстерності оператора. Новий показник артеріальної жорсткості, серцево-гомілковий судинний індекс (CAVI), корелює з іншими факторами серцево-судинного ризику, що відображає ступінь атеросклеротичних змін, зокрема в пацієнтів із цукровим діабетом 2-го типу, у пацієнтів з атеросклеротичним ураженням, які знаходяться на гемодіалізі [8, 9].
У пацієнтів з високим рівнем серцево-судинного ризику була встановлена прогностична цінність CAVI порівняно з іншими параметрами атеросклерозу для довгострокового прогнозування ризику серцево-судинних захворювань [19, 21]. CAVI відображає жорсткість аорти, стегнової артерії та великогомілкової артерії в цілому, але при цьому CAVI не залежить від величини артеріального тиску. CAVI корелює з коронарним стенозом, цукровим діабетом і метаболічним синдромом [22].
Ercan Aydın зі співавт. досліджували вплив інфекції COVID-19 на серцево-гомілковий судинний індекс у 115 пацієнтів середнього віку (65,7 ± ± 10,7 року) порівняно з контрольною групою, порівнянною за віком, індексом маси тіла (ІМТ), статтю і наявністю супутньої патології. В основній групі CAVI справа був 9,6 ± 2,4, у контрольній — 8,5 ± 1,1 (p = 0,004). CAVI зліва в основній групі був 9,4 ± 2,7, у контрольній — 8,5 ± 1,2 (p = 0,01). CAVI справа в пацієнтів з помірним і тяжким ступенем COVID-19 був 10,8 ± 3,4, у пацієнтів з м’яким перебігом COVID-19 — 8,8 ± 0,9 (р = 0,008). CAVI зліва в пацієнтів з помірним і тяжким ступенем COVID-19 був 10,7 ± 3,6, у пацієнтів з м’яким перебігом COVID-19 — 8,5 ± 1,5 (р < 0,001). Автори роблять висновок, що як справа, так і зліва CAVI був вищим у пацієнтів з інфекцією COVID-19 і залежав від тяжкості хвороби [7].
У доступній нам літературі ми не знайшли даних щодо впливу статинотерапії в пацієнтів європейської раси з артеріальною гіпертензією (АГ) на CAVI.
Метою даного дослідження було оцінити терапевтичну ефективність додавання статинотерапії до основної антигіпертензивної терапії (фіксованої подвійної або потрійної комбінації) і вплив на жорсткість судин з оцінкою серцево-гомілкового судинного індексу при застосуванні фіксованої потрійної комбінації валсартан/амлодипін/гідрохлортіазид і подвійної фіксованої комбінації валсартан/амлодипін у лікуванні пацієнтів з артеріальною гіпертензією ІІ–ІІІ ступеня.
Матеріали та методи
Завданням даного дослідження було вивчити вплив на артеріальну жорсткість додавання статинів до антигіпертензивної терапії в рамках дослідження терапевтичної ефективності фіксованої потрійної та подвійної комбінації в лікуванні артеріальної гіпертензії.
У дослідження було включено 99 пацієнтів з АГ ІІ–ІІІ ступеня за класифікацією ВООЗ, які проходили стаціонарне або амбулаторне лікування у відділі вторинних і легеневих гіпертензій ДУ «Національний науковий центр «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України».
Критерії включення в дослідження: вік 25–75 років, есенціальна АГ ІІ стадії, рівень систолічного (САТ) і/або діастолічного (ДАТ) артеріального тиску > 160/100 мм рт.ст. у кінці періоду відміни всіх антигіпертензивних препаратів, відсутність критеріїв виключення, підписання пацієнтом інформованої згоди на участь у дослідженні, здатність пацієнта до адекватного співробітництва.
Критерії виключення: рівень артеріального тиску (АТ) > 220/140 мм рт.ст.; вторинна і злоякісна АГ; наявність цукрового діабету; наявність в анамнезі таких ускладнень, як інфаркт міокарда, інвазивні й неінвазивні втручання на серці, порушення мозкового кровообігу; порушення серцевого ритму (постійна форма фібриляції передсердь, часта шлуночкова або суправентрикулярна екстрасистолія, атріовентрикулярна блокада ІІ і ІІІ ступеня, синдром слабкості синусового вузла); серцева недостатність ІІІ–IV функціонального класу (NYHA); стенокардія напруги ІІІ–IV функціонального класу; тромбоемболія легеневої артерії; виражена хронічна ниркова недостатність (швидкість клубочкової фільтрації (ШКФ) < 30 мл/хв, анурія); декомпенсоване ураження печінки; психічні розлади; онкологічні захворювання; вагітні жінки або з лактацією; підвищена чутливість до компонентів терапії в анамнезі; пацієнти, які беруть участь в інших клінічних дослідженнях.
Умовами припинення дослідження були: індивідуальна непереносимість препарату, поява тяжких або неочікуваних побічних реакцій, які потребують, на думку дослідника або пацієнта, відміни, значне погіршення загального стану в період дослідження, порушення пацієнтом протоколу дослідження, зміни лабораторних показників, що свідчать про потенційну загрозу для пацієнта, відкликання пацієнтом інформованої згоди.
Згідно з протоколом усім пацієнтами були проведені такі дослідження: збір анамнезу, вимірювання маси тіла і зросту, об’єктивне обстеження, вимірювання офісного САТ і ДАТ, частоти серцевих скорочень (ЧСС), біохімічне дослідження крові, загальноклінічні дослідження крові й сечі, визначення жорсткості судинної стінки за допомогою вимірювання серцево-гомілкового судинного індексу.
Жорсткість судинної стінки вимірювалось за допомогою серцево-судинного гомілкового індексу (прилад VaSera 1500, Fukuda Denshi, Японія), манжети накладалися на обидві руки й ноги в положенні лежачи, і одночасно відбувалося вимірювання жорсткості судинної стінки.
Проводили біохімічне дослідження крові: визначали рівень креатиніну, електролітів (калію та натрію), глюкози, загального холестерину (ЗХС), тригліцеридів (ТГ), холестерину ліпопротеїдів високої щільності (ХС ЛПВЩ), холестерину ліпопротеїдів низької щільності (ХС ЛПНЩ), холестерину ліпопротеїдів дуже низької щільності сироватки крові. Кліренс креатиніну, що відображає ШКФ, визначали розрахунково за формулою CKD-EPI. Визначення наявності атеросклеротичних бляшок у сонних артеріях проводили за стандартною методикою за допомогою ультразвукового діагностичного апарата Imagic Agile (Kontron Medical, Франція) з вимірюванням товщини інтими-медіа (ТІМ) сонних артерій. Усім пацієнтам проводили каротидну ультрасонографію загальної сонної артерії, внутрішньої та зовнішньої сонної артерії як справа, так і зліва на початку дослідження за рекомендаціями Товариства радіологів на конференції ультразвукового дослідження [8]. Максимальну ТІМ вимірювали в ділянці біфуркації загальної сонної артерії як сурогатний маркер серцево-судинної захворюваності. Головними критеріями оцінки в даному субдослідженні були зміни жорсткості судинної стінки за показниками CAVI [12].
Пацієнтам було призначено фіксовану потрійну комбінацію — таблетки валсартан/амлодипін/гідрохлортіазид. Препарат призначався по 1 таблетці (160 мг валсартану/5 мг амлодипіну/12,5 мг гідрохлортіазиду) один раз на добу вранці протягом 1 місяця. Або пацієнти отримували за аналогічною схемою подвійну фіксовану комбінацію препарату валсартан/амлодипін. Препарат призначався по 1 таблетці (160 мг валсартану/5 мг амлодипіну) один раз на добу вранці протягом 1 місяця. За необхідності, якщо не було досягнення цільового рівня офісного АТ менше за 140/90 мм рт.ст., доза титрувалась до добової дози 320/10/12,5 мг (валсартан/амлодипін/гідрохлортіазид) на фіксованій потрійній комбінації та до 320/10 мг (валсартан/амлодипін) на фіксованій подвійній комбінації.
Пацієнти були поділені на 2 групи. Одній групі додавали аторвастатин до фіксованої подвійної чи потрійної комбінації антигіпертензивних препаратів (пацієнтам з наявною дисліпідемією, яку визначали при рівні загального холестерину ≥ 5,0 ммоль/л, ХС ЛПНЩ ≥ 3,0 ммоль/л за показаннями відповідно до рекомендацій ESH з лікування АГ) у дозі 20–40 мг на добу протягом 6 місяців лікування. Через 6 місяців лікування відбувався контроль терапії.
Статистична обробка
Статистичну обробку результатів було проведено після створення баз даних у системах Microsoft Excel. Середні показники обстежених пацієнтів були визначені за допомогою пакета аналізу в системі Microsoft Excel. Усі інші статистичні розрахунки були проведені за допомогою програми SPSS 21.0. Нормальність рядів визначалася за допомогою критерію Шапіро — Уїлка. При нормальному розподілі достовірність різниці середніх на етапах лікування визначалася за допомогою парного двовибіркового тесту, достовірність різниці між групами — за допомогою незалежного t-тесту для середніх після визначення характеру розподілу показників. Ефективність у групах і різниця у групах за розподілом наявності тієї або іншої ознаки оцінювалася за дихометричною змінною за допомогою критерію χ2.
Результати
У дослідження було включено 99 пацієнтів з помірною і тяжкою АГ. Середній вік хворих становив 54,82 ± 1,25 (25–75) року. Середній ІМТ — 31,21 ± 0,48 кг/м2. Середні цифри офісного САТ/ДАТ
на початку дослідження становили 161,69 ± ± 1,25/98,55 ± 0,97 мм рт.ст. Середня офісна ЧСС — 70,81 ± 0,96 уд/хв. Основні клініко-демографічні показники пацієнтів, які були включені в дослідження, за групами (з додаванням статинотерапії або без неї) подані в табл. 1.
Пацієнти, які отримували статинотерапію, мали вищий рівень CAVI початково, були старші за віком, мали більший ІМТ, більшу тривалість АГ, у них був вищий рівень загального холестерину і ХС ЛПНЩ, мали більшу максимальну ТІМ сонних артерій. Рівні офісного АТ і АТ при добовому моніторуванні не відрізнялися.
При прийомі подвійної (на основі валсартану й амлодипіну) або потрійної (на основі валсартану, амлодипіну і гідрохлортіазиду) фіксованої комбінованої терапії відбувалося значне достовірне зниження офісного артеріального тиску в пацієнтів з помірною і тяжкою артеріальною гіпертензією. Зниження офісного САТ/ДАТ становило 35/19 мм рт.ст. (p < 0,05) і 42/26 мм рт.ст. (p < 0,05) на подвійній і потрійній комбінації відповідно. У групі подвійної терапії цільового офісного АТ було досягнуто в 90,9 %, у групі потрійної комбінації — у 95,7 % пацієнтів через 6 місяців лікування. Нами не відзначено достовірної динаміки лабораторних показників протягом 6 місяців лікування.
Оскільки дуже важливо в лікуванні пацієнтів з АГ оцінювати вплив терапії на ураження органів-мішеней, ми проаналізували динаміку жорсткості артерій за CAVI залежно від додавання аторвастатину до подвійної (валсартан/амлодипін) чи потрійної (валсартан/амлодипін/гідрохлортіазид) фіксованої комбінації. Дані наведені в табл. 2.
Офісний АТ та АТ при добовому моніторуванні достовірно і однаково знизилися в обох групах лікування.
Відомо, що CAVI не залежить від рівня АТ, ми в нашому дослідженні показали вплив статинотерапії на CAVI в пацієнтів з АГ європеоїдної раси при додаванні до АГ-терапії та виявили позитивний вплив на зменшення прогресування жорсткості артерій.
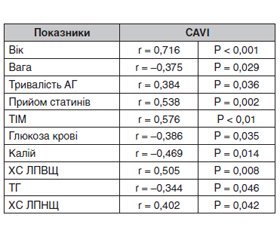
Ми виявили статистично значущі кореляційні зв’язки CAVI з віком, рівнем тригліцеридів крові до лікування, ХС ЛПНЩ до лікування, ХС ЛПВЩ до лікування, тривалістю АГ, рівнем глюкози крові, калію крові, максимальною ТІМ сонних артерій, прийомом статинів. Дані наведені в табл. 3.
Коли ми провели регресійний аналіз, то виявили зв’язок CAVI в групі пацієнтів, які приймали статини, з прийомом статинів — β = 0,403, p = 0,043; рівнем загального холестерину до лікування — β = 0,426, p = 0,041; рівнем тригліцеридів крові до лікування — β = 0,417, p = 0,046, і віком — β = 0,548, p = 0,008. У групі пацієнтів, які не приймали статини, зв’язок CAVI був виявлений тільки з віком пацієнтів — β = 0,327, p = 0,036.
Отже, терапія на основі фіксованих комбінацій валсартан/амлодипін і валсартан/амлодипін/гідрохлортіазид з додаванням статинів для лікування дисліпідемії сприяла достовірному зниженню артеріального тиску, що привело до кращого конт–ролю АТ, не мала негативного впливу на метаболічні порушення і гальмувала прогресування жорсткості артерій.
Обговорення
У даному дослідженні для оцінки ураження органів-мішеней у пацієнтів з АГ ми використали показник CAVI, який не залежить від рівня АТ. На фоні додавання статинів до антигіпертензивної терапії ми виявили зменшення прогресування жорсткості артерій у пацієнтів з АГ.
Вимірювання жорсткості артерій у рутинній медичній практиці важливе для оцінки прогресування атеросклерозу. До цього часу було запропоновано багато параметрів, які кількісно визначають жорсткість артерії. Серед них швидкість поширення пульсової хвилі найбільш часто застосовується в клінічній практиці, оскільки її можна виміряти просто й неінвазивно. Однак ШППХ істотно залежить від артеріального тиску на момент вимірювання. Тому ШППХ не підходить як параметр для оцінки жорсткості артерії, особливо для досліджень, пов’язаних зі зміною артеріального тиску. У 2006 році K. Shirai зі співавт. був запропонований новий параметр жорсткості артеріальної стінки, незалежний від артеріального тиску, — серцево-гомілковий судинний індекс (CAVI) [18].
Оскільки CAVI не залежить від артеріального тиску на момент вимірювання, за його допомогою можна оцінити реальний вплив артеріального тиску на жорсткість стінки артерії. Було показано, що фіксована комбінація лозартан/гідрохлортіазид знижує рівень CAVI [22]. Хоча тіазидні діуретики не змінювали рівень CAVI окремо. В нашому дослідженні на фоні подвійної чи потрійної комбінації ми не виявили змін у зниженні жорсткості артерій за CAVI.
G. Uehara [22] дослідив, що серед кандесартану, телмісартану і лозартану найбільше знижує CAVI кандесартан. Bukuda зі співавт. [3] вивчали вплив кандесартану порівняно з блокаторами кальцієвих каналів. Вони показали, що артеріальний тиск значно знизився в обох групах, а показники CAVI не відрізнялися в обох групах. У дослідженні Miyashita зі співавт. вивчали вплив амлодипіну й олмесартану на АТ та CAVI. АТ знижувався однаково, але CAVI значно знижувався лише в групі олмесартану порівняно з групою амлодипіну [12, 23].
Оскільки дані досліджень вказують на позитивний вплив блокаторів рецепторів ангіотензину II на еластичність судин, ми включили в дослідження оцінку CAVI. Але в нашому дослідженні ми не отримали достовірної динаміки CAVI після тримісячного лікування фіксованими комбінаціями валсартан/амлодипін і валсартан/амлодипін/гідрохлортіазид. Безпечність використовуваних у дослідженні комбінацій доводить відсутність негативної динаміки лабораторних показників через 6 місяців лікування.
CAVI був вивчений як неінвазивний маркер артеріальної жорсткості [5, 15, 16, 20]. CAVI був значно підвищеним у пацієнтів з метаболічним синдромом, а зниження маси тіла значно знижувало рівень CAVI у пацієнтів з ожирінням [16]. Що стосується товщини судинної стінки (ТСС) сонної артерії, то кілька дослідників виявили сильні кореляційні зв’язки між CAVI та ТСС, але виявилося, що наявність атеросклеротичної бляшки показала набагато сильнішу кореляцію з CAVI [14, 13, 25]. Кореляційні зв’язки CAVI та ТСС можуть бути важливим предиктором церебрального тромбозу в пацієнтів високого ризику атеросклерозу [25]. Повідомлялося, що препарати для зниження холестерину, такі як пітавастатин, езетиміб, і для зниження тригліцеридів, такі як –ейкозапентаєнова кислота, зменшують рівень CAVI [11]. Так, у дослідженні Takashi Yamaguchi зі співавт. вивчали вплив безафібрату на жорсткість судин, виміряну за допомогою CAVI в пацієнтів із цукровим діабетом і гіпертригліцеридемією, порівняно з ейкозапентаєновою кислотою. Дослідники показали достовірний позитивний прямий вплив безафібрату на зменшення жорсткості артерій (через зниження CAVI) через 12 тижнів лікування і відсутність такого впливу на фоні ейкозапентаєнової кислоти. Відбулося достовірне зменшення рівня тригліцеридів крові, поліпшення глікемічного профілю пацієнтів із цукровим діабетом через вплив на інсулінорезистентність. У нашому дослідженні достовірних змін рівня глюкози в обох групах лікування відзначено не було. Ми не включали пацієнтів із цукровим діабетом у наше дослідження.
XiaoXiao Zhao зі співавт. вивчали зв’язок CAVI з дисліпідемією і факторами серцево-судинного ризику. Вони показали, що CAVI в пацієнтів з АГ був вищим порівняно з пацієнтами без АГ. CAVI в даному дослідженні був пов’язаний з віком, АТ, рівнем загального холестерину, тригліцеридів, ХС ЛПНЩ. Автори не відзначили зв’язку в дослідженні між CAVI та прийомом статинів, а також між курцями і некурцями і наявністю цукрового діабету. Ми в нашому дослідженні виявили тісний зв’язок CAVI з прийомом статинів у пацієнтів з АГ, які приймали подвійну чи потрійну фіксовану комбінацію антигіпертензивних препаратів. Наші пацієнти не мали цукрового діабету і супутньої патології.
Однак більшість сучасних досліджень, що стосуються взаємозв’язку між CAVI та розвитком атеросклерозу, когнітивними порушеннями, метаболічним синдромом, проводилися в Японії [25].
Висновки
1. На фоні додавання статинів до антигіпертензивної фіксованої потрійної комбінації валсартан/амлодипін/гідрохлортіазид або подвійної фіксованої комбінації валсартан/амлодипін у лікуванні пацієнтів з резистентною артеріальною гіпертензією відбувалося зменшення прогресування жорсткості артерій за CAVI, тоді як в групі без додавання статинів такої тенденції відзначено не було.
2. Терапія на основі фіксованих комбінацій валсартан/амлодипін і валсартан/амлодипін/гідрохлортіазид з додаванням статинів для лікування дисліпідемії сприяла достовірному зниженню артеріального тиску, що привело до кращого контролю АТ, і не мала негативного впливу на метаболічні порушення.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів і власної фінансової зацікавленості при підготовці даної статті.
Внесок авторів. Рековець О.Л. — написання статті, збір матеріалу, статистичний аналіз даних, висновки; Сіренко Ю.М. — рецензування статті, ідея, план дослідження, висновки; Торбас О.О., Кушнір С.М., Приймак Г.Ф. — створення бази даних, збір матеріалу.
Отримано/Received 18.06.2023
Рецензовано/Revised 01.07.2023
Прийнято до друку/Accepted 10.07.2023
Список литературы
1. ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group. The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial. Major outcomes in high-risk hypertensive patients randomized to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic: The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). JAMA. 2002. Vol. 18. 288(23). P. 2981-2997. DOI:10.1001/jama.288.23.2998.
2. Aranda P., Ruilope L.M., Calvo C., Luque M., Coca A., de Miguel A.G. Erectile dysfunction in essential arterial hypertension and effects of sildenafil: results of a Spanish national study. Am. J. Hypertens. 2004. Vol. 17(2). P. 139-145. DOI: 10.1016/j.amjhyper.2003.09.006.
3. Bukuda К., Ichihara A., Sakoda M., Mito A., Kinouchi K., Itoh H. Blood pressure-independent effect of candesartan on cardio-ankle vascular index in hypertensive patients with metabolic syndrome. Vasc. Health Risk Manag. 2010. 6. 571-578. DOI:10.2147/vhrm.s11958.
4. Calhoun D.A., Lacourciere Y., Crikelair N., Jia Y., Gla–zer R.D. Effects of demographics on the antihypertensive efficacy of triple therapy with amlodipine, valsartan, and hydrochlorothiazide for moderate to severe hypertension. Curr. Med. Res. Opin. 2013. Vol. 29. P. 901-910. doi: 10.1185/03007995.2013.803057.
5. Choi S.Y., Oh B.H., Park J.B., Choi D.J., Rhee M.Y., Park S. Age-associated increase in arterial stiffness measured according to the cardio-ankle vascular index without blood pressure changes in healthy adults. J. Atheroscler. Thromb. 2013. 20. 911-923. DOI: 10.5551/jat.18267.
6. Doumas M., Tsakiris A., Douma S. Grigorakis A., Papadopoulos A., Hounta A. et al. Factors affecting the increased prevalence of erectile dysfunction in Greek hypertensive compared with normotensive subjects. J. Androl. 2006. Vol. 27(3). P. 469-477. DOI: 10.2164/jandrol.04191.
7. Aydın Е., Kant А., Yilmaz G. Evaluation of the cardio-ankle vascular index in COVID-19 patients. Rev. Assoc. Med. Bras. 1992. 2022 Jan. 68(1). 73-76. doi: 10.1590/1806-9282.20210781.
8. Grant E.G., Benson C.B., Moneta G.L., Alexandrov A.V., Baker J.D., Bluth E.I. et al. Carotid artery stenosis: gray-scale and Doppler US diagnosis — Society of Radiologists in Ultrasound Consensus Conference. Radiology. 2003 Nov. 229(2). 340-6. doi: 10.1148/radiol.2292030516.
9. Greenstein A., Chen J., Miller H., Matzkin H., Villa Y., Braf Z. Does severity of ischemic coronary disease correlate with erectile function? Int. J. Impot. Res. 1997. Vol. 9(3). P. 123-126. DOI:10.1038/sj.ijir.3900282
10. Horinaka S., Yabe A., Yagi H., Yagi H., Ishimura K., Hara H., Iemua T. Comparison of atherosclerotic indicators between cardio ankle vascular index and brachial ankle pulse wave velocity. Angiology. 2009. 60(4). 468-476. https://doi.org/10.1177/0003319708325443.
11. Ibata J., Sasaki H., Kakimoto T., Matsuno S., Nakatani M., Kobayashi M. et al. Cardio-ankle vascular index measures arterial wall stiffness independent of blood pressure. Diabetes Res. Clin. Pract. 2008. 80(2). 265-270. https://doi.org/10.1016/j.diabres.2007.12.016.
12. Kokubo Y., Watanabe M., Higashiyama A., Nakao Y.M., Nakamura F., Miyamoto Y. Impact of intima-media thickness progression in the common carotid arteries on the risk of incident cardiovascular disease in the suita study. J. Am. Heart Assoc. 2018. 7(11). e007720.
13. Mehlum M., Liestøl K., Julius S., Kjeldsen S.E., Hua T.A., Rothwell P.M. et al. Visit-to-visit blood pressure variability increases risk of stroke or cardiac events in patients given valsartan or amlodipine in the VALUE trial. J. Hypertens. 2015. Vol. 33. Suppl. 1. e40. doi: 10.1097/01.hjh.0000467454.55397.ea.
14. Miyashita Y., Endo K., Saiki A., Ban N., Yamaguchi T., Kawana H. et al. Effects of pitavastatin, a 3-hydroxy-3-methylglutaryl coenzyme a reductase inhibitor, on cardio-ankle vascular index in type 2 diabetic patients. J. Atheroscler. Thromb. 2009. 16. 539-545. https://doi.org/10.5551/jat.281.
15. Miyashita Y., Saiki A., Endo K., Ban N., Yamaguchi T., Kawana H. et al. Effects of olmesartan, an angiotensin II receptor blocker, and amlodipine, a calcium channel blocker, on Cardio-Ankle Vascular Index (CAVI) in type 2 diabetic patients with hypertension. J. Atheroscler. Thromb. 2009. 16. 621-626. DOI: 10.5551/jat.497.
16. Nakayama K., Kuwabara Y., Daimon M., Shindo S., Fujita M., Narumi H. et al. Valsartan Amlodipine Randomized Trial (VART): design, methods, and preliminary results. Hypertens. Res. 2008. Vol. 31(1). P. 21-28. doi: 10.1291/hypres.31.21.
17. Namekata T., Suzuki K., Ishizuka N., Shirai K. Establishing baseline criteria of cardio-ankle vascular index as a new indicator of arteriosclerosis: a cross-sectional study. BMC Cardiovasc. Disord. 2011. 11. 51. doi: 10.1186/1471-2261-11-51.
18. Saiki A., Sato Y., Watanabe R., Watanabe Y., Imamura H., Yamaguchi T. et al. The Role of a Novel Arterial Stiffness Parameter, Cardio-Ankle Vascular Index (CAVI), as a Surrogate Marker for Cardiovascular Diseases. J. Atheroscler. Thromb. 2016. 23(2). 155-68. doi: 10.5551/jat.32797.
19. Satoh N., Shimatsu A., Kato Y., Araki R., Koyama K., Okajima T. et al. Evaluation of the cardio-ankle vascular index, a new indicator of arterial stiffness independent of blood pressure, in obesity and metabolic syndrome. Hypertens. Res. 2008 Oct. 31(10). 1921-30. doi: 10.1291/hypres.31.1921.
20. Sawada T., Yamada H., Dahlf B., Matsubara H., for the KYOTO HEART Study Group. Effects of valsartan on morbidity and mortality in uncontrolled hypertensive patients with high cardiovascular risks: KYOTO HEART Study. Eur. Heart J. 2009. Vol. 30. P. 2461-2469. doi: 10.1093/eurheartj/ehp363.
21. Shirai K., Utino J., Otsuka K., Takata M. A novel blood pressure-independent arterial wall stiffness parameter; cardio-ankle vascular index (CAVI). J. Atheroscler. Thromb. 2006. 13(2). 101-107. doi: 10.5551/jat.13.101.
22. Shirai K., Song M., Suzuki J., Kurosu T., Oyama T., Nagayama D. et al. Contradictory effects of β1- and α1-aderenergic receptor blockers on cardio-ankle vascular stiffness index (CAVI) — CAVI independent of blood pressure. J. Atheroscler. Thromb. 2011. 18(1). 49-55. DOI: 10.5551/jat.3582.
23. Sison J., Ríos Vega R.M., Dayi H., Bader G., Brunel P. Efficacy and effectiveness of valsartan/amlodipine and valsartan/amlodipine/hydrochlorothiazide in hypertension: randomized-controlled versus observational studies. Current Medical Research and Opinion. DOI: 10.1080/03007995.2017.1412682.
24. Takaki A., Ogawa H., Wakeyama T., Iwami T., Kimura M., Hadano Y. et al. Cardio-ankle vascular index is superior to brachial-ankle pulse wave velocity as an index of arterial stiffness. Hypertens. Res. 2008 Jul. 31(7). 1347-55. doi: 10.1291/hypres.31.1347.
25. Uehara G., Takeda H. Relative effects of telmisartan, candesartan and losartan on alleviateing arterial stiffnes inpatients with hypertension complicated by diabetes mellitus: An evaluation using the cardiovascular index. J. Inter. Medical Res. 2008. 36. 1094-1102. doi: 10.1177/147323000803600529.
26. Wang L., Zhao J.W., Liu B., Shi D., Zou Z., Shi X.Y. Antihypertensive effects of olmesartan compared with other angiotensin receptor blockers: a meta-analysis. Am. J. Cardiovasc. Drugs. 2012. 12(5). P. 335-344. doi: 10.2165/11597390-000000000-00000.
27. Williams B., Mancia G., Spiering W., Agabiti Rosei E., Azizi M., Burnier M. et al; Authors/Task Force Members: 2018 ESC/ESH Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension. J. Hypertens. 2018. 36. 1953-2041. doi: 10.1097/HJH.0000000000001940.
28. Yamamoto N., Yamanaka G., Ishikawa M., Takasugi E., Murakami S., Yamanaka T. et al. Cardio-ankle vascular index as a predictor of cognitive impairment in community-dwelling elderly people: four-year follow-up. Dement. Geriatr. Cogn. Disord. 2009. 28(2). 153-158. doi: 10.1159/000235642.
/12.jpg)

/11.jpg)