Вступ
Травматичне ушкодження головного мозку (ТУГМ) є однією з найпоширеніших причин смерті, втрати працездатності й соціальної активності. Рівень смертності внаслідок ТУГМ коливається від 13/100 000 (Китай) [1] до 11/100 000 (Європа) і 17/100 000 (США) [2]. Спроби впровадження алгоритмів лікування на основі концепції Лунда згідно з першими рекомендаціями Brain Trauma Foundation (BTF) призвели до зниження смертності пацієнтів з діагнозом ТУГМ [3, 4]. Перші рекомендації BTF спільно з Американською асоціацією ней-
рохірургів (AANS), Конгресом неврологічних хірургів (CNS) і спільною секцією AANS/CNS з нейротравм та інтенсивної терапії було розроблено в 2007 році, а у 2016 році вийшло їх оновлення. Алгоритми ведення пацієнтів з ТУГМ базуються на огляді літератури. Основними цілями терапії є підтримка внутрішньочерепного тиску (ВЧТ) нижче за 22 мм рт.ст. і підтримання систолічного артеріального тиску на певних рівнях для різного віку. Згідно з цими рекомендаціями, основним цільовим рівнем церебрального перфузійного тиску має бути 60–70 мм рт.ст. Це змінило підхід до лікування ТУГМ, лікарі відмовилися від концепції Лунда, яка включала, серед іншого, альбумін і переливання крові. Найновіший підхід було представлено Міжнародною консенсусною конференцією з тяжкої черепно-мозкової травми в Сіетлі (SIBICC), у ньому використовувався метод Дельфі. Група експертів з усього світу відповідала на питання щодо терапевтичного й діагностичного консенсусу щодо лікування і моніторингу ТУГМ. На основі їхніх думок були запропоновані алгоритми, у яких відповідне лікування залежить від результатів моніторингу. Незважаючи на те, що за останні 30 років результати лікування поліпшилися, смертність серед пацієнтів з ТУГМ у всьому світі все ще залишається високою. У діагностиці й лікуванні ТУГМ головний акцент зараз робиться на обмеженні пошкоджень, пов’язаних із вторинною травмою. На сьогодні у фокусі постають діагностика й лікування вторинної ішемії, у тому числі порушення гематоенцефалічного бар’єра, набряк і, як наслідок, гіпоксія [3, 5]. Однак поки що немає консенсусу щодо прокогнітивного, нейропротекторного лікування як у плані використання цих препаратів, так і стосовно їх дозування і часу їх застосування.
Церебролізин — це низькомолекулярний нейропептидний препарат, отриманий з очищених білків головного мозку свиней, який має доведені нейропротекторні властивості in vitro та in vivo, включно з моделюванням проникності через ендотеліальну мембрану й протизапальною дією [6–8]. Fiani et al. виділив напрямки дії Церебролізину відповідно до періоду розвитку патології. Церебролізин діє як нейропротектор, впливаючи на нейрозапалення (зменшуючи кількість вільних радикалів і проапоптотичних факторів). При ТУГМ дуже важлива нейротрофічна активність, коли Церебролізин через схожість за активністю з нейротрофічними факторами (НТФ) активує шлях фосфоінозитид-кінази-3. На другому етапі основними напрямками дії Церебролізину є регенерація та нейропластичність. На цьому рівні варто звернути увагу на сигнал Sonic hedgehog (Shh), а також на комплекс Gli, який активується через Shh. Під впливом Shh Церебролізин також впливає на нейрогенез і гліогенез (особливо олігенендрогенез). У подальшому Церебролізин посилює нейропластичність шляхом збільшення синаптичної щільності та збереження нейронної комунікації [9]. Церебролізин розглядається як супутнє лікування кількох гострих і хронічних захворювань. Завдяки його здатності стимулювати нейрогенез, відновлення нейронів і нейропротекторним властивостям його призначали пацієнтам з гострою черепно-мозковою травмою (ЧМТ), інсультом, діагностованим субарахноїдальним крововиливом, а також з повільно прогресуючими нейродегенеративними захворюваннями, такими як хвороба Паркінсона, хвороба Альцгеймера або розсіяний склероз [6]. У своїй роботі Zhang et al. досліджували вплив Церебролізину на результати лікування щурів лінії Вістар. Вони дійшли висновку, що Церебролізин змінює кількість нейронів у ділянці зубчастої звивини й гіпокампу. Він також захищає цілісність основного дендриту в ділянці смугастого тіла [6]. Ці висновки підтверджують, що Церебролізин може чинити позитивний вплив на функцію пам’яті й процеси навчання, що дуже важливо в разі відновлення після ЧМТ. Церебролізин порівняно з фізіологічним розчином позитивно впливав на довготривале просторове навчання й непросторову пам’ять у щурів після експериментальної закритої легкої ЧМТ [7]. Церебролізин діє подібно до НТФ, запобігаючи розвитку гострої запальної відповіді в тканині мозку [6, 9].
Хоча вторинна травма при ТУГМ завжди призведе до нейрозапалення, тривале неконтрольоване запалення завжди призведе до втрати та дегенерації нейронів. Комплекс НТФ включає невеликі білки або пептиди, які мають щонайменше чотири групи факторів, відповідальних за імунологічний гомеостаз. Ми розрізняємо нейротрофіни, підгрупу циліарного нейротрофічного фактора, підгрупу нейротрофічного фактора, отриманого з лінії гліальних клітин, ефрини, епідермальний фактор росту та підгрупу трансформуючого фактора росту. Інший механізм нейропротекції Церебролізину включає шляхи Sonic hedgehog. Shh відіграє важливу роль у сигналізації щодо пошкодження нейронів ембріона, а також у дорослої людини. На останніх моделях ТУГМ було продемонстровано, що шлях Shh посилюється після пошкодження кори [6, 9, 10]. Церебролізин модулює експресію мРНК з метою активації самого шляху Shh, а також шляхом активації рецепторів Shh (гліогенез, нейрогенез) [9–11]. Ефектором для передачі сигналів шляху Shh є білковий комплекс Gli. Комплекс Gli бере участь не тільки в процесах розвитку, але й у нейровідновленні при патологічних станах. Діючи на нейротропні засоби, Церебролізин змінює активність ГАМКергічних і холінергічних шляхів у головному мозку. Доведено також, що Церебролізин впливає на клітини мікроглії. Ці клітини глії контролюють гомеостаз та імунологічні реакції, а Церебролізин модулює їхню функцію, щоб обмежити гостру запальну відповідь [12].
Дослідження in vivo на щурах показали зниження активації астроцитів, зменшення пошкодження аксонів і збільшення нейрогенезу при закритій експериментальній травмі головного мозку [13]. Дослідження in vivo з пацієнтами також показали його сприятливу роль у сповільненні активності ЕЕГ і поліпшенні реабілітації та результатів з точки зору когнітивної діяльності [14, 15].
Відповідно до рекомендацій Церебролізин можна застосовувати в різних дозах від 10 до 50 мл на добу. Для внутрішньовенної інфузії необхідно приготувати загальний об’єм 100 мл, додавши Церебролізин до 0,9% фізіологічного розчину, або розчину Рінгера, або 5% розчину глюкози. Тривалість інфузії повинна становити не менше за 15 хв. Час введення є вирішальним, особливо в умовах ТУГМ. У дослідженнях на тваринах було показано, що раннє введення Церебролізину асоціюється з кращими результатами щодо сенсорно-моторних функцій, набряку мозку і проникнення через гематоенцефалічний бар’єр [16].
Протипоказаннями до застосування Церебролізину є: алергія, судоми, тяжка ниркова недостатність.
Нещодавно польськими авторами (Konrad Jarosz і співавт.) був проведений систематичний огляд і метааналіз застосування Церебролізину в пацієнтів із травматичним ушкодженням головного мозку з метою аналізу клінічного ефекту Церебролізину щодо впливу на смертність, показники за шкалою результатів Глазго (GOS), показники за шкалою коми Глазго (GCS) і тривалість перебування в лікарні (ТПЛ) у пацієнтів після ТУГМ. Нижче подані основні моменти даної роботи.
Матеріали та методи
Пошук проводився в базах даних Pub Med, Cinahl, Web of Science та Embase. Відбиралися статті, датовані з моменту створення бази даних до 11 липня 2022 року, написані англійською мовою, які являють собою результати досліджень, спрямованих на оцінку ефективності Церебролізину в лікуванні пацієнтів з ТУГМ. Електронний пошук був доповнений ручним переглядом списків літератури з відповідних публікацій і відповідних оглядів.
Були застосовані такі критерії включення: дослідження на людях, вік пацієнтів понад 18 років, ТУГМ легкого, середнього або тяжкого ступеня (травма голови, черепно-мозкова травма).
Критерії виключення: дослідження на тваринах, дослідження in vitro, огляди, систематичні огляди, редакційні статті, звіти про окремі випадки, а також думки, редакційні чи перспективні статті, пацієнти, молодші за 18 років, вагітні пацієнтки, поліорганна недостатність, статті іншою мовою, окрім англійської, наявність тільки резюме. Супутніми первинними результатами були GOS і GCS, а також смертність і ТПЛ — усі вони відображали ефективність препарату в пацієнтів, госпіталізованих з приводу ТУГМ.
Результати
У результаті проведеного пошуку літературних джерел для метааналізу було відібрано 10 досліджень (табл.1), які відповідали вимогам пошуку і були включені в остаточний аналіз, включно з ретроспективними та проспективними дослідженнями 8749 пацієнтів.
У всіх дослідженнях пацієнтам внутрішньовенно вводили Церебролізин у дозі 10 мл/добу (Khalil et al., Ashgari et al.), 20 мл/добу (Muresanu et al., 2015), 50 мл/добу (Poon et al., Wong et al., Muresanu et al., 2020) внутрішньовенно, а найпоширенішою дозою була доза 30 мл/добу (Alvarez et al., 2003, 2008, Chen et al., Lucena et al., Muresanu et al., 2015). Тривалість лікування становила від 5 днів (Chen et al.), 10 днів (Muresanu et al., 2015), 20 днів (Poon et al., Wong et al., Muresanu et al., 2020) до 20–30 днів (Alvarez et al., 2003, Alvarez et al., 2008; Lucena et al., Khalil et al.). Загальна тривалість досліджень дорівнювала 6 місяцям.
Лише в кількох пацієнтів спостерігалися судоми під час перебування в лікарні (дослідження Alvarez etal., Chen et al., Khalil et al.) [20, 24, 25]. Вік пацієнтів коливався від 30,1 до 64 років. У всіх проаналізованих дослідженнях відсоток чоловіків був вищим, ніж відсоток жінок.
Обговорення та висновки
У метааналізі було порівняно результати лікування Церебролізином у пацієнтів з ТУГМ у клінічних дослідженнях, наведених в базах даних Pub Med, Cinahl, Web of Science та Embase від початку створення відповідної бази даних до 11 липня 2022 року. Було відібрано як проспективні рандомізовані дослідження [15, 25, 27], так і спостереження або історичні когорти [20–23, 26]. У більшості проаналізованих досліджень автори вказують на неоднорідність груп і відсутність консенсусу щодо дози препарату й тривалості його застосування [15, 27]. Більшість досліджень довели, що Церебролізин дає позитивний лікувальний ефект у пацієнтів з ТУГМ щодо когнітивних функцій, GOS і GCS, але не змінює рівень смертності або ТПЛ [21, 22, 28, 29]. Обмеження даного метааналізу включають відсутність великих рандомізованих досліджень, різні дози препарату, що вводяться в різний час після первинної травми, неоднорідну групу респондентів і неоднорідні результати. Тому не було можливості порівняти всі згадані публікації в усіх запланованих аспектах.
За ступенем тяжкості ураження мозку у більшості хворих діагностовано ТУГМ середнього і тяжкого ступеня. Призначена доза Церебролізину коливалася від 10 мл у дослідженні Ashgari et al. до 50 мл у дослідженнях Muresanu et al. (2020) і Poon et al. [15, 21, 27]. Час до початку лікування Церебролізином варіював від 24 годин до понад 20 місяців.
Позитивний ефект Церебролізину був доведений invitro (зниження активності мікроглії, ексайтотоксичності, продукції вільних радикалів, підвищення виживаності нейронів), а також був продемонстрований invivo в дослідженнях на тваринах [7, 16, 33, 34] і в клінічних дослідженнях [15, 20–28]. Зокрема, заслуговує на увагу роль моделювання імунної відповіді. Діючи через нейротрофічні фактори, а також впливаючи на активність ГАМКергічних і холінергічних шляхів, Церебролізин впливає на реакцію, яка розвивається у відповідь на первинне пошкодження, а також впливає на вторинне пошкодження в ушкодженому мозку. Варто відзначити, що Церебролізин завдяки своїм нейропротекторним властивостям купірує патологічні процеси на всіх етапах після початкової травми. Це може бути корисним для початку лікування на кожному етапі після ТУГМ — у перші 24 години, а також через 20 місяців після травми. Автори Sharma, Zhang і Chopp дійшли висновку, що ефективність лікування Церебролізином залежить від дози та часу в дослідженнях на тваринах і розумно припустити, що клінічний ефект у дослідженнях на людях також залежатиме від дози й часу введення препарату [7, 16]. Слід зазначити, що позитивні ефекти лікування Церебролізином при ТУГМ також очевидні в умовах реабілітації після відстроченого введення Церебролізину через тривалий час після травми [23, 24].
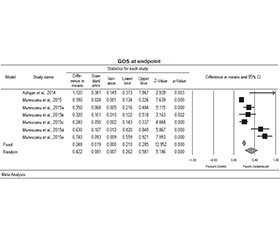
У роботі Muresanu et al. (2015) показано, що Церебролізин у дозах 20 мг/день, а також 30 мг/день поліпшує показники за GOS і RDS (модифікована шкала інвалідності Ранкіна) у пацієнтів з ТУГМ середнього і тяжкого ступеня через 10 і 30 днів після травми [22]. Результати дослідження Alvarez et al. (2003; 2008) вказують на те, що Церебролізин може сприяти ефекту ЕЕГ-активації в підгострому періоді після травми в пацієнтів із ТУГМ середнього і тяжкого ступеня [23, 24]. Chen et al. (2013) продемонстрували, що Церебролізин поліпшує оцінку за інструментом скринінгу когнітивних здібностей (CASI) у пацієнтів з ТУГМ легкого ступеня [25]. Khalil et al. (2017) відзначили, що лікування Церебролізином у пацієнтів із ТУГМ тяжкого ступеня пов’язане зі збільшенням балів за розширеною шкалою результатів Глазго (GOSE) і зниженням смертності [20]. Lucena et al. (2022) у своїй роботі з пацієнтами з ТУГМ тяжкого ступеня підтвердили, що Церебролізин має сприятливий вплив на результати за GCS, GOS, а також на ТПЛ [26]. Ashgari et al. (2014) показали, що результати за GCS були вірогідно вищими в групах лікування порівняно з контролем [21]. Дослідження CAPTAIN I і II, як це показано Poon et al. (2019) і Muresanu et al. (2020), продемонстрували когнітивне поліпшення в пацієнтів (тест Струпа і тест кольорових слідів) у разі додаткового лікування Церебролізином [15, 27].
/15.jpg)
На даний момент опубліковано декілька статей, що підсумовують ефекти Церебролізину та інших нейропротекторних препаратів [29, 35, 36]. Один метааналіз використання Церебролізину при ТУГМ проведений Ghaffarpasand et al. у 2018 р. [28], куди автори включили дослідження Wong et al. (2005), Alvarez et al. (2008), Ashgari et al. (2014), Muresanu et al. (2015) і Khalil et al. (2017). Основний висновок Ghaffarpasand et al. полягав у тому, що призначення Церебролізину при ТУГМ поліпшувало показники за mRS і GOS.
Метааналіз, зроблений авторами статті, яка є предметом даного огляду, підтвердив поліпшення показників за GCS у пацієнтів з ТУГМ при лікуванні Церебролізином. Це зазначено в дослідженнях Alvarez et al. (2003), Chen et al. (2012), Poon et al. (2019), Muresanu et al. (2020) і Lucena et al. (2022).
У базовому лікуванні ТУГМ ми, як правило, дотримувалися алгоритмів Traumatic Brain Foundation [3]. У випадку пацієнтів із моніторингом ВЧТ ми також можемо слідувати SIBICC або іншим алгоритмам, коли ми не маємо можливості оцінити ВЧТ прямим, інвазивним способом (у тому числі за алгоритмами залежно від змін на комп’ютерній томограмі) [3–5]. Також варто звернути увагу на алгоритми, створені на основі консенсусу груп експертів, наприклад SIBICC або Рекомендації 2023 року з когнітивної реабілітації після черепно-мозкової травми, у яких Церебролізин згадується як препарат, який варто призначати для лікування ЧМТ [5, 37]. Рекомендації INCOG подають консенсус, досягнутий групою експертів на основі публікацій, що датовані 2014 роком. Він включає фармакологічні й нефармакологічні стратегії для поліпшення уваги після ТУГМ помірного і тяжкого ступеня. Оскільки період після ТУГМ пов’язаний з розладами нейромедіаторів, що впливають на когнітивні здібності й увагу, у цій статті, серед інших, пропонуються фармакологічні речовини, які позитивно впливають на поліпшення уваги. На думку авторів, Церебролізин є одним із препаратів, які можуть бути використані з потенційною користю для цієї групи пацієнтів. Проте автори зазначають, що в даний час бракує ширших доказів, які були б отримані з досліджень [37].
Проведений метааналіз підтверджує позитивний ефект лікування Церебролізином на клінічні результати за аспектами GCS та GOS у пацієнтів з ТУГМ. Авторам не вдалося встановити вірогідний вплив на смертність або ТПЛ, можливо, також через відносно невеликий розмір вибірки. Тому необхідні додаткові рандомізовані дослідження використання Церебролізину при ТУГМ, щоб підтвердити й розширити висновки щодо клінічної користі Церебролізину при ТУГМ.
Також у дослідженнях Alvarez et al. (2003) і Poon et al. (2020) було отримано докази рівня 1b про те, що Церебролізин є ефективним засобом, який може поліпшити увагу в осіб із ТУГМ помірного і тяжкого ступеня. За даними Alvarez et al. (2003), Церебролізин поліпшив біоелектричну активність мозку, на що вказує значне підвищення швидких бета-частот. Оцінка загального нейро-психологічного стану (тест SKT), що включає 9 субтестів, була проведена для оцінки пам’яті й уваги в пацієнтів, які отримували Церебролізин. Спостерігалося вірогідне поліпшення загального стану після лікування, що вказує на когнітивні переваги Церебролізину. Результати дослідження Poon et al. (2020) показали актуальність комбінованого лікування з використанням Церебролізину в осіб з ТУГМ завдяки плейотропним нейропротективним ефектам і посиленню нейрорегенерації. У нещодавньому метааналізі (Vester et al., 2021) також було підтверджено, що Церебролізин є безпечним та ефективним препаратом для лікування осіб із ТУГМ помірного і тяжкого ступеня.
Підготовлено за матеріалами статті
Konrad Jarosz та співавт. Cerebrolysin in Patients
with TBI: Systematic Review and Meta-Analysis, 2023.
https://doi.org/10.3390/brainsci13030507
Оригінал статті надруковано в
Brain Sci. 2023. 13. 507
Список литературы
1. Jiang J.-Y., Gao G.-Y., Feng J.-F., Mao Q., Chen L.-G., Yang X.-F. et al. Traumatic brain injury in China. Lancet Neurol. 2019. 18,.286-295.
2. Majdan M., Plancikova D., Brazinova A., Rusnak M., Nieboer D., Feigin V., Maas A. Epidemiology of traumatic brain injuries in Europe: A cross-sectional analysis. Lancet Public Health. 2016. 1. e76-e83.
3. Carney N., Totten A.M., O-Reilly C., Ullman J.S., Hawryluk G.W.J., Bell M.J. et al. Guidelines for the Management of Severe Traumatic Brain Injury. Fourth Edition. Neurosurgery. 2016. 1. 1-10.
4. Gerber L.M., Chiu Y., Carney N., Hartl R., Ghajar J. Marked reduction in mortality in patients with severe traumatic brain injury. J. Neurosurg. 2013. 119. 1583-1590.
5. Hawryluk G.W.J., Aguilera S., Buki A., Bulger E., Citero G., Cooper D.J. et al. A management algorithm for patients with intracranial pressure monitoring: The Seattle International Severe Traumatic Brain Injury Consensus Conference (SIBICC). Intensive Care Med. 2019. 45. 1783-1794.
6. Zhang Y., Chopp M., Meng Y., Zhang Z.G., Doppler E., Mahmood A., Xiong Y. Improvement in functional recovery with administration of Cerebrolysin after experimental closed head injury. J. Neurosurg. 2013. 118. 1343-1355.
7. Zhang Y., Chopp M., Meng Y., Zhang Z.G., Doppler E., Winter S. et al. Cerebrolysin improves cognitive performance in rats after mild traumatic brain injury. J. Neurosurg. 2015. 122. 843-855.
8. Shmakova A.A., Androsova L.W. Investigating the effect of central nervous system drugs on leukocyte elastase activity in vitro. Eur. Neuropsychopharmacol. 2018. 28. 13-14.
9. Fiani B., Covarrubias C., Wong A., Doan T., Reardon T., Nikolaidis D., Sarno E. Cerebrolysin for stroke, neurodegeneration, and traumatic brain injury: Review of the literature and outcomes. Neurol. Sci. 2021. 42. 1345-1353.
10. Chen S.-D., Yang J.-L., Hwang W.-C., Yang D.-I. Emerging roles of sonic hedgehog in adult neurological diseases: Neurogenesis and beyond. Int. J. Mol. Sci. 2018. 19. 2423.
11. Lai K., Kaspar B.K., Gage F.H., Schaffer D.V. Sonic hedgehog regulates adult neural progenitor proliferation in vitro and in vivo. Nat. Neurosci. 2003. 6. 21-27.
12. Masliah E., Diez-Tejedor E. The pharmacology of neurotro-phic treatment with Cerebrolysin: Brain protection and repair to counteract pathologies of acute and chronic neurological disorders. Drugs Today. 2012. 48. 3-24.
13. Zhang Y., Chopp M. Cerebrolysin reduces astrogliosis and –axonal injury and enhances neurogenesis in rats after closed head injury. Neurorehabil. Neural Repair. 2019. 33. 15-26.
14. Wong G.K.C., Zhu X.L., Poon W.S. Beneficial effect of cerebrolysin on moderate and severe head injury patients: Result of a cohort study. In Intracranial Pressure and Brain Monitoring XII; Springer: Vienna, Austria. 2005. Vol. 95.
15. Muresanu D.F., Florian S., Homberg V., Matula C., Von Steinbuchel N., Vos P.E. et al. Efficacy and safety of cerebrolysin in neurorecovery after moderate-severe traumatic brain injury: Results from the CAPTAIN II trial. Neurol. Sci. 2020. 41. 1171-1181.
16. Sharma H.S., Zimmermann-Meinzingen S., Johanson C.E. Cerebrolysin reduces blood-cerebrospinal fluid barrier permeability change, brain pathology, and functional deficits following traumatic brain injury in the rat. Ann. N. Y. Acad. Sci. 2010. 1199. 125-137.
17. DerSimonian R., Laird N. Meta-analysis in clinical trials. Control Clin. Trials 1986. 7. 177-188.
18. Egger M., Davey Smith G., Chneider M., Minder C. Bias in meta-analysis detected by a simple, graphical test. BMJ. 1997. 315. 629-634.
19. Duval S., Tweedie R.A. Nonparametric “Trim and Fill” Me-thod of Accounting for Publication Bias in Meta-Analysis. J. Am. Stat. Assoc. 2000. 95. 89-98.
20. Khalili H., Niakan A., Ghaffarpasand F. Effects of cerebrolysin on functional recovery in patients with severe disability after traumatic brain injury: A historical cohort study. Clin. Neurol. Neurosurg. 2017. 152. 34-38.
21. Asghari M., Meshkini A., Salehpoor F., Aghazadek J., Sha-keri M., Shokohi G. et al. Investigation of the effect of cerebrolysin on patients with head trauma and diffuse axonal injury. Int. J. Curr. Res. Acad. Rev. 2014. 2. 1-8.
22. Muresanu D.F., Ciurea A.V., Gorgan R.M., Gheoghita E., Florian S., Stan H. et al. A retrospective, multi-center cohort study evaluating the severity-related effects of cerebrolysin treatment on clinical outcomes in traumatic brain injury. CNS Neurol. Disord. Drug Targets. 2015. 14. 587-599.
23. Alvarez X.A., Sampedro C., Figueroa J., Tellado I., Gonzalez A., Garcia-Fantini M. et al. Reductions in qEEG slowing over 1 year and after treatment with Cerebrolysin in patients with moderate-severe traumatic brain injury. J. Neural Transm. 2008. 115. 683-692.
24. Alvarez X.A., Sampedro C., Perez P., Laredo M., Couceiro V., Hernandez A. et al. Positive effects of Cerebrolysin on electroencephalogram slowing, cognition and clinical outcome in patients with postacute traumatic brain injury: An exploratory study. Int. Clin. Psychopharmacol. 2003. 18. 271-278.
25. Chen C.C., Wei S.-T., Tsaia S.-C., Chen X.-X., Cho D.-Y. Cerebrolysin enhances cognitive recovery of mild traumatic brain injury patients: Double-blind, placebo-controlled, randomized study. Br. J. Neurosurg. 2013. 27. 803-807.
26. Lucena L.L., Briones M.V.A. Effect of Cerebrolysin in severe traumatic brain injury: A multi-center, retrospective cohort study. Clin. Neurol. Neurosurg. 2022. 216. 107216.
27. Poon W., Matula C., Vos P.E., Muresanu D.F., Steinbuchel N., Wild K., Homberg V., Wang E., Lee T.M.C., Strilciuc S. et al. Safety and efficacy of Cerebrolysin in acute brain injury and neurorecovery: CAPTAIN I — A randomized, placebo-controlled, double-blind, Asian-Pacific trial. Neurol. Sci. 2020. 41. 281-293.
28. Ghaffarpasand F., Torabi S., Rasti A., Niakanm M.H., Aghakablou A., Pakzad F., Beheshtian M.S., Tabrizi R. Effects of cerebrolysin on functional outcome of patients with traumatic brain injury: A systematic review and meta-analysis. Neuropsychiatr. Dis. Treat. 2018. 15. 127-135.
29. El Sayed I., Zaki A., Fayed A.M., Shehat G.M., Abdelmonem S. A meta-analysis of the effect of different neuroprotective drugs in management of patients with traumatic brain injury. Neurosurg. Rev. 2018. 41. 427-438.
30. Shin D.-S., Hwang S.-C. Serial Brain CT Scans in Severe Head Injury without Intracranial Pressure Monitoring. KJNT. 2014. 10. 26-30.
31. Brazinova A., Rehorcikova V., Taylor M.S., Buckova V., Majdan M., Psota M. et al. Epidemiology of Traumatic Brain Injury in Europe: A Living Systematic Review. J. Neurotrauma. 2021. 38. 1411-1440.
32. Feng J., van Veen E., Yang C., Huijben J.A., Lingsma H.F., Gao G., Jiang J. Comparison of care system and treatment approaches for patients with traumatic brain injury in China versus Europe: A CENTER-TBI survey study. J. Neurotrauma. 2020. 37. 1806-1817.
33. Muresanu D., Birle C., Muresanu I., Costin C., Vester J., Rafila A. Neuroprotection in TBI. In Neurotrauma: A Comprehensive Textbook on Traumatic Brain Injury and Spinal Cord Injury; Wang K.K.W., Ed.; Oxford University Press: New York, NY, USA, 2018. Р. 333-346.
34. Sharma H.S., Muresanu D.F., Sahib S., Tian Z.R., Lafuente J.V., Buzoianu A.D. et al. Cerebrolysin restores balance between excitatory and inhibitory amino acids in brain following concussive head injury. Superior neuroprotective effects of TiO2 nanowired drug delivery. Prog. Brain Res. 2021. 266. 211-267.
35. Wheaton P., Mathias J.L., Vink R. Impact of pharmacological treatments on cognitive and behavioral outcome in the postacute stages of adult traumatic brain injury: A meta-analysis. J. Clin. Psychopharmacol. 2011. 31. 745-757.
36. Vester J.C., Buzoianu A.D., Florian S.I., Homberg V., Kim S.-H., Lee T.M.C. et al. Cerebrolysin after moderate to severe traumatic brain injury: Prospective meta-analysis of the CAPTAIN trial series. Neurol. Sci. 2021. 42. 4531-4541.
37. Bayley M., Ponsford J., Jeffay E., Ponsford J., Harnett A., Janzen S. et al. INCOG 2.0 Guidelines for Cognitive Rehabilitation Following Traumatic Brain Injury, Part III: Executive Functions. J. Head Trauma Rehabil. 2023. 38. 52-64.

/14.jpg)
/15.jpg)