Артеріальна гіпертензія (АГ) є одним з основних факторів ризику розвитку серцево-судинних захворювань і однією з основних причин смертності у світі. Незважаючи на суттєві досягнення фармакології, відкриття нових лікарських засобів і нових класів препаратів, розробку національних рекомендацій, клінічних протоколів і стандартів, кількість пацієнтів, які страждають від АГ і гинуть від її ускладнень, продовжує зростати, що обумовлено недостатнім контролем артеріального тиску (АТ) [1]. Великі рандомізовані клінічні дослідження, у яких оцінювалась ефективність того чи іншого режиму антигіпертензивної терапії у хворих на АГ, переконливо продемонстрували, що у 18–55 % учасників досягти цільових значень АТ не вдається, незважаючи на прийом трьох і більше антигіпертензивних препаратів (АГП) [2–4].
Дефініція, поширеність та причини розвитку резистентної артеріальної гіпертензії (РАГ)
Згідно з рекомендаціями Європейського товариства з артеріальної гіпертензії (ЕSН-2023), схваленими Європейською асоціацією захворювань нирок (ERA) та Міжнародним товариством артеріальної гіпертензії (ІSH), резистентна АГ визначається як недосягнення цільових цифр артеріального тиску (< 140/90 мм рт.ст.) при зміні способу життя й одночасному використанні оптимальних доз 3 антигіпертензивних препаратів різних класів, включно з діуретиком, у пацієнтів, прихильних до терапії [5].
За даними реєстру NHANES (США), поширеність резистентної АГ протягом останніх 30 років постійно збільшується і в середньому становить 8,9 %. Статистика Франції, Німеччини, Великобританії й Іспанії демонструє більшу поширеність резистентності до лікування — від 14,6 до 17,5 % [6, 7]. За даними ESН [5], РАГ зустрічається більше ніж у 5 % випадків.
Причинами резистентної гіпертензії є швидке збільшення ваги, надмірне вживання алкоголю або солі. Також до факторів, що сприяють розвитку РАГ, належить прийом НПЗП, оральних контрацептивів, симпатоміметиків, циклоспорину, еритропоетину, стероїдів, наркотичних препаратів (кокаїн, амфетаміни, анаболічні стероїди), деяких рослинних засобів (ефедра, ма-хуанг) [5].
Резистентна АГ асоціюється з літнім віком (особливо часто виникає у пацієнтів > 75 років), чоловічою статтю, негроїдною расою, більш високими вихідними значеннями АТ, дуже високими показниками максимального АТ, частими амбулаторними візитами до лікаря, ожирінням, цукровим діабетом, атеросклерозом, ураженням органів-мішеней, опосередкованих гіпертензією, хронічною хворобою нирок (ХХН) і 10-річним коронарним ризиком за Фремінгемською шкалою > 20 % [5].
Діагностика резистентної артеріальної гіпертензії
Діагностика резистентної гіпертензії повинна починатися з ідентифікації псевдорезистентної АГ. Цей стан часто помилково приймається за резистентну гіпертензію, визначається як стійке збільшення рівнів АТ вище від нормальних значень при вимірюванні в лікувальному закладі у пацієнта, який не має резистентної гіпертензії. Сприяти підтримці підвищеного артеріального тиску та створювати картину резистентної АГ можуть безліч факторів, розпізнавання і усунення яких, у свою чергу, може привести до нормалізації рівнів артеріального тиску й, отже, виключення діагнозу резистентної гіпертензії.
У порядку звичайної діагностичної послідовності ці стани включають: низьку прихильність до призначеної терапії, феномен «білого халата», порушення правил вимірювання офісного АТ, виражений кальциноз плечової артерії та клінічну інертність.
Низька прихильність до призначеної терапії є частою причиною псевдорезистентності, яка виявляється у ≤ 50 % пацієнтів, яких обстежили за допомогою методів моніторування прийому препаратів. Причому цей показник прямо залежить від кількості призначених пігулок [5]. Феномен «білого халата» визначається підвищенням рівня АТ вище від цільових значень при вимірюванні в медичному закладі та визначенні АТ на рівні або нижче від цільових значень за даними добового моніторування артеріального тиску (ДМАТ) (переважно) або самоконтролю. Це обумовлено активацією симпатичної нервової системи при виникненні тривоги, пов’язаної з відвідуванням медичного закладу [10].
Частими помилками можна вважати одноразове (замість 2–3-кратних) вимірювання АТ, використання манжети недостатнього розміру, недотримання хворим умов перебування у спокої протягом декількох хвилин, куріння перед вимірюванням АТ, розташування манжети вище або нижче від рівня серця [8, 9].
Іноді причиною псевдорезистентної АГ може бути кальциноз плечової артерії у пацієнтів похилого віку з вираженим кальцинозом судин або клінічна інертність — призначення препаратів у неадекватних дозах або нераціональних комбінацій антигіпертензивних препаратів.
Наступним діагностичним кроком є виключення вторинної гіпертензії. У великих спостережних дослідженнях найпоширенішими причинами порушення або недостатньої реакції на комбіновану антигіпертензивну терапію були хвороби паренхіми нирок, хвороби ниркових артерій та гіперальдостеронізм [26].
Наявність первинного гіперальдостеронізму слід завжди виключати у пацієнтів з тяжкими формами АГ. У дослідженні Veglio та ін. (2001) за участю понад 1500 пацієнтів з резистентною гіпертензією було встановлено, що у 11,3 % цих хворих насправді мав місце первинний гіперальдостеронізм. В інших дослідженнях це захворювання становило до 20 % випадків резистентної гіпертензії. Необхідно відзначити, що ця популяція складалася переважно з хворих на АГ з рівнями АТ > 140/90 мм рт.ст. на тлі прийому трьох антигіпертензивних препаратів, включно з діуретиком.
Недостатній сон і синдром нічного апное також були ідентифіковані як потенційні причини помірно-тяжких форм АГ, зокрема маскованої гіпертензії (наприклад, підвищені рівні АТ вдома і нормальні — у кабінеті лікаря) та резистентна гіпертензія [26].
Після виключення псевдорезистентної та вторинної АГ необхідно підтвердити діагноз РАГ. Він вимагає наступної детальної інформації [5]:
— анамнез пацієнта, включно з особливостями ожиріння, кількістю вживаного алкоголю й натрію, прийомом лікарських препаратів чи інших субстанцій, станом сну;
— характер антигіпертензивної терапії та дози препаратів;
— фізикальний огляд, особлива увага повинна приділятися виявленню уражень органів-мішеней, опосередкованих гіпертензією, та ознакам вторинної АГ;
— підтвердження резистентності до лікування за допомогою оцінки позаофісного АТ (ДМАТ);
— лабораторне обстеження для виявлення електролітних порушень (гіпокаліємії), асоційованих факторів ризику (діабет), ураження органів (виражена дисфункція нирок) і ознак вторинної АГ;
— підтвердження прихильності до антигіпертензивної терапії.
Сучасні рекомендації ESН-2023 щодо лікування резистентної АГ [5]
Основною метою лікування АГ є досягнення цільових значень амбулаторного АТ. У більшості пацієнтів віком від 18 до 64 років цей показник становить < 130/80 мм рт.ст., в осіб віком від 65 до 79 років — < 140/80 мм рт.ст. (зниження рівня АТ < 130/80 мм рт.ст. у цій віковій групі можливе тільки за доброї переносимості лікування). У віковій групі від 80 років рекомендовано знизити АТ до рівня САТ 140–150/ДАТ < 80 мм рт.ст. (зниження амбулаторного САТ до рівня 130–139 мм рт.ст., ДАТ < 70 мм рт.ст. — тільки за доброї переносимості). У пацієнтів зі старечою астенією цільові цифри АТ повинні бути індивідуальними, не слід прагнути до зниження амбулаторного АТ нижче від рівня 120/70 мм рт.ст. [5].
У контексті найбільш ефективної доказової стратегії лікування для поліпшення контролю АТ ESH-2023, як і раніше, рекомендує стартову комбіновану терапію у більшості пацієнтів з АГ, що покращує довгострокову прихильність до лікування [11], супроводжується ліпшим контролем АТ [12], знижує частоту несприятливих наслідків [13–15], дозволяє досягти цільового рівня АТ.
Для лікування АГ актуальне призначення 5 основних класів лікарських засобів, включно з інгібіторами ангіотензинперетворювального ферменту (ІАПФ), блокаторами рецепторів ангіотензину II (БРА), β-адреноблокаторами, антагоністами кальцію і тіазидними/тіазидоподібними діуретиками.
Першим кроком у лікуванні АГ є призначення подвійної комбінації антигіпертензивних препаратів — ІАПФ або БРА + блокатор кальцієвих каналів (БКК) або діуретик. Монотерапія може бути застосована у хворих низького кардіоваскулярного ризику, при 1-му ступені АГ або в осіб дуже похилого віку (> 80) і слабких пацієнтів.
Коли не вдається контролювати АТ, другим кроком є застосування потрійної комбінації — ІАПФ або БРА + БКК або діуретик, краще в одній таблетці. При неможливості контролю АТ потрійною комбінацією (третій крок) АГ вважається резистентною, що диктує необхідність підвищення дози вже призначеного діуретика або його заміни на потужніший тіазидоподібний препарат (хлорталідон або індапамід). Петльовий діуретик має бути призначений замість тіазидного/тіазидоподібного препарату, якщо швидкість клубочкової фільтрації (ШКФ) < 30 мл/хв. Хоча зазвичай АТ знижується у хворих на резистентну АГ при збільшенні дози діуретиків, більшості пацієнтів потрібне призначення додаткових препаратів.
Усе більше даних свідчать про те, що терапія четвертої лінії повинна додавати четвертий препарат, який буде здійснювати блокаду біологічних ефектів альдостерону. Це відбувається за рахунок призначення антагоністів мінералокортикоїдних рецепторів (АМР), найчастіше спіронолактону в дозі 25–50 мг/добу. Однак не всі пацієнти добре переносять терапію спіронолактоном унаслідок побічних ефектів, обумовлених антиандрогеновою дією, що призводять до ущільнення молочних залоз або гінекомастії (~ 6 %), імпотенції у чоловіків і порушень менструального циклу в жінок. Крім того, ефективність і безпека спіронолактону для лікування резистентної АГ не підтверджені для пацієнтів зі значущим порушенням функції нирок. Відповідно, призначення спіронолактону з приводу резистентної АГ необхідно обмежити хворим зі швидкістю клубочкової фільтрації ≥ 45 мл/хв і концентрацією калію у плазмі ≤ 4,5 ммоль/л. Навіть більше, рівень електролітів і ШКФ необхідно контролювати незабаром після початку лікування та не рідше ніж 1 раз на рік надалі.
За поганої переносимості спіронолактону, а також при ХХН I–III стадії та ШКФ ≥ 30 мл/хв на 1,73 м2 експерти ESH-2023 рекомендують розглянути призначення β-адреноблокаторів, або блокаторів α1-адрено-рецепторів, або препаратів центральної дії (II, В) [5].
За відсутності контролю АТ можливе проведення ренальної денервації як варіант лікування у пацієнтів зі ШКФ > 40 мл/хв на 1,73 м2 при неконтрольованому АТ, незважаючи на використання комбінованої антигіпертензивної терапії або в разі, якщо медикаментозне лікування викликає серйозні небажані явища та погіршує якість життя (II, В) [5].
Еферентні симпатичні волокна, що іннервують нирки, збільшують вивільнення реніну через β1-адрено-рецептори, а посилена сигналізація аферентних чутливих нервів у відповідь на ішемію нирок, травму або запальні процеси призводить до рефлекторної симпатичної активації з периферичною вазоконстрикцією та підвищенням АТ [30]. Сенс ренальної денервації полягає у зниженні надмірної активації симпатичної нервової системи за рахунок радіочастотного впливу на симпатичні закінчення нервових волокон нирок [31]. Ренальна денервація являє собою один із варіантів додаткового лікування, що проводиться в умовах спеціалізованих центрів [32].
Можливості антагоністів α1-адренорецепторів для лікування резистентної АГ: у фокусі урапідил (Ебрантил, «Асіно») з двома механізмами дії
У низці досліджень було показано, що призначення антагоністів α1-адренорецепторів (α-блокаторів) або препаратів центральної дії як додаткової терапії призводило до ефективного зниження АТ у пацієнтів з резистентною гіпертензією [10, 11]. Крім впливу на АТ, антагоністи α1-адренорецепторів мають й інші позитивні ефекти: поліпшують ліпідний профіль і метаболізм глюкози, зменшують симптоми доброякісної гіперплазії простати (ДГП) [11], що може відігравати важливу роль для пацієнтів з резистентною АГ та супутніми захворюваннями.
Серед усіх препаратів — антагоністів α1-адрено-рецепторів особливу увагу привертає урапідил (Ебрантил, «Асіно»), який має подвійний механізм дії: чинить α-блокувальну та центральну гіпотензивну дію.
Основний антигіпертензивний ефект препарату обумовлений селективною блокадою постсинаптичних α1-адренорецепторів, завдяки чому шляхом зниження загального периферичного судинного опору (ЗПСО) знижуються систолічний та діастолічний АТ, перед- і постнавантаження на серце [26]. У печінці блокада рецепторів цього типу гальмує гліконеогенез, активує ліпопротеїнліпази, що створюють додаткові сприятливі метаболічні ефекти — знижується рівень атерогенних ліпідів крові, поліпшується метаболізм глюкози й уродинаміка при ДГП.
Крім того, урапідил є агоністом рецепторів 1-го типу 5НТ-1А, розташованих у хемочутливій зоні довгастого мозку [22]. У результаті його впливу на цю зону знижується активність прегангліонарних симпатичних нейронів, внаслідок чого, незважаючи на виражену судинорозширювальну дію, антигіпертензивний ефект урапідилу не супроводжується підвищенням частоти серцевих скорочень.
Це було підтверджено у мультицентровому дослідженні за участю 206 пацієнтів з резистентною АГ, які приймали урапідил у дозі 30, 60 або 90 мг двічі на добу протягом трьох років [16]. У перший рік систолічний артеріальний тиск знизився на 25 мм рт.ст.: зі 174 ± 13 до 149 ± 10 мм рт.ст., а діастолічний тиск — на 17 мм рт.ст.: зі 103 ± 6 до 86 ± 6 мм рт.ст. При одній і тій же середній дозі це зниження артеріального тиску зберігалося на другий рік: 150 ± 12/86 ± 7 мм рт.ст.; на третій рік: 146 ± 10/85 ± 7 мм рт.ст., що свідчить про відсутність зниження ефекту урапідилу та феномену звикання (рис. 1).
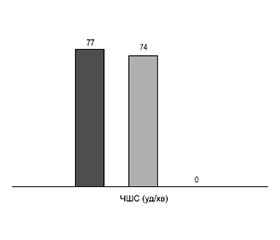
Частота шлуночкових скорочень зменшилася з 77 ± 8 до 74 ± 6 уд/хв і залишалася практично постійною протягом наступних 2 років (рис. 2).
При цьому відмічалася добра переносимість препарату, тільки у 2 % випадків спостерігалися побічні ефекти: у 2 пацієнтів — недостатня відповідь на лікування, ще у 2 — нудота, запаморочення, сонливість і втома [16].
Клінічно доведено, що центральні ефекти урапідилу дозволяють уникнути небажаних побічних явищ, характерних для інших α-адреноблокаторів, — тахікардії й ортостатичної гіпотензії [21]. У рандомізованому подвійному сліпому плацебо-контрольованому дослідженні, яке включало 12 здорових добровольців, порівнювали дію урапідилу і доксазозину на частоту шлуночкових скорочень (ЧШС) у спокої та при фізичному навантаженні й рівень АТ. Урапідил призначався в дозі 60 мг, доксазозин — 4 мг.
Результати дослідження продемонстрували, що доксазозин, але не урапідил (Ебрантил) (p < 0,05) вірогідно збільшував частоту серцевих скорочень у спокої (25 та 12 % відповідно), хоча обидва препарати мали однакову ефективність щодо зниження артеріального тиску. Крім того, доксазозин, але не урапідил (Ебрантил) вірогідно збільшував добуток частоти серцевих скорочень на тиск у спокої (індекс Робінсона), це говорить про те, що збільшення доксазозином частоти серцевих скорочень має більш виражений характер, ніж його знижувальний вплив на САД [29].
Також виявлена залежність розвитку гіпотонії й ортостатичних ускладнень від дози призначеного урапідилу (60–90–120 мг): одноразові дози 90 та 120 мг мають частіші прояви; від маси пацієнта (частіше виникають при масі менше від 60 кг) та ортостатичного положення тіла. Однак ці ефекти будь-яких доз швидко коригувалися шляхом розміщення пацієнта лежачи (рис. 3).
Слід підкреслити, що при призначенні урапідилу не спостерігаються зміни серцевого викиду [17]. Навіть більше, завдяки зниженню перед- і постнавантаження на серце урапідил сприяє підвищенню ефективності серцевих скорочень [18]. Препарат розслабляє тонус легеневої артерії, а тому може застосовуватися у пацієнтів з підвищеним АТ на тлі хронічної легеневої патології [19].
Антигіпертензивна дія урапідилу супроводжується не зниженням, а підвищенням перфузії певних органів і тканин, зокрема нирок, кишечника, кінцівок. Це відбувається через те, що урапідил не перешкоджає симпатичним реакціям на фізіологічний стимул і не впливає на депресорні та пресорні реакції, індуковані барорецепторами, тобто здатність барорецепторів регулювати системне й органне кровопостачання зберігається [20].
Урапідил (Ебрантил) доступний у вигляді капсул пролонгованої дії для перорального прийому (для лікування резистентної АГ) і у вигляді розчину для внутрішньовенних ін’єкцій (для лікування гіпертонічних кризів, періопераційної й постопераційної гіпертензії та прееклампсії).
Ебрантил («Асіно») завдяки пролонгованій дії капсули slow release гарантує уповільнене вивільнення препарату, поступове досягнення ефективної концентрації й уповільнене її зниження, що забезпечує зменшення коливань максимальної та залишкової концентрації препарату у крові. Це також дозволяє уникнути тяжких ортостатичних реакцій і поліпшує стан ортостатичної регуляції АТ [24]. При прийомі капсульної форми препарату урапідил має досить високу біодоступність — близько 92 %. Антигіпертензивний ефект триває від 4,5 до 8 годин саме завдяки формі slow release.
Таким чином, Ебрантил (урапідил) завдяки подвійному механізму дії — центральному, обумовленому стимуляцією серотонінових 5НТ-1а-рецепторів судинорухового центру, і периферичному, з блокадою постсинаптичних α1-адренорецепторів — має значні переваги у лікуванні пацієнтів з резистентною АГ порівняно з препаратами центральної дії (моксонідин) або тільки α-блокаторами (доксазозин).
Ебрантил здійснює збалансоване зниження САТ і ДАТ, без впливу на ЧШС, тоді як доксазозин викликає рефлекторну тахікардію, а моксонідин обмежений за наявності брадикардії. На відміну від доксазозину, який викликає ортостатичну гіпотензію, і моксонідину, який спричиняє сухість у роті та сонливість, для Ебрантилу характерна відсутність рефлекторної тахікардії, орто-статичної гіпотензії та інших несприятливих побічних ефектів. Ебрантил ефективний у тривалому контролі, без зменшення ефективності, не має синдрому відміни. Також, як доксазозин і моксонідин, Ебрантил знижує рівень атерогенних ліпідів крові та поліпшує метаболізм глюкози.
Доксазозин не має обмежень при призначенні пацієнтам із хворобами нирок, моксонідин при ШКФ 30–60 мл/хв на 1,73 м2 призначається в дозі 0,4 мг, при ШКФ менш ніж 30 — 0,3 мг, Ебрантил може потребувати зниження дози при порушенні функції нирок. І тільки Ебрантил, порівняно з препаратами центральної дії й α-блокаторами, має безсумнівні переваги при використанні у пацієнтів з гострим коронарним синдромом (ГКС), гострою серцевою недостатністю та хронічною серцевою недостатністю.
Це підтверджується доказовою базою Ебрантилу (урапідилу). Так, у дослідженні E. Arosio et al. [25] у хворих з АГ оцінювали антигіпертензивну ефективність урапідилу в дозі 60 мг двічі на добу та вплив тривалої терапії на структуру і функцію міокарда лівого шлуночка (ЛШ). АТ знижувався до 6-го тижня терапії на 9,7 мм рт.ст. Це зниження зберігалося і при більш тривалій терапії (до 6 місяців). При цьому ЧШС вірогідно не змінювалася. Тривала терапія урапідилом призводила також до зменшення товщини задньої стінки ЛШ і міжшлуночкової перегородки, маси міокарда ЛШ і його кінцевого діастолічного розміру [25].
У кількох дослідженнях із застосуванням урапідилу (60–180 мг/добу) у пацієнтів з гіпертрофією ЛШ (ГЛШ), у яких ефективність терапії контролювали за допомогою ЕхоКГ, відзначений регрес ГЛШ, про що свідчила динаміка товщини стінок, маси та/або індексів маси ЛШ [26].
Вивчена можливість застосування урапідилу при гострому коронарному синдромі. При дослідженні перфузії міокарда у хворих з ГКС із підйомом сегмента ST на електрокардіограмі під час виконання первинної ангіопластики показано, що урапідил може поліпшувати коронарний кровотік, перфузію міокарда та функцію ЛШ [27].
Урапідил показав добрі результати при використанні у літніх пацієнтів з АГ, ЦД та серцевою недостатністю (СН). Yang et al. (2015) провели рандомізацію 72 пацієнтів літнього віку, використовуючи урапідил і порівнюючи його з нітрогліцерином. У групі, яка отримувала урапідил, був вірогідно нижчий систолічний тиск, вірогідно менший рівень про-N-термінального В-натрійуретичного пептиду і більш високі фракція викиду ЛШ, серцевий індекс, кінцевий діастолічний об’єм ЛШ. Автори дійшли висновку щодо поліпшення функції серця та зниження АТ: урапідил кращий за нітрогліцерин і є корисним терапевтичним засобом у хворих із серцевою недостатністю [28].
У проспективному 3-річному дослідженні PRIHAM оцінювали ефекти урапідилу на кардіоваскулярні наслідки більш ніж у 3000 хворих з артеріальною гіпертензією середньої тяжкості та високим ризиком (діагностований атеросклероз судин, ішемічна подія в анамнезі). Показано, що зниження артеріального тиску, яке досягалося в більшості випадків (> 80 %), супроводжувалося зменшенням частоти кардіоваскулярних ускладнень, зокрема цереброваскулярних. Це зниження було значущим (26 %) і спостерігалося вже з 15-го місяця лікування. З огляду на це урапідил можна розглядати як препарат, що не тільки ефективно знижує і контролює АТ в найбільш складних ситуаціях, але й впливає на прогноз пацієнтів з АГ та кардіоваскулярним ризиком [26].
Висновки
Відповідно до сучасних рекомендацій ЕSН-2023, резистентна АГ визначається як недосягнення цільових цифр артеріального тиску (< 140/90 мм рт.ст.) при зміні способу життя й одночасному використанні оптимальних доз 3 антигіпертензивних препаратів різних класів, включно з діуретиком, у пацієнтів, прихильних до терапії.
Діагностика резистентної гіпертензії повинна починатися з ідентифікації псевдорезистентної АГ та виключення вторинної АГ.
За поганої переносимості спіронолактону, а також при ХХН I–III стадії та ШКФ ≥ 30 мл/хв на 1,73 м2 експерти ESH-2023 рекомендують розглянути призначення β-адреноблокаторів, або блокаторів α1-адрено-рецепторів, або препаратів центральної дії (II, В) для лікування резистентної АГ.
Урапідил (Ебрантил) має подвійний механізм антигіпертензивної дії: центральний, обумовлений стимуляцією серотонінових 5НТ-1а-рецепторів судинорухового центру, і периферичний, викликаний блокадою постсинаптичних α1-адренорецепторів, завдяки чому забезпечує ефективне зниження АТ у пацієнтів з резистентною гіпертензією. Має мінімальний вплив на ЧШС, що важливо при терапії β-блокаторами та при брадикардії, а також мінімальний ризик виникнення ортостатичних ускладнень і гіпотензії. Капсульна форма Ебрантилу slow release гарантує безпечне зниження АТ без ускладнень і тривалу дію до 8 годин.
Урапідил (Ебрантил) порівняно з препаратами центральної дії й α-блокаторами має безсумнівні переваги при використанні у пацієнтів з гострим коронарним синдромом, гострою серцевою недостатністю та хронічною серцевою недостатністю.
/11.jpg)
/12.jpg)